N、C掺杂比例对锐钛矿TiO2电子结构影响的第一性原理研究
李宗宝,贾礼超,王 霞,王梁杰
(1.铜仁学院a.物理与电子科学系;b.生物科学与化学系,贵州 铜仁554300;2.华中科技大学材料科学与工程学院,材料加工与模具重点实验室,武汉430074)
0 引 言
TiO2因在太阳光的转换和储存、温室气体光催化氧化还原及环境有机污染物降解等方面得到广泛应用,已成为最具应用潜力的光催化剂[1-4]。但基于较大的禁带宽度(3~3.2eV),纯净TiO2只对紫外光(λ<400nm)有响应,而对占太阳光能43%的可见光没有响应,因此如何改进TiO2,并使其光响应范围从紫外光区扩展到可见光区成为目前研究的重点。当前对TiO2进行改性采用方法主要由非金属离子掺杂[5]、半导体复合[6]、金属沉积[7]等。然而实验发现:通过过渡金属离子体掺杂可以依托d电子的迁移来提高TiO2的光催化活性[8],但过渡金属掺杂会促使载流子发生复合并降低TiO2热稳定性。大量实验也证明贵金属原子的表面沉积,如等,对TiO2光催化活性的提高具有显著的作用。但贵金属的大量使用必然增加制造成本,不利于工业化生产的推广。自Sato等[12]报道了N掺杂的TiO2具有更好的光催化活性,并提出非金属掺杂能有效降低TiO2的禁带宽度并调节能带分布以来,非金属如C[13]、N[14]、S[15]、B等掺杂的TiO2的报道日益增多。
Sato等[12]通过NOx掺N制备了TiO2-xNx可见光响应催化剂,但存在制备效率低、成本高等缺点。Cui[16]等通过在空气中焙烧TiN得到N掺杂的TiO2,并发现其在可见光下可以有效催化分解水制取H2。刘守新等[17]制备的N掺杂TiO2在可见光下具有较好的光响应效率。对于C掺杂,Khan等[18]发现C掺杂TiO2薄膜在可见光440nm和535nm处有两条吸收带边;Sakthivel和Kisch等[19]报道了其制备的C/TiO2的光催化效率比未掺杂高出5倍。Chen等[20]通过高温氧化法制备C、N和S单掺杂锐钛矿TiO2粉末,发现N掺杂的可见光催化效果最明显,而C的杂质能级则较深。由于材料制备过程中掺杂粒子的替位方式受生长环境的影响较大,因此不同化学环境下C、N掺杂TiO2体系的结果会有较大差异。然而,至今为止掺杂方式,缺陷存在形式以及掺杂比例的变化对光催化性能的影响尚未有系统的研究报道。
本文从第一性原理出发,采用超原胞模型计算了C、N不同比例掺杂TiO2的形成能、晶体结构以及电子结构的变化。从理论上分析了C、N原子替位掺杂的位置,不同比例掺杂对TiO2电子结构和光学性质等的影响,并揭示了单掺杂对TiO2性能的影响。
1 计算方法
基于密度泛函理论的平面波超软赝势方法,采用GGA+PBE交换关联方法[21]对TiO22×2×2的超原胞结构进行优化,获得最佳结构参数。在倒格子空间[22]选取平面波截断能:Ecut=400eV,K点取为4×4×4,自洽场运算精度设为单原子能量收敛至2.0×10-6eV。由于传统GGA理论在能带计算时会低估能带,为与实验形成对比,本文采用GGA+U[23]方法对计算的能带结构和态密度进行修正使其与实验结果相吻合。计算中所选修正参数为:U=6.3eV和J=1eV[24]。后文所有掺杂所选参数均采用相同的设置,以保证计算结果的可比性。为构建多浓度掺杂,在锐钛矿型TiO2在2×2×2优化的超原胞结构基础上,并用N或C随机取代晶格中1~4个O或Ti原子,得到与实验方案相近的掺杂比例。因为极高的形成能及不稳定性,N和C的填隙缺陷模型在本文中不做讨论。另外,由于N与O原子在元素周期表中位置的相近性,已经证明N只能取代O原子掺杂;但对于C替位,由于其在周期表中位置的特殊性,其掺杂方式尚未明确,为获取其真实替位方式,本文对C的替位方式分别采用了取代Ti位和O位的不同方式进行,并在此基础上进行结构优化。本文所有计算均在VASP软件包中进行[25-26]。
2 结果与讨论
为有效讨论C、N不同比例掺杂对TiO2的影响,首先计算了C、N不同位置掺杂后形成能的大小。根据C在元素周期表中的特殊位置,本文认为C在TiO2晶体可能出现C2-和C4+两种离子类型。基于不同掺杂后体系的稳定性条件,为了进一步明确元素掺杂后在TiO2中真实的占据位置,计算了不同掺杂体系杂质的形成能Eform:
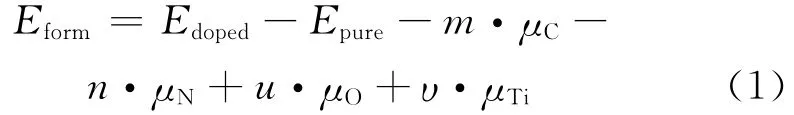
式中Epure和Edoped分别是掺杂前、后锐钛矿TiO2的能量;μN、μC、μO和μTi分别代表N、C、O、Ti 4种元素的化学势;m、n、u、υ对应体系掺杂后掺入原子数目和被替位的原子数目。采用上述公式计算C和N分别取代一个Ti或者O后所得形成能见表1。
由表1可见,N@O的形成能比N@Ti低,C@Ti的形成能比C@O低。表明,N原子倾向于替位O位而C则倾向于Ti位。该结果与张晓艳等[27]的实验推测不同。
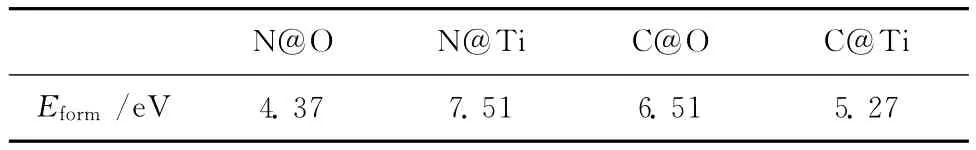
表1 各掺杂体系的杂质形成能Table 1 Formation energies Eformof different doped TiO2
表2列出了结构优化后3种体系的结构参数。由表2可见,优化后的2×2×1纯TiO2超晶胞的晶格参数为a=b=7.577Å,c=9.541Å,与实验结果吻合较好[4]。掺杂后,由于杂质元素离子半径不同,掺杂后导致晶体结构对称性下降,晶格发生畸变。因为N3-离子半径比O2-半径大,N掺杂后Ti-N键长比未掺杂的Ti-O键长。C4+离子半径为0.16Å,远远小于Ti4+离子的半径0.68Å,因此C取代Ti所形成的C-O键较Ti-O键(1.961Å)要小得多,仅为1.242Å。由于杂质离子的掺杂,引起的晶格畸变同样会导致内部偶极矩的产生。偶极矩的变化对TiO2的光催化性能有促进作用。
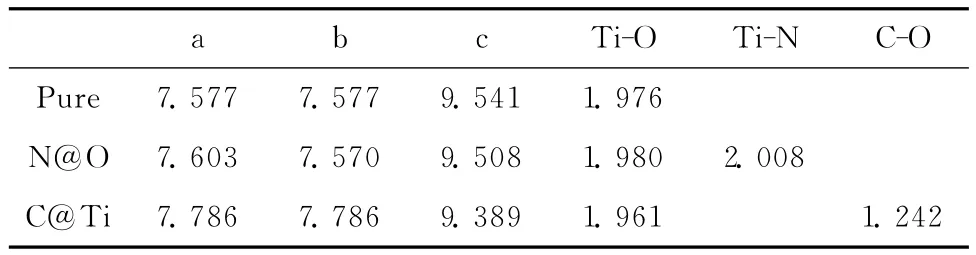
表2 结构优化后各掺杂TiO2体系的晶格参数和平均键长 (Å)Table 2 Lattice parameters and average bond lengths of the doped TiO2after geometry optimization(inÅ)
2.1 不同浓度N掺杂TiO2的电子结构
基于替位结果,研究了N@O体系掺杂量与材料性能的变化趋势。基于该模型计算了各比例条件下TiO2的能带结构和态密度,见图1和图2。晶格中N原子取代部分O原子后,在晶格内部形成了O-Ti-N键,且由于N与O原子半径的差异而引起晶体结构发生畸变,导致掺杂后的禁带宽度(Eg)以及杂质能级与导带底之间的带宽 (Im-CBM)发生变化,具体数值详见表3。由图1和表2可见,N掺杂对禁带宽度大小的影响较小,均在4种掺杂结构的价带顶产生了新的杂质能级。在忽略杂质能级条件下,禁带宽度在掺杂浓度为2.08%时最小(为2.97eV)。若考虑杂质能级对跃迁的辅助作用,杂质能级叠加后使TiO2的吸收带边移动到可见光区。且随着掺杂浓度的增大,杂质能级的密度增加,从而增加了电子的跃迁几率。通过对比图1和图2费米面附近杂质能级的密度,由图2可见,掺杂比例为3.13%时,离子跃迁的几率最大,为较佳掺杂比例。当掺杂浓度继续增加时 (>4.17%),杂质能级将交叠于价带顶部,并使整个价带顶发生上移。该结果在一定条件下有利于光生载流子的传输,但若N含量过高则容易形成TiN结构并使掺杂后的体系呈现金属性,在可见光区域不透明。并且随着N含量的增长,其还将导致晶格中大量缺陷的产生,成为电子-空穴对的复合中心,从而降低材料的光催化活性。因此,N掺杂只有在恰当浓度范围内有利于提高TiO2的光催化性能。
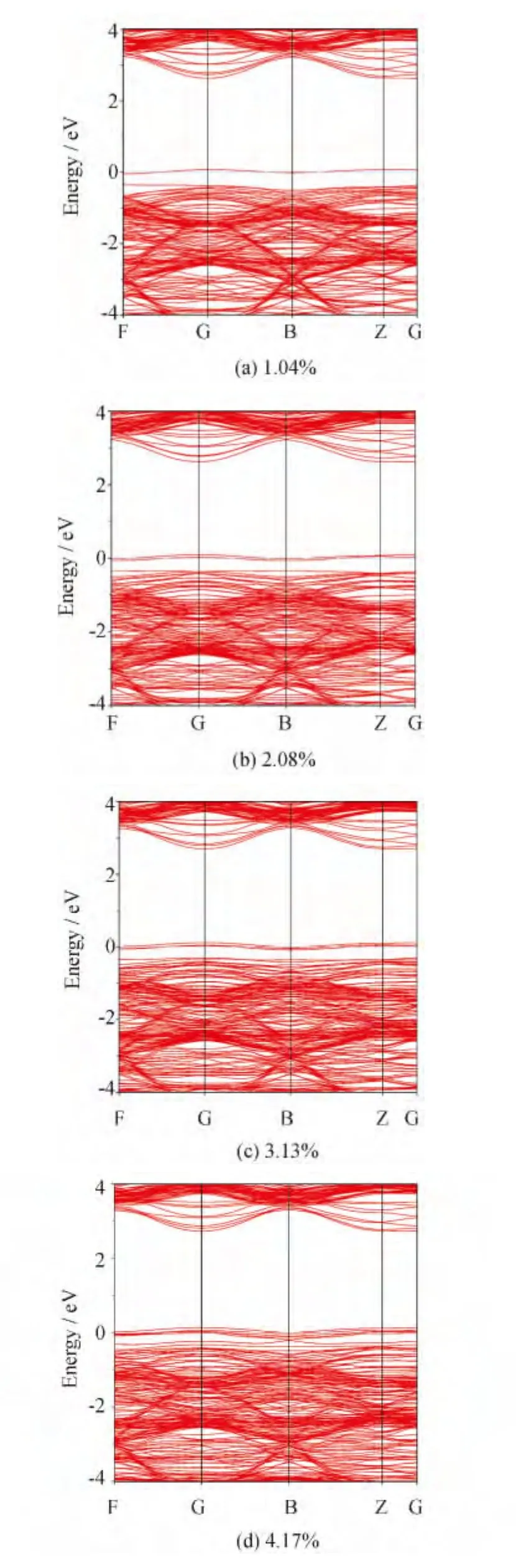
图1 不同浓度N掺杂TiO2体系的能带结构图Fig.1 Band structure for N-doped configurations with various doping levels
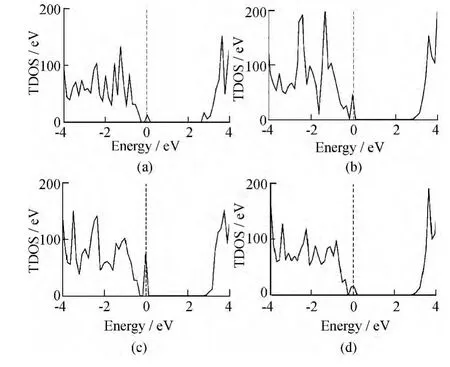
图2 N不同浓度掺杂TiO2的态密度Fig.2 Total DOS of N-doped configurations with different ratios

表3 N不同浓度掺杂后的禁带宽度(eV)Table 3 Band gaps of N-doped configurations with different ratio(in eV)
为进一步了解N掺杂对TiO2能级的影响,给出了不同掺杂浓度的分波态密度,见图3。费米能级附近的杂质能级主要由N-2p态组成且弛豫于价带顶,而O-2p和Ti-3d态的贡献则较小。通过上述比较可见,N掺杂后,体系的价带顶位置主要由N-2p态决定,O-2p态则与N-2p发生交叠使能带密度增加。而掺杂和未掺杂TiO2的导带底均由Ti-3d态决定,并未发生明显变化。掺杂浓度为2.08%和3.13%时,由于N-2p与Ti-3d态之间的p-d杂化作用,导带中Ti-3d态相对有微小的下移。
通过上述分析可见:在较低浓度掺杂时,掺杂浓度的变化对TiO2电子结构的影响并不明显,N的最佳含量为2.08%和3.13%时对TiO2光催化性能的提升最为有利。

图3 N掺杂TiO2体系的分波态密度蓝线:Ti-3d,红色实线:N-2p,虚线:O-2pFig.3 PDOS for N-doped configurations N-2p and O-2p are shown with red solid and dash lines while blue ones indicate the Ti-3dlevels
2.2 不同浓度C掺杂TiO2的电子结构
基于单掺杂体系中C原子更倾向于取代Ti原子并以C4+的阳离子形式存在,因此在构建C掺杂TiO2晶体模型时,所有计算仅考虑C原子替位取代Ti原子的情况,忽略其取代O原子情况。图4给出了不同浓度C掺杂TiO2的能带结构。由图4可见,由于C的非金属性,虽取代Ti但未在禁带中引入杂质能级,而是直接导致导带向低能级移动并降低禁带宽度,增加电子的跃迁几率。比较不同浓度掺杂的禁带宽度可见:当掺杂量为3.13%和4.17%时禁带宽度相同,均为2.51eV;掺杂浓度为1.04%时禁带宽度最大,为2.60eV;当掺杂浓度为2.08%时,禁带宽度最小,为2.30eV。证明掺杂后TiO2均发生明显红移,且C掺杂浓度为2.08%时现象尤为明显。
为进一步揭示C对TiO2掺杂的浓度效应,还计算了不同浓度掺杂体系的分波态密度,见图5。由图5可见,C掺杂后TiO2的价带主要由O-2p态和T-3d态组成,且主要占据低能区域。O-2p态主要贡献费米面附近能级,决定了价带顶的位置;导带主要由Ti-3d态和C-2p态组成,且强烈的pd轨道杂化使导带发生明显下移,从而减小禁带宽度。当掺杂浓度为2.08%和4.17%时,Ti-3d态和C-2p态之间的pd杂化现象非常明显,出现了较强的杂化尖峰。通过对不同体系中O-2p态的态密度对比,可见当掺杂浓度为4.17%时,O-2p态在费米能级附近的杂质峰明显强于其它3种掺杂情况,从而证明在可见光条件下,价电子向导带跃迁的几率增加,有利于TiO2的光催化效率的提高。

图4 不同浓度C掺杂TiO2体系的能带结构Fig.4 Band structure for C-doped configurations with various doping levels
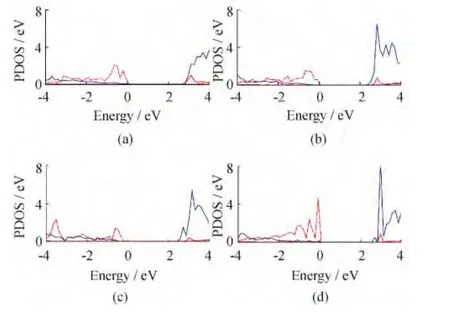
图5 不同浓度C掺杂TiO2体系的分波态密度Fig.5 PDOS for C-doped configurations with different ratios
通过上述分析可见C随掺杂浓度变化时,C-2p态与Ti-3d态之间的杂化效应直接导致导带向低能方向移动,从而引起了禁带宽度的减小并使其吸收带边产生明显红移。根据对禁带宽度的对比可见:当掺杂浓度为2.08%时,对可见光的响应最强,此时催化活性应为最高。通过与N掺杂TiO2结果比较可见:浓度效应对C掺杂体系光催化性能的影响更为明显。
3 结 论
基于密度泛函理论的第一性原理,计算了N、C原子不同比例掺杂锐钛矿TiO2的形成能、晶格结构及电子结构。通过对形成能的比较可见N原子倾向于替代O位而C则取代Ti位;通过对不同比例掺杂晶体的能带和带密度的分析可见N在较低浓度掺杂时,掺杂浓度对TiO2电子结构的影响并不明显,且N含量为2.08%和3.13%时TiO2对可见光的响应最佳,此时光催化性能较好;C掺杂浓度为2.08%时,其对可见光的响应最佳。与N掺杂TiO2相比,浓度效应对C替位Ti位掺杂体系光催化性能的影响更为明显。
[1]Fujishima A,Honda K.Electrochemical photolysis of water at a semiconductor electrode[J].Nature,1972,238:37-39.
[2]Gole J L,Stout J D,Burda C,et al.Highly efficient formation of visible light tunable TiO2-xNxphotocatalysts and their transformation at the nanoscale[J].The Journal of Physical Chemistry B,2004,108:1 230-1 240.
[3]Sinsebigler A L,Lu G,Yates J T.Photocatalysis on TiO2surface:principles,mechanism and selected results[J].Chemical Reviews,1995,95:735-758.
[4]Fujishima A,Rao T N,Tryk D A.Titanium dioxide photocatalysis.Journal of Photochemistry and Photobiology C[J].Photochemistry Reviews,2000,1:1-21.
[5]Asahi R,Morikawa T,Ohwaki T.Visible-light photocatalysis in nitrogen-doped titanium oxides[J].Science,2001,293:269-271.
[6]程 刚,周孝德,李 艳,等.纳米ZnO-TiO2复合半导体的La3+改性及其光催化活性 [J].催化学报,2007,28(10):885-889.
[7]李宗宝,王 霞,贾礼超.N/Fe共掺杂锐钛矿TiO2(101)面的协同作用的第一性原理研究 [J].物理学报,2013,20:1-5.
[8]Hou Q Y,Zhang Z D,Li C.First-principles study of the electronic life and red shift effect of Sm-doped anatase TiO2[J].Journal of Functional Materials,2012,43(19):2 599-2 604.
[9]Subrahmanyam A,Biju K P,Rajesh P,et al.Surface modification of solgel TiO2surface with sputtered metallic silver for Sun light photocatalytic activity:Initial studies[J].Solar Energy Materials &Solar Cells,2012,101:241-248.
[10]Li Z B,Wang X.First-principle study of electronic structure and enhanced visible-light photocatalytic activity of anatase TiO2through C and F codoping[J].Advanced Materials Research,2013,746:400-405.
[11]Zhang M Y,He G Z,Ding C C,et al.Mechanism of arsenate(V)adsorption on TiO2surfaces[J].Acta Phys.Chim.Sin,2009,25,2 034-2 038.
[12]郑树凯,吴国浩,刘 磊.P掺杂锐钛矿相TiO2的第一性原理计算[J].物理学报,2013(4):94-100.
[13]Carp O,Huisman C L,Reller A.Photoinduced reactivity of titanium dioxide[J].Progress in Solid State Chemistry,2004,32(1-2):33-177.
[14]Suda Y,Kawasaki H,Ueda T,et al.Preparation of high quality nitrogen doped TiO2thin film as a photocatalyst using apulsed laser deposition method[J].Thin Solid Films,2004,453:162-166.
[15]Umebayashi T,Yamaki T,Itoh H,et al.Band gap narrowing of titanium dioxide by sulfur doping[J].Applied Physics Letters,2002,81:454-456.
[16]Cui X L,Ma M,Zhang W,et al.Nitrogen-doped TiO2from TiN and its visible light photoelectrochemical properties[J].Electrochem Commun.,2008,10:367-371.
[17]刘守新,陈孝云,李晓辉.N掺杂对TiO2形态结构及光催化活性的影响 [J].无机化学学报,2008,24:253-259.
[18]Khan S U M,Al-Shahry M,Ingler Jr W B.Efficient potochemical water splitting by a chemically modified n-TiO2[J].Science,2002,297:2 243-2 245.
[19]Sakthivel S,Kisch H.Daylight photocatalysis by carbon-modified titanium dioxide[J].Angew Chem-Int Edit,2003,42(40):4 908-4 911.
[20]Chen V,Burda C.The electronic origion of the visible-light absorption properties of C-,N-and S-doped TiO2nanomaterials[J].J.Am.Chem.Soc,2008,130:5 018-5 019.
[21]Monkhorst H J,Pack J D.On special points for brillouin zone integrations[J].Phys.Rev.B.,1976,13:5 188-5 192.
[22]Dudarev S L,Botton G A,Savarsov S Y.Electron-energy-loss spectra and the structural stability of nickel oxide:An LSDA+U study[J].Phys.Rev.B.,1998,57:1 505-1 509.
[23]Kavan L,Gratzel M,Gilbert S E.Electrochemical and photoelectrochemical investigation of single-crystal anatase[J].J.Am.Chem.Soc.,1996,118:6 716-6 723.
[24]Jia L C,Wu C C,Li Y Y,et al.Enhanced visiblelight photocatalytic activity of anatase TiO2through N and S codoping[J].Appl.Phys.Lett.,2011,98:211 903-211 905.
[25]Kresse G,Furthermuller J.Efficiency of ab-initio total energy calculations using aplane-wave basis set[J].Phys.Rev.B.,1996,54:11 169-11 186.
[26]Perdew J P,Burke K.Generalized gradient approximation made simple[J].Phys.Rev.Lett.,1996,77:3 865-3 868.
[27]张晓艳,崔晓莉.C-N共掺杂纳米TiO2的制备及其光催化制氢活性[J].物理化学学报,2009,25(9):1 829-1 834.
