HPLC法测定小儿消食颗粒中熊果酸的含量
李华玉,林永强,郭东晓
(1.临沂市食品药品检验检测中心,山东临沂276001;2.山东省食品药品检验所,山东济南250101)
HPLC法测定小儿消食颗粒中熊果酸的含量
李华玉1,林永强2,郭东晓2
(1.临沂市食品药品检验检测中心,山东临沂276001;2.山东省食品药品检验所,山东济南250101)
目的采用高效液相色谱法测定小儿消食颗粒中熊果酸的含量。方法以十八烷基硅烷键合硅胶为填充剂,甲醇-0.5%醋酸铵溶液(83∶17)为流动相,检测波长为215 nm。结果熊果酸的进样量在0.168 6~3.372 0 μg之间与峰面积线性关系良好,相关系数r=1.000 0,平均加样回收率为96.5%(RSD=0.59%,n=6)。结论该方法简便、准确,可用于小儿消食颗粒中熊果酸的含量测定。
小儿消食颗粒;熊果酸;含量测定
1 仪器与试药
1.1 仪器 Agilent 1200高效液相色谱仪;Sartorius CP225D电子天平。
1.2 试药 熊果酸对照品(中国食品药品检定研究院提供,批号:110742-200517);供试品批号为100801、110905、110906(规格1,产地山西,每袋装1.5 g),1110002、1111001、1111002(规格2,产地山东,每袋装1.2 g),由生产厂家提供,阴性对照为自制;甲醇为色谱纯,水为Millipore制备的纯化水,其他试剂均为分析纯。
2 方法与结果
2.1 供试品溶液制备方法的考察
2.1.1 提取溶剂的考察 熊果酸极性较低,易溶于脂溶性较强的溶剂。参照《中国药典》2010年版(一部)小儿消食片项下的提取条件,比较乙醚、二氯甲
烷、甲醇三种脂溶性溶剂的提取效果。结果测得每袋含量依次为0.76、0.66、0.76 mg。以二氯甲烷为提取溶剂时含量测定结果最低,其他两种结果相当。但是甲醇提取的供试品溶液放置后,有结晶析出,可能会影响色谱柱使用寿命,所以采用乙醚作为提取溶剂。
2.1.2 提取方法的考察 考察的提取方法包括:超声处理(功率500W,频率40 kHz)30、60、90 min,回流提取1、2 h。测得每袋含量依次为0.744、0.763、0.763、0.758、0.763 mg。由测定结果可知,超声提取60、90 min与加热回流提取2 h结果相当。为了节省能源,确定提取方法为超声提取60 min。
2.1.3 提取次数的考察 以乙醚作为提取溶剂,超声提取60 min,对比了1次和2次提取的测定结果,发现二者差距不大,结果分别为每袋0.763、0.764 mg。所以确定超声提取1次即可。
2.1.4 取样量的考察 考察三个取样量(分别为1、2、3 g)对含量测定结果的影响。结果每袋含量分别为0.763、0.763、0.746 mg。取样量1 g和2 g时测定结果差异不大,取样量3 g时测定结果偏低。为了确保取样的均匀性,确定规格2取样量为2 g。由于规格1的处方量与规格2相同,制成总量是规格2的2.5倍,故规格1的取样量定为5 g。
2012年11月 起,五建每隔三年开展一轮“情系千里,爱暖身边”异地慰问活动,对分布于甘肃、陕西、四川、河南、吉林、上海等14个省市的离退休老同志进行入户和集中慰问,累计行程5万余公里136个县市地区。
2.2 供试品溶液的制备 取重量差异项下的样品,研细,取规格1约5 g或规格2约2 g,精密称定,置具塞锥形瓶中,加乙醚100 mL,超声处理(功率500 W,频率40 kHz)1 h,放冷,摇匀,滤过,滤渣用乙醚洗涤2次,每次25 mL,合并乙醚液,挥干,残渣用石油醚(30~60℃)浸泡2次,每次10 mL(约浸泡1 min),倾去石油醚,残渣用甲醇溶解并转移至10 mL量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液作为供试品溶液。
2.3 对照品溶液的制备 精密称取熊果酸对照品15.08 mg,置25 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,精密量取5 mL,置25 mL量瓶中,加甲醇稀释至刻度,摇匀,即得到浓度为0.120 6 mg·mL-1的对照品溶液。
2.4 流动相的考察 参考有关文献[1~3],选择色谱柱Thermo BDS Hypersil C18(4.6mm×250mm,5μm),检测波长215 nm,考察三种流动相:甲醇-0.05%冰醋酸溶液(88∶12)、甲醇-0.05%冰醋酸溶液(83∶17)和甲醇-0.5%醋酸铵溶液(83∶17)。
精密吸取供试品溶液及对照品溶液各10μL,注入液相色谱仪,在三种流动相下进行测定,熊果酸色谱峰与相邻峰分离度依次为1.35、1.45、1.77。故确定以甲醇-0.5%醋酸铵溶液(83∶17)作为流动相。
2.5 色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂;以甲醇-0.5%醋酸铵溶液(83∶17)为流动相,流速1 mL·min-1;柱温:35℃;检测波长为215 nm。理论板数按熊果酸峰计算应不低于8 000。
2.6 耐用性试验 考察三种色谱柱:依利特Hypersil BDSC18(4.6 mm×250 mm,5μm);Kromasil 100-5 C18(4.6 mm×250 mm,5μm);Thermo BDSHypersil C18(4.6 mm×250 mm,5μm);按“2.5”项下确定的条件进行试验。三种不同品牌的色谱柱分离度依次为1.81、1.60、1.77。结果表明,熊果酸色谱峰峰形较好,分离度均大于1.5,试验条件适用范围广。
2.7 线性关系的考察 分别精密吸取熊果酸对照品溶液(C对为0.168 6 mg·mL-1)1、2、5、10、15、20μL,注入液相色谱仪,分别测定峰面积。以熊果酸对照品的进样量为横坐标,峰面积为纵坐标,进行线性回归,得回归方程,Y=241.160 0X+1.070 5(r=1.000 0)。试验结果表明,熊果酸进样量在0.168 6~3.372 0μg之间进样量与峰面积呈良好的线性关系。
2.8 精密度试验 精密吸取熊果酸对照品溶液(0.168 6 mg·mL-1)10μL,注入液相色谱仪,连续进样6次,测其峰面积,RSD为0.19%,说明仪器精密度良好。
2.9 稳定性试验 取批号为1111002(规格2)的样品,照“2.3”项下供试品溶液的制备方法制成供试品溶液。每隔5 h进样一次,每次10μL,测定熊果酸峰面积,共考察25 h,计算,RSD为0.47%,结果表明供试品溶液在25 h内稳定性良好。
2.10 重复性试验 取批号为1111002(规格2)的样品,照“2.3”项下供试品溶液的制备方法制成供试品溶液,平行制备6份,分别精密吸取供试品溶液10μL,注入液相色谱仪,测定,计算含量。结果平均含量为每袋0.759 3 mg(RSD为0.31%),说明方法重复性良好。
2.11 加样回收率试验 取批号为1111002(规格2,熊果酸含量为0.759 3 mg/袋,每袋装1.2 g)的样品约1 g,精密称定,精密加入熊果酸对照品溶液(浓度为:0.674 4 mg·mL-1)1 mL及乙醚99 mL,按供试品溶液的制备方法平行制备6份,用上述色
谱条件进行测定,计算回收率,结果见表1。

表1 加样回收率试验结果
结果表明,测定方法的回收率良好。
2.12 专属性试验 取处方中除去山楂的其他药味,按处方比例制成缺山楂阴性对照样品,照“2.3”项下供试品溶液的制备方法制得阴性对照溶液。分别精密吸取熊果酸对照品溶液、供试品溶液及阴性对照溶液各10μL,注入液相色谱仪进行测定。结果供试品色谱中,在与对照品色谱保留时间相同的位置上,有相应色谱峰,而阴性对照色谱中无相应色谱峰。说明处方中其他药味对测定结果无干扰。结果见图1。
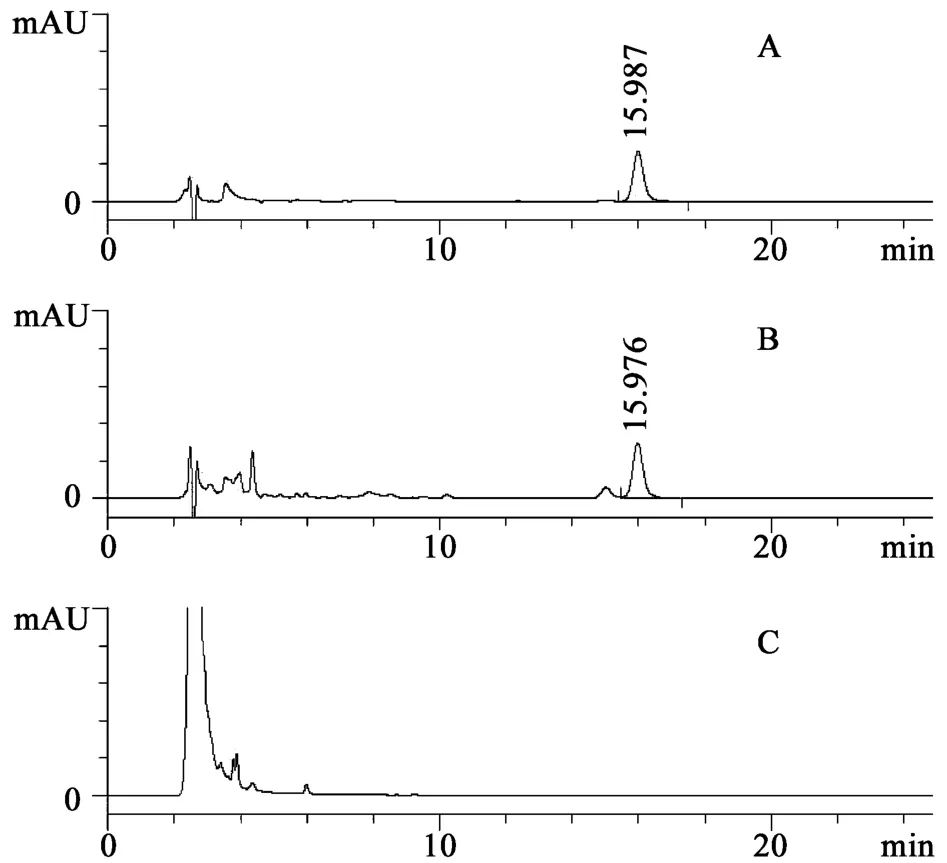
图1 专属性试验HPLC色谱图A.对照品;B.样品;C.阴性对照
2.13 样品含量测定 按供试品溶液的制备方法及上述色谱条件对6批样品进行测定,结果见表2。
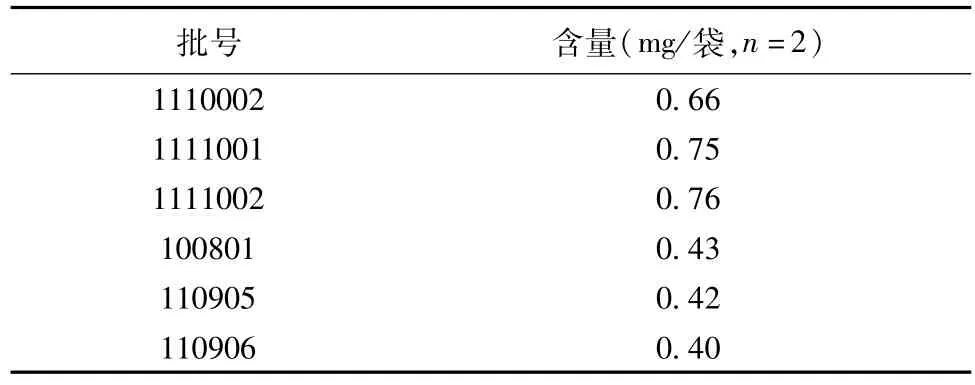
表2 熊果酸含量测定结果
3 讨论
3.1 本实验中的供试品溶液,是参照《中国药典》2010年版(一部)小儿消食片的提取条件进行制备的,这有利于系列制剂标准的统一。但是在后续的实验过程中发现,在《中国药典》小儿消食片的HPLC条件下[流动相为甲醇-0.05%冰醋酸溶液(88∶12)],小儿消食颗粒供试品溶液中熊果酸的色谱峰未能达到合适的分离度,即使换用多种不同品牌的色谱柱,分离度始终低于1.5。采用流动相[2~4]:甲醇-0.5%醋酸铵溶液(83∶17),熊果酸峰的分离效果好,对色谱柱选择性不强。
3.2 同一中药制剂质量标准不同,是当前中药检验和质量控制中遇到的一大问题。本文建立的熊果酸含量测定方法,对分别执行两个不同标准的两个生产厂家的小儿消食颗粒均适用,为其质量标准的统一提供了实验依据。
[1]国家药典委员会.中华人民共和国药典2010年版(一部)[S].北京:中国医药科技出版社,2010:493-494.
[2]李涛,郝武常,徐长根,等.HPLC-ELSD法测定不同产地女贞子中齐墩果酸与熊果酸的含量[J].中药材,2005,28(5):391-393.
[3]高文分,袁文娟.HPLC法测定毛萼香茶菜不同药用部位中熊果酸和齐墩果酸的含量[J].药物分析杂志,2009,29(11):1947-1949.
[4]梁瑞雪,张新军,贾元印,等.HPLC法测定天中胶囊中刺囊酸和齐墩果酸的含量[J].药学研究,2013,32(11):626-628.
Determination of usolic acid of Xiao′er Xiaoshi Granules by HPLC
LI Hua-yu1,LIN Yong-qiang2,GUO Dong-xiao2
(1.Linyi Center for Food and Drug Control,Linyi276001,China;2.Shandong Institute for Food and Drug Control,Jinan 250101,China)
ObjectiveTo establish an HPLC method for the determination of usolic acid in Xiao′er Xiaoshi Granules.MethodsC18column was adopted with methanol-0.5%ammonium acetate solution(83∶17)as mobile phase,and the detection wavelength was 215 nm.ResultsThe linear range of usolic acid was 0.168 6~3.372 0μg(r=1.000 0)and the average recovery was 96.5%(RSD=0.59%,n=6).ConclusionThe simple and accurate method can be used to determinate usolic acid of Xiao′er Xiaoshi Granules.
Xiao′er Xiaoshi Granules;Usolic acid;Determination
R927.2
A
2095-5375(2014)01-0011-003
2011年国家药品标准提高课题(No.741)
李华玉,男,副主任药师,研究方向:药物分析,E-mail:820998279@qq.com
郭东晓,男,博士研究生,研究方向:药物分析,Tel:0531-81216523,E-mail:guodx0212@126.com。

