枞酸单离与应用研究进展
农韦健,陈小鹏,梁杰珍,王琳琳,黄科林,史磊,吴睿,李克贤
(1 中国科技开发院广西分院,广西 南宁530022;2 广西大学化学化工学院,广西 南宁 530004;3 广西有色金属集团汇元锰业有限公司,广西 来宾 546138)
松香是中国最大宗的林业产品之一,根据原材料来源可划分为脂松香、浮油松香和木松香3种。中国以脂松香生产为主,年产松香约70万吨,主要集中在广西、广东、云南、江西、福建、湖南、湖北七大产区。中国松香产量和国际贸易量居世界第一位,近几年产量和国际贸易量分别占世界总量的50%~60%和 60%~70%[1]。2011年中国松香产量约77.3万吨,然而由于世界经济低迷,国内外市场对中国松香的需求锐减,当年出口量仅为48%,为近5年来最少的一年[2]。供需矛盾突出,使松香价格大幅度下降。经历了2011年产量剧增,价格大跌的严峻考验后,相比前两年行业剧烈扩张,2012年中国松香行业转入了明显收缩阶段,可以说 2012年是中国松香行业面对新的内外部环境大调整的一年。自2011年下半年以来,松香行业一直面临着低迷的市场环境,2013年的松香行业仍然处于弱势的低迷状态,出口的推动乏力,松香行业仍处于理性调整的平稳发展阶段。
松香一般包含枞酸、新枞酸、脱氢枞酸、长叶松酸、海松酸、异海松酸、左旋海松酸等13种树脂酸[3-4],其化学结构见文献[4]。松香的主要成分是枞酸,它的化学结构如图1所示。从枞酸的结构可知,枞酸是三环菲骨架一元羧酸,属二萜类化合物,分子中存在多个手性中心,而且存在共轭双键,独特的结构使枞酸具有广阔的应用前景,在合成生物活性物质、医药、农药等方面有广泛应用。因此,加快松香的深度开发利用对促进中国林产化学工业的发展有着重要的战略意义。
1 枞酸单离方法
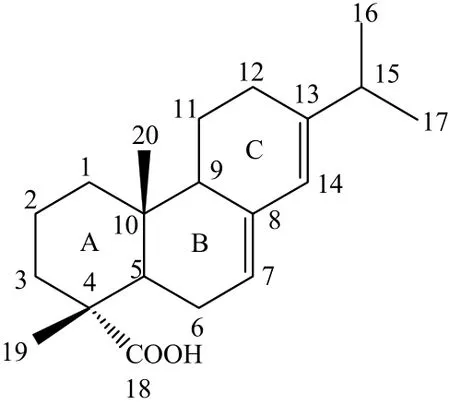
图1 枞酸的化学结构
松香是含有13种树脂酸的混合物,由于其所含各种树脂酸多为同分异构体,从而导致它们的分子间作用力与物理性质很接近,采用物理方法很难对其进行分离提纯,通常要结合化学方法进行分离。根据文献报道,目前枞酸单离的方法[5-12]主要有溶剂重结晶法、钠盐结晶法以及有机胺盐结晶法等。
1.1 溶剂重结晶法
溶剂重结晶法,即以乙醇或乙酸等有机溶剂为重结晶剂,对松香进行反复重结晶制备枞酸的方法。Maly采用75%乙醇为重结晶剂,在50℃下对松香进行重结晶提取枞酸,不溶物用85%热乙醇重结晶数次,并发现加入水可以使枞酸快速结晶出来。Ellingson[5]采用与Maly类似的方法提取枞酸,发现不加入水,而是让枞酸从95%热乙醇溶液中自然出来,可以提高枞酸的纯度。Knecht等用冰乙酸溶解松香,溶液静置一周,所得结晶经抽滤后用乙酸、甲醇和乙醇重结晶20次以上,得到枞酸产品,但是收率和纯度都很低。Gubelmann等[6]以精制松香为原料,用80%乙醇对精制松香进行多次重结晶,得到白色晶体枞酸,其熔点为165℃。Steele[7]采用乙醇和乙酸反复重结晶的方法从松香酸中分离提纯枞酸,该法步骤繁琐,枞酸的纯度及收率都比较低。
1.2 钠盐结晶法
钠盐结晶法提取枞酸的具体过程为[8]:用浓盐酸使松香异构化,用碱(氢氧化钠)中和盐酸,然后加入乙醇钠转化成枞酸钠盐,再用乙醇反复重结晶枞酸钠盐,最后用硫酸酸化得到枞酸产品,其熔点为 171~173℃,比旋光度为-100.5°。Cox[9]也采用钠盐结晶法从松香中分离提纯得到枞酸。采用钠盐结晶法提取枞酸,由于松香中的其他异构体也会形成结晶状钠盐 C19H29COONa·3C20H30O,所以钠盐结晶法不仅选择性低,产品的纯度和收率也很低,因此,该法目前无实际性进展。
1.3 有机胺盐结晶法
王文军等[10]发现借助有机碱和松香酸形成的盐进行枞酸分离纯化非常有效,而且极具大规模纯化制备前景。Harris等[11]总结前人工作,归纳出了有机胺盐结晶法分离提纯枞酸的方法,其过程为:①异构化,即在惰性气体(CO2)保护下,用浓盐酸使松香异构化,提高松香中枞酸的含量;②胺化反应,即以丙酮为溶剂溶解异构化松香,在高强度搅拌下缓慢滴加二戊胺,使枞酸与二戊胺反应生成枞酸二戊胺盐;③胺盐重结晶,以丙酮为重结晶剂,对反应生成的二戊胺盐反复重结晶,得到纯枞酸二戊胺盐;④酸化,以95%乙醇为溶剂溶解枞酸二戊胺盐,采用强酸置换弱酸的原理,在强烈搅拌条件下往溶液中加冰乙酸,将枞酸置换出来,得到枞酸粗品,再用95%乙醇对枞酸粗品进行重结晶得到纯品枞酸。此法获得的枞酸紫外最大吸收波长为241nm,比旋光度为-106°。采用有机胺盐结晶法分离提纯枞酸虽然步骤繁琐,但是枞酸的纯度及得率都较高,是工业化生产枞酸最可行的方法。该法的主要缺点在于用丙酮作为重结晶剂,而且用量很大,对环境污染比较严重,而且有机碱二戊胺的价格昂贵,造成生成成本较高,从而在一定程度上限制了高附加值枞酸下游产品的研究开发。王文军等[10]采用二戊胺盐结晶法分离纯化枞酸,并通过紫外光谱等对其结构进行确定。韩春蕊等[12]以自制价格低廉的A胺为有机碱,采用有机胺盐结晶法分离提纯枞酸,得到纯度为90.91%的枞酸产品。
1.4 其他方法
随着微波超声波技术的发展,许多科研工作者将其引入到枞酸的分离纯化当中,而且取得良好效果。姚兴东等[13]发明了一种微波辅助酸异构、再以丙酮为重结晶剂反复重结晶异构松香制备枞酸的发方法,该法枞酸的纯度达96%,得率达15%~25%。高艺美等[14]采用超声波辅助酸异构,再用95%乙醇反复重结晶异构松香制备枞酸,枞酸的纯度为97.32%,得率为 31.71%。高艺美等[15]应用超声波辅助胺盐重结晶法进行枞酸单离研究,所得枞酸产品纯度为 98.42%,得率为 49.73%,比旋光度为-106.3°。刘红军等[16]用固体酸-阳离子交换树脂作为催化剂,在固定床反应器中进行松香异构反应,再用有机溶剂反复重结晶异构松香制备枞酸,收率达到 85%以上,纯度达到 96%以上,比旋光度在-105°~-108°。Jin等[17]利用共晶法制备枞酸,但该法不仅周期长,而且得率很低,只有9.5%。还有研究者采用气相色谱法[18]、液相色谱法[19-20]以及毛细管电泳法[21]等将松香的成分逐一分开,但是这些方法只能用于实验室成分分析,许多情况下只能作为枞酸物理常数和化学特性测定以及气相色谱分析的标准样品的制备方法,不适合作为枞酸产品提纯制备的方法,更不适合作为枞酸工业化生产的方法。
2 枞酸的应用研究进展
2.1 枞酸用于合成生物活性物质
通过枞酸的活性基团,可以合成具有各种生物活性的枞酸衍生物。枞酸经立体专一性合成的 12-脱氧罗列酮具有很高的抗利什曼原虫活性[22],A lvarez等[23]以枞酸为原料经过定位氧化获得的雷公藤内酯酮和雷公藤内酯醇具有抗肿瘤、抗炎症等生物活性。González等[24]合成了多种枞酸衍生物,并对其活性进行评价,结果发现含醛基的枞酸衍生物具有抗真菌和抗肿瘤活性,枞酸醇具有较弱的抗病毒活性,枞酸甲酯具有很高的细胞抗病毒活性。Gigante等[25]由枞酸制得茶多酚,并评价其生物活性,结果表明合成的茶多酚具有抗菌、抗病毒、抗肿瘤、抗恶性细胞增生等生物活性。Berettoni等[26]以枞酸为原料合成了多种具有生物活性的化合物。枞酸及其衍生物还具有抗串珠镰刀菌和根腐丝囊菌活性[27],抗疟疾活性[28],抗疱疹病毒复制的功效等[29]。Santos等[30]以枞酸为前体,经化学转化法可制得有抗金葡萄菌、枯草芽孢杆菌、藤黄微球菌,抗黑素瘤和乳腺癌等生物活性的枞酸衍生物。
此外,由于枞酸的分子结构中存在多个手性中心,经定位选择性氧化,定位选择性还原等方法,可获得各种手性合成子,是合成各种手性生物活性物质的有效前体[31-32]。Presser等[33-34]通过雷福尔马茨基反应和迈克尔加成反应对枞酸的B环和C环进行选择性进攻,获得多种枞酸氧化衍生物以及手性合成子,可用于合成更高萜类手性生物活性物质。
2.2 枞酸在医药上的应用
枞酸的衍生物四氢化三羟基枞酸和三羟基枞酸有利胆作用[35-36],四羟基枞酸碱金属盐有很强的刺激胆汁分泌的功能[37-38]。枞酸胺盐衍生物能降低血清中的胆固醇,降低动脉硬化的危险[39]。由枞酸制成的外用药膏可用于治疗烧伤等引起的皮肤外伤和糖尿病等引起的皮肤溃烂[40-41]。四氢枞酸及其酯类衍生物有杀灭口腔细菌的功效,能有效杀死革兰氏阳性厌氧细菌[42],还能有效抑制粉刺,播散性座疮等病毒[43]。一份美国专利报道,枞酸及其衍生物有抗癌功能,而且对正常细胞无影响,可选择性抑制癌细胞增长和肿瘤增大[44]。米彩峰等[45]利用松香提取物枞酸和其他辅料制成一种中药,该中药用于治疗银屑病具有服用方便、无毒性和副作用小等优点。Nobuyuki等[46]对枞酸具有消炎作用的机理进行了研究,结果发现,枞酸不仅可以用来消炎,而且可以调节脂类代谢和抗动脉硬化。Fernández等[47]评估了枞酸的抗炎活性,认为经过口服或外用均能发挥积极的抗炎功效,同时枞酸还能抑制一些引起炎症的中间体的产生。Ulusu等[48]的研究表明,枞酸是大豆5-脂肪氧化酶抑制剂(IC50=29.5±1.29μmol/ L),可抑制人的 5-脂肪氧化酶,有望用在治疗诸如过敏、哮喘、关节炎、银屑癣等疾病。
此外,枞酸在医药方面还可以作为药物包衣、微囊,在药物缓释控制方面有广泛应用。枞酸及其衍生物作为肠溶包衣膜,具有较强的抗胃酸能力,药物缓释可达3h以上,同时这种膜有较好的吸湿性能,可用作易受潮药物的包膜材料[49]。枞酸甘油酯具有优良的耐酸性能,酸值为 54的枞酸甘油酯(AaG-54)和酸值为20的枞酸甘油酯(AaG-20)具有良好的抗湿性能,用作药物微囊材料其缓释时间可达 3h以上[50]。枞酸及其衍生物作为微胶囊壁膜形成材料,在人体容易溶解,具有优良的传递性能,而且对胃有保护作用[51]。Ramani等[52]以双枞酸作为药片基体材料,发现其不仅成膜性能好,而且具有良好的耐酸、耐碱以及疏水性,可使水溶性药物缓释时间达到24h。Barabde等[53]将枞酸与甘油和马来酸酐反应得到枞酸衍生物(RGM),该衍生物具有优良的成膜性能以及低的吸湿率和水蒸气透过率,适合用作耐湿药物的包膜,该包膜容易降解,质量分数为 12%的包膜可使药物缓释达到8h。Nande等[54]将枞酸与聚乙二醇(PEG200)和马来酸酐反应得枞酸酯类衍生物,并研究其玻璃转化温度、水蒸气透过率等理化性质,结果表明,该枞酸酯类衍生物可用于药物缓释。Fulzele等[55]对合成的二枞酸季戊四醇酯进行了研究,发现二枞酸季戊四醇酯膜用于药物缓释可使缓释时间长达90天,而且该膜具有良好的生物相容性。
2.3 枞酸在农业方面的应用
枞酸及其衍生物有抗虫害、杀菌、防霉的功效,在农业中具有广泛用途。美国田纳西公司在 1958年研制出新的有机杀菌剂TO-90,该杀菌剂的有效成分为枞酸铜和脂肪酸,经过对27个州的37种植物进行试验,结果表明该杀菌剂对甜菜、花生等植物的叶斑病及番茄、马铃薯等作物的晚疫病具有良好的预防效果[56]。枞酸碱金属盐有杀菌防霉的功效,法国Tohoku Hordness公司研制出一种含有枞酸碱金属盐杀菌防霉剂,能有效抑制稻枯病和小麦雪疫病[57]。Koushi等[58]发明了一种含有枞酸的农作物杀虫剂,对稻瘟病效果显著,而且毒性低,对作物无毒害。此外,枞酸还可以作为有机磷杀虫剂的稳定剂[59]。
2.4 枞酸在日用化学品上的应用
利用枞酸的活性基团(羧基和共轭双键),可以合成一系列与脂肪醇、脂肪酸、脂肪胺类表面活性剂结构相似但又独具特色的日用化学品,可作为洗涤剂、抗泡沫剂、乳化剂、破乳剂、颜料分散剂等[60-65],而且因为枞酸是天然产物的提取物,通过它合成的表面活性剂一般具有良好的生态性能,符合化工合成原料绿色化要求。有专利报道枞酸的酯类衍生物在软饮料的制备中可以作软饮料的稳定剂[66-67]。枞酸作为护发素的一种有效成分具有优良的保湿效果,能有效改善头发的干枯状况,增加头发的光泽,使头发光滑柔顺[68-69]。枞酸甘油三酯用在化妆品中对皮肤无刺激作用[70],枞酸胍盐可作为羊毛纺织品的防蛀剂[71]。
2.5 枞酸在其他方面的应用
枞酸除了在医药、农业、日用化学品等方面的应用之外,在其他行业也有广泛应用。宋湛谦等[72]通过异构的方法消除枞酸的共轭双键结构,并经过局部酯化工艺和复配工艺制备出满足电子工业要求的高稳定松香树脂。一份美国专利[73]报道了一种以枞酸及其衍生物为主要成分的成膜剂,这种成膜剂形成的感光保护膜适用于半导体集成电路产品。利用枞酸共轭双键的Diels-Alder反应合成各种树脂,广泛应用于高分子材料中[74]。枞酸与马来酸酐的Diels-A lder反应产物具有优良的力学性能和黏着力,适用于钢铁防腐[75]。Atta等[76]将枞酸的Diels-A lder反应产物与二乙醇胺反应制得可用于钢铁防腐的四官能团环氧树脂。枞酸还可以用于制备各种固化剂[77-78],Liu等[79]合成了枞酸基生物固化剂,可作为石化基固化剂的替代品,而且在合成方面,枞酸基固化剂更简单、环境更友好、反应器和催化剂更容易获得。Liu等[80]还发现枞酸基环氧树脂固化剂比偏苯三酸酐衍生物环氧树脂固化剂拥有更高的拉伸强度、黏弹性和更高的玻璃转化温度,以含酰亚胺基的松香二酸衍生物作为固化剂比石油基的类似物有更高的热稳定性。此外,枞酸衍生物还可以作为蔬果保鲜的涂膜剂[81]。
3 结 语
松香是含有多种树脂酸的混合物,由于分离纯化困难,长期以来是以混合物的形式应用于各种工业领域,其用途和价值受到了一定的限制,如同刚开采出来的石油一样,没有经过分离纯化,其用途和价值非常有限。目前,枞酸的应用研究已经受到人们的广泛关注,在诸多领域显示出了很好的应用前景。因此,将松香所含的多种树脂酸逐一分离提纯,并以之作为化学合成的原料,充分利用枞酸的多个手性中心,合成一系列具有生物活性的物质和手性药物,促进高附加值枞酸下游产品的开发,是枞酸应用开发的重点。
[1] 张樟德.中国松香工业的现状及发展对策[J].北京林业大学学报,2008,30(3):147-152.
[2] 刘国杰.可再生天然树脂——松香在涂料中应用前景探讨[J].中国涂料,2013,28(1):18-23.
[3] 王琳琳,李丽明,陈小鹏,等.Pd/C上松香催化歧化反应集总动力学[J].化工学报,2007,58(2):371-377.
[4] 安鑫南.林产化学工艺学[M].北京:中国林业出版社,2002:34.
[5] Ellingson E O.On abietic acid and some of its salts[J].Journal of the American Chemical Society,1914,36(2):325-335.
[6] Gubelmann I,Henke C O,Lee H R.Process of preparing abietic acid:US,1846639 (A)[P].1932-2-23.
[7] Steele L L.Abietic acid and certain metal abietates1[J].Journal of the American Chemical Society,1922,44(6):1333-1341.
[8] Palkin S,Harris T H.The preparation of l-abietic acid (Schulz) and properties of some of its salts[J].Journal of the American Chemical Society,1934,56(9):1935-1937.
[9] Cox R F B.Preparation of abietic acid[P].US,2296503(A),1942-09-22.
[10] 王文军,戴乾圜.(-)-7,13-二烯-18-枞酸的提取与纯化及其结构鉴定[J].北京工业大学学报,2000,26(4):77-79.
[11] Harris G C,Sanderson T F.Resin acids.I.An improved method of isolation of resin acids;the isolation of a new abietic-type acid,neoabietic acid[J].Journal of the American Chemical Society,1948,70(1):334-339.
[12] 韩春蕊,宋湛谦,商士斌.提纯枞酸的新方法[J].林产化学与工业,2007,27(4):42-46.
[13] 姚兴东,聂园梅,蓝丽红,等.一种枞酸的制备方法:中国,101020630A,[P].2007-8-22.
[14] 高艺美,廖晨伊,韦小杰,等.松香树脂酸异构化反应研究[J].化学研究与应用,2009,21(11):1533-1538.
[15] 高艺美,廖晨伊,韦小杰,等.超声波强化胺盐法单离枞酸的研究[J].高校化学工程学报,2009,23(4):725-728.
[16] 刘红军,周永红.一种枞酸的制备方法:中国,101219949A[P].2008-7-16.
[17] Jin Z M,Pan Y J,Liu J G,et al.Separation of rosin acids by molecular recognition:Crystal structure of the complex of neoabietic acid w ith 2-am ino-6-methyl-pyridine[J].Journal of Chemical Crystallography,2000,30(3):195-198.
[18] Osete-Cortina L,Doménech-Carbó M T,Mateo-Castro R,et al.Identification of diterpenes in canvas painting varnishes by gas chromatography-mass spectrometry w ith combined derivatisation[J].Journal of Chromatography A,2004,1024(1-2):187-194.
[19] M cMartin D W,Headley J V,Winkler M,et al.Evaluation of liquid chromatography–negative ion electrospray mass spectrometry for the determination of selected resin acids in river water[J].Journal of Chromatography A,2002,952:289-293.
[20] Lee B L,Koh D,Ong H Y,et al.High-performance liquid chromatographic determ ination of dehydroabietic and abietic acids in traditional Chinese medications[J].Journal of Chromatography A,1997,763:221-226.
[21] Luong J H T,Rigby T,Male K B,et al.Separation of resin acids using cyclodextrin-modified capillary electrophoresis[J].Electrophoresis,1999,20(7):1546-1554.
[22] A lvarez-Manzaneda Roldán E J,Chahboun R,Bentaleb F,et al.First enantiospecific synthesis of antileishmanial 12-deoxyroyleanone from abietic acid[J].Synlett,2004(15):2701-2704.
[23] Alvarez-Manzaneda E,Chahboun R,Bentaleb F,et al.Regioselective routes towards 14-hydroxyabietane diterpenes.A formal synthesis of immunosuppressant (-)-triptolide from (+)-abietic acid[J].Tetrahedron,2007,63(45):11204-11212.
[24] González M A,Correa-Royero J,Agudelo L,et al.Synthesis and biological evaluation of abietic acid derivatives[J].European Journal of Medicinal Chemistry,2009,44(6):2468-2472.
[25] Gigante B,Santos C,Silva A M,et al.Catechols from abietic acid:Synthesis and evaluation as bioactive compounds[J].Bioorganic & Medicinal Chemistry,2003,11(8):1631-1638.
[26] Berettoni M,Chiara G D,Iacoangeli T,et al.A formal total synthesis of (+)-methyl trachyloban-18-oate and (+)-methyl 16-oxo-17-norkauran-18-oate:regio- and diastereoselective preparation of methyl (13S)-13-hydroxyisoatisiren-18-oate from (-)-abietic acid[J].Helvetica Chimica Acta,1996,79(7):2035-2041.
[27] Spessard G O,Matthews D R,Nelson M D,et al.Phytoalexin-like activity of abietic acid and its derivatives[J].Journal of Agricultural and Food Chemistry,1995,43(6):1690-1694.
[28] Muellner U,Huefner A,Haslinger E.Behaviour of terpene peroxides from abietic acid in the presence of heme and non-heme iron (Ⅱ)[J].Tetrahedron,2000,56:3893-3899.
[29] Tagat J R,M cCombie S W,Puar M S.A scalemic synthesis of the scopadulcic acid skeleton.Ⅰ:An efficient γ-alkylation at C-9 in abietane framework and subsequent aidol reaction[J].Tetrahedron Letters,1996,37(47):8459-8462.
[30] Santos C D,Zukerman-Schpector J,Imamura P M.Chem ical transformation of abietic acid to new chiral derivatives[J].Journal of the Brazilian Chemical Society,2003,14:998-1004.
[31] Haslinger E,Hüfner A.New chiral synthons from abietic acid:Oxidation of the C-ring and degradation of the carbon skeleton[J].Monatshefte für Chemie-Chemical Monthly,1995,126(10):1109-1123.
[32] Santos C D,Rosso C R S D,Imamura P M.Synthesis of new chiral synthons through regioselective ozonolysis of methyl abietate[J].Synthetic Communications,1999,29(11):1903-1910.
[33] Presser A,Haslinger E,Weis R,et al.Synthetic transformations of abietic acid Ⅳ[1].B- and C-ring oxidation[J].Monatshefte für Chemie-Chemical Monthly,1998,129(8):921-930.
[34] Presser A,Pötschger I,Haslinger E,et al.Synthetic transformations of abietic acid V a:Structure modification and ozonization[J].Monatshefte für Chemie-Chemical Monthly,2002,133(3):231-239.
[35] Winterstein A.Tetrahydro trihydroxy-abietic acid:US,2370900(A)[P].1945-03-06.
[36] Roche Products Ltd.Process for the manufacture of trihydroxy-abietic acid:GB,562014(A)[P].1944-06-14.
[37] Hoffmann La Roche.Process for the manufacture of therapeutically valuable derivatives of abietic acid:GB 553190(A),[P].1943-05-11.
[38] Leo S.Alkali metal acid salts of oxidation products of abietic acid:US,2357613[P].1944-09-05.
[39] Hiroshi M,Katsuya O,Hiroshi E,et al.Abietam ide derivatives,their production and use: US,4210671(A)[P].,1980-07-01.
[40] Shulman M J.Methods of treating burns using colophony containing preparation:US,3943248(A)[P].1976-03-09.
[41] Andre L.Use of abietic acid as a film-form ing product to be used on wounds and burns:FR,2557799(A1)[P].1985-07-12.
[42] Yokogawa Y,Tsutsum i Y.Composition for oral cavity:JP,02138116[P].1990-05-28.
[43] Yokogawa Y,Tsutsum i Y.Skin drug for external use:JP,2188513(A) [P].1990-07-24.
[44] Lin C H,Chuang H S.Use of abietic acid and derivatives thereof for inhibiting cancer:US,7015248B2[P].2006-03-21.
[45] 米彩峰,石会丽,李富贤.一种治疗银屑病的植物药及其原料药松香酸的制备工艺: 中国,1883519(A)[P].2006-12-27.
[46] Nobuyuki T,Teruo K,Tsuyoshi G,et al.Abietic acid activates peroxisome proliferator-activated receptor-γ( PPARγ) in RAW 264.7 macrophages and 3T3-L1 adipocytes to regulate gene expression involved in inflammation and lipid metabolism[J].FEBS Lett.,2003,550:190-194.
[47] Fernández M A,Tornos M P,García M D,et al.Anti-inflammatory activity of abietic acid,a diterpene isolated from pimenta racemosa var.grissea[J].Journal of Pharmacy and Pharmacology,2001,53(6):867-872.
[48] Ulusu N N,Ercil D,Sakar M,et al.Abietic acid inhibits lipoxygenase activity[J].Phytotherapy Research,2002,16(1):88-90.
[49] Pathak Y V,Dorle A K.Study of rosin and rosin derivatives as coating materials for controlled release of drug[J].Journal of Controlled Release,1987,5(1):63-68.
[50] Puranik P K,Dorle A K.Study of abietic acid glycerol derivatives as m icroencapsulating materials[J].Journal of Microencapsulation,1991,8(2):247-252.
[51] Puranik P K,Manekar N C,Dorle A K.Preparation and evaluation of abietic acid m icrocapsules by a solvent evaporation technique[J].Journal of Microencapsulation,1992,9(4):425-435.
[52] Ramani C C,Puranik P K,Dorle A K.Study of diabietic acid as matrix form ing material[J].International Journal of Pharmaceutics,1996,137:11-19.
[53] Barabde U V,Fulzele S V,Satturwar P M,et al.Film coating and biodegradation studies of new rosin derivative[J].Reactive and Functional Polymers,2005,62(3):241-248.
[54] Nande V S,Barabde U V,Morkhade D M,et al.Synthesis and characterization of PEGylated derivatives of rosin for sustained drug delivery[J].Reactive and Functional Polymers,2006,66(11):1373-1383.
[55] Fulzele S V,Satturwar P M,Dorle A K.Novel biopolymers as implant matrix for the delivery of ciprofloxacin:Biocompatibility,degradation, and in vitro antibiotic release[J].Journal of Pharmaceutical Sciences,2007,96(1):132-144.
[56] 王琳琳,陈小鹏,刘幽燕,等.松香松香树脂酸的单离与应用[J].化工进展,2005,24(11):1301-1305.
[57] Tohoku K,Kagakukogyo K.Compositions pour usages agricoles:FR,1381645(A)[P].,1964-12-14.
[58] Koushi M,Fujii R,Ishihara K,et al.Agricultural fungicide: JP,57088102(A)[P].,1982-06-01.
[59] Chem I H D,Hans-Herbert K,Ing D M D,et al.Stabilised solid-substance formulations of dimethoate:DE,3821790(A1)[P].1990-01-11.
[60] 王延,宋湛谦.松香类表面活性剂的开发及应用[J].表面活性剂工业,1994 (2):7-17.
[61] 宋湛谦.新型松香类表面活性剂系列产品[J].精细与专用化学品,2000(11):19-20,14.
[62] 周永红,宋湛谦.松香的精细化工利用(Ⅳ)——松香类表面活性剂的合成与应用[J].林产化工通讯,2003,37(1):28-32.
[63] 宋湛谦,周永红.利用生物质资源,发展表面活性剂[J].精细与专用化学品,2005,13(20):1-3,13.
[64] 连锦花,孙果宋,黄科林.松香系列表面活性剂现状与发展[J].化工技术与开发,2009,38(5):28-32,15.
[65] Carnes J J,Booth W T.Ethenoxyn-monoethanolam ides of abietic acid-containing compounds:CA,547480(A)[P].1957-10-15.
[66] Schwartz H A,Moldenhauer O L,Greenman S M.Soft drink stabilizer:US,3857978(A)[P].1974-12-31.
[67] Polak Frutal Works.Cloud emulsions containing hydrogenated abietic acid and esters for use in beverages:GB,1537160(A)[P].1978-12-29.
[68] M iyamoto N,Ikeuchi T.Hair cosmetic composition:JP,60001112(A)[P].1985-01-07.
[69] Joerg K,Hermann H,Detlef H,et al.Hair conditioner for improving the dry combability of fine hair:DE,4438115(A1)[P].1996-05-02.
[70] Sato K.Pigment surface-treated w ith abietic ester,and cosmetic containing same:JP,2000095966(A),[P].2000-04-04.
[71] Jayne D W.Rosin and abietic acid salts of a guanidine as a mothproofer:US, 2347688(A)[P].1944-05-02.
[72] 宋湛谦,王振洪,唐元达,等.电子与胶粘剂工业高稳定专用松香树脂[J].精细与专用化学品,2000,8(18):21-22.
[73] Katsuaki K,Maki K,Yoshio Y,et al.Process for forming photoresist pattern using contrast enhancement layer w ith abietic acid:US,4889795[P].1989-12-26.
[74] 孔振武,夏建陵,黄焕.松香的精细化工利用(Ⅱ)——松香在高分子材料中的应用[J].林产化工通讯,2002,(5):21-28.
[75] Atta A M,Mansour R,Abdou M I,et al.Epoxy resins from rosin acids:Synthesis and characterization[J].Polymers for Advanced Technologies,2004,15(9):514-522.
[76] Atta A M,Mansour R,Abdou M I,et al.Synthesis and characterization of tetra-functional epoxy resins from rosin[J].Journal of Polymer Research,2005,12(2):127-138.
[77] Wang H H,Liu B,Liu X Q,et al.Synthesis of biobased epoxy and curing agents using rosin and the study of cure reactions[J].Green Chemistry,2008,10(11):1190-1196.
[78] Wang H H,Liu X Q,Liu B,et al.Synthesis of rosin-based flexible anhydride-type curing agents and properties of the cured epoxy[J].Polymer International,2009,58(12):1435-1441.
[79] Liu X Q,Xin W B,Zhang J W.Rosin-based acid anhydrides as alternatives to petrochem ical curing agents[J].Green Chemistry,2009,11(7):1018-1025.
[80] Liu X Q,Xin W B,Zhang J W.Rosin-derived im ide-diacids as epoxy curing agents for enhanced performance[J].Bioresource Technology,2010,101:2520-2524.
[81] A lberto S.Combinations of abietic acid esters w ith one or more terpenes and thereof for coating fruit or vegetables:US,2010092631(A1)[P].2010-04-15.

