香樟叶片中氟化物监测方法比较
余益军,戴玄吏,孙佳,陈桥,何沁华,杨雨佳,王强
(1. 常州市环境监测中心,江苏 常州 213001;2. 江苏理工学院,江苏 常州 213001)
大气氟化物是人们关注的污染物之一,其含量升高也促使植物对氟化物的吸收增强,从而成为了植物叶片中氟的最主要来源。植物在整个生长季节都在吸收和积累大气中的氟化物,主要积累在叶片中,几乎不向其他器官转移[1]。叶片含氟量与大气氟化物浓度显著相关,用以评价大气氟化物污染水平具有很高的灵敏度和可靠性[2-4],利用植物叶片氟化物含量及其叶片受害症状反映大气氟化物污染程度的研究方法引起了大量关注[5]。这种生物监测方法可以有效补充滤膜采样/石灰滤纸采样-氟离子选择电极法等标准方法在采样时间、生物有效性方面的不足[6-7]。
植物叶片中氟化物监测前处理方法主要有灰化、酸浸提、酸碱浸提等。江苏省内环境监测机构多采用HClO4浸提,该方法曾列入《生物监测技术规范》(征求意见稿),但至今未正式颁布;浙江省颁布的地方标准中规定采用HNO3-KOH浸提测定桑叶氟化物[8]。可见植物叶片中氟化物监测工作开展虽广泛,但是无统一方法可循。系统比较这些方法的差异,对推进叶片中氟化物监测方法标准化十分必要。笔者以香樟叶片中氟化物的测定为例,初步探讨了几种常用浸提方法及检测手段的差异。
1 材料与方法
1.1 仪器与试剂
F-1氟离子选择性电极和饱和甘汞电极(江苏江分电分析仪器有限公司);离子色谱仪(瑞士万通881/863C);磁力搅拌器;超声波清洗器。
硝酸钾、柠檬酸钠、氢氧化钾、浓硝酸、高氯酸,以上试剂均为分析纯。
1.2 样品预处理
新鲜样品洗净后自然风干,在60~80 ℃下干燥至恒重,剔除叶柄及粗大的叶脉,粉碎,过60目筛孔,充分混匀后用四分法取样装入聚乙烯瓶中,置于干燥器内保存。
1.3 实验方法
准确称取约0.50 g样品,分别采用以下方法浸提:① HNO3-KOH浸提,主要参考《蚕桑区桑叶氟化物含量控制标准》(DB 33/392-2003)附录方法,即在超声或磁力搅拌辅助下,先用0.05 mol/L硝酸浸提20 min,再以0.10 mol/L KOH浸提20 min,然后依次加入0.2 mol/L硝酸和0.4 mol/L柠檬酸钠溶液,最后浸提5 min后测定;② HClO4浸提,用0.1 mol/L HClO4浸提样品,为便于比较,超声辅助浸提方式同上;③ 超纯水浸提,在相同间歇方式下以超纯水超声浸提45 min,浸提液加入缓冲液后以电极法测定。如以离子色谱法测定,部分浸提液经离心后取上清液,其余部分则加入缓冲液供电极法测定。
1.4 离子色谱分析条件
采用Metrosep A Supp 5 150/4.0分离柱、Metersep A 4/5 保护柱,流动相为Na2CO3/NaHCO3(3.2/1.0 mmol/L),流速0.7 mL/min,进样20 μL,电导检测器。
2 结果与讨论
2.1 磁力搅拌与超声的效果比较
普通磁力搅拌相对超声处理效率较低,为提高样品处理通量,在相同环境条件下,以HNO3-KOH浸提为例,比较磁力搅拌和超声在相同间歇方式处理45 min的差异,以氟离子选择电极标准曲线法测定。
结果表明,搅拌和超声测得某一实验样品氟化物含量分别为22.4±1.1 μg/g(n=3)和21.7±0.7 mg/kg(n=3),单因素方差分析显示,两结果间无显著性差异,故后续实验中均选用超声方式进行。以超声取代搅拌浸提叶片中氟化物也有较多案例[9-10]。
2.2 不同浸提-电极测定的比较
2.2.1 校正曲线比较
在相同温度(27 ℃)和搅拌速度下,分别在不同日期制作3种浸提基质的E-lgρ(F-)校正曲线,比较其差异,结果如图1所示。E-lgρ(F-)曲线线性关系均良好(R2>0.993),但重合性有一定差异,HNO3-KOH浸提曲线重合性最好,HClO4浸提漂移相对较大,这应与氟离子选择电极的特点相关,一般认为氟离子选择电极最适宜的pH值范围是5.0~5.5[11]。
E-lgρ(F-)曲线斜率表示F-活度每变化10倍所引起的电位变化值, Nurst方程可以计算其理论值,而实得斜率与理论值的比值称为斜率转化系数,该系数过低说明电极性能较差,测定误差较大。在该实验条件下,斜率理论值应为-59.5 mV,实验用电极在HNO3-KOH、HClO4和纯水3种基质的实测斜率绝对值分别为55.9~63.2(59.0,均值,下同)、45.3~54.6(48.9)、54.0~59.8(56.1),可见HClO4基质的转化系数相对最低,波动也大。
为提高可比性,在HClO4浸提液中加入碱性柠檬酸钠-硝酸钾缓冲液,调节pH值和总离子强度与另外两种基质一致,结果如图1所示,校正曲线之间重叠性明显改善,斜率绝对值为54.0~56.4(55.2),与其他2种基质的结果相似。
2.2.2 电极法的定量方法比较
校正曲线法与标准加入法是氟离子选择电极分析中2种常用的定量方法,该实验比较了它们测定同一个样品的差异。
系统智能化,客户资源数字化已是酒店未来发展的必然趋势,在客户管理系统的科学化、智能化之后,设立各品牌酒店间的客户资源共享,通过信息系统对分享资源管理后的查询和数据开采功能管理客户,提供具有针对性的个性服务,也将成为酒店业未来维护、提高客户的忠实度、酒店的美誉度的必然需要,酒店的消费者更应是酒店品牌的推广者。
校正曲线法测得该样品植物叶片中氟化物的含量相对标准偏差为8.9%~11.4%,标准加入法的则为0.5%~9.8%。标准加入法中采用两个水平电位差(ΔE1和ΔE2)分别定量,结果显示两者结果偏差小于5.5%;校正曲线法结果与标准加入法结果均值相比,以HClO4基质相对偏差最大(9.1%),超纯水和HNO3-KOH浸提相对偏差分别为3.1%和4.7%。具体结果见表1,括号内数据为相对标准偏差。
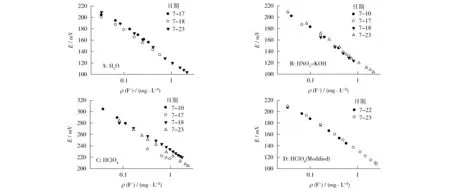
图1 几种浸提基质的标准曲线

表1 标准曲线法和标准加入法定量同一样品的结果*
*n=5。
标准加入法基质性质基本保持不变,准确度更高,从实验看标准曲线法与标准加入法结果基本可比,仅HClO4浸提结果偏差接近10%,标准加入法两水平电位差定量结果高度吻合,因此采用标准加入法进行定量可靠度高。
2.2.3 浸提时间影响
为考察浸提效果随时间变化,45 min超声浸提后密闭隔夜静置,临测定前再次间歇超声45 min,以标准加入法定量观察与仅45 min超声浸提的差异。结果表明,隔夜静置2次超声超纯水、HClO4、HNO3-KOH浸提结果分别为仅浸提45 min的91%,119%和106%。王娅等[10]用超纯水超声波浸提茶叶中氟化物实验表明,浸提30 min已基本稳定,因此间歇超声45 min已基本满足要求。
2.2.4 浸出方法结果差异
基于同一样品的比较实验表明,浸出方法差异带来很大结果差异,定量方法差异同时也有影响。为相对全面考察不同浸出方式和定量方法效果差异,采用3种基质浸提7份不同样品,分别以校准曲线法和标准加入法定量,其中HClO4浸出液分别以不添加缓冲液和添加碱性缓冲液两种方式测定(修正HClO4法)。
以标准加入法定量结果比较浸出差异(图2)。
就均值而言,修正HClO4、超纯水、HNO3-KOH法测定此7份样品相对HClO4法结果均值分别为0.92,0.83和1.06。从具体样本看,部分为HClO4浸提结果最高,更多则以HNO3-KOH浸提结果最高。不同处理方法之间结果相关性好(表2)。
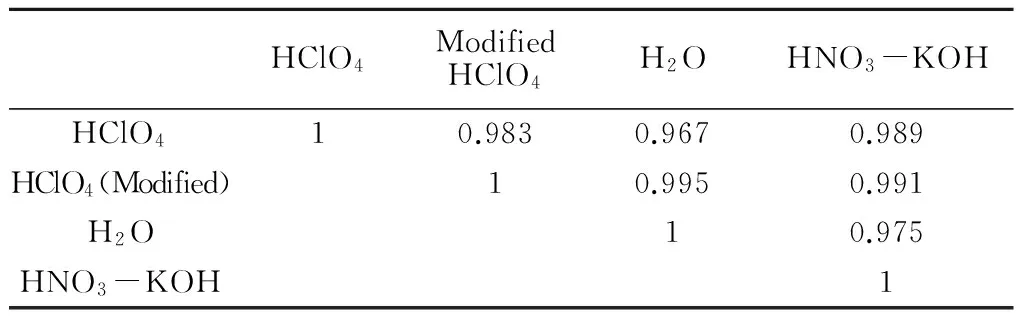
表2 不同浸提基质结果相关系数*
*n=7。
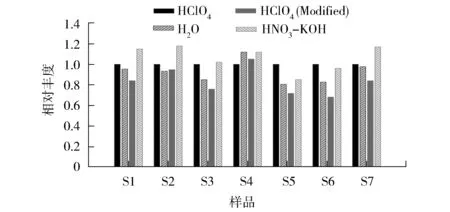
图2 不同基质浸提不同样品的标准加入法测定结果差异
2.3 离子色谱测定与电极测定的差异
以超纯水间歇超声浸提方式处理,部分浸提液经离心静置后取上清液以离子色谱法测定,另一部分则加入缓冲液后以电极法测定,结果表明结果差异极大。离子色谱法(图3)分别测定某样品浸提45 min和隔夜静置两次超声处理,氟化物含量为322±14.7 μg/g(n=5)和419±9.2 μg/g(n=2),远高于选择电极标准加入法测定值(13.1 μg/g),其他样品结果差异亦然。从电极法测定结果看,纯水浸提量明显低于其他方式,这与陈练等[12]采用超纯水浸提-离子色谱法测定茶叶中氟化物、溴化物结论基本一致。由于测定的为同一份浸提液,可以肯定这种结果差异与最终测定仪器有关,原因待查。
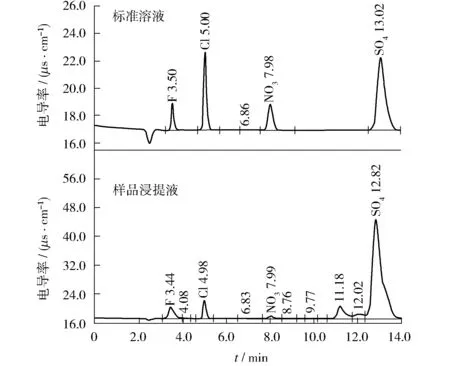
图3 离子色谱法分析樟树叶片超纯水浸提液色谱
3 结论与建议
文中初步比较了HClO4、超纯水、HNO3-KOH对香樟叶片中氟化物浸提效果的区别,以及氟离子选择电极法定量方式之间的差异,并尝试了离子色谱测定。结果表明:
(1)间歇超声45 min,浸提程度基本满足测定要求;氟离子选择电极标准加入法定量结果更可信。(2)HClO4基质校准曲线重合性、斜率转化系数较差,但浸提效果较好,操作简单,仅需加入HClO4一种试剂;HNO3-KOH浸提效果与HClO4相当或更高,校准曲线之间重合性、斜率转化率好,精密度高,但操作相对复杂,需4次分别加入不同试剂;超纯水浸提平均效果是前两者的80%左右,氟化物含量越低的样品浸提效率越与酸浸提相近。(3)浸提过程不变,在HClO4浸提液中加入碱性缓冲溶液,控制pH值与总离子强度与另外2种方法一致,可改善校准曲线性能,结果与原法基本可比。(4)采用离子色谱法测定过滤后叶片的超纯水浸提液,结果与氟离子选择电极差异甚大,原因待查。(5)由于浸提方式和定量方法都对测定结果有较大影响,建议出台叶片中氟化物测定的参考方法或标准方法,同时研制此类植物叶片的标准样品。
[1] 缪昆,王雁,彭镇华.植物对氟化物的吸收积累及抗性作用[J].东北林业大学学报,2002,30(3):100-106.
[2] 郑海,肖春,张勇,等. 利用植物含氟量监测大气氟化物污染的探讨[J]. 内蒙古水利,2011(4):40-41.
[3] 贾陈忠,秦巧燕,侯延军,等. 荆州大气氟污染与植物叶片含氟量监测分析[J]. 环境工程,2006,22(3):64-68.
[4] 张德强,郁梦德,林志红,等.污染区域大气环境质量生物监测的数学模式[J] . 热带亚热带植物学报,2003,11(4):393-399.
[5] 李寒娥,王志云,胡羡聪,等. 佛山市几种绿地植物氟化物时空累积特征[J]. 生态学杂志,2007,26(10):1600-1605.
[6] HJ 480-2009 环境空气 氟化物的测定 滤膜采样氟离子选择电极法[S].
[7] HJ 481-2009 环境空气 氟化物的测定 石灰滤纸采样氟离子选择电极法[S].
[8] DB 33/392-2003 蚕桑区桑叶氟化物含量控制标准[S].
[9] 范美容,黄懿.高氯酸浸提氟离子电极法测定氟化物[J]. 企业技术开发,2000(2):6-7.
[10] 王娅,陈伯涛,姚福荣,等.超声波萃取-离子选择电极法测定茶叶中氟含量[J]. 安徽农业科学,2012,40(3):1445-1447.
[11] 武汉大学化学系. 仪器分析[M]. 北京:高等教育出版社,2001:284.
[12] 陈练,陈新焕,罗丽容,等.离子色谱法同时测定茶叶中氟化物、溴化物[J]. 食品工业,2012,33(11):158-160.

