胶原贴敷料联合他扎罗汀凝胶治疗痤疮60例效果观察
符 梅,傅琳玲,刘安齐,丁 琦(南通大学附属医院皮肤性病科,江苏226001)
胶原贴敷料联合他扎罗汀凝胶治疗痤疮60例效果观察
符 梅,傅琳玲,刘安齐,丁 琦
(南通大学附属医院皮肤性病科,江苏226001)
目的:探讨胶原贴敷料联合0.05%他扎罗汀凝胶治疗Ⅰ、Ⅱ级痤疮的效果及不良反应。方法:将患者随机分为观察组和对照组各60例。观察组用胶原贴敷料、0.05%他扎罗汀凝胶,对照组单用0.05%他扎罗汀凝胶。结果:观察组有效53例(88.3%),对照组有效42例(70.0%),两组有效率比较差异有统计学意义(χ2=6.114,P<0.05)。观察组无不良反应,对照组出现皮肤轻度潮红,烧灼感,少量脱屑5例。结论:胶原贴敷料联合0.05%他扎罗汀凝胶治疗Ⅰ、Ⅱ级痤疮疗效肯定。
痤疮;胶原贴;他扎罗汀
痤疮是好发于青春期男女的毛囊皮脂腺慢性炎症性疾病。青春期雄性激素水平明显升高,使皮脂腺细胞的增殖和脂类的合成增加。由于毛囊和皮脂腺导管异常角化,使皮脂腺排泄障碍,形成粉刺;痤疮棒状杆菌引起炎症性皮损[1]。因生痤疮后的色素沉着、永久的瘢痕影响美观,因而越来越引起青年患者的重视。我科于2011年5月—2013年5月应用胶原贴敷料联合外用0.05%他扎罗汀凝胶治疗Ⅰ、Ⅱ
级痤疮60例取得了满意疗效,现报告如下。
1 资料与方法
1.1 一般资料 门诊就诊Ⅰ、Ⅱ级痤疮患者120例,年龄18~28岁,随机分为观察组和对照组各60例,观察组男39例,女21例,平均年龄23±5岁,病程8个月~8年,平均48±4个月。对照组男38例,女22例,平均年龄23.5±5岁,病程9个月~8年,平均47±5个月。皮损表现为∶Ⅰ级痤疮为仅有粉刺,Ⅱ级痤疮为除粉刺外还有炎症性丘疹。6周内无口服及外用治疗痤疮药物史,两组患者性别、病程及皮损的总评分具有可比性。
1.2 方法 (1)治疗方法∶观察组用普通洗面奶及温水洁面后,予胶原贴敷料(生产许可证号∶粤药管械生产许20030745号)外敷面部30~40分钟/次,隔日1次,3周1个疗程,联合外用0.05%他扎罗汀凝胶(重庆华邦制药股份有限公司)每晚1次。对照组单用0.05%他扎罗汀凝胶。两组患者均连续治疗2个疗程,并于治疗后第3、6、9周各随访1次,观察其治疗效果及不良反应。(2)疗效指标及评分标准∶对患者治疗前后皮损进行分类计数。根据粉刺、炎性丘疹、色素沉着数目,计算疗效指数,并根据评分标准进行评分,疗效指数=(治疗前皮损数-治疗后皮损数)/治疗前皮损数×100%。痊愈∶皮损基本消退,基本无色素沉着,疗效指数≥90%;显效∶60%≤疗效指数<90%,有少量色素沉着;好转∶20%≤疗效指数<60%,有色素沉着;无效∶疗效指数<20%。有效率以痊愈加显效计算。
1.3 统计学处理 采用SPSS13.0统计学软件进行数据处理,计数资料组间差异性比较采用χ2检验,P<0.05为差异有统计学意义。
2 结 果
2.1 治疗结果 两组病例均完成6周治疗,完成疗程后,观察组有效率高于对照组,差异有统计学意义(χ2=6.114,P<0.05),见表1。
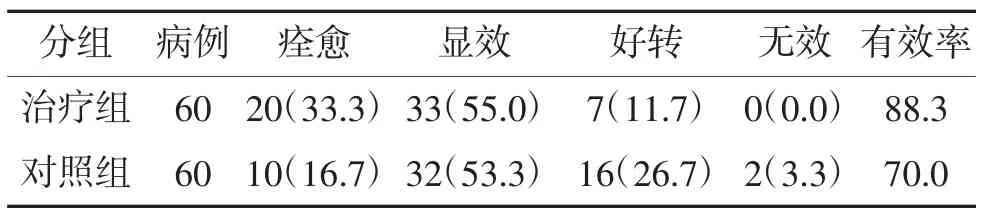
表1 两组治疗效果比较 例(%)
2.2 不良反应 观察组无不良反应,对照组出现皮肤轻度潮红,烧灼感,少量脱屑5例。
3 讨 论
胶原蛋白是由成纤维细胞合成的一种生物性高分子物质,具有维持皮肤形态结构和修复的作用。胶原贴作用于痤疮发病的多个环节,能溶解和软化角质层,防止过度角化,利于皮脂排出[2]。其pH4.5~5.5,对细菌有直接的抑制和杀灭作用;能修复毛囊壁的损伤,减少毛囊壁的破损,防治游离脂肪酸刺激毛囊壁引起炎症。能吸附皮肤表面多余的油脂,对轻中度痤疮后的色素沉着、早期浅表性瘢痕具有显著疗效[3]。
他扎罗汀为乙炔维A酸。主要能抑制皮脂的过度分泌和毛囊皮脂腺导管壁的角化过度及抗炎作用,对Ⅰ、Ⅱ级痤疮具有较好的治疗作用[4]。偶可引起皮肤烧灼感、潮红及脱屑,对照组中出现类似不良反应5例,观察组患者未见此类不良反应,可能与胶原贴敷料具有保湿和收敛作用,同时有减轻炎症性疼痛和瘙痒作用有关。
本文采用胶原贴敷料联合外用0.05%他扎罗汀,治疗Ⅰ、Ⅱ级痤疮取得了满意的疗效。治疗6周后观察组疗效明显优于对照组(P<0.05)。同时能减轻和预防外用维A酸类制剂引起的不良反应,患者耐受性和依从性好,满意度高,具有良好的临床应用前景。
[1]张学军.皮肤性病学[M].8版.北京:人民卫生出版社,2013∶175-177.
[2]中国医师协会皮肤科医师分会《中国痤疮治疗指南》专家组.中国痤疮治疗指南(讨论稿)[J].临床皮肤科杂志,2008,37(5)∶339-342.
[3]郭建美,孙楠,刘慧贤,等.胶原贴敷料对于面部轻度痤疮的屏障功能作用观察[J].实用皮肤病学杂志,2013,6(5)∶274-276.
[4]华鹏,杨敏.罗红霉素联合他扎罗汀乳膏治疗寻常型痤疮疗效观察[J].广州医药,2012,43(2)∶42-43.
R758.73+3
B
2014-07-21
1006-2440(2014)05-0470-02
——《幸福的拉扎罗》解读

