后路 I 期全脊椎整块切除治疗胸腰椎原发和转移性肿瘤的疗效分析
栗向东 王臻 郭征 李靖 范宏斌 付军 陈国景 石磊
后路 I 期全脊椎整块切除治疗胸腰椎原发和转移性肿瘤的疗效分析
栗向东 王臻 郭征 李靖 范宏斌 付军 陈国景 石磊
目的探讨后路 I 期全脊椎整块切除( total en bloc spondylectomy,TES )治疗胸腰椎原发和转移性肿瘤的疗效。方法回顾性分析 2007 年 1 月至 2012 年 7 月,我科行 TES 的 21 例,男 11 例,女 10 例,年龄 21~66( 平均 47.8 )岁。原发肿瘤 8 例,孤立性转移瘤 13 例。原发肿瘤分别为骨巨细胞瘤 3 例,浆细胞瘤2 例,骨肉瘤、软骨肉瘤及上皮样血管内皮瘤各 1 例;转移性肿瘤原发肿瘤分别为乳腺癌 4 例,肺癌 3 例,肾癌 2 例,甲状腺癌、前列腺癌、膀胱癌和原发灶不明转移性腺癌各 1 例。肿瘤节段分布于 T3~L3,其中胸椎12 例、腰椎 9 例,单一椎体 19 例、多椎体 2 例( 均位于 3 个相邻胸椎 )。根据 Tomita 脊柱肿瘤外科分期进行评估:I 型 5 例、II 型 10 例、III 型 1 例、V 型 2 例、VI 型 3 例。术前均有顽固性腰背痛或神经功能损害。切除椎体的骨缺损用钛网+自体骨或异体骨+钉棒系统进行固定和重建。手术均经后路 I 期完成。结果手术时间 4.0~8.5 h,平均 6.4 h;出血量 1300~11 600 ml,平均 4500 ml。本组 21 例均获 12~80 个月的随访,平均40 个月,术后腰背部局部疼痛均达到缓解。脊髓功能损伤的患者术后 Frankel 分级均有一级以上恢复,和术前Frankel 分级比较,差异有统计学意义( Z=-2.232,P<0.05 )。3 例死亡,平均死亡时间为术后 16 个月,4 例带瘤生存,14 例无瘤存活,总生存率为 85.7%。局部复发 3 例,复发率为 14.3%,复发时间为平均术后 22 个月。本组除 1 例胸腔积液伴肺部感染、1 例气胸伴双肺感染、1 例左侧 L3神经根一过性麻痹外,未出现严重并发症,并发症发生率 14.3%。所有病例均无术中由于大血管或节段血管引起的大出血发生,植骨均完全愈合,无内固定失败或钛网移位。结论后路 I 期 TES 治疗脊柱原发恶性肿瘤、侵袭性良性肿瘤和孤立性转移瘤能有效降低局部复发率,无严重的并发症,是一种有效的手术方式。
脊椎肿瘤;肿瘤转移;胸椎;腰椎;全脊椎整块切除
由于解剖结构的限制,脊柱肿瘤难以做到在肿瘤假包膜外切除,而瘤内刮除或分块切除后有较高的局部复发率,并可导致患者预后不良[1-2]。随着脊柱外科技术的进步和内固定器械的发展,脊柱肿瘤的整块切除成为可能。自 Stener 等[3]首次报道全脊椎整块切除( total en bloc spondylectomy,TES )技术治疗脊柱骨巨细胞瘤后,国外已有较多报道 TES 可以降低脊柱肿瘤的局部复发率、提高生存率且技术上可行。国内近几年虽已开展了 TES 手术,但报道较少。本研究通过回顾性分析 2007 年 1 月至 2012年 7 月我科行后路 I 期 TES 治疗胸腰椎原发和转移性肿瘤的病例,现总结其治疗效果。
资料与方法
一、一般资料
本组行后路 I 期 TES 胸椎及腰椎肿瘤患者21 例,其中男 11 例,女 10 例,年龄 21~66 岁,平均 47.8 岁。所有病例术前均经活检确诊,并行骨扫描排除多发病变。病理诊断:原发肿瘤 8 例,孤立性转移瘤 13 例。原发肿瘤分别为骨巨细胞瘤 3 例,孤立性浆细胞瘤 2 例,骨肉瘤、软骨肉瘤和上皮样血管内皮瘤各 1 例;转移瘤中来自乳腺 4 例,肺部3 例,肾脏 2 例,甲状腺、前列腺、膀胱和原发灶不明转移性腺癌各 1 例。肿瘤节段分布于 T3~L3,其中胸椎 12 例,腰椎 9 例。单一脊椎 19 例,多脊椎 2 例( 均为胸椎相邻 3 个脊椎 )。
二、术前脊柱肿瘤外科分期评估
所有病例术前均根据 Tomita 脊柱肿瘤外科分期进行评估[4]。在本组病例中,16 例为间室内,5 例为间室外,其中 I 型 5 例,II 型 10 例,III 型 1 例,V 型 2 例,VI 型 3 例。
三、后路 I 期 TES 手术方法
手术按照 Tomita 等[5]描述的后路 I 期 TES 方法进行。为减少术中出血,3 例术前行病椎的选择性节段动脉栓塞。患者俯卧位,后路正中切口入路,剥离椎板后首先进行病椎上下椎体的椎弓根内固定置入,然后用 T-saw 锯断病椎的椎弓根,整块切除椎板附件,骨蜡封闭残留椎弓根断端,在硬膜囊周围分离,将突入椎管内的肿瘤在包膜外推开。自侧方结扎切断椎体节段血管,在胸椎切断肋间神经。钝性分离椎体周围组织,并用特制挡板保护好前方的大血管等重要结构和后方的硬膜囊。先行单侧钉棒固定,然后用线锯和骨刀自上下椎间盘或上位椎体下缘及下位椎体上缘切断病椎与脊柱的联系,将病椎沿脊柱纵轴旋转取出。钛网内填充自体肋骨或异体骨后进行前方椎体重建,然后完成后路内固定并适当加压,使硬膜囊处于松弛状态。术后卧床 3~4 天后佩戴支具下地活动。切除的肿瘤标本由有经验的病理医生检查外科边界( 图1 )。
四、辅助治疗
骨肉瘤患者行新辅助化疗和辅助化疗;浆细胞瘤行辅助化疗;上皮样血管内皮瘤行术后放疗;转移瘤患者有 11 例行术后放疗后,其中 9 例行辅助化疗。
五、随访
所有病例术后每 3 个月复查 1 次,评价其术后神经功能,了解患者术后生存、肿瘤复发、并发症情况及手术的局部安全性。神经功能用 Frankel 分级进行评价[6]。
六、统计学方法
采用 SPSS 17.0 统计学软件进行数据分析,检验水准 α=0.05,P<0.05 为差异有统计学意义。
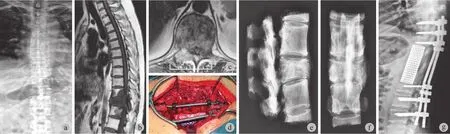
图1 典型病例,女,49 岁,乳腺癌术后 11 年出现 T10~12转移 a:术前 X 线片示 T11椎体病理骨折,椎弓根模糊;b~c:MRI 示肿瘤累及 T10~12三个椎体并椎旁软组织肿块形成;d:术中肿瘤切除重建后;e~f:术后整块切除标本 X 线片;g:术后重建 X 线片Fig.1 A typical case. A 49-year-old woman had metastatic tumors in T10-12at 11 years after the surgery of breast cancer a: The preoperative X-ray showed pathological fractures of T11vertebral body and unclear vertebral pedicle; b-c: The MRI showed 3 vertebral bodies of T10-12were involved and paraspinal soft tissue tumors were found; d: During the operation, the tumors were resected and the spinal column was reconstructed; e-f: The X-ray showed en bloc resection specimens after the operation; g: The X-ray showed reconstruction of the spine column
结 果
本组 21 例均获得后路 I 期 TES,15 例获得广泛边界,其它为边缘性边界。手术过程中无肿瘤的破裂。手术时间 4.0~8.5 h,平均 6.4 h。术中失血量 1300~11 600 ml,平均 4500 ml。所有病例均随访12~80 个月,平均 40 个月。
一、神经功能
所有病例术前都有持续性腰背痛,部分患者有双下肢的瘫痪症状,其中 Frankel 分级 E 级 15 例,D 级 3 例,C 级 1 例,B 级 2 例。
腰背局部疼痛在术后都得到缓解,术前脊髓功能受损的患者术后均有至少一级以上的恢复。术后 Frankel 分级 E 级 20 例,D 级 1 例,与术前Frankel 分级比较,差异有统计学意义( Z= -2.232,P<0.05 )。
二、生存情况
8 例原发瘤中,3 例骨巨细胞瘤、1 例浆细胞瘤、1 例软骨肉瘤和 1 例上皮样血管内皮瘤患者无瘤生存,1 例骨肉瘤由于肿瘤局部复发截瘫,1 例浆细胞瘤出现全身多发病灶死亡;13 例转移瘤中,3 例带瘤生存,2 例因原发病转移死亡,8 例无瘤存活。死亡的 3 例,平均死亡时间为术后 16 个月,总的生存率为 85.7%。
三、复发情况
至最后一次随访,3 例复发,骨巨细胞瘤、骨肉瘤和软骨肉瘤各 1 例,复发率为 14.3%。复发时间为术后 12~36 个月,平均 22 个月。复发病例均再行局部切除,骨巨细胞瘤患者局部再切除后行辅助放疗。
四、并发症
本组未出现严重并发症。术中行神经根切断的13 例,术后无严重的感觉和运动障碍。1 例术后胸腔积液伴肺部感染,1 例右侧气胸伴双肺感染,1 例左侧 L3神经根一过性麻痹,并发症发生率 14.3%。胸腔积液的患者进行了闭式引流,最终获得康复。
五、局部安全性
本组均无术中由于大血管或节段血管引起的大出血发生。所有植骨均获得完全愈合,无内固定失败或钛网移位。
讨 论
根据 Enneking 骨骼肌肉系统肿瘤分期,骨的原发和继发恶性肿瘤须采用广泛切除进行治疗。但相对于四肢来说,脊柱由于其前方毗邻大血管和重要脏器、中央容纳脊髓和其发出的神经根,使得获得广泛的切除边界非常困难。瘤内切除不可避免地造成肿瘤污染和最终导致肿瘤的局部复发,并影响患者的预后[7]。为了减少手术所致的肿瘤播散、降低局部复发率和延长生存时间,近 20 年来发展了不同的脊柱肿瘤整块切除技术:Stener 等[8]和 Roy-Camille 等[9]率先从后路将附件和部分椎弓根切除,然后将位于椎体的肿瘤整块切除,这对于位于椎体的原发性肿瘤获得了肿瘤学意义上合适地切除。Tomita 等[4]采用经椎弓根截骨,将背侧附件整块切除后再将腹侧椎体整块切除。国外许多学者证实脊柱肿瘤的整块切除可以降低局部复发率,Boriani等[10]比较了瘤内切除和整块切除治疗脊柱软骨肉瘤的手术效果,经过至少 5 年的随访,整块切除的12 例中只有 3 例局部复发,而瘤内切除的 10 例全部出现至少 1 次的局部复发,并且 80% 的患者死于肿瘤。对于生物学特性良好、预期生存时间较长的孤立性转移瘤,采用整块切除的方式也能获得良好的局部控制。Sundaresan 等[11]对 80 例孤立性转移瘤患者进行了不同方法的切除,总的局部复发率为 32%,而采用整块切除局部复发率只有 17%,中位生存时间超过 30 个月,有近 20% 的患者生存时间超过 5 年。本组 21 例整块切除术后经平均 40 个月的随访,局部复发率 14.3%,与文献报道相近,表明整块切除技术可有效地降低局部复发率。目前普遍接受的脊柱转移瘤整块切除的适应证为:( 1 )无潜在的可能成为系统性疾病的肿瘤;( 2 )肿瘤的生物学性状较好,有较长的生存期,如肾癌和乳腺癌;( 3 )原发性肿瘤已进行根治性切除;( 4 )转移灶的诊断较原发灶的切除有更长的时间间隔;( 5 )CT、骨扫描或 PET 证实为孤立性转移瘤[6]。
在脊柱肿瘤整块切除大量实践的基础上,Boriani 等[12]提出了指导脊柱肿瘤手术切除的 WBB分期,根据肿瘤在脊椎所处的位置来决定手术的入路和整块切除的方式;而 Tomita 等[4]将四肢肿瘤切除的原则应用于脊柱肿瘤并做了修订,如果肿瘤位于椎体、椎弓根和附件内称为间室内( I~III 型 ),如果肿瘤突破骨皮质进入椎管、椎旁或者椎间隙称为间室外( IV~VII 型 )。肿瘤位于间室内相对容易获得广泛切除,但一旦突破了间室要获得广泛切除就比较困难,需要将邻近的组织一并切除。如肿瘤突入椎管可将硬膜囊一并切除从而获得广泛切除,如果肿瘤包绕了椎体前方的血管,广泛切除是很难实现的。根据 Tomita 脊柱肿瘤的分型,经椎弓根截骨的 TES 的绝对适应证是 Tomita 分期的 III~V 型,I、II、VI 型为相对适应证,而 VII 型为禁忌证。本组病例中最多的是 Tomita II 型,其次是 I 型和VI 型。
脊柱肿瘤手术分期和技术改进的主要目的是获得良好的外科边界。Tomita 等[4]采用经椎弓根截骨进行 TES 后,对切除的标本作了组织学检查和评估,7 例标本除了椎弓根切断处和少数椎管内病灶的外科边界为病灶内以外,其余各个层面均获得边缘或广泛的外科边界。Boriani 等[13]经过对标本的术后放射学和组织学分析发现,运用 WBB 分期进行的 29 例 TES 中,21 例成功获得边缘或广泛的外科边界。Hasegawa 等[14]在 13 例脊柱肿瘤的外科治疗报告中指出,为了获得理想的外科边界,在脊柱肿瘤切除时应该把覆盖于肿瘤表面的部分胸膜或腰肌一并切除。本组 15 例获得广泛切除,其余获得边缘切除。采用 TES 最大的弊端在于受累的脊椎必须分两块切除,往往获得的是边缘切除,并且在椎弓根截骨处容易有肿瘤细胞的污染。Tomita 等[4]报道了在椎弓根处可能存在肿瘤细胞污染的 20 例,平均13 个月随访,无 1 例在截骨处复发;Abe 等[1]报道了 14 例行 TES 方法进行的整块切除中,有 10 例在椎弓根截骨处可能有肿瘤细胞的污染,但没有 1 例在椎弓根截骨处复发。Abdel-Wanis 等[15]的裸鼠体内实验发现,运用 T-saw 进行囊内切割时,接触到的肿瘤细胞较其它器械明显减少,而且线锯上残留的多为肿瘤细胞碎片,其再生能力较弱。因此,在进行肿瘤囊内切除时,T-saw 是一种较为安全的工具。为了减少术中的肿瘤污染,注意在椎板附件切除后及时用骨蜡封闭被切断的椎弓根;另外还可以用蒸馏水及高浓度顺铂( 0.5 g / L )浸泡 2.5 min 的方法来消灭残留的肿瘤细胞[2]。
本研究中,肿瘤侵犯椎旁 5 例中,有 3 例出现局部复发,而肿瘤位于间室内或侵犯硬膜外的16 例无 1 例局部复发。国外也有类似的报道,Abe等[1]报道在 8 例侵犯椎旁的病例中有 2 例局部复发;Sakaura 等[16]报道 4 例肿瘤侵犯椎旁的病例中2 例术后出现局部复发,而 8 例位于间室内或侵犯硬膜外腔的病例肿瘤均未见局部复发。这些报道表明,对于累及椎旁的脊椎肿瘤,可能容易造成肿瘤的残留最终导致肿瘤局部复发,对于这类病例可能不适合行单纯后路 TES。
虽然后路 I 期 TES 创伤较前后路联合小、手术时间短、失血少,但单纯后路 TES 须牺牲节段神经根,行长节段的融合。在 L2以上节段,神经根的切除不至于引起严重的功能障碍,但切断 L3、L4神经根会影响行走功能。L3、L4椎体较大,行后路 TES旋出椎体时易损伤神经根,影响行走功能。另外,由于双侧髂骨的存在,在下腰椎向外显露较为困难。基于上述理由,病变位于 L3以上时可以采用单一后路进行,如病变位于 L3~L5须行前后路联合进行。如果肿瘤突破椎体前缘并累及节段血管,无论肿瘤位于脊柱的哪个节段,均须采用前后路联合的方法进行切除,因为虽然胸膜和腰肌容易分离从而达到边缘切除,但无法将受累的节段血管和肿瘤一并完整切除。
后路 TES 虽然能取得良好的临床效果,但技术要求高,且可能有明显的围手术期并发症。由于手术时间长、围手术期的放疗或化疗的影响,术中出血或术后感染的发生率比常规手术高;其它可能的并发症为椎弓根截骨时硬膜囊和神经根的损伤;在进行椎旁组织分离时可能出现胸膜破裂引起气胸或血胸,或者损伤前方的大动脉和腔静脉引起致命性出血;在进行椎体右侧分离时可能损伤乳糜管引起乳糜漏;节段血管的结扎和硬膜囊周围静脉丛的过度失血可引起脊髓的缺血。为避免并发症,手术操作须小心谨慎。本组病例没有发生伤口愈合和深部感染的问题,但有 2 例术后出现胸腔积液并发气胸、肺部感染,其原因可能在于术中钝性分离椎体旁组织时出现胸膜破裂,手术时间长,创面大,失血多。因此,对于出现胸腔积液的病例及时进行胸腔闭式引流,术中、术后应用抗生素,术后伤口引流管至少保持 3~5 天,预防术后血肿的形成。
总之,经椎弓根截骨 TES 虽然对于大多数病例不是严格的瘤外切除,但对于具有适应证的原发性脊柱恶性肿瘤、侵袭性良性肿瘤和部分孤立性转移瘤病例,采用该术式能够有效地降低局部复发率,在技术熟练时并不引起严重的并发症,是一种较好的手术方式。
[1] Abe E, Kobayashi T, Murai H, et al. Total spondylectomy for primary malignant, aggressive benign, and solitarymetas-tatic bone tumors of the thoracolumbar spine. J Spinal Disord, 2001, 14(3):237-246.
[2] 杨荣利, 郭卫, 汤小东, 等. 后路I期整块全脊椎切除治疗胸椎及腰椎肿瘤初步经验. 中华外科杂志, 2009, 47(24): 1908-1910.
[3] Tomita K, Kawahara N, Baba H, et al. Total en bloc spondylectomy for solitary spinal metastases. Int Orthop, 1994, 18(5): 291-298.
[4] Tomita K, Kawahara N, Baba H, et al. Total en bloc spondylectomy. A new surgical technique for primary malignant vertebral tumors. Spine, 1997, 22(3):324-333.
[5] Tomita K, Toribatake Y, Kawahara N, et al. Total en bloc spondylectomy and circumspinal decompression for solitary spinal metastasis. Paraplegia, 1994, 32(1):36-46.
[6] Frankel HL, Hancock DO, Hyslop G, et al. The value of postural reduction in the initial management of closed injuries of the spine with paraplegia and tetraplegia. Paraplegia, 1969, 7(3):179-192.
[7] Melcher I1, Disch AC, Khodadadyan-Klostermann C, et al. Primary malignant bone tumors and solitary metastases of the thoracolumbar spine: results by management with total en bloc spondylectomy. Eur Spine J, 2007, 16(8):1193-1202.
[8] Stener B. Total spondylectomy in chondrosarcoma arising from the seventh thoracic vertebra. J Bone Joint Surg Br, 1971, 53(2):288-295.
[9] Roy-Camille R, Saillant G, Bisserié M, et al. [Total excision of thoracic vertebrae (author’stransl)]. Rev Chir Orthop Reparatrice Appar Mot, 1981, 67(3):421-430.
[10] Boriani S, De Iure F, Bandiera S, et al. Chondrosarcoma of the mobile spine: report on 22 cases. Spine, 2000, 25(7):804-812.
[11] Sundaresan N, Rothman A, Manhart K. Surgery for solitary metastases of the spine: rationale and results of treatment. Spine, 2002, 27(16):1802-1806.
[12] Boriani S, Weinstein JN, Biagini R. Primary bone tumors of the spine. Terminology and surgical staging. Spine, 1997, 22(9): 1036-1044.
[13] Boriani S, Biagini R, De Iure F, et al. En bloc resections of bone tumors of the thoracolumbar spine. A preliminary report on 29 patients. Spine, 1996, 21(16):1927-1931.
[14] Hasegawa K, Homma T, Hirano T, et al. Margin-free spondylectomy for extended malignant spine tumors: surgical technique and outcome of 13 cases. Spine, 2007, 32(1): 142-148.
[15] Abdel-Wanis Mel-S, Tsuchiya H, Kawahara N, et al. Tumor growth potential after tumoral and instrumental contamination: an in-vivo comparative study of T-saw, Gigli saw, and scalpel. J Orthop Sci, 2001, 6(5):424-429.
[16] Sakaura H, Hosono N, Mukai Y, et al. Outcome of total en bloc spondylectomy for solitary metastasis of the thoracolumbar spine. J Spinal Disord Tech, 2004, 17(4):297-300.
( 本文编辑:代琴 )
An analysis of therapeutic effects of one-stage posterior total en bloc spondylectomy for primary and metastatic tumors of the thoracolumbar spine
LI Xiang-dong, WANG Zhen, GUO Zheng, LI Jing, FAN Hong-bin, FU Jun, CHEN Guo-jing, SHI Lei. Department of Orthopedics, Xijing Hospital, The Fourth Military Medical University, Xi’an, Shaanxi, 710032, PRC
ObjectiveTo evaluate the clinical outcomes of one-stage posterior total en bloc spondylectomy( TES )in the treatment of primary and metastatic tumors of the thoracolumbar spine.MethodsFrom January 2007 to July 2012, 21 patients with primary and metastatic tumors of the thoracolumbar spine underwent TES, whose clinical data were retrospectively analyzed. There were 11 males and 10 females, whose average age was 47.8 years old( range; 21-66 years ). There were 8 cases of primary tumors and 13 cases of solitary metastatic tumors. Among the 8 cases of primary tumors, there were 3 cases of giant cell tumors of bone, 2 cases of plasmacytoma, 1 case of osteosarcoma, 1 case of chondrosarcoma and 1 case of epithelioid hemangioendothelioma. Among the 13 cases of metastatic tumors, there were 4 cases of breast cancer, 3 cases of lung cancer, 2 cases of renal cancer, 1 case of thyroid cancer, 1 case of prostate cancer, 1 case of bladder cancer and 1 case of unknown adenocarcinoma. The tumors were located from T3to L3, including the thoracic vertebra( n=12 )and the lumbar vertebra( n=9 ). The tumors were detected in the single vertebral body in 19 cases and multiple vertebral bodies( 3 adjacent vertebral bodies )in 2 cases. According to Tomita surgical classifcation system, there were 5 cases of type I, 10 cases of type II, 1 case of type III, 2 cases of type V and 3 cases of type VI. All the patients had intractable back pain or neurologic disturbances before the operation. Vertebral bone defects were repaired, and internal fxation and reconstruction were performed with titanium mesh, allograft orautograft and pedical screws. The operation was completed in all patients through the posterior approach at the frst stage.ResultsThe mean operation time was 6.4 hr( range; 4.0-8.5 hr ). The average amount of blood loss was 4500 ml( range; 1300-11 600 ml ). Perioperative complications occurred in 2 cases, including 1 case of pleural effusion and pulmonary infection and 1 case of pneumothorax and bilateral pulmonary infection. All patients were followed up for an average period of 40 months( range; 12-80 months ). Remarkable relief of local back pain was achieved after the surgery. As to the patients with spinal cord injuries, at least a one-grade improvement was obtained after the surgery based on the Frankel scale, when compared with that before the operation. The differences between them were statistically signifcant( Z=-2.232, P<0.05 ). A total of 3 patients died, and the mean death time was at 16 months after the operation. Four patients lived with tumors and 14 patients lived without tumors. The total survival rate was 85.7%. Local recurrence was detected in 3 patients, and the recurrence rate was 14.3%. The mean recurrence time was at the 22nd months after the operation( range; 12-36 months ). No serious complications were noticed, and the complication rate was 14.3%. No uncontrollable bleeding in the great vessels or segmental vessels was found during the operation. All patients obtained bone union, without internal fxation failure or titanium mesh displacement.ConclusionsOnestage posterior TES is an effective surgical method in the treatment of primary malignant tumors, invasive benign tumors and solitary metastatic tumors of the thoracolumbar spine, with the advantages of lower local recurrence rate and no serious complications.
Spinal neoplasms; Neoplasm metastasis; Thoracic vertebrae; Lumbar vertebrae; Total en bloc spondylectomy
10.3969/j.issn.2095-252X.2014.05.004
R738.1
710032 陕西省西安市第四军医大学西京医院骨科
王臻,Email: wangzhen@fmmu.edu.cn
2014-02-25 )

