造纸法再造烟叶工艺过程中多酚类物质的变化
苏 雷,严新龙,张 钰,张大坤
上海烟草集团太仓海烟烟草薄片有限公司,江苏省太仓市港口开发区东方东路19号 215433
烟草中多酚类化合物含量较高,其中绿原酸、莨菪亭和芸香苷是烟草中主要的酚类化合物,且烤烟中多酚类物质含量较白肋烟高[1-3]。由于多酚类化合物是多种香味成分的前体物,因此成为影响烟草品质的重要因素,如2,6-二甲基苯酚具有甜味、丁子香酚具有强烈的芳香气味等[4-5]。一般认为,多酚含量越高烟叶品质越好[6]。但是,一些多酚类化合物如绿原酸的热裂解产物可能会对烟草制品的安全性产生一定的影响,而儿茶酚是一种活性高的辅助致癌物质[7]。目前,关于烟草植物中多酚类物质的存在形态、生理功能及对烟草品质的影响研究较多[8-11],但是关于再造烟叶中多酚类物质的研究鲜见报道。在造纸法再造烟叶的萃取工艺阶段会有大量水溶性物质存在于萃取液中[12],且多酚类物质含有亲水性的羟基。因此,研究了再造烟叶工艺过程中多酚的变化情况,旨在为生产中多酚的调控提供参考。
1 材料与方法
1.1 材料、试剂和仪器
烟梗、烟末和碎烟片由上海烟草集团太仓海烟烟草薄片有限公司提供。
绿原酸、莨菪亭(纯度>98%)、甲醇(色谱纯)(北京百灵威科技有限公司);芸香苷(纯度>98%,德国Dr.Ehrenstorfer 公司);乙酸(AR,国药集团化学试剂有限公司);无水乙醇(AR,江苏强盛功能化学股份有限公司)。
Agilent 1260 高效液相色谱仪(配置四元梯度泵、自动进样器、柱温箱、可变波长紫外检测器和OpenLAB CDS ChemStation 工作站);Milli-Q Advantage A10 超纯水仪(美国Millipore 公司);R-215 旋转蒸发仪(瑞士Buchi有限公司);DF-101T 集热式恒温加热磁力搅拌器(巩义市予华仪器有限责任公司);KQ3200DV 型数控超声波清洗仪(昆山市超声仪有限公司);Venticell 111 鼓风干燥箱(德国MMM 公司);RK-2A 纸页成型器(奥地利PTI 公司);ZSP-300 高浓实验盘磨机(转速2700 r/min,盘磨直径300 mm,吉林市晨鸣机械制造有限公司);XP205 电子分析天平(感量:0.00001 g,瑞士Mettler Toledo 公司)。
1.2 方法
1.2.1 造纸法再造烟叶工艺流程
取300 g 烟梗,加入1.05 kg 蒸馏水,60 ℃下浸泡20 min,过滤,所得烟梗用高浓实验盘磨机疏解;将疏解后的烟梗与150 g 烟末和150 g 碎烟片均匀混合,加入6 kg蒸馏水,70 ℃下萃取30 min;将分离得到的萃取液于70 ℃下真空浓缩;浆料经打浆、抄造过程得到基片,将浓缩液涂布于基片上即得再造烟叶。为了区分两种萃取液,将烟梗单独浸泡后过滤所得滤液称为烟梗浸泡液,混合萃取后分离得到的溶液称为萃取液。
1.2.2 固相和水相中多酚的制备
烟梗、烟末、碎烟片、基片和再造烟叶分别磨成粉末,过0.42 mm(40 目)筛,称取100.0 mg 样品,置于50 mL 锥形瓶,准确加入20.0 mL 提取液(50%甲醇水溶液),40 ℃下超声提取20 min,取1.5 mL 提取液经0.22 μm微孔滤膜过滤后检测。烟梗浸泡液和萃取液分别用提取液稀释20 倍,浓缩液用提取液稀释200 倍,均过微孔滤膜后检测。白水(纸页成型网布滤水)过滤后直接检测。采用Eclipse XDB-C18色谱柱(250 mm×4.6 mm,5 μm),高效液相色谱泵的后运行时间设为10 min,其他条件同文献[13]。
1.2.3 工艺参数考察
在不同水温(40~90 ℃)条件下分别对烟末进行萃取(料液比1∶10);用0~80%不同浓度(体积分数)乙醇水溶液在70 ℃分别对烟末进行萃取(料液比1∶10);分别称取25.00 g 烟末萃取液于50,70,90,110,130,150 和170 ℃烘箱中挥发2.5 h,所得浓缩物用蒸馏水稀释至原来质量,分别检测浓缩前后的多酚含量。
2 结果与分析
2.1 再造烟叶工艺流程中多酚的转移规律
再造烟叶工艺过程中固相的多酚含量如表1 所示。由表1 可知,原料烟梗、烟末和碎烟片中3 种多酚含量均是绿原酸>芸香苷>莨菪亭。3 种多酚在3 种原料中各自所占比例不同,其中烟末和碎烟片接近,但烟梗中莨菪亭占总多酚的比例较烟末和碎烟片高。基片中3 种多酚含量极少。除莨菪亭外,再造烟叶中其他两种多酚的含量介于烟梗和碎烟片之间。
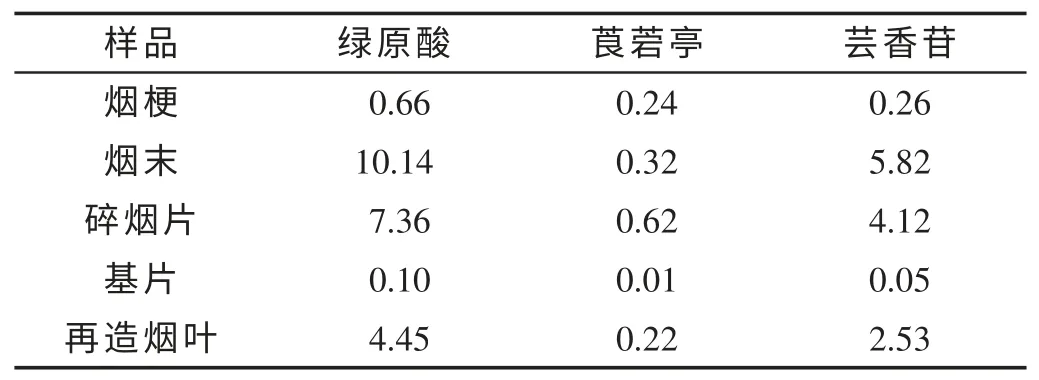
表1 再造烟叶工艺过程中固相的多酚含量Tab.1 Polyphenol concentrations in solid phase in the process of reconstituted tobacco (mg/g)
再造烟叶工艺过程中水相的多酚含量如表2 所示。由表2 可知,由于烟梗结构紧密及其本身多酚含量较小,故烟梗浸泡液中多酚含量较小。萃取液中多酚含量较大,且在浓缩过程中损失较少。在打浆过程中,浆料纤维分丝帚化,同时浆料加水调浓,从而使纤维细胞中的多酚进一步溶出。白水中多酚含量极小。
为了更加准确地判断3 种多酚在整个工艺流程中的转移规律,取10 g 烟梗、5 g 烟末和5 g 碎烟片的绝干物料(原料)作为研究对象,后续工艺段的多酚总量均按照相应比例计算得到。结果如表3 和表4 所示。由表3 可知,20 g 原料中多酚的总量分别为:绿原酸94.07 mg,莨菪亭7.11 mg,芸香苷52.31 mg。试验得到基片的绝干量为8.25 g,基片涂布率为44.8%,涂布所用浓缩液为15.28 g,剩余3.40 g(浓缩液密度为1.225 g/mL)。由表4 可知,再造烟叶中的3 种多酚总量(包括白水、烟梗浸泡液、剩余浓缩液中的多酚)分别为:绿原酸93.51 mg,莨菪亭7.10 mg,芸香苷51.55 mg,与原料中多酚的总量基本相当。多酚的有效利用率(再造烟叶中多酚总量/原料中多酚总量)分别为:绿原酸70.8%,莨菪亭47.1%,芸香苷72.4%;白水体积27.26 L,由此计算出多酚随白水的流失率(白水中多酚/原料中多酚总量)分别为:绿原酸8.4%,莨菪亭18.3%,芸香苷7.9%。
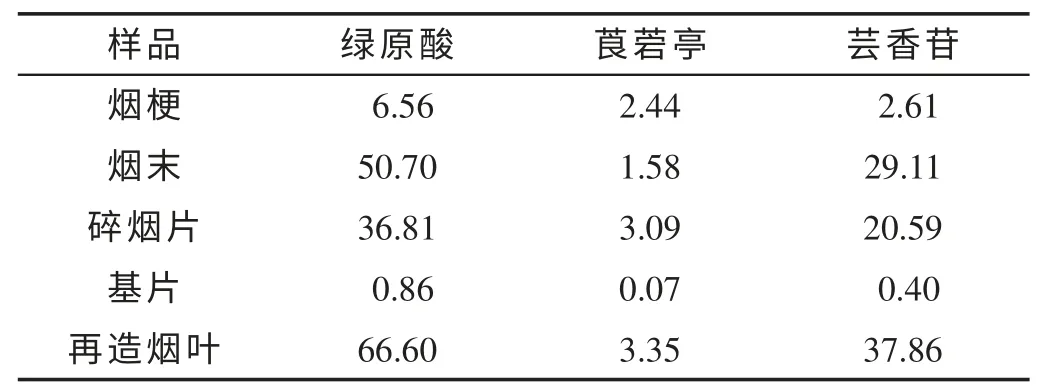
表3 再造烟叶工艺过程中20 g 绝干原料固相的多酚含量Tab.3 Polyphenol concentrations in solid phase of 20 g over-dry material in the process of reconstituted tobacco (mg)
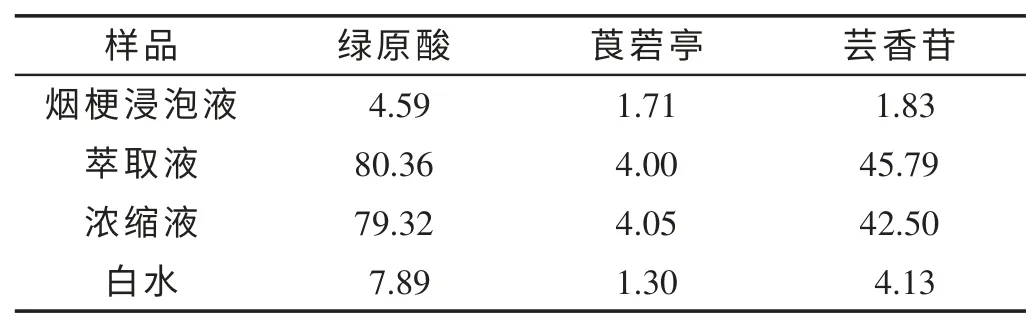
表4 再造烟叶工艺过程中20 g 绝干原料水相的多酚含量Tab.4 Polyphenol concentrations in aqueous phase of 20 g over-dry material in the process of reconstituted tobacco (mg)
2.2 萃取温度对烟末中多酚萃取效率的影响
由萃取温度对烟末中多酚萃取效率的影响(图1)可知,在40~90℃时,随着萃取温度的升高,3种多酚的萃取量均呈增加趋势,其中,70~80℃时增幅最大,80~90℃时增幅减小,这说明在80℃之后,原料中的多酚已基本上被萃取出来。上述结果显示,在40~90℃温度范围内,提高萃取温度对多酚的萃取有利。在实际生产中,萃取温度一般不超过90℃。
2.3 不同浓度乙醇水溶液对烟末中多酚萃取效率的影响[14]
不同乙醇浓度对烟末中多酚萃取效率的影响如图2 所示。由图2 可知,当乙醇浓度小于70%时,3 种多酚萃取量随乙醇浓度的增加而增加,且均在70%处最大;当乙醇浓度在70%~80%时,3 种多酚的萃取量明显减少,这说明在水中加入一定比例的乙醇能提高3 种多酚的萃取效率。
2.4 萃取液浓缩温度对烟末萃取液中多酚含量的影响
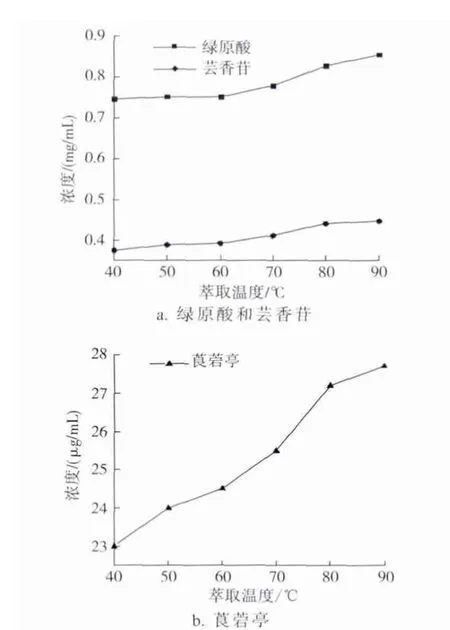
图1 萃取温度对烟末中多酚萃取效率的影响Fig.1 The effect of extraction temperature on polyphenols in tobacco dust extract
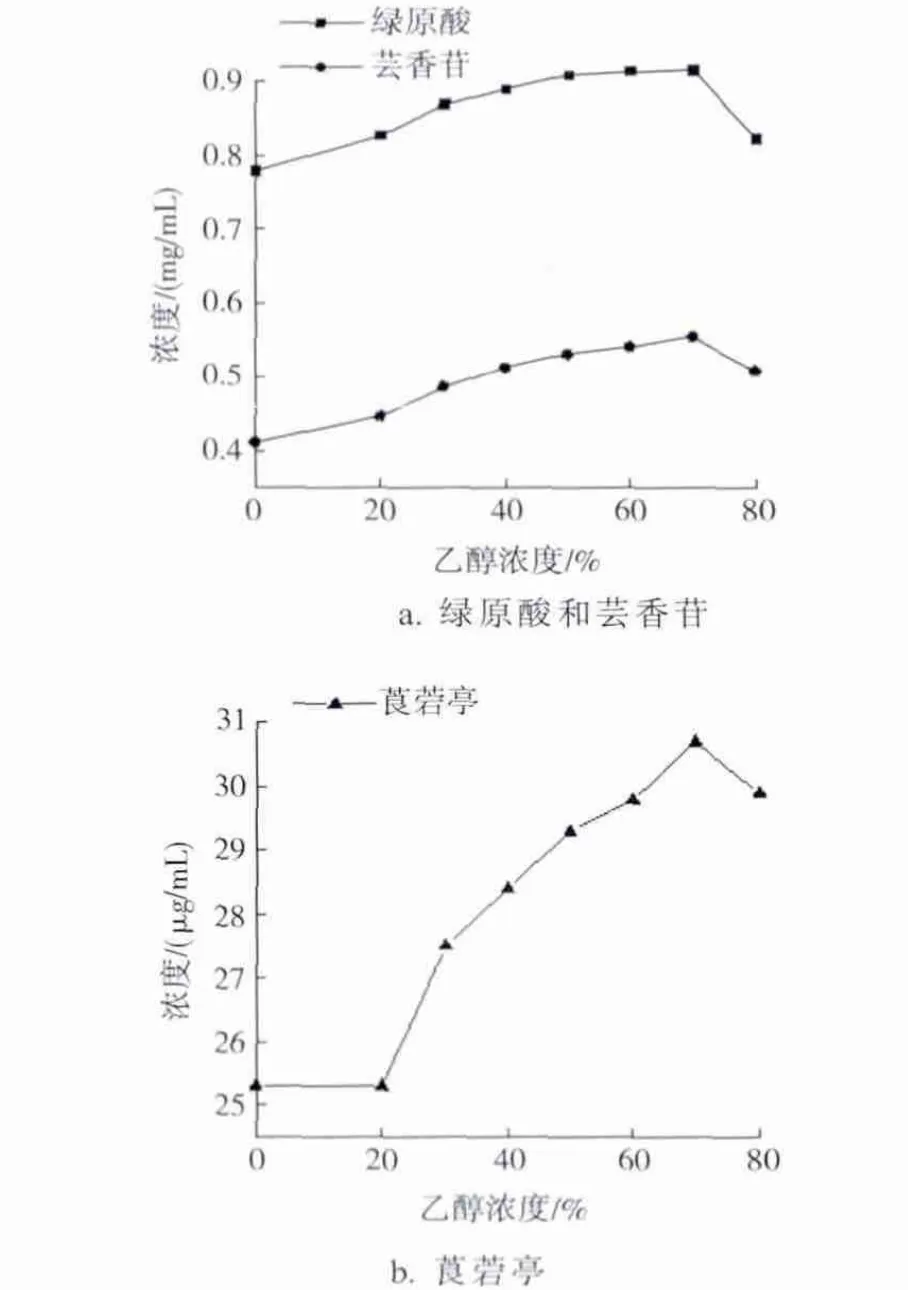
图2 乙醇浓度对烟末中多酚萃取效率的影响Fig.2 The effect of ethanol concentration on polyphenols in tobacco dust extract

图3 浓缩温度对烟末萃取液中多酚的影响Fig.3 The effect of concentration temperature on polyphenols in tobacco dust extract
浓缩温度对萃取液中多酚含量的影响如图3 所示。当浓缩温度从50℃升至170℃时,萃取液中3种多酚的含量总体上呈降低趋势。其中,绿原酸和芸香苷的含量在50~150℃时逐渐下降,且降幅逐渐增加,130~150℃时,降幅最大。而在150~170℃时,两者均有所增加,这可能是由于其他物质的转化而来。对于莨菪亭,在50~70℃时,其含量略有增加,但随后一直降低,且在130~150℃时降幅最大。综上所述,在较高温度下,3种多酚的含量逐渐降低主要是由于三者与空气接触后发生了氧化反应。在实际生产中大都采用真空浓缩,且浓缩温度较低,因而对3种多酚的影响较小。
3 小结
烟末和碎烟片中3 种多酚含量均较烟梗多,但烟梗中莨菪亭占总多酚的比例较大。萃取液于70 ℃真空浓缩多酚损失较小,基片和白水中多酚含量较小,但多酚随白水流失较多。多酚的有效利用率分别为:绿原酸70.8%,莨菪亭47.1%,芸香苷72.4%。因此提高多酚的利用率可以通过增加涂布率,增加浆料的挤干程度,增加抄造过程中浆料的留着率,减少多酚随白水的流失量来实现。
萃取温度在40~90 ℃时,随萃取温度的提高,多酚的萃取效率逐渐增大;多酚的萃取效率随萃取剂中乙醇浓度的增加而呈现先升高后降低的趋势,当乙醇浓度为70%时,多酚的萃取效率最高;萃取液中多酚含量随浓缩温度的升高总体上呈逐渐降低的趋势,浓缩温度低于90 ℃时,对3 种多酚的影响较小。研究多酚类物质在造纸法再造烟叶工艺过程中变化规律,对于再造烟叶的生产工艺参数优化及其品质调控具有一定的参考价值。
[1]徐晓燕,孙五三,王能如.烟草多酚类化合物的合成与烟叶品质的关系[J].中国烟草科学,2003,24(1):3-5.
[2]李丛民.植物多酚对烟草制品品质的影响[J].烟草科技,2000(1):27-28.
[3]张秋芳,刘奕平,刘波,等.烟草主要酚类物质研究进展[J].福建农业学报,2006,21(2):158-163.
[4]王瑞新.烟草化学[M].北京:中国农业出版社,2003:110.
[5]刘静,侯英,杨蕾,等.烟草中多酚热裂解产物研究[J].化学研究与应用,2011,23(1):63-65.
[6]左天觉.烟草的生产、生理和生物化学[M].朱尊权,等译.上海:上海远东出版社,1993.
[7]Czégény Z,Blazsó M,Várhegyi G,et al.Formation of selected toxicants from tobacco under different pyrolysis conditions[J].Journal of Analytical Applied Pyrolysis,2009,85(1/2):47-53.
[8]Snook M E,Mason P F,Sisson V A.Polyphenols in the nicotiana species[J].Tobacco Science,1986,30(18):43-52.
[9]Kallianos A G.Phenolics and acids in leaf and their relationship to smoking quality and aroma [J].Recent Advances in Tobacco Science,1976,2:61-79.
[10]冯丽婷,徐杰,闫克玉,等.河南烤烟(40 级)酚类物质含量及规律性研究[J].烟草科技,1999(1):22-24.
[11]Chorinuchit P,Puaugnak W.Major chemical changes during flue-cured tobacco[J].Thailand Journal of Agricultural Science,1987,20:121-130.
[12]缪应菊,刘维涓,刘刚,等.烟草薄片制备工艺的现状[J].中国造纸,2009,28(7):55-60.
[13]YC/T 202—2006 烟草及烟草制品 多酚类化合物绿原酸、莨菪亭和芸香苷的测定[S].
[14]陈开波,田振峰,陈闯.RP-HPLC 法测定烟草中绿原酸含量的研究[J].分析测试技术与仪器,2005,11(1):60-62.

