HPLC法测定异丙托溴铵原料药中的有关物质
陈 红,朱 蓉(成都市食品药品检测中心,成都 610045)
HPLC法测定异丙托溴铵原料药中的有关物质
陈 红*,朱 蓉(成都市食品药品检测中心,成都 610045)
目的:建立测定异丙托溴铵原料药中有关物质的方法。方法:采用高效液相色谱法。色谱柱为SHISEIDO C18,流动相为磷酸盐溶液(含0.1mol/L磷酸二氢钠和0.01mol/L四丙基氯化铵,pH 5.5)-甲醇(87∶13,V/V),流速为1m l/min,检测波长为220 nm,柱温为40℃,进样量为5μl。结果:异丙托溴铵和杂质B、C、D、E检测质量浓度分别在6.24~62.4、4.25~53.1、4.59~57.4、10.35~129.4、4.00~50.01μg/m l范围内与各自峰面积积分值呈良好的线性关系(r=0.999 6、0.999 0、0.999 8、0.999 7、0.999 7);精密度、稳定性、重复性试验的RSD<10%;杂质B、C、D、E平均加样加收率分别为103.8%、104.3%、101.6%、104.4%,RSD分别为3.8%、2.2%、1.8%、3.5%(n=9)。结论:该方法准确、简便、快速,可用于异丙托溴铵原料药中有关物质的测定。
异丙托溴铵;有关物质;高效液相色谱法
支气管哮喘是呼吸系统常见病、多发病,其发病与多种细胞因子和炎性介质的表达异常有关[1]。异丙托溴铵是一种具有抗胆碱能(副交感)特性的四价铵化合物,可竞争性抑制乙酰胆碱对气道平滑肌的收缩作用,通过抑制细胞内环磷酸鸟苷(cGMP)生成,减少cAMP降解,降低细胞内钙离子浓度,使气道平滑肌松弛、肥大细胞释放炎性介质减少,终止气道扩张,呼吸阻力减小[2]。异丙托溴铵可联合布地奈德、沙丁胺醇、氨溴索治疗小儿毛细支气管炎和哮喘,能迅速改善症状,缩短病程,疗效显著[2-4]。有研究以乙腈-0.25%庚烷磺酸钠溶液(pH 3.2)为流动相测定了吸入用异丙托溴铵溶液的有关物质[5],但并未对其原料药中的有关物质进行定量检测。因此,笔者采用高效液相色谱(HPLC)法对异丙托溴铵原料药中的有关物质进行测定,以为其质量控制提供参考。
1 材料
2695型HPLC仪,含2988型二极管阵列检测器(美国Waters公司);BP211D型电子天平(德国Sartorius公司)。
异丙托溴铵及其杂质A、B、C、D、E对照品(四川大冢制药有限公司,批号:WS/IPRA-BP/05、NPRS/IPTBR IMPA/12/01、1025862、NPRS/IPTBR IMAC/12/01、09080337、PID/IB-VI/ 100。杂质A:(1R,3r,5S,8r)-3-羟基-8-甲基-8-(1-甲基乙基)-8-氮杂双环[3.2.1]辛烷;杂质B:(1R,3r,5S,8s)-3-{[(2RS)-3-羟基-2-苯丙酰]氧代}-8-甲基-8-(1-甲基乙基)-8-氮杂双环[3.2.1]辛烷;杂质C:(2RS)-3-羟基-2-苯丙酸(DL-托品酸);杂质D:2-苯基丙烯酸(阿托酸);杂质E:(1R,3r,5S)-8-氮杂双环[3.2.1]辛烷基(2RS)-3-羟基-2-苯基丙酸乙酯);异丙托溴铵原料药(四川大冢制药有限公司,批号:IB-10002、IB-11001、IB-11002);四丙基氯化铵、甲醇为色谱纯,其余试剂为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:SHISEIDO C18(4.6mm×150mm,5μm);流动相:磷酸盐溶液(含0.1mol/L磷酸二氢钠和0.01mol/L四丙基氯化铵,pH 5.5)-甲醇(87∶13,V/V);检测波长:220 nm;柱温:40℃;进样量:5μl;流速:1m l/min。
2.2 溶液的制备
2.2.1 对照品溶液 称取异丙托溴铵对照品适量,用流动相溶解并稀释,制成每1m l含0.02 mg的溶液,摇匀,作为对照品溶液。
2.2.2 杂质混合对照品溶液 精密称取杂质B、C、D、E对照品约5mg,置于25m l量瓶中,加流动相溶解并稀释至刻度,摇匀,精密量取1m l置于10m l量瓶中,加流动相稀释至刻度,摇匀,作为杂质混合对照品溶液。
2.2.3供试品溶液 称取样品约100mg,分别置于10m l量瓶中,加流动相溶解并稀释制成每1m l中约含10mg的溶液,作为供试品溶液。
2.3 系统适用性试验
取“2.2”项下对照品溶液(与杂质混合对照品溶液混合)和供试品溶液各5μl,分别注入HPLC仪,记录色谱,详见图1。结果,杂质C、异丙托溴铵和杂质B、D、E之间的分离度依次为8.9、4.4、5.6、3.8;异丙托溴铵和杂质B、C、D、E理论板数分别为6 748、7 591、8 189、8 914、8 047。
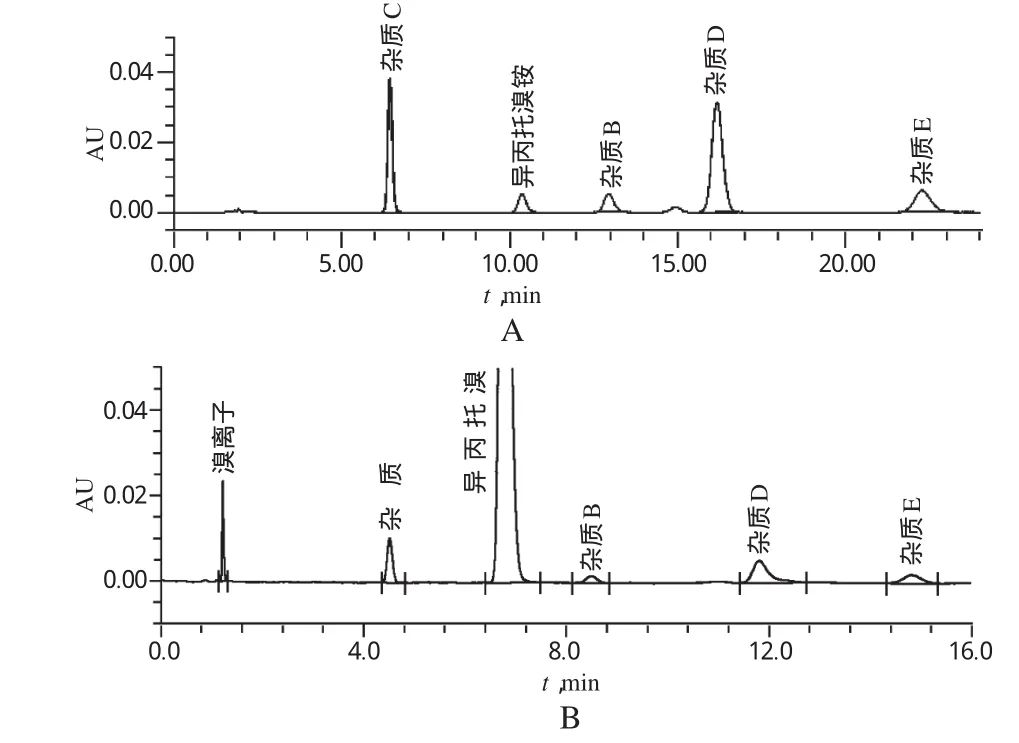
图1 高效液相色谱图A.对照品+杂质混合对照品;B.供试品Fig 1 HPLC chrom atogram sA.substance control+impurity and m ixed control;B.test samples
2.4 专属性试验
为了考察该方法能否有效检测出异丙托溴铵在生产及贮存过程中可能产生的降解产物,根据药物结构特点、合成工艺及贮存条件等,进行了以下强制降解试验,以验证分析方法对相关降解产物检查的专属性。
2.4.1强碱破坏试验 取样品100mg,置于10m l量瓶中,加0.1mol/L氢氧化钠溶液1m l,放置1 h后,用0.1mol/L盐酸溶液中和至中性,加流动相稀释至刻度,摇匀。取此溶液适量,注入HPLC仪,记录色谱,详见图2A。由图2A可见,杂质C面积明显增加,在相对保留时间4.6处有一明显杂质峰,记为杂质F。
2.4.2高温破坏试验 取样品100mg,置于10m l量瓶中,于60℃加热1.5 h,精密取此样品1m l,置于10m l量瓶中,加流动相溶解稀释至刻度,摇匀。取此溶液适量,注入HPLC仪,记录色谱,详见图2 B。由图2B可见,杂质C峰面积略有增加。
2.4.3强酸、强氧化剂、强光照射破坏试验 (1)取样品100 mg,置于10m l量瓶中,加0.1mol/L盐酸溶液1m l,放置0.5 h后,用0.1mol/L氢氧化钠溶液中和至中性,加流动相稀释至刻度,摇匀,备用;(2)取样品100mg,置于10m l量瓶中,加0.3%过氧化氢溶液1m l,放置0.5 h后,加流动相稀释至刻度,摇匀,备用;(3)取样品100mg,置于10m l量瓶中,置于4 000 lx条件下强光照射48 h后,取此溶液适量,置于10m l量瓶中,加流动相稀释至刻度,摇匀,备用。取上述3种溶液适量,分别注入HPLC仪,记录色谱图,详见图2 C、D、E。由图2 C、D、E可见,未见有明显的杂质峰出现。
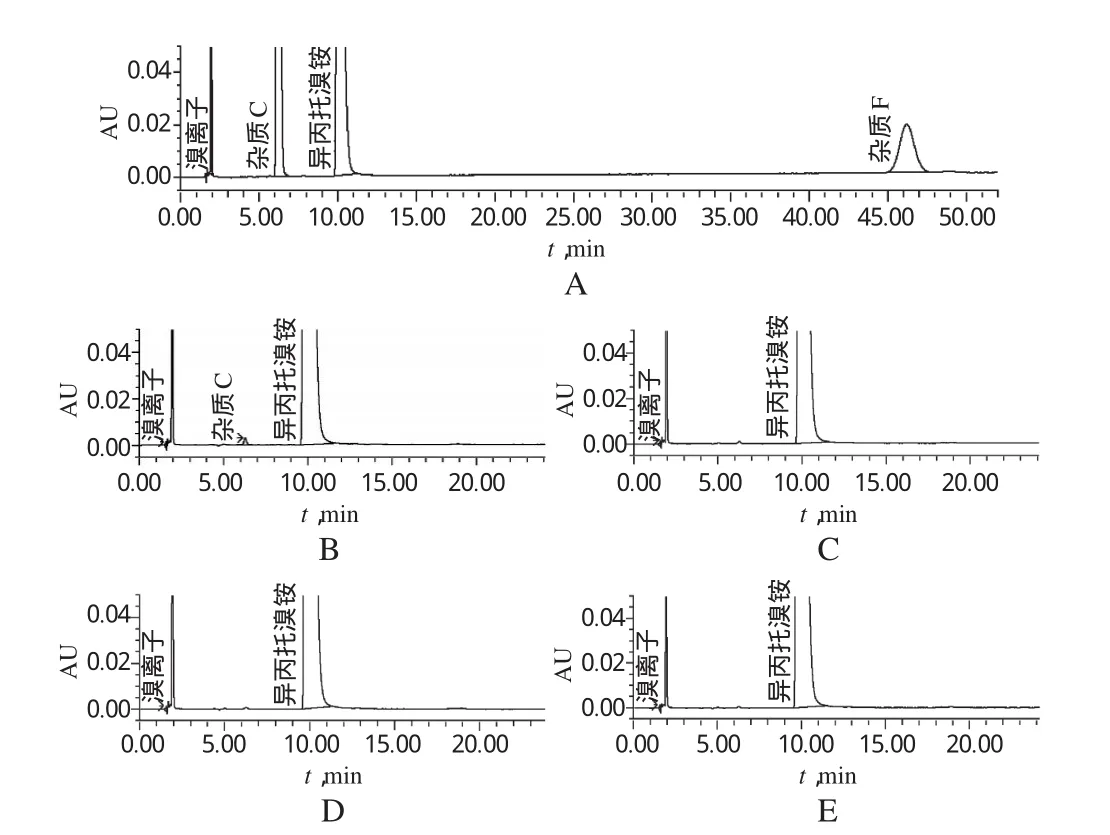
图2 破坏试验高效液相色谱图A.碱破坏样品;B.高温破坏样品;C.酸破坏样品;D.氧化破坏样品;E.光照破坏样品Fig 1 HPLC chromatogram s of treated testA.treated w ith alkali;B.treated w ith high temperature;C.treated w ith acid;D.treated w ith oxidation;E.treated w ith light
上述破坏试验证明在此色谱条件下能有效考察各杂质,且与主峰完全分离。本品为溴化物,采用0.2%的溴化钾溶液进样,溶剂峰处出现的大杂质峰为溴离子峰,在结果计算中应扣除。上述试验结果表明,本方法具有良好的专属性,适用于本品在生产及贮存过程中因各种影响所产生的有关物质检查。
2.5 线性关系考察
将“2.2”项下对照品溶液与杂质混合对照品溶液混合后,精密量取10、6、4、2、1m l,置于10m l量瓶中,用流动相稀释至刻度,得系列不同浓度的溶液。以检测质量浓度(x,μg/m l)为横坐标,峰面积(y)为纵坐标,进行线性回归,线性范围和回归方程见表1。

表1 线性范围和回归方程Tab 1 Linear range and regression equation
2.6 检测限和定量限
将“2.2”项下对照品溶液与杂质混合对照品溶液混合后,取适量用流动相稀释后按“2.1”项下色谱条件进样,记录色谱,以信噪比S/N=3∶1计算异丙托溴铵和杂质B、C、D、E的检测限,以信噪比S/N=10∶1计算异丙托溴铵和杂质B、C、D、E的定量限,结果见表2。

表2 各杂质检测限和定量限结果Tab 2 Results of detection lim its and quantification lim it
2.7 精密度试验
取“2.2.2”项下杂质混合对照品溶液5μl,按“2.1”项下色谱条件重复进样测定6次。结果,杂质B、C、D、E的RSD均<2.0%,表明仪器精密度良好。
2.8 稳定性试验
取“2.2.2”项下杂质混合对照品溶液适量,按“2.1”项下色谱条件,于25℃,分别放置0、2、7、10、24 h时进样测定。结果,杂质B、C、D、E的RSD均<2.0%,表明杂质混合对照品溶液在24 h内质量稳定。
2.9 重复性试验
取样品(批号:IB-10002)适量,共6份,分别按“2.2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定。结果,异丙托溴铵和杂质B、C、D、E的RSD均<10%,表明本方法重复性良好。
2.10 加样回收率试验
精密称取样品(批号:IB-10002)约100mg,共9份,分别置于10m l量瓶中,每3份分别加入杂质混合对照品溶液1、2.5、4 m l,按“2.2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,计算加样回收率,结果见表3。
2.11 耐用性试验
分别选用3根不同型号色谱柱,分别以流速为1、1.5m l/ min作有关物质的检查,结果,杂质B、C、D、E平均相对保留时间基本相同(偏差<20%),杂质之间及与主成分间均能达到较好分离(分离度>3),结果见表4。
2.12 样品有关物质测定
分别取3批样品适量,按“2.2.3”项下方法制备供试品溶液,并按“2.1”项下色谱条件进样测定,计算有关物质的量,结果见表5。
3 讨论
3.1 检测波长的选择
将含异丙托溴铵和杂质B、C、D、E的对照品溶液在210~400 nm波长范围内进行二极管阵列扫描。结果发现,异丙托溴铵和杂质B、C、E均未见有明显吸收,只有杂质D在242 nm波长处有最大吸收。但是,在220 nm波长处异丙托溴铵和杂质B、C、D、E均有较大吸收。因此,选择220 nm波长为检测波长。
3.2 进样浓度和色谱记录时间的选择
异丙托溴铵为苯基丙酰结构,异丙托溴铵及其杂质共轭基团少,紫外吸收弱,因此配制约10mg/m l浓度的样品溶液测定时色谱峰各效能参数均能达到测定要求。样品经强碱破坏后,杂质明显增加,在相对保留时间4.6处有一明显杂质峰。有文献[6]报道,样品在相当于主成分峰保留时间的5.1倍处有一杂质峰,记为杂质F。因此,将记录时间定为主成分峰保留时间的6倍。
3.3 其他杂质检查
异丙托溴铵主要杂质有A、B、C、D、E、F。其中,杂质A极性强,在色谱柱中几乎无保留,因此笔者采用薄层色谱法单独检查;另外,因未得到杂质F对照品,未进行检测。
3.4 样品溶液的稳定性
在溶液稳定性考察中,当样品在25℃下放置0~24 h时,测定发现杂质C的峰面积增加,24 h内杂质C增加量<0.02%,总杂质量由0.04%增至0.07%。当样品在25℃下及时进样(0 h),杂质C低于检测限;当样品在低温(约10℃)下进样时,均未检出杂质C;当样品在室温(25℃)放置较长时间(约5 d)时,杂质C增加量小于0.1%。考虑到样品在24 h内杂质C增加量<0.02%,在8 h内不影响总杂质量结果,故本方法在常温下测定可行。
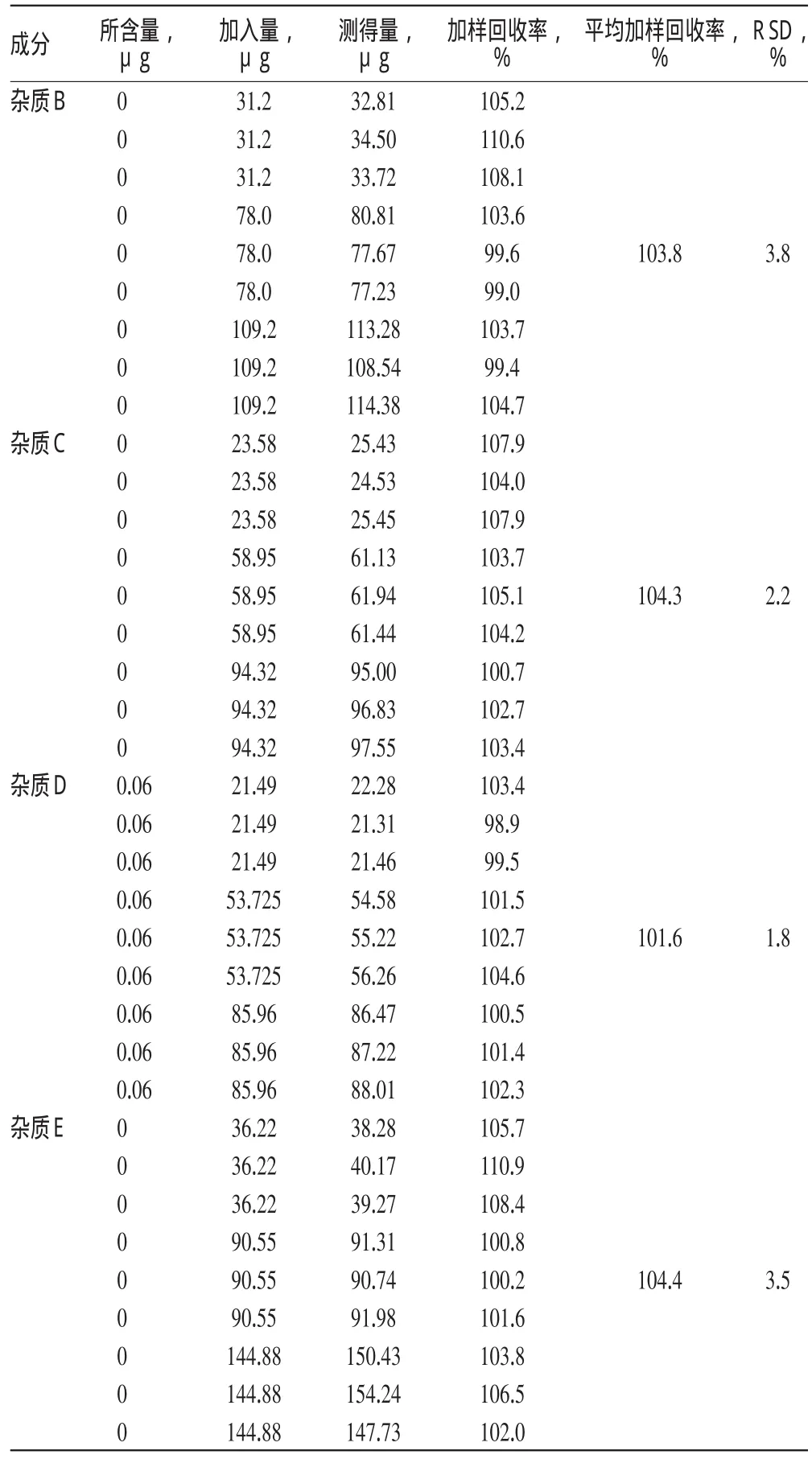
表3 加样回收率试验结果(n=9)Tab 3 Results of recovery tests(n=9)

表4 不同色谱柱测定的平均相对保留时间Tab 4 Relative retention times of different columns

表5 样品有关物质测定结果(n=3,%)Tab 5 The determ ination of related substance in sam p les(n=3,%)
综上所述,本方法准确、简便、快速,可用于异丙托溴铵原料药中有关物质的测定。
[1] 刘莉敏,谢艳丽,王以炳,等.异丙托溴铵联合舒利迭治疗重度哮喘的疗效[J].临床肺科杂志,2013,18(1):80.
[2] 杨岚.复方异丙托溴铵联合布地奈德混悬液治疗儿童急性哮喘发作的疗效评价[J].中国医药科学,2013(18):108.
[3] 刘海平.布地奈德、沙丁胺醇、异丙托溴铵三联吸入治疗小儿毛细支气管炎的疗效观察[J].中国医药指南,2013,11(19):532.
[4] 滕箭,赵炜,王建华,等.吸入用布地奈德混悬液和吸入用异丙托溴铵溶液雾化吸入治疗慢性阻塞性肺疾病的疗效分析[J].中国现代医药杂志,2013,15(4):18.
[5] 卢来春,张蓉,刘同华,等.反相高效液相色谱法测定吸入用异丙托溴铵溶液中的有关物质[J].重庆医学,2007,36(11):1 067.
[6]European pharmacopeia.EP7.0[S].2012:2 277.
Determ ination of Related Substances in Ipratropium Brom ide by HPLC
CHEN Hong,ZHU Rong(Chengdu Center for Food and Drug Control,Chengdu 610045,China)
OBJECTIVE:To establish a method for the determ ination of related substances in ipratropium bromide.METHODS:HPLC method was adopted.The determination was performed on SHISEIDO C18column w ith mobile phase consisted of phosphate solution(containing 0.1mol/Lmonosodium orthophosphate and 0.01mol/L tetrapropylammonium chloride,pH 5.5)-methanol(87∶13,V/V)at the flow rate of 1 m l/min.The detection wavelength was set at 220 nm.The column temperature was 40℃and sample size was 5μl.RESULTS:The linear range of ipratropium brom ide and impurities B,C,D and E were 6.24-62.4μg/m l(r=0.999 6),4.25-53.1μg/m l(r=0.999 0),4.59-57.4μg/m l(r=0.999 8),10.35-129.4μg/m l(r=0.999 7)and 4.00-50.01μg/m l(r=0.999 7),respectively.RSDs of precision,stability and reproducibility tests were all lower than 10%.Average recoveries of impurities B,C,D and E were 103.8%(RSD=3.8%,n=9),104.3%(RSD=2.2%,n=9),101.6%(RSD=1.8%,n=9)and 104.4%(RSD=3.5%,n=9),respectively.CONCLUSIONS:Themethod is accurate,simple and rapid,and can be used for the determ ination of related substances in ipratropium brom ide.
Ipratropium brom ide;Related substance;HPLC
R917
A
1001-0408(2014)12-1128-04
DOI 10.6039/j.issn.1001-0408.2014.12.25
*副主任药师,硕士。研究方向:药物分析与质量控制。电话:028-85362213。E-mail:redchen333@sohu.com
2013-06-14
2013-10-06)

