碳热还原合成钒掺杂的球形LiFePO4/C
陈少辉,杜春雨,卢文斌,熊 凯
(1.深圳市计量质量检测研究院,广东深圳 518055;2.哈尔滨工业大学化工学院,黑龙江哈尔滨 150001)
磷酸铁锂(LiFePO4)的工作电压平稳、容量较高、安全性较高且热稳定性好,但电导率低、振实密度低。表面包覆、金属离子掺杂、颗粒细化等方法可改善LiFePO4导电性的问题[1]。钒元素存在多种氧化态,能形成多面体,有可能掺入八面体结构的Fe位中,在金属离子掺杂方面受到关注。
为了解决振实密度问题,有人提出制备球形LiFePO4材料[2]。球形材料虽然具有相对较高的振实密度,但尺寸较大、结构紧实,会影响材料的导电性。有鉴于此,本文作者先使用控制结晶法制备球形FePO4,再碳热还原合成钒掺杂的球形LiFePO4/C复合材料,并研究了产物的性能。
1 实验
1.1 材料的制备
控制结晶法制备前驱体FePO4:用蠕动泵(上海产)将1 mol/L NH4H2PO4(天津产,AR)溶液按体积比1∶1逐滴加入1 mol/L Fe(NO3)3(广东产,AR)溶液中,用氨水(天津产,AR)将pH值调至6.5,混合液搅拌1 h后,倒入水热反应釜中,在150℃下水热反应10 h,将水热产物过滤,并用清水洗涤多次,最后在真空烘箱(真空度为0.09 MPa)中、60℃下干燥5 h,即得到球形FePO4·xH2O。将得到的FePO4·xH2O在氩气气氛中、650℃下煅烧10 h,得到前驱体。
碳热还原合成LiFe1-xVxPO4/C:按化学计量比称取前驱体 FePO4、LiOH·H2O(天津产,AR)和 NH4H2PO4(天津产,AR)、NH4VO3(天津产,AR),加入理论量过量15%的蔗糖(天津产,AR)粉末,混合后在小瓶中搅拌均匀,再转移至管式炉中,通入氢氩混合气体,以3℃/min的速度升温到700℃,并恒温12 h,制备得到不同钒掺杂量(x)的LiFe1-xVxPO4/C复合材料(x=0、0.03、0.05、0.07 和0.09)。
1.2 结构与形貌分析及电化学性能测试
用D/max-γB型X射线衍射仪(日本产)分析样品的物质组成及晶胞参数,CuKα,管压36 kV、管流 30 mA,λ=1.541 8 nm,步长为0.02°,扫描速率为8(°)/min;用S-4700型扫描电子显微镜(日本产)观察样品的形貌特征。
用BST高精度电池测试仪(广东产)进行恒流充放电测试,电压为2.5~4.2 V;用CHI604B电化学工作站(上海产)进行循环伏安测试,电位为2.5~4.2 V(vs.Li+/Li),扫描速率为0.05 mV/s。
2 结论与讨论
2.1 LiFe1-xVxPO4/C材料的结构与形貌
对LiFe1-xVxPO4/C材料进行XRD分析,结果见图1。
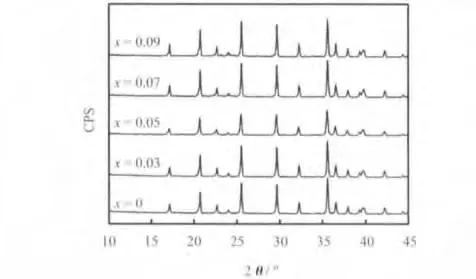
图1 LiFe1-xVxPO4/C材料的XRD图Fig.1 XRD patterns of LiFe1-xVxPO4/C materials
从图1可知,制备的样品衍射峰的位置及强度都与LiFePO4标准谱(JCPS:83-2092)的衍射特征峰吻合,没有发现任何杂质峰的存在,说明在实验条件下,可以生成纯净的LiFePO4/C材料,且钒掺杂后,进入了LiFePO4晶胞结构的晶体中。
LiFe1-xVxPO4/C材料的晶胞参数和体积见表1。
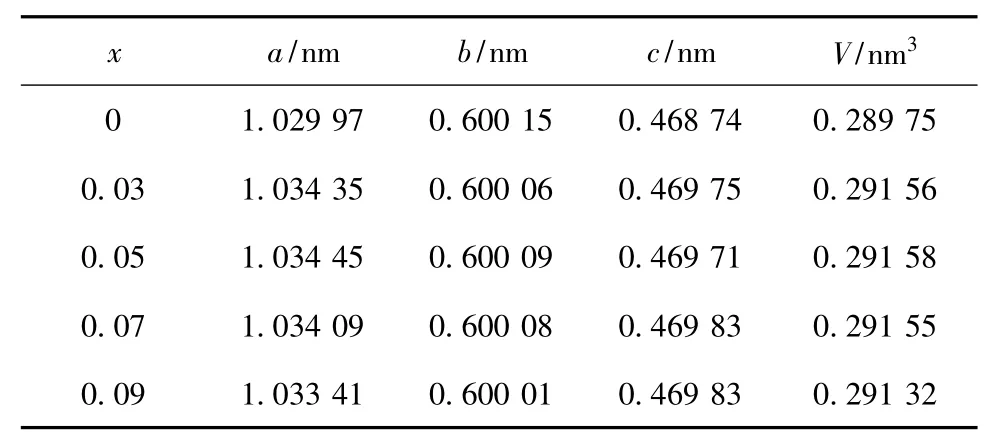
表1 LiFe1-xVxPO4/C材料的晶胞参数和体积Table 1 Lattice parameters and volume of LiFe1-xVxPO4/C materials
从表1可知,相对于未掺杂材料,掺杂材料的晶胞参数a、c及晶胞体积V都有所增加,说明:钒离子掺杂进入晶格中,取代了部分 Fe2+,形成了 VO6八面体结构[3],改变了晶胞中原子之间的距离和部分区域的原子排布,从而增大了晶格中的离子传输通道。这将会提高Li+在晶格中的迁移能力,改善材料的导电性。
研究中用矩形区域表示物体可能存在的位置,采用穷举法计算区域内所有质点位置物体的漂移速度范围,当Δt时间足够小时,物体的漂移运动可以假设为匀速运动,将区间内任一质点位置进行更新,得到Δt后物体的更新区域,因此在理论上有一定的可靠性。
前驱体 FePO4和 LiFe1-xVxPO4/C材料的 SEM图见图2。

图2 前驱体FePO4和LiFe1-xVxPO4/C材料的SEM图Fig.2 SEM photographs of precursor FePO4and LiFe1-xVxPO4/C materials
从图2可知,所有材料都基本上维持了前驱体FePO4的球形结构,LiFe1-xVxPO4/C材料的分散性都不如FePO4,且粒径均比FePO4大。这是因为在碳热还原过程中发生了钒和铁元素的氧化还原反应,存在着相的转化和新相的形成,导致前驱体FePO4变得蓬松,颗粒粒径增大。当x达到0.05时,材料的颗粒尺寸相应增大,说明当x超过一定值时,体相掺杂达到饱和,在材料表面开始生成少量的Li3V2(PO4)3,Li3V2(PO4)3的含量很低,在XRD结果中无法发现[4],但少量的Li3V2(PO4)3也能使材料团聚尺寸变大、Li+扩散路径增长,导致材料的电导性变差。
2.2 LiFe1-xVxPO4/C材料的电化学性能
LiFe1-xVxPO4/C材料的循环伏安曲线见图3。
从图3可知,当x=0、0.03和0.05时,循环伏安曲线只在3.6 V/3.3 V处出现一对氧化还原峰,为LiFePO4与Fe-PO4之间的两相反应的氧化还原峰,掺杂的钒离子含量很低,并未参与反应。当x=0.07和0.09时,除了出现Fe3+/Fe2+氧化还原峰外,在3.61 V/3.57 V、3.69 V/3.65 V及4.09 V/4.04V的位置同时出现了3对氧化/还原峰,对应于Li3V2(PO4)3的氧化/还原峰[5],对应着 V3+与 V4+的转化。
当x<0.07时,Fe3+/Fe2+氧化还原峰之间的电压差随着x的增加而减小,循环伏安曲线的峰值电流随着x的增加而增大,表明少量的钒掺杂,能提高材料的导电性和可逆性。当x≥0.07时,材料表面生成了很少量的Li3V2(PO4)3。因为Li3V2(PO4)3的导电性不好,导致x=0.07和0.09的材料导电性降低,所以x=0.05的材料具有最好的电化学性能。
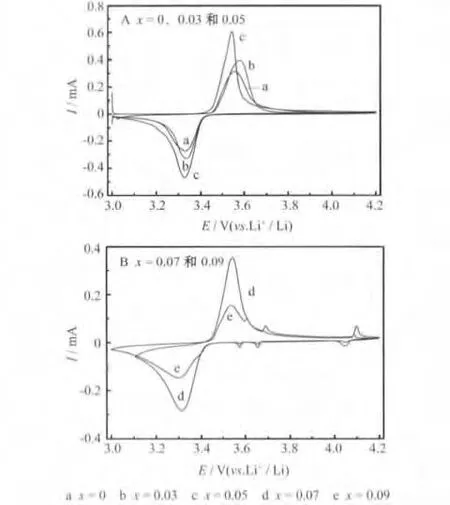
图3 LiFe1-xVxPO4/C材料的循环伏安曲线Fig.3 CV curves of LiFe1-xVxPO4/C materials
LiFe1-xVxPO4/C材料的0.1 C充放电曲线见图4。
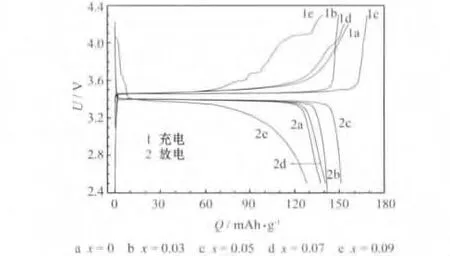
图4 LiFe1-xVxPO4/C材料的0.1 C充放电曲线Fig.4 0.1 C charge/discharge curves of LiFe1-xVxPO4/C materials
材料的导电性和可逆性直接影响到制备的电池的容量。x=0、0.03、0.05、0.07 和0.09 的材料,首次放电比容量分别为 137.6 mAh/g、141.9 mAh/g、151.1 mAh/g、140.2 mAh/g及128.1 mAh/g,其中x=0.05材料的比容量最高,x=0.09材料的比容量最低,验证了之前对材料性能的预测。
LiFe1-xVxPO4/C材料的循环性能见图5。
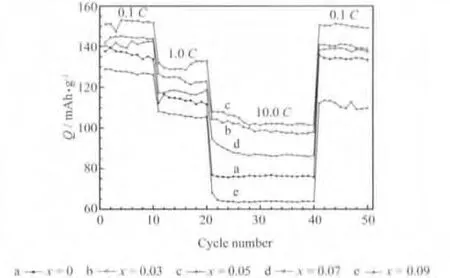
图5 LiFe1-xVxPO4/C材料的循环性能Fig.5 Cycle performance of LiFe1-xVxPO4/C materials
从图5可知,当x<0.09时,在各个倍率下,掺杂材料的比容量都高于未掺杂材料,在高倍率时更加明显;当x=0.09时,由于Li3V2(PO4)3的生成及颗粒粒径的增加,导致材料电化学性能变差。
经过一系列倍率循环后,除了x=0.09的材料,其他材料的循环稳定性和重现性都很好;同时,x=0.05的材料,充放电比容量最高、循环性能最好。
3 结论
通过碳热还原,合成了不同钒掺杂量的球形LiFePO4/C复合材料。
适量的钒掺杂可以改善LiFePO4/C材料的电化学性能:x=0.05的材料性能最好,在2.5~4.2 V充放电,0.1 C首次放电比容量为151.1 mAh/g,10.0 C倍率时,首次放电比容量仍能维持在104.4 mAh/g。
[1]ZHANG Xin-long(张新龙),HU Guo-rong(胡国荣),PENG Zhong-dong(彭忠东),et al.锂离子电池正极材料LiFePO4的研究进展[J].Battery Bimonthly(电池),2003,33(4):252 -254.
[2]Xie H,Wang R,Ying J et al.Optimized LiFePO4-polyacene cathode material for lithium-ion batteries[J].Adv Mater,2006,18(19):2 609-2 613.
[3]Sun C S,Zhou Z,Xu Z G,et al.Improved high-rate charge/discharge performances of LiFePO4/C via V-doping[J].J Power Sources,2009,193(2):841 -845.
[4]Ma J,Li B H,Du H D,et al.The effect of vanadium on physicochemical and electrochemical performances of LiFePO4cathode for lithium battery[J].J Electrochem Soc,2011,158(1):26 -32.
[5]Yang M R,Ke W H,Wu S H.Improving electrochemical properties of lithium iron phosphate by addition of vanadium[J].J Power Sources,2007,165(2):646-650.

