LiMnPO4/C复合正极材料的固相合成及性能
辜 健,胡国荣,杜 柯,曹雁冰
(中南大学冶金科学与工程学院,湖南 长沙 410083)
0 前言
近年来,橄榄石型 LiMPO4(M=Fe,Mn,Co,Ni)锂离子电池正极材料由于成本低,循环性能优异,安全性好、容量较高等诸多优点已成为新能源材料领域的研究热点[1]。LiMnPO4具有更高的4.1 V平台电压,LiMnPO4的能量密度被认为是在碳酸酯基电解液的电化学稳定窗口下所能达到的最大能量密度,因此LiMnPO4正极材料更具有应用潜力[2-3]。一旦磷酸锰锂材料的研发取得突破,他不仅能够抢占磷酸铁锂的市场份额,而且能够挤压锰酸锂和三元材料的市场空间,打破目前正极材料的市场格局。目前,磷酸锰锂材料在全球范围内仍处于研发阶段,没有实施量产的先例,这主要是由于没能找到合适的解决磷酸锰锂材料高性能化问题的低成本规模化生产方法[4-6]。
LiMnPO4/C(以下简称为:LMP)的制备方法主要有固相合成法[7-9]、水热法[10-12]、溶胶凝胶法等[13-14]。但是目前报导的方法都存在以下不足:a制备的LMP材料放电比容量很少有超过100 mA·h/g,且放电平台很差[15];b 大多数高性能LMP材料的合成方法都很复杂,不利于批量生产,且一致性不好;c大多数制备方法涉及昂贵的化学试剂和危险药品,容易导致安全和环保问题;d大部分报道的LMP复合材料都引入了大量的包覆碳(质量比≥20%)[16-17],不利于体积能量密度的发挥,降低了材料加工性能。固相合成法的工艺和设备相对简单,易于工业化,所以固相合成法被大量的应用于生产锂离子电池材料上[18]。但主要缺点是物相不均且煅烧时间长,不利于控制产物结构和形貌。
本文针对LiMnPO4材料导电性差的缺点,以合成结晶度良好、颗粒细小均匀碳包覆的LMP复合材料为目标,首先选择MnO、高温可分解的 MnCO3、MnC2O4·2H2O及 Mn(CH3COO)2为原料,制备LMP复合材料,比较不同锰源获得LiMnPO4材料的性能。采用分步活化煅烧法进行工艺改进,改善材料电化学活性。
1 实验部分
1.1 样品制备
按照LiMnPO4化学计量比准确称取Li2CO3(四川产,99.5%),NH4H2PO4(武汉产,98.0%)和不同锰源 MnO(湖南产,99.5%),MnCO3(湖南产,99.5%),MnC2O4·2H2O(湖南产,99.0%)和醋酸锰(天津产,99.0%)。葡萄糖(江苏产,99.0%)为碳源,碳源添加量为0.1 mol产物对应6 g葡萄糖。一步法合成方式:将原料混合物置于钢球球磨罐中,加适量的酒精作分散剂,转速为400 r/min,球磨4 h,获得混合均匀的前驱料浆。将料浆在真空鼓风干燥箱中干燥12 h,过筛得到前驱体粉末。前驱体粉末置于充满氩气的气氛炉中650℃下煅烧6 h,获得最终产物LMP正极材料。分步活化煅烧法处理方式:前驱料的混合方式如一步法,得到的前驱体粉末于氩气气氛炉中升温至450℃,升温速度2℃/min,随炉冷却,至室温后将样品置入钢球球磨罐,加入少量酒精做分散剂,于钢球球磨罐中450 r/min转速下球磨2 h,得到中间料浆,将料浆置于55℃鼓风干燥箱中干燥,干燥后的粉末置于充满氩气的气氛炉中650℃下煅烧6 h,获最终产物LMP粉末。
1.2 电极制备及半电池组装
将材料制作成CR2025型扣式电池进行充放电循环测试。采用涂膜法制备电极,以N-甲基-2-吡咯烷酮(NMP)为溶剂(天津产,AR),按质量比75∶15∶10分别称取活性物质、乙炔黑(焦作产,AR)和PVDF(日本产),混合均匀后,涂在预处理过的铝箔上,放入真空干燥箱中在120℃干燥得到正极片。在充满氩气的手套箱中,以金属锂片(江苏产,AR)为负极,1 mol/L LiPF6溶解于碳酸乙烯酯(EC)+二甲基碳酸酯(DMC)+乙基甲基碳酸酯(EMC)(体积比为 1∶1∶1,江苏产,电池级)为电解液,Celgard2400多孔聚丙烯膜(美国产)为隔膜,组装成扣式电池。
1.3 表征测试
采用日本Rigaku公司生产Minflex型的X射线自动衍射仪(XRD,D/max-r A type Cu Ka1,40 kV,300 mA,10(°)~70(°),日本)进行晶体结构分析。样品的微观形貌研究采用日本JEOL公司JSM-5600LV型扫描电子显微镜。采用的差热—热重分析仪为SDTQ600(美国产),测试软件为V8.0 Build 95,测试模块为DSC-TGA Standard。升温速率为10 K/min,氩气气流速率为100 mL/min。在Land电化学仪上进行电化学测试,充电终止电压为4.5 V,恒压充电过程的截止条件为充电电流<0.01 C,放电终止电压为2.5 V。其中,碳包覆的LiMnPO4中碳的重量被看作活性物质,测试过程中电流密度1 C=170 mA/g。循环伏安测试在 Potentiostat/Galvanostat Model 2273A(PerkinElmer Instrument,USA)电化学工作站上进行,采用的程序为Electrochemistry Powersuite Program。电位扫描区间2.8 ~4.8 V,扫描速度 0.15 mV/s。LMP的碳含量分析,采用HW2000型红外碳硫分析仪。
2 结果与讨论
图1为不同锰源一步法获得的LMP样品的XRD图。
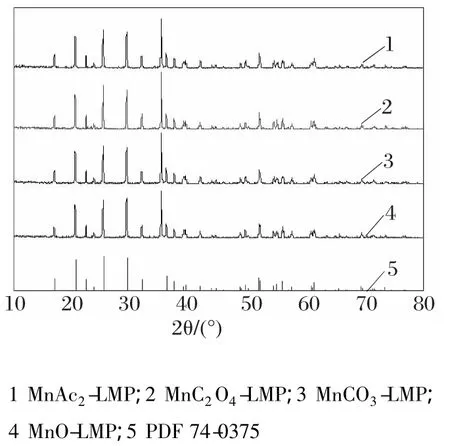
图1 不同锰源为原料合成LiMnPO4材料的XRD
从图1中可以看出,用不同锰源为原料均可获得结晶良好的橄榄石型LiMnPO4,且产物中没有其他杂相峰,属于正交晶系,空间群为Pnma。衍射峰中未出现碳的特征衍射峰,说明热解生成的碳为无定形。不同锰源制备的LMP的XRD衍射峰峰强度不一样,说明不同原料对产物的形貌和结构有一定的影响[19]。从XRD数据可以得到样品的晶体结构参数,见表1。
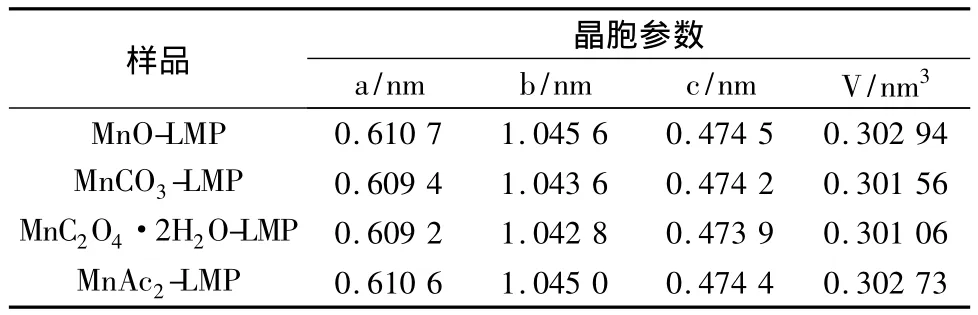
表1 不同锰源对应LiMnPO4的晶体结构参数
从表1中很容易可以看出,不同的锰源作为前驱体得到的材料的晶胞参数不一样,其中以MnC2O4·2H2O为锰源对应的样品晶胞参数最小,晶胞体积也随之变小。
图2给出了各种前驱体锰源和对应LMP的SEM对比图。
从图2中可以看出,锰源影响LiMnPO4的形貌。用MnO合成的LMP颗粒粒度较大,为1~5 μm之间,产物表面致密,说明在合成LMP过程中,产物基本保持了MnO的形貌特征。B1和B2是碳酸锰和与之相对应的LMP的SEM图,对比可以看出LMP与前驱体形貌相差很大,得到100~500nm左右的细小LMP颗粒,二次颗粒不规则且烧结现象明显。高能机械活化对颗粒的破碎和缺陷化学能的提供及热处理过程中MnCO3的热分解作用使前驱体和LiMnPO4形貌相差很大。和碳酸锰一样,草酸锰在热处理过程中也发生分解,产物为200~500 nm的细小颗粒,粒径分布比MnCO3得到的LiMnPO4均匀,属于软团聚体。在机械活化条件下,晶体结构受破坏,产生严重的晶格畸变、高密度的缺陷及纳米级的亚稳定结构,部分机械能转变成化学潜能[20]。机械力作用可以使反应物和反应产物颗粒破碎而得到细化,同时又可以促进反应原料之间的快速反应。D1和D2对应Mn(CH4COO)2和对应LMP的SEM图,产物颗粒团聚比较严重,且醋酸盐做前驱体得到的前驱料浆不易干燥,工艺操作麻烦。

图2 不同锰源为原料前驱体与对应产物LiMnPO4的SEM对比
不同LMP活性物质在0.05 C下的首次充放电曲线如图3所示。
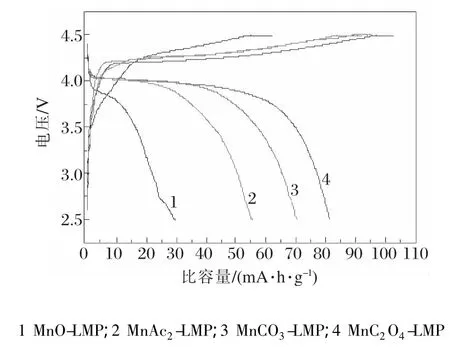
图3 不同锰源制备LMP材料0.05 C倍率下首次充放电性能比较
从图3中可以看出,以MnC2O4·2H2O为锰源对应的样品有最高的放电比容量,为81 mA·h/g,且表现出较好的放电平台。MnCO3、Mn(CH4COO)2和MnC2O4·2H2O为锰盐反应物均能得到细化颗粒的效果,但前2者作原料容易产生产物烧结现象,晶胞参数存在一定的差异,影响材料性能。另外,以醋酸盐为原料存在难干燥易成胶等现象,工艺操作困难。MnC2O4·2H2O合成的LMP在一定程度上利于Li+的脱嵌,但由于LiMnPO4本身离子和电子电导率差,200~500 nm尺寸的颗粒还是满足不了LMP发挥潜在电活性的要求。
图4为以不同锰源制备LMP为电极材料的半电池0.05 C循环性能图。
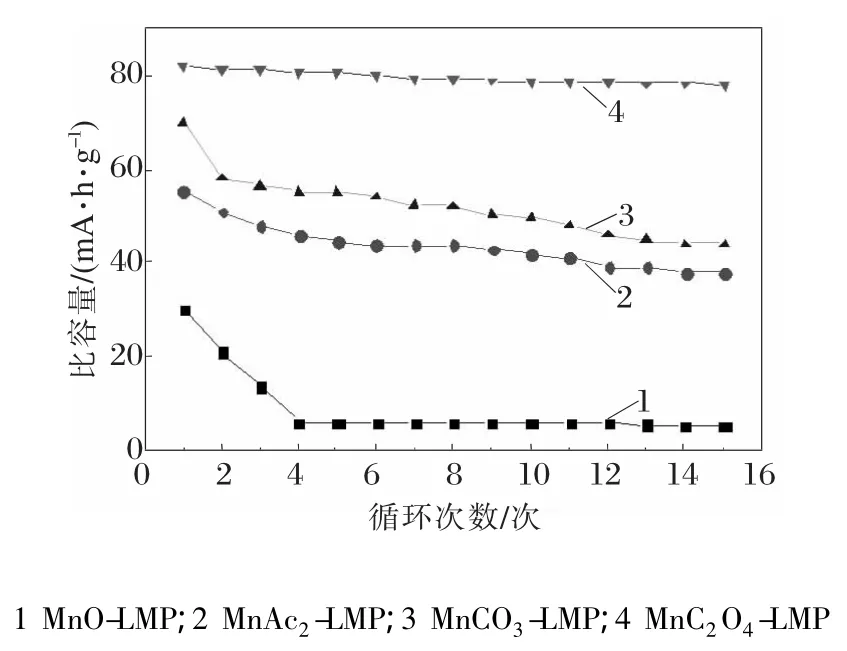
图4 不同锰源在0.05 C下充放电循环性能比较
从图4中可以看出,不同锰源获得的样品都存在容量衰减的现象。MnC2O4·2H2O为原料合成的样品表现出最好的循环性能。
草酸锰在合成LMP过程中会发生分解,185℃左右时失去2个结晶水,而在440℃左右草酸根分解,形成二价金属氧化物,且伴随着更细新相的生成[21]。在上面的实验中得知,在650℃时,LiMnPO4样品的颗粒达200~500 nm,颗粒分散性好,且分布均匀。由于LiMnPO4材料Li+扩散通道为一维通道,扩散系数很小,较小的颗粒可以缩短锂离子扩散距离,提高活性物质利用率,电化学性能得到改善。因此,借助草酸盐分解的特性,实验采用分步煅烧法来制备颗粒尺寸更小的LiMnPO4材料。
图5 为 Li2CO3、MnC2O4·2H2O、NH4H2PO4和葡萄糖球磨混合物在惰性气氛中的差热曲线(DSC)和热重曲线(TGA)图。
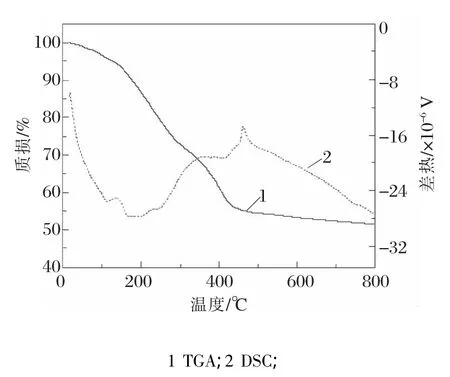
图5 Li2CO3、MnC2O4·2H2O、NH4H2PO4和葡萄糖惰性气氛中的DSC和TGA
从图5中的TGA曲线可以看出,室温到470℃温度范围内都有质量损失,损失的成分包括吸附水、结晶水、CO、CO2和NH3的脱出。DSC曲线上出现了4个热效应峰,~110℃和~170℃处的吸热峰对应着明显失重,此为脱去吸附水和结晶水的过程。~450℃处的吸热峰主要为无水草酸盐的分解。~460℃处的放热峰对应着橄榄石结构LMP生成。从TGA曲线可以看出,曲线从600℃开始趋于平缓,说明此时材料结晶已经完全。整个分解—合成反应方程式如下:
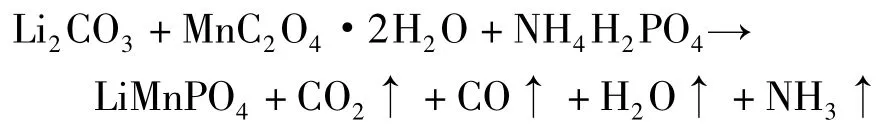
反应物料在460℃左右已基本不失重,说明前驱体中的 CO2、CO与 H2O脱除完全,本文选择450℃作为预分解温度,第2段选择650℃作为合成LiMnPO4的煅烧温度。
图6为一步法和分步活化煅烧法得到LMP复合正极材料的SEM对比图。

图6 一步法和两段活化煅烧法合成的LMP复合正极材料SEM对比
从图6可以看出,分步活化煅烧法对颗粒细化效果非常明显,颗粒粒度由一步法的200~500 nm之间被细化到100 nm左右。分段机械活化有效地减小了颗粒尺寸。
图7给出了分步活化煅烧法和一步法制备的LMP复合正极材料0.05 C下充放电曲线对比(图7A)及两段活化煅烧法制备LiMnPO4材料的不同倍率循环性能曲线(图7B)。两步法制备的LMP有更优的电化学性能,放电比容量达105.3 mA·h/g,平台率为82%,中值电压为4.01 V,表现出LiMnPO4材料高电压的特性,而国内外报道的多数研究中LMP材料中很少有比容量超过100 mA·h/g,且有较好平台的。所以分段活化煅烧工艺在激发材料电化学活性上具有明显的改进效果,对后续改性制备高能量密度磷酸锰锂非常有意义。
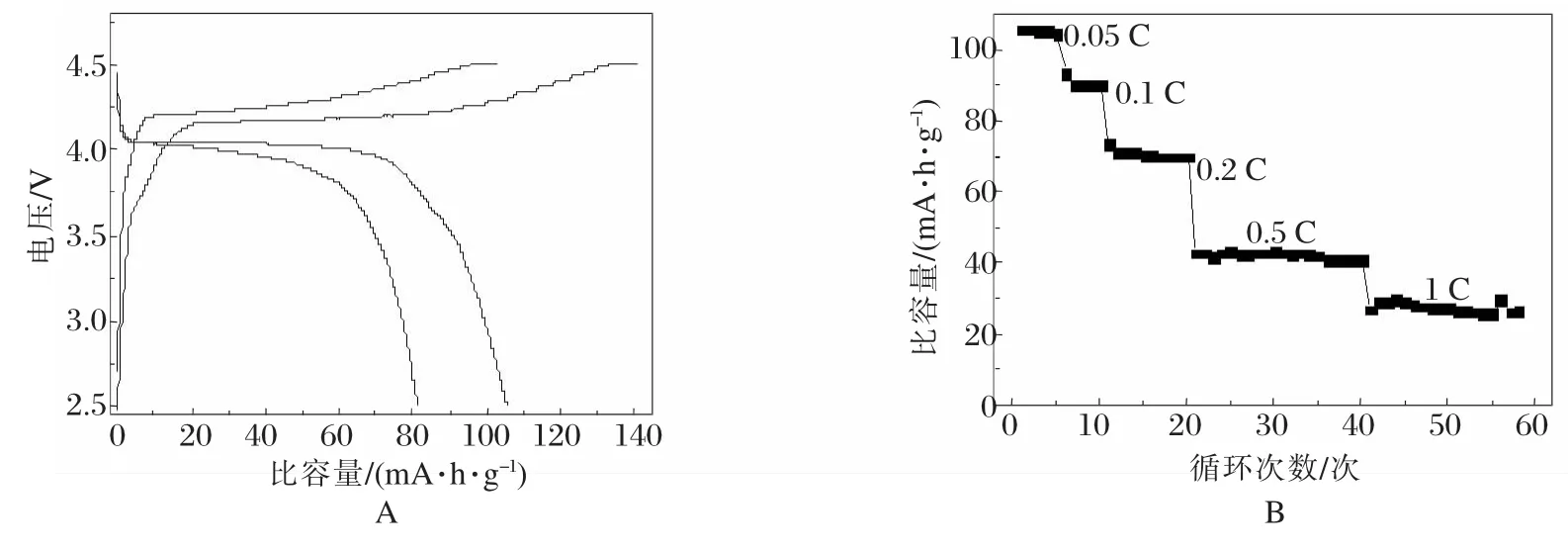
图7 不同方法合成的LMP复合正极材料首次充放电曲线(A)和分步活化煅烧法合成的LMP倍率循环曲线(B)
从图7B中可以看出,LMP材料在较低倍率下的循环性能比较稳定,但材料倍率性能仍然较差。
图8给出了LMP复合材料的TEM图。

图8 分步法制备LMP正极材料的TEM
从图8可以看出,样品的粒子尺寸细小,约100 nm。并且大部分微小粒子通过表面碳层和分散其间的碳膜连接形成一定的软团聚体。碳分析结果显示,材料包覆碳质量含量为8.2%。高倍率透射电镜图像上可以看出在颗粒表面形成了4 nm的均匀碳包覆层,微小粒子通过表面碳连接,而使晶粒与晶粒或晶粒与颗粒之间相互连接,构成典型的碳网络结构。这种碳导电结构使样品颗粒间形成有效的导电连接,有利于颗粒与电解液的接触和增大Li+有效脱嵌表面积,促使电极过程中离子与电荷的快速转移,提高活性物质利用率。
循环伏安法是研究锂电池脱嵌锂动力学过程的重要手段。图9为分步煅烧工艺制备的LMP复合正极材料循环伏安曲线。
从图9中可以看出,曲线存在一对强的氧化还原峰,分别对应着Li+在电极中的脱出和嵌入过程,氧化峰和还原峰有较好对称性,说明复合正极材料具有较好的可逆性。但是电池具有较小的峰值电流,Li+扩散阻力很大。LMP材料的氧化峰峰位出现位置为4.47 V,对应的还原峰峰位出现的位置为 3.80 V,相对应氧化还原峰的电位差为0.67 V。

图9 分步煅烧工艺制备的LMP复合正极材料循环伏安曲线
3 结语
以MnC2O4·2H2O通过一步法制备的LMP颗粒粒径在200~500 nm之间,颗粒界线分明,较其他原料合成的LMP有较好的电化学性能。MnC2O4·2H2O为锰源,机械活化混合的前驱粉末经过450℃预烧,冷却后机械球磨活化2 h,再进行高温固相反应得到的LMP材料粒径约100 nm,而且表现出更优的电化学活性。
[1]Padhi A K,Nanjundaswamy K S,Goodenough J B.Phospholivinesas positive electrode materials for rechargeable lithium batteries[J].J Electrochem Soc.,1997,144(4):1188 -1194.
[2]Ellis B L,Lee K T,Nazar L F.Positive Electrode Materials for Li-Ion and Li-Batteries[J].Chem Mater,2010,22(3):691 -714.
[3]Martha S K,Markevich E,Burgel V,et al.A short review on surface chemical aspects of Li batteries:A key for a good performance[J].J Power Sources,2009,189(1):288 -296.
[4]Nie Z X ,Ouyang C Y,Chen J Z,et al.First principles study of Jahn_Teller effects in LixMnPO4[J].Solid State Commun,2010,150(1/2):40-44.
[5]Nadja W,Gunter B,Loser W,et al.Challenges in the crystal growth of Li2CuO2and LiMnPO4[J].J Cryst Growth,2011,318(1):995–999.
[6]Qin Z,Zhou X,Xia Y,et al.Morphology controlled synthesis and modification of high-performance LiMnPO4cathode materials for Li-ion batteries[J].J Mater Chem,2012,22:21144-21153.
[7]Li G,Hideto A and Masayuki T.LiMnPO4as the Cathode for Lithium Batteries[J].Electrochem Solid-State Lett,2002 ,5(6):A135-A137.
[8]Li G,Hideto A and Masayuki T.Optimized LiMnyFe1-yPO4as the Cathode for Lithium Batteries[J].J Electrochem Soc,2002,149(6):A743-A747.
[9]Jeffrey W F.Recent developments in cathode materials for lithium ion batteries[J].J Power Sources,2010,195(4):939 –954.
[10]Wang Y,Yang Y,Yang Y,et al.Enhanced electrochemical performance of unique morphological LiMnPO4/C cathode material prepared by solvothermal method[J].Solid State Commun,2010,150(1/2):81-85.
[11]Prabeer B,Karim D,Nadir R,et al.Direct and modified ionothermal synthesis of LiMnPO4with tunable morphology for rechargeable Li-ion batteries[J].J Mater Chem,2011,21:10143–10152.
[12]Ni J,Gao L.Effect of copper doping on LiMnPO4prepared via hydrothermal route[J].J Power Sources,2011,196(15):6498–6501.
[13]Kim J S,Seo D H,Kim S W,et al.Mn Based Olivine Electrode Material with High Power and Energy [J].Chem Commun,2010,46:1305-1307.
[14]Dominko R,Bele M,Gaberscek M,et al.Porous olivine composites synthesized by sol-gel technique[J].J Power Sources,2006,153(2):274–280.
[15]Wang L,Sun W,Li J,et al.Synthesis of Electrochemically Active LiMnPO4via MnPO4·H2O with Different Morphology Prepared By Facile Precipitation [J].Int J Electrochem Sci,2012,7:3591-3600.
[16]Martha S K,Markovsky B,Grinblat J,et al.LiMnPO4as an Advanced Cathode Material for Rechargeable Lithium Batteries[J].J Electrochem Soc,2009,156(7):A541-A552.
[17]Bakenov Z,Izumi T.Physical and electrochemical properties of LiMnPO4/C composite cathode prepared with different conductive carbons[J].J Power Sources,2010,195(21):7445 - 7451.
[18]Hong J,Wang F,Wang X,et al.LiFexMn1-xPO4:A cathode for lithium-ion batteries[J].J Power Sources ,2011,196(7):3659–3663.
[19]Drezen T,Kwon N H,Bowen P,et al.Effect of particle size on LiMnPO4cathodes[J].J Power Sources ,2007,174(2):949 –953.
[20]李运姣,李洪桂,孙培梅.LiMn2O4的机械活化湿化学合成机理[J].功能材料,2004,35(2):183-185.
[21]陈刚,陈鼎,严红革.固液反应球磨工艺[J].材料导报,2005,19(5):222-224.

