犊牛支原体肺炎的诊断和防治措施
刘东军
(新疆石河子大学动物科技学院,新疆石河子 832000)
牛支原体是危害我国养牛业的重要致病性支原体,目前已证实该病呈世界性分布,病原除导致牛肺炎、乳腺炎外,还导致关节炎、角膜结膜炎、耳炎、生殖道炎症、流产与不孕等多种病症。据报道,欧美国家约四分之一至三分之一的牛呼吸道疾病综合征是由牛支原体引起的。同时,牛支原体与其它病原的混合感染和协同致病性是牛支原体肺炎重要的致病机制之一。据报道,混合感染的常见病原菌主要包括:多杀性巴氏杆菌、化脓隐秘杆菌、溶血性曼氏杆菌、昏睡嗜血杆菌等;混合感染的常见病毒有:牛副流感病毒3型、疱疹病毒Ⅰ型、牛呼吸道合胞体病毒、牛病毒性腹泻病毒和牛冠状病毒。随着新疆奶牛业的迅速发展,牛支原体肺炎造成的犊牛死亡成为制约奶牛业健康发展的严重障碍,给奶牛业造成严重的损失。通过我们对牛支原体肺炎的流行病学调查,制定了支原体肺炎的综合防治技术措施,减少肺炎支原体的危害,提高犊牛成活率,为犊牛健康提供技术保障,促进了新疆奶牛业的健康发展。
一、支原体的生物学特性
(一)形态与染色特征 支原体是一类能在无活细胞培养基中繁殖的最小微生物,无细胞壁,繁殖形式多种多样。支原体的大小为0.2~0.3 um,可通过滤菌器,常给细胞培养工作带来污染的麻烦。无细胞壁,不能维持支原体结构固定的形态而呈现多形性。革兰氏染色不易着色,故常用Giemsa染色法将其染成淡紫色。细胞膜中胆固醇含量较多,约占36%,对保持细胞膜的完整性具有一定作用。凡能作用于胆固醇的物质(如两性霉素B、皂素等)均可引起支原体膜的破坏而使支原体死亡。 支原体基因组为一环状以双链DNA,分子量小(仅有大肠杆菌的五分之一),合成与代谢很有限。肺炎支原体的一端有一种特殊的末端结构,能使支原体粘附于呼吸道黏膜上皮细胞表面,与致病性有关。
(二)营养要求与培养特性 营养要求比一般细菌高,除基础营养物质外还需加入10%~20%动物血清以提供支原体所需的胆固醇。最适pH7.8~8.0,低于7.0则死亡,但解脲支原体最适pH6.0~6.5。大多数兼性厌氧,有些菌株在初分离时加入5%CO2生长更好。生长缓慢,在琼脂含量较少的固体培养基上孵育2~3 d,出现典型的“荷包蛋样”菌落:圆形(直径10~16 um),核心部分较厚,向下长入培养基,周边为一层薄的透明颗粒区。此外,支原体还能在鸡胚绒毛尿囊膜或培养细胞中生长。
繁殖方式:繁殖方式多样,主要为二分裂繁殖,还有断裂、分枝、出芽等方式。
二、牛传染性支原体肺炎流行病学特点
(一)牛支原体肺炎的发病机制牛支原体肺炎的发病机制主要由于支原体穿过宿主呼吸道黏膜表面的粘液纤毛层,粘附于黏膜上皮细胞上,此粘附作用与肺炎支原体表面的P1蛋白末端结构有关。当此粘附因子附着于呼吸道黏膜上皮细胞时,释放的有毒代谢产物可导致纤毛运动减弱,细胞损伤。感染肺炎支原体后,可引起体液免疫和细胞免疫反应。体液免疫应答先出现特异性IgM抗体,然后出现IgG抗体,持续较长时间。鼻咽部局部产生的分泌性IgA抗体,能有效地抑制肺炎支原体与呼吸道上皮结合。呼吸道IgA抗体比血清中抗体对宿主的免疫状态有更直接关系。在感染防御上局部抗体甚为重要。局部免疫除IgA外,局部细胞免疫也发挥作用。因为初次感染使幼畜致敏,促使再次感染时发生较重的临床表现,表明本病与感染肺炎支原体后机体产生超敏反应的关系。
(二)流行病学特点
1.潜伏期。牛支原体自然感染的潜伏期较难确定。国外有报道 ,在健康犊牛群中引入感染牛 24 h后 ,就有犊牛从鼻腔中排出牛支原体 ,但大部分牛在接触感染牛 7 d后经鼻腔排出牛支原体 。有的牛在接触感染牛 2周后发病。
2.感染日龄。一月龄的犊牛容易感染支原体肺炎,特别是一周龄的犊牛最易感染,而且病情急剧,症状明显,发病急,病情重,死亡率较高。1~2月龄的犊牛发病率较低,2月龄以上的犊牛病例较少。
3.感染途径。牛群一旦感染支原体发病或潜伏感染后很难被清除。如果牛群伴发其他呼吸道疾病 ,如溶血性巴氏杆菌病、牛传染性鼻气管炎、呼吸道合胞体病毒病、副流感、病毒性腹泻-黏膜病牛的死亡率显著增加。感染牛支原体的牛可携带病原体数月甚至数年而成为一个传染源。牛之间通过飞沫经呼吸道传播是主要途径 ,其次是近距离接触、吸乳汁或生殖道传播 ,感染牛支原体公牛配种或使用其冻精进行人工授精都可导致牛支原体的传播和扩散 。
4.牛品种差异。荷斯坦、娟姗牛等引进品种的犊牛发病率和死亡率较高,本地原有的品种的犊牛发病率和死亡率较低。新引入的荷斯坦、娟姗牛犊牛在新引入的1~2年内发病率和死亡率较高,经过2~3年的风土驯化后发病率和死亡率稍稍降低。
5.混合感染。由于牛支原体感染对机体免疫系统造成极大的破坏作用 ,导致继发感染或混合感染的其他病原微生物的致病力增强。国外报道的混合感染病原微生物有溶血性巴氏杆菌、牛传染性鼻气管炎病毒、呼吸道合胞体病毒、副流感病毒、病毒性腹泻-黏膜病病毒等。
6.发病率和死亡率。牛支原体肺炎的发病率和死亡率和饲养管理水平相关,饲养管理较好的牛场发病的死亡率较低。一般冬季12月、1月、2月、3月发病率在15%~40%,其他月份发病较少,偶尔有发病的犊牛。
(三)犊牛支原体肺炎的临床症状 根据病程和临床症状可分为最急性、急性和慢性。临床上急性、慢性病例较常见,最急性病例较少见。
1.最急性。最急性病例较少,病初体温升高40.5℃~41.7℃,精神沉郁,食欲废绝,呼吸急促,咳嗽,并流浆液性带血液的鼻液,呈铁锈红色。肺部叩诊出现浊音,听诊肺泡呼吸音呈捻发音。随着病程加重病犊牛卧地不起,呼吸极度困难,全身颤抖,可视黏膜发绀。目光呆滞,有痛苦的呻吟声,死亡较快。病程2~3 d,有些急性病例病程仅1 d左右。
图1 病牛精神沉郁且被毛粗乱无光泽
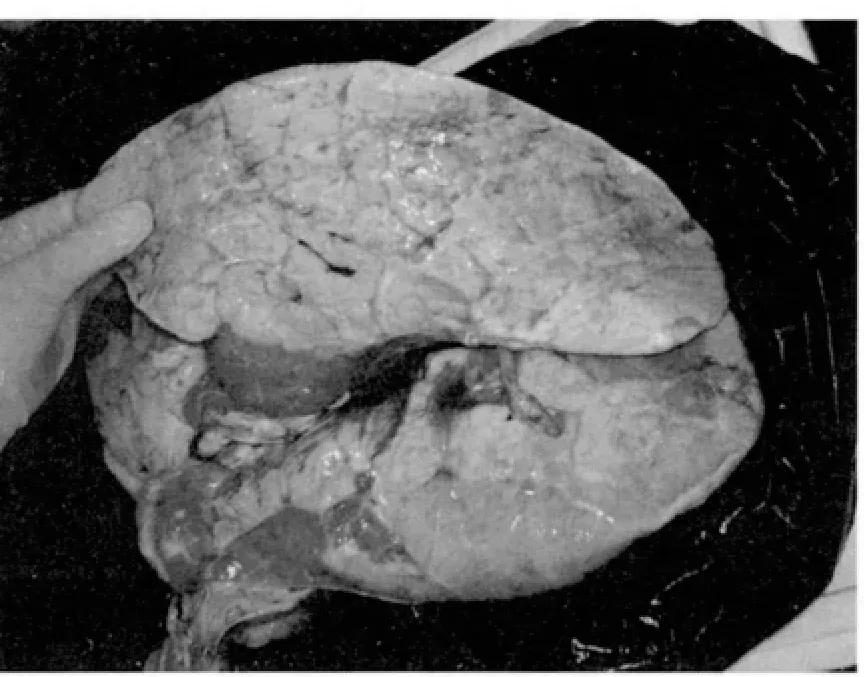
图2 牛支原体肺炎的肺部发生病理变化
2.急性。开始病犊牛咳嗽、有浆液性的鼻液,体温升高,不爱运动,常卧于圈舍四周,驱赶后常出现咳嗽症状。2~3 d后咳嗽症状加重,鼻液变为粘液性、脓性并呈铁锈红色或红棕色,粘附在鼻孔周围和上唇,形成干涸的污垢块。按压胸部病犊牛表现敏感、疼痛,听诊肺部出现支气管呼吸音和喘鸣声。病犊牛精神沉郁,反刍减少或停止。呼吸困难,腰背拱起,头颈伸直。眼睑肿胀,粘液性的分泌增加。最后病犊牛卧地不起,衰竭。有的发生瘤胃臌气,有个别发生腹泻。腹部的皮肤发生丘疹。濒死期体温降至常温以下。病程通常7~10 d,不死的转为慢性病例。
3.慢性。慢性病例较常见,多见于1~2月龄以上的犊牛。病犊牛全身症状较轻微,病牛有时侯咳嗽和腹泻,鼻涕时有时无,身体衰弱,被毛粗乱无光。在此期间,如果饲养管理条件改善病犊牛可以自然康复,如果饲养管理条件较差,很容易病情加重或继发其他疾病而死亡。
4.剖检症状。病变多集中在胸部,打开胸腔,常可闻到异样的气味或腐败臭味,胸腔内常有淡黄色的积液,常混有腐败的组织而呈现灰黄色或黄白色。暴露在空气中积液形成纤维蛋白凝块。急性病例肺部的损害多集中在一侧,病变多集中在肺组织的心叶、尖叶、膈叶,肺脏上有肝变区,肝变区凸出于肺脏表面,颜色红至灰色不等。切面呈大理石样。纤维蛋白渗出液充盈使肺小叶间组织变宽,小叶界限明显。肺气肿,支气管、细支气管内有大量的白色泡沫样液体。胸膜变厚表面有大量的纤维蛋白性渗出物附着而变得粗糙。胸膜与肋骨或心包粘连。支气管淋巴结和纵隔淋巴结肿大,切面多汁并有出血点。心包积液,心肌松弛、变软。急性病例还可见肝脏肿大,胆囊充盈。肾脏肿大,表面有出血点。病程较长的病例肺肝变区机化,结缔组织增生,甚至形成包囊化的坏死灶。
5.病理变化。主要为支气管炎、毛细支气管炎及间质性肺炎。管壁水肿、增厚、有浸润斑。支气管及细支气管内有粘液甚至脓性分泌物。镜下所示为急性细支气管炎伴有间质性肺炎。肺泡内可见有少量水肿液及巨噬细胞。细支气管壁有水肿、充血以及单核细胞和淋巴细胞浸润,腔内可见到中性粒细胞、脱落上皮细胞及细胞残片。附近的肺泡间隔内有淋巴细胞及单核细胞浸润。重症可见弥漫性肺泡坏死和透明膜病变。
三、牛支原体肺炎的综合防治措施
(一)支原体疫苗免疫接种 牛支原体可诱导细胞免疫与体液免疫。给新生牛气管内接种牛支原体后 ,血清中 IgM在攻菌两周后出现高峰 ,随后出现了 Ig G1和 Ig G2。攻菌 4周后 Ig G1亚型抗体占优势。感染后 2~4周可观察到含有 Ig的细胞聚集在肺实质的坏死灶区域 ,且以 Ig G1型细胞为主 ,其次为 Ig G2型细胞。鼻腔和气管的黏膜下层可检测到 IgA阳性细胞。给犊牛气管内与鼻腔内同时接种活的牛支原体后 ,也证实牛支原体主要诱导 Th2型免疫反应 ,抗体以 Ig G1型为主。实际生产中采用奶牛产前60 d注射牛支原体灭活氢氧化铝佐剂疫苗取得良好的效果,接种的奶牛产的犊牛支原体病的发病率明显降低,病情较轻,病程短,死亡率降低。
(二)治疗措施 发病犊牛及时使用抗生素治疗,可以取得较好效果。常用的抗生素主要有氧氟沙星、环丙沙星、氟苯尼考、泰乐菌素、强力霉素等。生产中注意避免长时间小剂量预防用药,以免产生抗药性,影响治疗效果。
1.胸腔注射。5%氧氟沙星10 ml胸腔注射对治疗本病效果良好。具体做法是:病犊牛左侧卧保定在肩关节水平线上距肘关节5 cm处剪毛、消毒,垂直进针3~5 cm穿透皮肤、肋间隙到达胸腔,但不能刺伤肺脏,注射药物。在操作时穿透皮肤后感觉到进针的阻力突然减小,这是针尖到达了胸腔,当针尖刺入肺脏时可以感觉到针尖随着肺脏有节奏的来回运动,这时应当将针头稍稍抽回一些。在操作中应注意注射针头和注射部位的消毒,防止感染。胸腔注射还可以采用氟苯尼考、强力霉素、林可霉素等药物。胸腔注射每天注射一次,连续治疗5~7 d,为一个疗程。
2.对症治疗。对症状较重的病犊牛可采用输液治疗,5%碳酸 氢 钠50~80 ml,25%葡 萄糖200~250 ml,葡萄糖酸钙50~80 ml,阿奇霉素0.5~0.75 g,0.5%甲硝唑注射液200~250 ml,地塞米松5~10 mg,静脉注射一天一次连用5~7 d。在肺部炎症初期为防止渗出,促进炎性分泌物消散和吸收,可肌肉注射呋塞米4~5 ml,维生素C 5 ml。
3.预防用药。饲料添加抗生素也有较好的预防效果。每吨精料添加土霉素1 800~2 000 g或恩诺沙星200~400 g连续饲喂7~10 d也有较好的预防治疗效果。
(三)预防措施
1.加强犊牛饲养管理。犊牛群注意加强饲养管理,提高犊牛的抵抗力,减少损失,在生产中我们发现冬季圈舍保持10℃~15℃的温度时,进行舍饲,并且尽量减少舍饲密度,可以有效降低发病率。新生犊牛加强饲养管理,出生1 h以内灌服3~4 kg初乳,间隔12 h灌服2 kg。出生3 d后注射亚硒酸钠-VE注射液和牲血素注射液。一周后注射维丁胶钙注射液,牛奶中适量添加葡萄糖酸钙和维生素D。通过以上措施可以有效提高犊牛的健康水平。
2.加强犊牛圈舍卫生。犊牛圈舍保持清洁干燥,粪便污水及时清除干净,冬季注意保暖,在提高温度的前提下,加强通风,排除有害气体,减少发病。圈舍垫草及时更换,发霉垫草及时清除。犊牛饲养器具和环境及时消毒,避免病菌滋生。
3.隔离治疗患病犊牛。在预防本病时除了一般的预防措施以外,关键是防止引入病犊牛或带菌犊牛,在引种时要了解当地的疫情,加强检疫防止患病犊牛的引入。新引进的犊牛隔离饲养一个月以上,隔离检疫确认无病后才能混群饲养。发病时及时对犊牛群逐头检查,病犊牛和假定健康犊牛要分开饲养。病犊牛污染的圈舍、饲草、场地要加强消毒或进行无害化处理。
4.使用空气消毒仪减少空气中的病原菌。臭氧可以有效杀灭养殖环境中的病原微生物,消除空气中的氨气、硫化氢等有害气体,改善养殖环境,促进动物福利。通过改善养殖环境,减少疾病的发生,减少化学药品的使用,消除动物产品的药物残留,生产有机的动物产品。
(略)

