固相萃取-高效液相色谱法测定水中氯酚类
吴海鹏
(江门融浩水业股份有限公司,广东 江门 529000)
酚类化合物有毒,是造成环境污染的工业化学品,天然有机物氯化或水消毒剂能产生卤代酚副产物,可使水带有难闻的气味[1,2]。我国制订的“水中优先控制污染物”中酚类包括苯酚、4-硝基酚、3-甲酚、2,4-二氯酚、2,4,6-三氯酚、五氯酚等。《城市供水水质标准》(CJ/T 206—2005)规定氯酚总量(2-氯酚、2,4-二氯酚、2,4,6-三氯酚)浓度不得超过 0.010mg/L[3]。
酚是一种比碳酸还要弱的弱酸,在水的溶解度很小,一般为10-3数量级或更低。因此,测定酚类化合物需要通过合适的方法,将样品中的酚类进行富集和分离,再进行检测。本文通过正交试验来说明利用SPE技术富集水中7种酚类时各因素的主次关系,优化SPE条件,提高样品的回收率,从而提高检测的准确性。
1 材料与方法
1.1 主要仪器与试剂
主要仪器:Agilent 1100高效液相色谱系统(包括二元泵、自动进样器、紫外分光检测器和荧光检测器);美国Agilent公司的ZORABX SB-C18色谱柱;美国Waters公司的真空提取装置;美国Millipiore公司的 Milli-QA超纯水器;Oasis HLB固相萃取小柱(500mg/6 mL,美国Waters公司);Supelclean ENVI-chrom P 固相萃取小柱(500mg/6 mL,美国 Supelco公司);strata C18-E 固相萃取小柱(500mg/6 mL,美国 phenomenex公司);K-D浓缩器。
甲醇、二氯甲烷、四氢呋喃为HPLC级,美国J.T.Baker公司;硫酸为GR级、超纯水、酚类标样,中国计量科学研究院生产。除3-甲基酚的浓度为1100mg/L和2-氯酚为500mg/L外,其余6种酚类(苯酚、4-硝基酚、2,4-二氯酚、2,4,6-三氯酚、五氯酚)的浓度均为1000mg/L。按要求稀释成7种不同浓度绘制标准曲线,按照不同的要求配制不同浓度进行加标回收试验。
1.2 样品的前处理[4]
样品采集在棕色玻璃瓶中,样品量为1000 mL。若样品有余氯,则每升水加1 g无水亚硫酸钠脱氯。水样置于暗处,于4℃冰箱保存,在24h内尽快进行样品预处理。SPE小柱首先用10~15 mL甲醇浸泡20min洗去甲醇后,再用30 mL纯水洗去甲醇。在对SPE柱进行活化和条件化时,不要将柱床抽干,以防止填料层产生裂隙,降低回收率。在水样中加入1 mol硫酸使pH达到2,然后以5 mL/min的速度使水样通过富集柱,富集完毕,通空气净化30min,使吸附好的SPE小柱彻底干燥。SPE小柱直接储存在冰箱中,20 d内将酚类从SPE柱上洗脱下来。SPS小柱用四氢呋喃分2次洗脱,每次1.0 mL,合并后用K-D浓缩器浓缩至0.50 mL,再用四氢呋喃定容至1.0 mL,供HPLC分析用。
1.3 色谱条件
流动相:
A:甲醇/1%(V/V)醋酸;B:纯水/1%(V/V)醋酸。
梯度洗脱:
0min 60%A∶40%B,流速:0.90 mL/min;
7.0 min 35%A∶65%B,流速:0.50 mL/min;
11.5 min 90%A∶10%B,流速:0.90 mL/min;
15.0 min 60%A∶40%B,流速:0.90 mL/min;
分析总时间为15.5min;柱温为35℃;进样量为40μL;检测器为紫外分光检测器。利用紫外检测器具有波长扫描并能在检测中变换波长的特点,取得7种酚类的最佳波长[5],其中苯酚和3-甲基酚为275 nm、2-氯酚为280 nm、2,4-二氯酚和 2,4,6-三氯酚为295 nm、4-硝基酚为310 nm、五氯酚为320 nm。
在上述条件下,7种酚类混标的色谱图如图1所示。
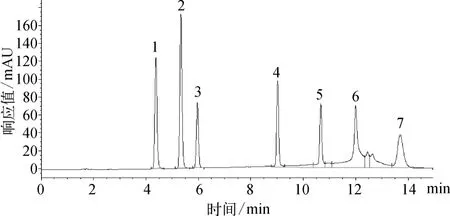
图1 酚类的色谱图Fig.1 Chromatograms of Phenols
1.4 正交试验方案设计
本次试验从富集和洗脱两方面进行2组正交试验。选取SPE小柱、样品的pH、样品流速作为富集正交方案考察的因素。另外选取洗脱溶剂、洗脱体积和洗脱次数三方面作为洗脱正交试验考察的三个因素。每个因素选取三个水平,以测定7种酚类混标加标到某市出厂水中的平均回收率作为考察指标。选用L9(33)正交表安排试验方案,各因素水平表如表1所示,试验结果如表2所示。

表1 因素水平表Tab.1 Factor Levels
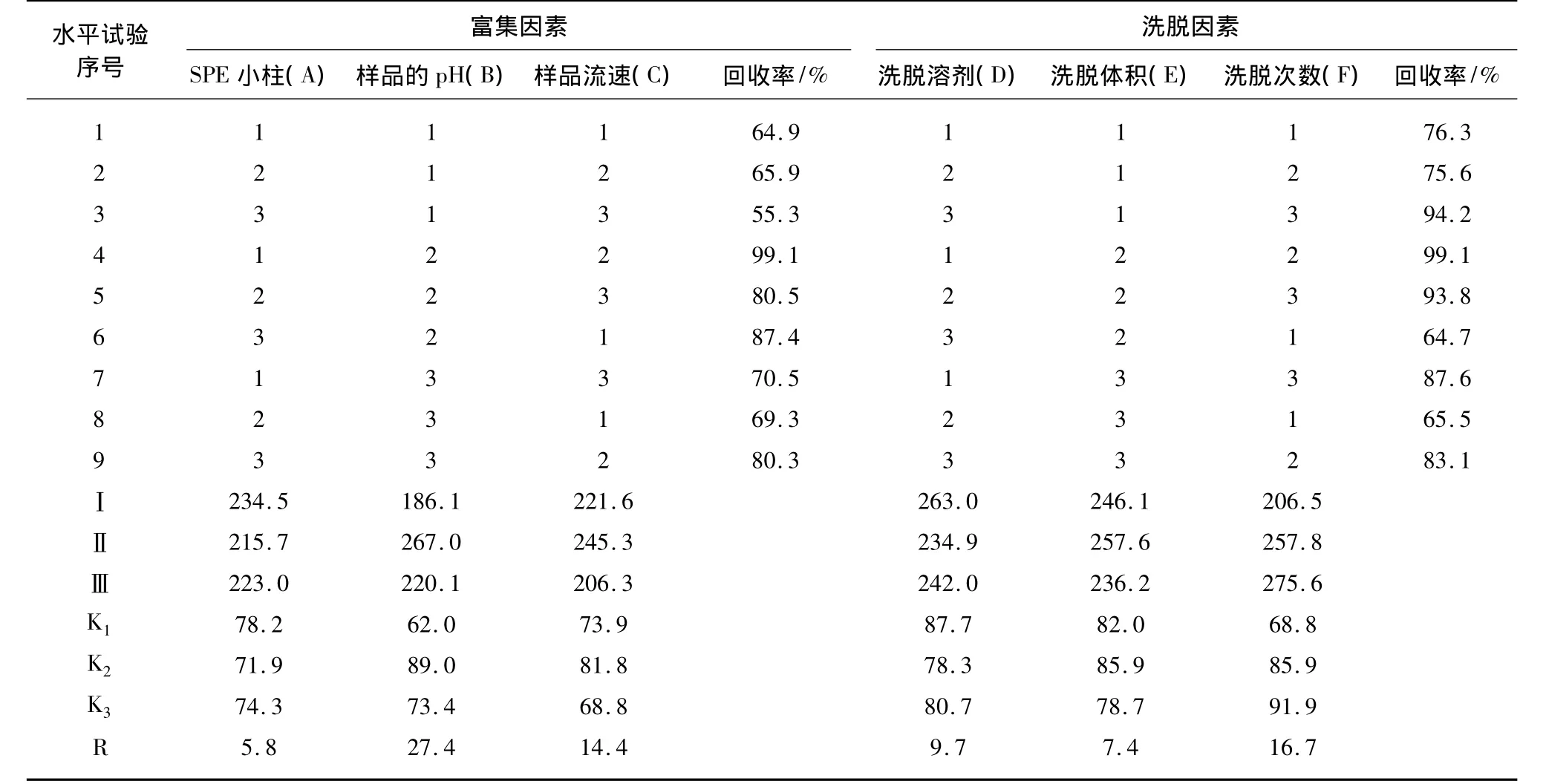
表2 富集因素和洗脱因素正交试验方案及结果Tab.2 Factors Orthogonal Test Scheme and Results of Enrichment and Elution
2 结果和讨论
2.1 正交试验与结果
由表2可知RB>RC>RA,即各因素对富集影响主次为样品的pH、样品流速、SPE小柱,最佳的试验方案为试验4。富集最佳方案:样品的pH为2、SPE小柱为Waters Oasis HLB、样品流速为5 mL/min。表2还表明RF> RD> RE,即各因素对洗脱影响主次为洗脱次数、洗脱溶剂、洗脱体积,最佳的试验方案为试验4。洗脱最佳方案:洗脱溶剂为四氢呋喃,洗脱体积为2.0 mL,分2次进行洗脱。洗脱次数和样品的pH对SPE效果的影响最大,其次为样品的流速,影响稍弱的是洗脱溶剂、洗脱体积、SPE小柱。
2.2 验证试验与结果
根据正交试验的结果,对SPE的主要影响因素,洗脱次数和样品的pH进行验证试验。
2.2.1 洗脱次数的验证试验
配制7种酚类混标加入到某市的出厂水中,进行洗脱次数为1、2、3次的加标回收试验,具体结果如表3所示。结果表明经过2次洗脱后,酚类的回收率在94.2% ~105.1%,符合要求。洗脱次数增加到3次时,回收率提高不明显。
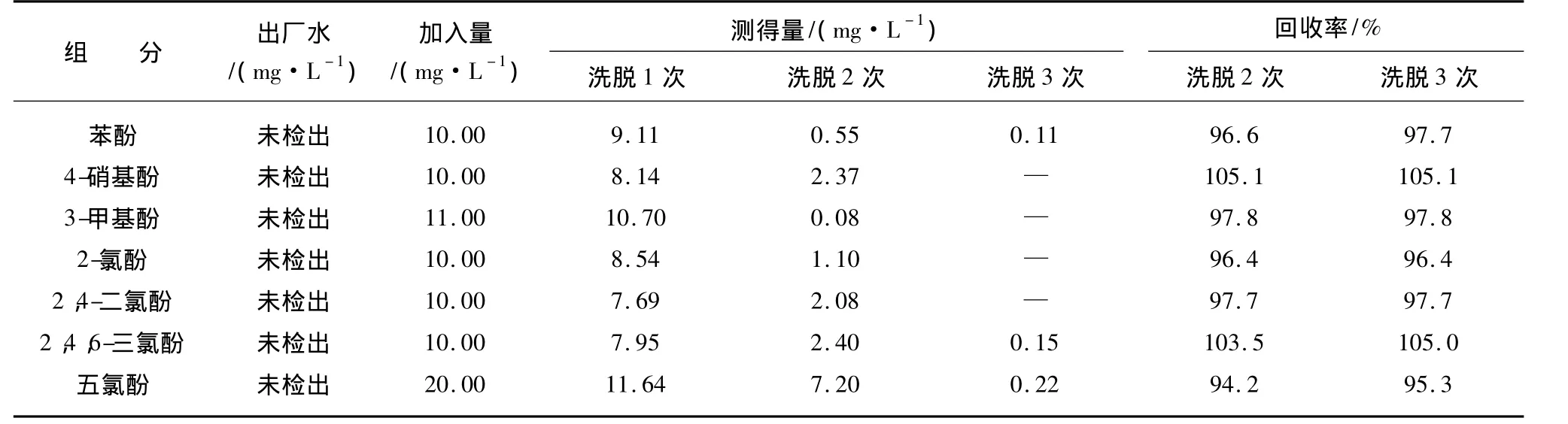
表3 不同洗脱次数的酚类加标回收结果Tab.3 Phenols Standard Addition Recovery Rate under Different Elution Times
2.2.2 样品的pH的验证试验
将7种酚类混标加标到某市的出厂水中,加标浓度与2.3一致。分别把样品pH调至1~11进行加标回收试验[6,7],结果如表 4所示。试验结果表明pH为2时样品的回收率最佳。
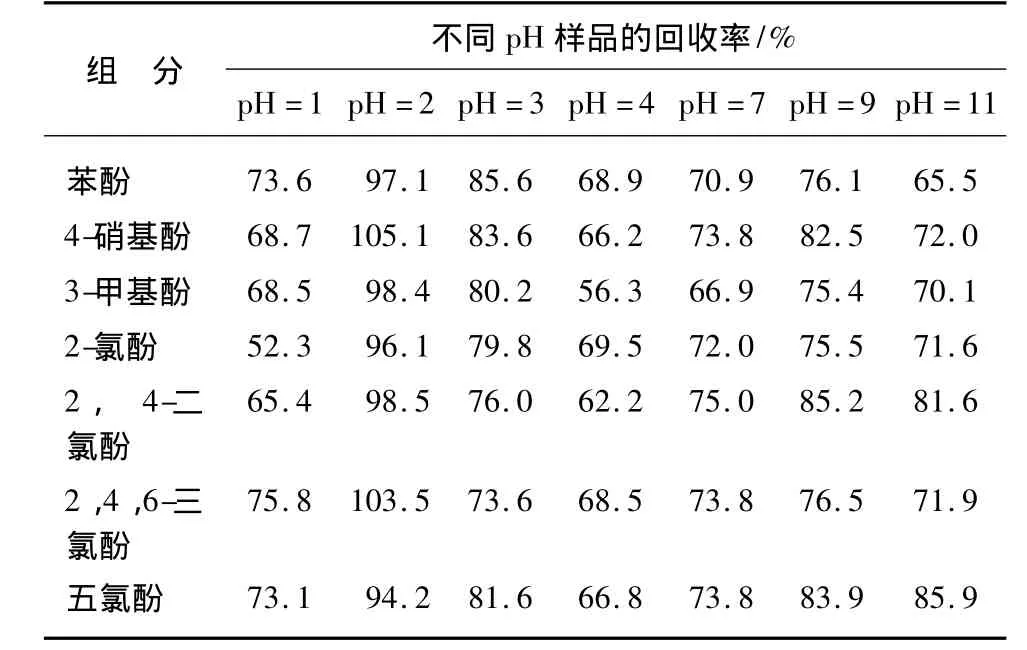
表4 不同pH值样品的加标回收率Tab.4 Standard Addition Recovery Rate under Different pH Values
2.3 标准曲线、检出限、相对标准偏差
按照以上的试验条件,按要求稀释成7种不同浓度的酚类混合标准溶液绘制标准曲线,其中3-甲基酚的标准浓度为0.00、5.50、11.00、16.50、22.00、27.50mg/L;五氯酚的标准浓度为0.00、10.00、20.00、30.00、40.00、50.00mg/L;其余 5 种酚类的标准浓度为0.00、5.00、10.00、15.00、20.00、25.00mg/L。以峰面积Y对应质量浓度X绘制标准曲线,以信噪比S/N=5来计算最低检测浓度,并除以样品的浓缩倍数1000得出方法的检出限,酚类各组分的线性方程如表5所示。由表5可知各组分均相关系数在0.9995~0.9999之间,呈现良好的线性。配制标准曲线上限浓度50%的混合标准加标到某市出厂水中,重复进样6次,计算各组分的相对标准偏差(RSD),结果如表5所示。由表6可知相对标准偏差在1.2% ~3.9%之间,符合检测要求。
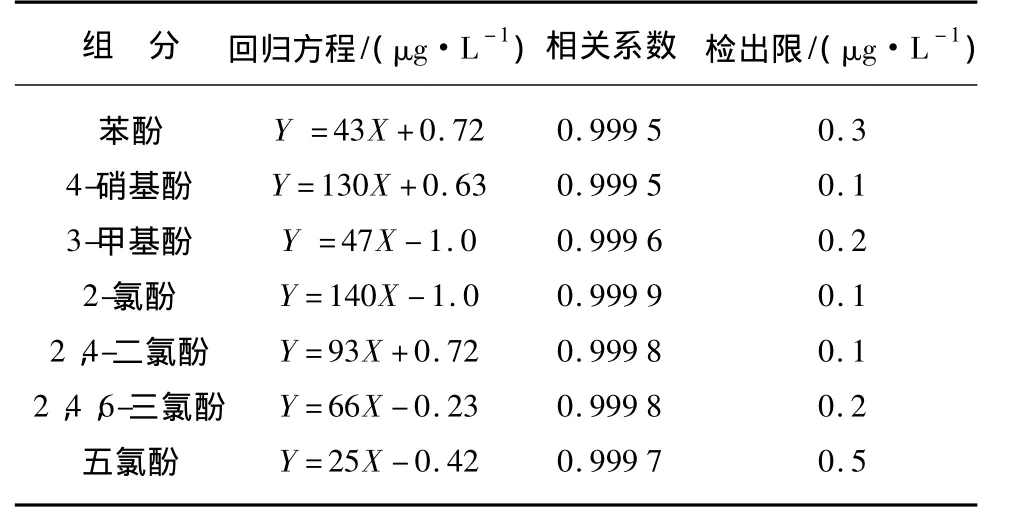
表5 酚类的标准曲线和检出限Tab.5 LinearEquationsand Detection Limits of Phenols
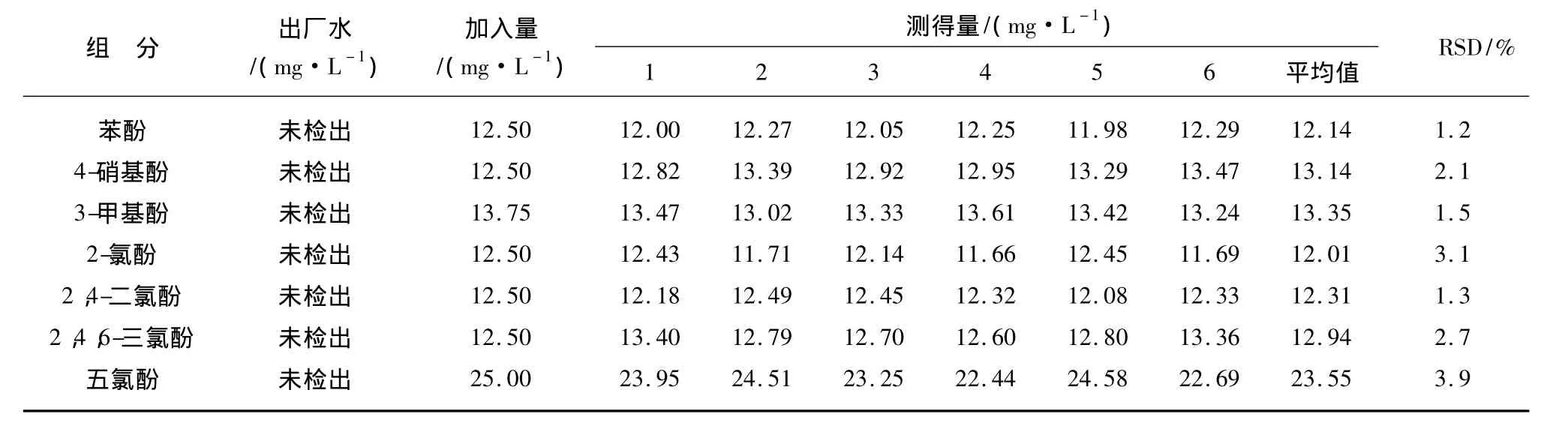
表6 酚类的相对标准偏差Tab.6 Relative Standard Deviation of Phenols
3 结论
通过正交试验和验证试验探讨固相萃取技术富集水中酚类中各种因素的影响,优化得到SPE条件。富集最佳方案:样品的pH为2、SPE小柱为Waters Oasis HLB、样品流速为5 mL/min、洗脱溶剂为四氢呋喃、洗脱体积为2.0 mL,分2次进行洗脱。洗脱次数超过2次或洗脱体积超过2 mL,对酚类的回收率没有提高。在SPE的各因素中样品的pH和洗脱次数对SPE效果的影响最大,其次为样品流速,影响稍弱的是洗脱溶剂、SPE小柱和洗脱体积。各组分均相关系数在0.9995~0.9999之间,呈现良好的线性。相对标准偏差在1.4%~3.9%之间,精密度好。检出限为0.1~0.5μg/L,符合水中酚类测定的要求。
[1]董瑞圣,张立尖.高效液相色谱法测定酚类化合物[J].净水技术,2001,20(1):36-39.
[2]吴梅贤.高效液相色谱法同时测定水中的9种酚类化合物[J].净水技术,2008,27(6):66-68.
[3]CJ/T 206—2005,城市供水水质标准[S].
[4]CJ/T 146—2001,城市供水酚类化合物的测定[S].
[5]王碧云.反相高效液相色谱法测定水中酚类化合物[J].福建分析测试,2006,15(3):20-22.
[6]胡秋芬,杨光宇,黄章杰,等.固相萃取-高效液相色谱法测定水中酚类物质[J].分析化学,2002,30(5):560-563.
[7]胡江涛,张克荣,郑波,等.固相萃取-高效液相色谱法测定自来水中氯代酚[J].中国卫生检验杂志,2005,15(12):1432-1434.

