纳米壳聚糖对桑蚕丝织物抗菌抗皱性能的影响
王 成,林 红,陈宇岳,路艳华
(1.浙江纺织服装职业技术学院纺织学院,浙江宁波315100;2.苏州大学纺织与服装工程学院,江苏苏州215021;3.辽东学院 化工与材料学院,辽宁丹东118001)
桑蚕丝作为一种天然的蛋白质纤维,一直很受人们的欢迎。由于存在易皱、易变形及泛黄等缺点,采用适当的措施来对桑蚕丝进行改性一直是个研究热点。随着科技的发展,目前出现了应用纳米材料、等离子体、微胶囊等技术来改性桑蚕丝制品的技术。
壳聚糖(Chitosan,CS)是天然生物大分子甲壳素脱乙酰基而得的碱性多糖,自然资源非常丰富。由于它无毒、可降解,且含有多种官能团,可进行交联、接枝、酰化、磺化、羧甲基化等多种反应,在医学、印染、化工、食品和农业等方面有广泛的用途[1-2]。纳米壳聚糖作为壳聚糖的一种衍生物,目前在药物载体、基因等方面有广阔的应用前景。由于其兼有壳聚糖和纳米材料的优势特点,本文在前期研究的基础上[3-5],将稳定的纳米壳聚糖处理液应用于桑蚕丝面料的改性整理,来评价其对桑蚕丝面料抗菌抗皱性能上的作用。
1 实验
1.1 实验材料和仪器
材料:桑蚕丝电力纺面料(64 g/m2),壳聚糖(粘均相对分子质量约21 000、脱乙酰度92%),柠檬酸、三聚磷酸钠(TPP)、Tween-80均为化学纯。
仪器:HPPS 5001型激光粒度分布仪(英国马尔文公司),TecnaiG220型透射电镜(美国FEI公司),NICOLET 5700傅立叶红外变换光谱仪(美国热电尼高力公司),D/MAX-3C型X射线衍射仪(日本理学公司),YG541E型折皱回复测定仪(宁波纺织仪器厂)。
1.2 实验方法
1.2.1 纳米壳聚糖处理液的制备
取一定量壳聚糖溶解于乙酸溶液中,加入适量柠檬酸和分散剂Tween-80,溶液在一定转速的搅拌状态下,逐滴加入一定质量分数的三聚磷酸钠(TPP)溶液,使壳聚糖的氨基和三聚磷酸钠的磷酸基团之间的静电吸引作用而产生纳米壳聚糖微粒,从而制得纳米壳聚糖处理液。
1.2.2 纳米壳聚糖的表征
取适量纳米壳聚糖处理液,在HPPS-激光粒径分布仪上测定其粒径分布情况;将一定量纳米壳聚糖处理液加水稀释10倍,取适量滴加于铜网上,用透射电镜观察其形态;利用超离心、低温烘干获得纳米壳聚糖固体颗粒,对其进行红外光谱和X射线衍射测试。
1.2.3 桑蚕丝织物的纳米壳聚糖整理工艺
桑蚕丝织物→按浴比1︰50分别置于质量分数0.2%、0.4%、0.6%、0.8% 的处理液中浸渍60 min→80℃预烘5 min→160℃焙烘3 min→去离子水漂洗→80℃烘干。
1.2.4 织物的抑菌性测试
参照 FZ/T 73023—2006《抗菌针织品》中附录D,以振荡法测定织物的抗菌性能。所用菌种为大肠杆菌和金黄色葡萄球菌,试样的抗菌性能以抑菌率表示,按下式计算:
抑菌率/%=(A-B)/A×100
式中:A为未处理织物上的活菌数;B为处理织物上的活菌数。
1.2.5 织物的抗皱性测试
采用 YG541E型折皱回复测定仪,按照 GB 3819—1997《纺织品织物折痕回复性的测定回复角法》,采用垂直法,以5次测试经+纬的急、缓弹性回复角的平均值作为试样的折皱回复角。
2 结果与分析
2.1 纳米壳聚糖制备和表征
纳米壳聚糖在整理液中良好的分散是应用的前提条件。在制备过程中,加入Tween-80来作为液相分散剂,柠檬酸的引入可在纳米壳聚糖和桑蚕丝面料改性处理时起到交联作用[6]。
由图1可以发现,处理液中纳米壳聚糖的平均粒径是34.26 nm,主要粒径分布在15~45 nm。约41%的粒子尺寸在15~20 nm;约51%在20~30 nm;约7.96%在30~40 nm,约0.04% 大于100 nm。由纳米壳聚糖的透射电镜照片(图2),可以看出分散液中粒子形态接近球形,分散效果较好。
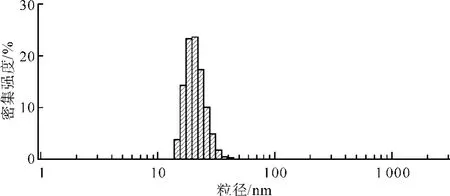
图1 纳米壳聚糖粒径分布情况Fig.1 Particle size distribution of nano-chitosan

图2 纳米壳聚糖的透射电镜照片Fig.2 TEM protogroph of nano-chitosan
2.2 纳米壳聚糖的红外光谱分析
为了进一步表征纳米壳聚糖的生成,利用红外光谱对降解壳聚糖和纳米壳聚糖进行了测试分析。从图3可以看到,降解壳聚糖和纳米壳聚糖的红外光谱有较大不同。壳聚糖与TPP作用后,3 427.2 cm-1处的O—H伸缩振动吸收峰移至3 390.6 cm-1处,向低波数移动了约30 cm-1,这表明形成了较强的分子内和分子间氢键[7-9];1 632.2 cm-1处尖峰消失,1 633.7 cm-1出现了尖峰,并有新峰 1 538.2 cm-1生成,说明三聚磷酸钠上的磷酸基团(—PO-3)与溶解于乙酸中的壳聚糖氨基(—NH+3)发生了作用[10-11],形成的结构;壳聚糖在1 258.2 cm-1处有游离羟基峰,而在生成的纳米壳聚糖红外光谱曲线中消失,这说明游离的羟基峰在纳米粒子中形成了分子间氢键[9]。此外,在1 219.3 cm-1~1 093.1 cm-1处出现了一系列峰,这是由于P—O键的伸缩振动吸收引起的;在1 000 cm-1~850 cm-1处出现峰是由于P—O键弯曲振动吸收引起的。
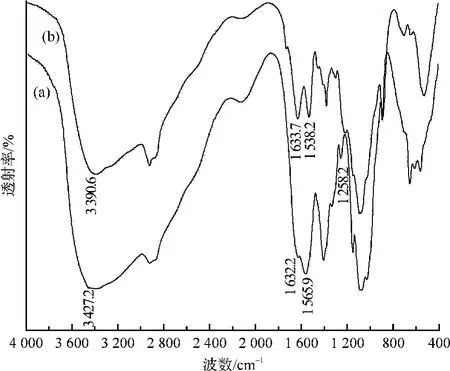
图3 红外光谱对比曲线Fig.3 FTIR spectrum comparison of chitosan and nano-chitosan
2.3 纳米壳聚糖的X衍射分析
从图4 可以看出,壳聚糖在 11.2°和 20.9°处出现了如文献[12-13]所说的两个特征吸收峰,在18.1°处也存在一个吸收峰。在纳米壳聚糖的X衍射曲线上,18.1°处的吸收峰增强,这可能是壳聚糖和TPP作用后的结果;另外,位于20.9°处的吸收峰几乎消失,结晶度显著降低,表明壳聚糖和TPP之间发生了较强的相互作用,与红外分析结果一致[11]。
2.4 纳米壳聚糖整理桑蚕丝织物的抗菌性能
用质量分数为 0.2%、0.4%、0.6%、0.8% 的纳米壳聚糖处理液分别处理桑蚕丝织物,根据1.2.4对桑蚕丝织物进行抑菌性能的测试,结果如图5所示。
由图5可以看出,桑蚕丝织物本身就具有抑菌性,对大肠杆菌和金黄色葡萄球菌的抑制率差不多,分别为30.3%和28.1%。经纳米壳聚糖处理的丝织物抑菌率较桑蚕丝织物有明显提高,这是因为纳米壳聚糖微粒容易渗入织物内部,并与织物纤维牢固结合,呈现出纳米抗菌效应[14]。随着处理液质量分数提高,纳米壳聚糖含量增加对织物抗菌性能提升有较显著的影响。同时还可以看出,处理后的丝织物对金黄色葡萄球菌的抑菌性略高于大肠杆菌的抑菌性。
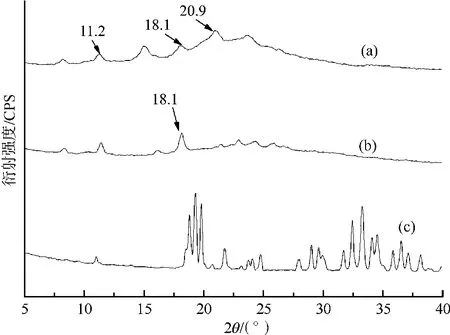
图4 纳米壳聚糖、壳聚糖和TPP的X射线衍射曲线Fig.4 X-ray diffraction curve of nano-chitosan,chitosan and TPP
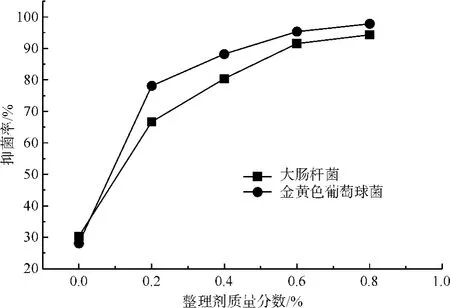
图5 不同质量分数处理液整理桑蚕丝织物的抗菌性能Fig.5 Anti-bacterial performance of mulberry silk fabrics treated by treating fluids with different mass fractions
2.5 纳米壳聚糖整理桑蚕丝织物的抗皱性能
用质量分数为 0.2%、0.4%、0.6%、0.8% 的纳米壳聚糖处理液分别处理桑蚕丝织物,根据1.2.5对桑蚕丝织物进行折皱性能的测试,结果如图6所示。
由图6可以看出,经不同质量分数的纳米壳聚糖处理后,桑蚕丝织物的急、缓弹性折皱回复角有了
不同程度的提高,抗皱性有所改善,这是因为纳米壳聚糖在丝纤维内部沉积后进一步提高丝纤维,大分子间盐键、氢键和范德华力,使其具有足够的约束力回到原来的位置,从而起到防皱作用。同时也可以发现,但质量分数超过0.2%后,随着纳米壳聚糖质量分数提高,桑蚕丝织物抗皱效果略有提高,但变化并不明显。
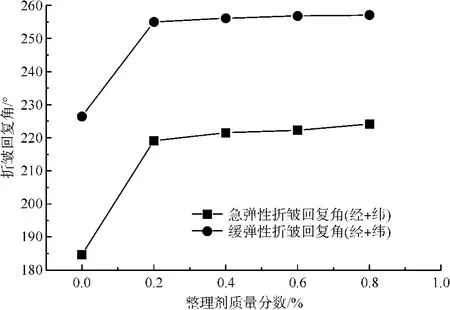
图6 不同质量分数处理液整理桑蚕丝织物的抗皱性能Fig.6 Wrinkle-resistant performance of mulberry silk fabric treated by treating fluids with different mass fractions
3 结论
1)利用离子凝胶法可以成功制备纳米壳聚糖,并呈现良好的分散和稳定性。
2)经纳米壳聚糖处理后的桑蚕丝织物在抗菌性能上有明显提高,而且处理液质量分数提高对织物抗菌性能提升有较显著的影响。
3)经纳米壳聚糖处理后的桑蚕丝织物在抗皱性能上有明显提高,但超过0.2%后,纳米壳聚糖质量分数的提高对桑蚕丝织物抗皱效果的改善并不明显。
[1]NO H K,PARK N Y,LEE S H.Antibacterial activities of chitosan and chitosan oligomers with different molecular weights on spoilage bacteria isolated from tofu[J].Journal of Food Science,2002,67(4):1551-1514.
[2]JIONG Y J,CHA S Y,YU W R,et al.Changes in the mechanical properties of chitosan-treated wool fabric[J].Textile Research Journal,2002,72(1):70-76.
[3]王成,陈宇岳,路艳华.纳米壳聚糖的制备及其对真丝纤维性能的影响[J].丝绸,2006(8):32-34.WANG Cheng,CHEN Yuyue,LU Yanhua.Preparation of chitosan nanoparticles and their effect on performance of silk fiber[J].Journal of Silk,2006(8):32-34.
[4]王成,林红,路艳华,等.经纳米壳聚糖处理的桑蚕丝纤维聚集态结构[J].纺织学报,2007,28(9):1-3.WANG Cheng,LIN Hong,LU Yanhua,et al.Aggregation structure of B.mori silk treated with chitosan nanoparticle dispersed solution[J].Journal of Textile Research,2007,28(9):1-3.
[5]WANG C,LIN H,CHEN Y Y.Study on the preparation of steady-state chitosan nanoparticle as silk-fabric finishing agent[J].Advanced Materials Research,2011,175-176:745-749.
[6]李维贤,师严明,赵耀明.壳聚糖的柠檬酸溶液用于真丝抗皱的研究[J].印染,2001(11):5-7.LI Weixian,SHI Yanming,ZHAO Yaoming.Studies on antiwrinkle of silk with CA solution[J].Journal of Dyeing and Finishing,2001(11):5-7.
[7]YU J H,DU Y M,ZHENG H.Blend films of Chitosan/Gelation[J].Journal of Wuhan University of Technology:Materials Science Edition,1999,45(4):440-444.
[8]CHEN X,LI W J,YU T Y.Investigation of adsorption properties of Chitosan/Cu(II)complex in Chitosan-Silk fibroin blend membranes as adsorbents for urea[J].Chinese Journal of Biomedical Engineering,1997,16(3):284-288.
[9]BROW D D,FLORD A J,Sainburg M.Organic Spectroscopy[M].New York:John Wiley Inc,1988:24-50.
[10]徐咏梅,杜予民.低分子量壳聚糖纳米粒子缓释药物性能的研究[J].武汉大学学报:理学版,2003,49(4):470-474.XU Yongmei,DU Yumin.Studies on controlled release of protein drugs from chitosan nanoparticles with low molecular weight[J].Journal of Wuhan University of Technology:Edition of Science,2003,49(4):470-474.

