表面功能化磁性纳米微球的制备研究
焦艳华,郭卫强,梁媛媛
(1. 杭州师范大学生物医药与健康研究中心,浙江 杭州 310012;2. 浙江大学化学生物工程系,浙江 杭州 310027)
表面功能化磁性纳米微球的制备研究
焦艳华1,郭卫强1,梁媛媛2
(1. 杭州师范大学生物医药与健康研究中心,浙江 杭州 310012;2. 浙江大学化学生物工程系,浙江 杭州 310027)
以苯乙烯和丙烯酸作为聚合单体,以对氯甲基苯甲酸为引发剂进行原子转移自由基聚合(ATRP)反应,详细讨论了影响聚合反应的因素如反应时间、反应温度、投料配比等,找到了较优的实验条件.制备得到的磁性高分子复合微球,其表面羧基含量最高可达0.50 mmol/g,SEM照片显示磁微球的平均粒径为50 nm左右,粒径分布比较均匀.
ATRP;磁性高分子微球;合成
磁性高分子复合微球由高分子化合物(或聚合物)外壳与无机磁性内核两部分复合而成,其性质依赖于无机磁性内核、高分子化合物外壳的性质及其复合机制.这种复合微球因其内部有磁性物质存在,在外加磁场的作用下可以快速地分离,有效地富集、回收和再利用,因此,在环境检测、免疫分析、生物工程、蛋白分离等众多领域已有广泛的应用[1-5].但目前磁性复合微球的制备中还存在许多急需解决的问题,如磁含量不高、粒径不均匀等.必须探索新的磁性复合微球制备方法,以期制备出粒径较小、粒径分布窄、且表面性能优异的磁性高分子微球,以保证较多特异抗体(抗原)在磁性纳米粒子表面的有效固定.
原子转移自由基聚合(ATRP)作为近年来发展起来的一种活性/可控自由基聚合方法[6],不仅兼具活性聚合和自由基聚合的一些优点,而且适用单体广、操作简单、反应条件相对温和,使人们能够在较为简便的条件下得到相对分子质量可控、相对分子质量分布较窄的聚合物,同时可进行复杂聚合物的合成和设计[7-9],
本文采用ATRP技术制备磁性高分子复合微球,并在此基础上详细讨论了ATRP法制备磁性复合微球的影响因素,如反应时间、温度、投料比及搅拌转速等,得到了较优的制备条件.
1 实验部分
1.1 试剂
FeCl2·4H2O,AR,上海强顺化工试剂有限公司;FeCl3·6H2O,AR,上海强顺化工试剂有限公司;氨水,AR,江苏强盛功能化学股份有限公司;对氯甲基苯甲酸,98%,安耐吉化学;丙烯酸,CP,上海五联化工厂;苯乙烯,CP,阿拉丁试剂公司;二联吡啶(BPY),AR,阿拉丁试剂公司;氯化亚铜,AR,阿拉丁试剂公司;环己酮,AR,杭州高晶精细化工有限公司.
1.2 制备方法
1.2.1 Fe3O4磁性粒子的制备
Fe3O4磁性粒子采用化学共沉淀法制备[10]:称取0.025 mol/L的FeC12·4H2O和0.05 mol/L的FeC13·6H2O各50 mL加入到反应器中,在N2保护下,加入约30 mL质量分数为25%~28%的浓氨水并检测pH值,至体系pH>10,将温度升到70 ℃,搅拌,恒温反应1 h.磁性分离,然后用超纯水与无水乙醇交替洗多次,直至中性,真空冷冻干燥过夜,研磨粉碎即得纳米Fe3O4磁性粒子.
1.2.2 对氯甲基苯甲酸的包覆
在100 mL三口烧瓶中,加入50 mL蒸馏水,取前面制备得到的纳米Fe3O4磁性粒子1.0 g及对氯甲基苯甲酸0.5 g,加热到80 ℃,机械搅拌6 h后,磁性分离,洗涤数次,制备得到表面包覆了一层对氯甲基苯甲酸的Fe3O4磁性粒子.
1.2.3 Fe3O4@P(St-AA)磁性微球的制备
取100 mL三口烧瓶,加入40 mL环己酮,通氮气15 min,取前面制备得到的包覆了对氯甲基苯甲酸的纳米Fe3O4磁性粒子1 g,BPY 0.35 g,CuCl 0.08 g,苯乙烯6 mL及丙烯酸3 mL.以220 r/min的速度机械搅拌,加热到90 ℃,恒温反应12 h后,冷却到室温,磁性分离,清洗数次,便得到表面富含羧基的聚苯乙烯磁性微球.
1.2.4 磁性高分子微球表面羧基含量的测定
对于磁性高分子微球表面羧基含量的测定,本文选择用NaOH来滴定.用电子分析天平称取一定量的样品放入100 mL锥形瓶中,加入20 mL超纯水,超声波分散,磁分离清洗3次后加入20 mL的甲醇,然后向锥形瓶中滴加酚酞,用0.12 mol/L的NaOH滴定,记录至变色消耗的NaOH的体积V.用同样的方法对甲醇空白液进行空白滴定,记录此时消耗的NaOH的体积V0.然后计算测得的羧基含量(mmol/g):CCOOH=(V-V0)×C/m,其中,V、V0为二者消耗NaOH的体积(L),C为NaOH溶液的浓度(mol/L),m为加入的磁性高分子复合微球的质量.
2 结果与讨论
以表面包覆有引发剂对氯甲基苯甲酸的磁性Fe3O4粒子为种子,选用苯乙烯及丙烯酸作为单体进行原子转移自由基聚合(ATRP)反应,并对直接影响聚合反应效率的因素(如反应温度、时间、投料配比等)进行了系统研究.
2.1 反应温度对磁微球表面羧基含量的影响
磁性微球的生物分离功能是通过表面的功能基来实现的,表面功能基团含量的多少是磁性微球的一个重要的性能指标,含量越高才能保证较多特异抗体(抗原)在磁性粒子表面的有效固定,因此本文以磁性微球表面羧基的含量作为考察参数,优化制备工艺.
具体的实验条件如1.2.3中所述,在其他试剂和反应条件不变的情况下,仅改变反应的温度,分别设定反应的温度为70、80、90、100、120℃,结果如图1所示.
从图1中可以看出,随着反应温度的升高,羧基含量先升高后降低,反应的最佳温度为90 ℃左右.这可能是因为随着温度的升高,各分子的活跃程度、运动能力大幅增强,但是在超过90 ℃之后,由于分子的运动能力太过强大,反而不能让单体聚合在磁微球表面.
2.2 反应时间对磁微球表面羧基含量的影响
按照实验部分1.2.3方法,在其他试剂和反应条件不变的情况下,改变反应的时间,分别设定反应的时间为8、10、12、16、24 h,结果如图2所示.
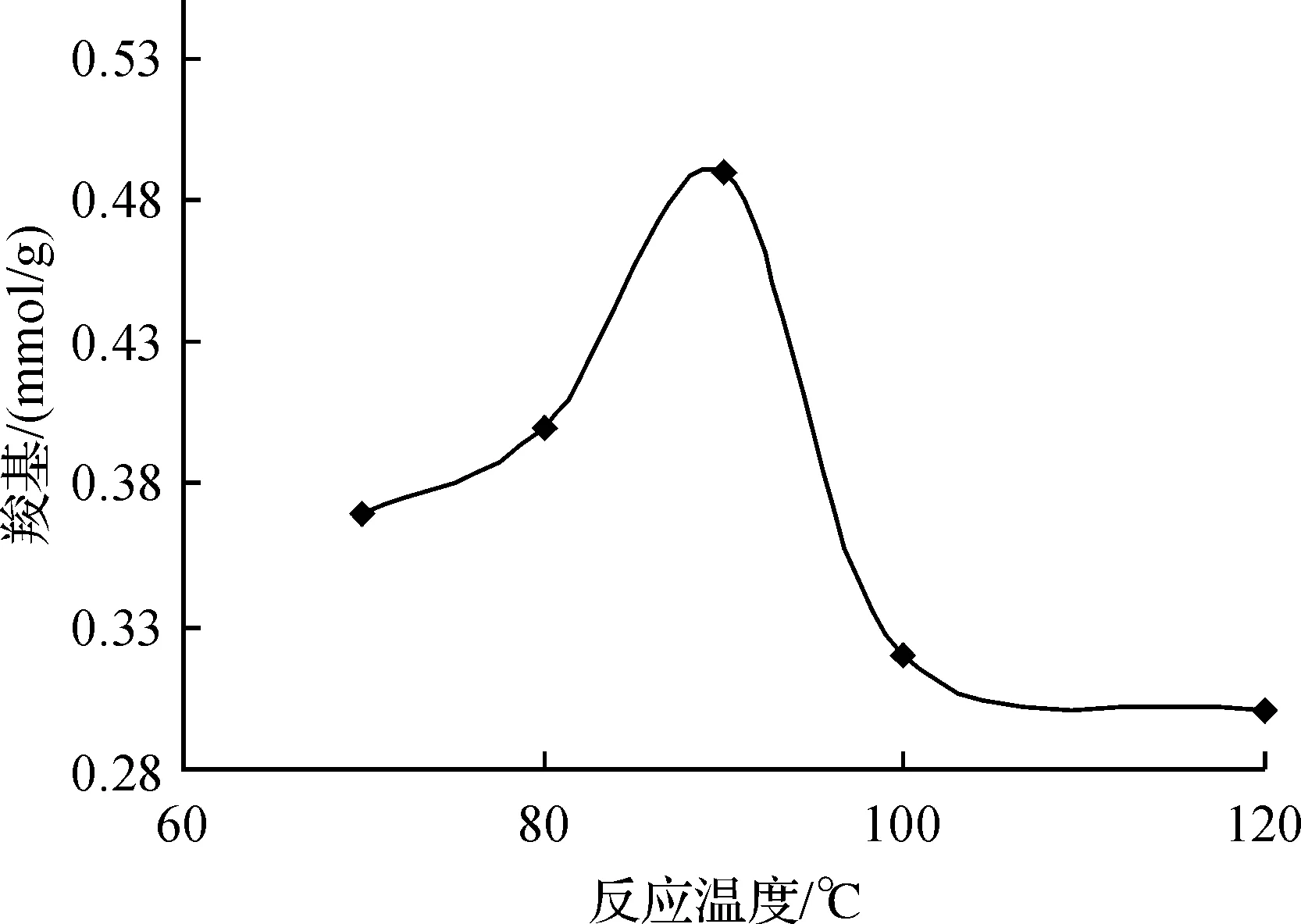
图1 反应温度对磁微球表面羧基含量的影响Fig. 1 Effect of reaction temperature on surface carboxyl amount

图2 反应时间对磁性微球表面羧基含量的影响Fig. 2 Effect of reaction time on surface carboxyl amount
从图2可以看出,在反应时间从8 h延长到24 h的过程中,磁性微球表面的羧基含量先升高,再逐渐下降.在反应时间为12 h左右时,磁微球表面的羧基含量达到最大值.因此选择12 h为最佳反应时间.
2.3 反应原料的投入量比对磁微球表面羧基含量的影响
根据实验部分1.2.3方法,在其他试剂和条件不变的情况下,改变反应的单体苯乙烯和丙烯酸的量比,分别设定苯乙烯和丙烯酸的体积比为1、1.5、2、2.5、3,结果如图3所示.随着苯乙烯体积比的增大,磁微球表面的羧基含量逐渐增大,但是增长的量越来越少.这可能是在聚合的过程中,苯乙烯优先于丙烯酸结合到磁微球表面,但随着苯乙烯包覆的增加,丙烯酸聚合在磁微球表面的效率也会得到提高,从而导致在丙烯酸单体总量不增加的条件下,磁微球表面的羧基含量得到了提升.因此,投料比以V(苯乙烯)∶V(丙烯酸)=2比较好.
2.4 搅拌转速对磁微球表面羧基含量的影响
按照实验部分1.2.3方法,改变机械搅拌的搅拌速度,分别设定反应的搅拌速度为160、220、290、350、420 r/min,结果如图4所示.随着搅拌速度的提升,磁性微球表面羧基的含量先升高后降低再又升高,搅拌速度对磁性微球表面羧基含量的影响还是很大的,所以在实验过程中须严格控制搅拌速度不变,这样才能保证实验结果的可信性.搅拌速度为220 r/min时比较好.

图3 原料投量比对磁性微球表面羧基含量的影响Fig. 3 Effect of reactants ratio on surface carboxyl amount

图4 搅拌速度对磁性微球表面羧基含量的影响Fig. 4 Effect of stirring speed on surface carboxyl amount
通过以上讨论可以得出,ATRP法制备磁性高分子复合微球的较优条件为:反应温度90 ℃左右,反应时间12 h左右,V(单体苯乙烯)∶V(丙烯酸)=2∶1,在该条件下制备得到的磁性高分子复合微球其表面羧基含量最高可达0.50 mmol/g,其扫描电镜(SEM)照片如图5所示.从图中可以看出磁微球的平均粒径约50 nm,粒径分布比较均匀.

图5 高分子磁性微球的SEM照片Fig. 5 The SEM photograph of magnetic polymer micropheres
3 结 论
利用对氯甲基苯甲酸引发苯乙烯和丙烯酸ATRP聚合反应,最优反应时间为12 h左右,反应温度为90 ℃,搅拌转速为220 r/min.制备得到的磁性高分子复合微球其表面羧基含量最高可达0.50 mmol/g,SEM照片显示磁微球的平均粒径为50 nm左右,粒径分布比较均匀.
[1] 盖青青,屈锋,梅芳,等.磁性粒子在蛋白质分离纯化中的应用[J].化学通报,2010,73(2):99-105.
[2] 顾银君,王秀玲,赵勤,等.荧光磁性双功能树状分子微球的制备与表征[J].高等学校化学学报,2012,33(5):885-891.
[3] 熊国权,周红雨.磁分离技术及其在食源性致病菌监测中的应用[J].中国卫生检验杂志,2008,18(12):2840-2842.
[4] Eberbeck D, Dennis C L, Huls N F,etal. Multicore magnetic nanoparticles for magnetic particle imaging[J]. IEEE Transantions on Magnetics,2013,49(1):269-274.
[5] Mok H, Zhang Miqin. Superparamagnetic iron oxide nanoparticle-based delivery systems for biotherapeutics[J]. Expert Opinion on Drug Delivery,2013,10(1):73-87.
[6] Wang Jinshan,Matyjaszewski K. Controlled/living radical polymerization.Atom transfer radical polymerizaion in the presence of transition-metal complexes[J]. J Am Chem Soc,1995,117(20):5614-5615.
[7] 高超,钱卉,王寿柏,等.用ATRP法构筑核壳型梯度极性的多羟基多臂星状超支化聚合物及聚合物刷:双层聚合物刷的合成与表征[J].高分子学报,2004(6):877-883.
[8] 华慢,杨伟,薛乔,等.两亲性嵌段共聚物PS-b-PMAA的合成与胶束化行为研究[J].化学学报,2005,63(7):631-636.
[9] Polyxeni M,Stergios P,Nikos H. Mutlifunctional ATRP initiators:Synthesis of four-arm star homopolymers of methyl methacrylate and graft copolymers of polystyrene and poly(t-butyl methacrylate)[J]. J Polym Sci Polym Chem,2001,39(5):650-655.
[10] 高道江,王建华.超微磁性Fe3O4粒子的制备[J].四川师范大学学报:自然科学版,1997,20(6):94-97.
ResearchonthePreparationofSurface-functionalMagneticPolymerMicropheres
JIAO Yanhua1, GUO Weiqiang1, LIANG Yuanyuan2
(1.Center for Biomedicine and Health, Hangzhou Normal University, Hangzhou 310012, China; 2.Department of Chemical and Biological Engineering, Zhejiang University, Hangzhou 310027, China)
Using styrene (St) and acrylic acid(AA) as monomers, the magnetic polymer microspheres P(St-AA)/Fe3O4were synthesized by atom transfer radical polymerization(ATRP) with an initiator 4-chloromethyl benzoic acid. The paper discussed some influencing factors, such as reaction temperature, reaction time and molar ratio of reactants in detail, and found optimum experiment conditions. The surface carboxyl content of the prepared microspheres is up to 0.50 mmol/g, and the average particle size is about 50 nm, the distribution of which is relatively uniform.
ATRP; magnetic polymer microspheres; synthesis
2013-04-11
国家自然科学基金项目(21005025); 浙江省公益技术应用研究项目(2010C33132);浙江省博士后科研项目择优资助(Bsh1201028);杭州市科技局社会发展项目(20101133N04).
焦艳华(1976—),女,副研究员,博士,主要从事化学发光免疫分析、功能性化合物的合成及应用研究.E-mail:yhjiao@hznu.edu.cn
10.3969/j.issn.1674-232X.2013.04.004
O631;TQ316.3
A
1674-232X(2013)04-0304-04

