鱼藤属植物的化学成分及药理作用研究进展
杨巡纭,马瑞婧,王利勤,李 婷
云南师范大学化学化工学院,昆明 650092
豆科(Leguminosae)鱼藤属(Derris)植物主要分布在亚洲的热带和亚热带,大洋洲、南美洲和非洲也有分布。全球约有800种,我国有25种,2变种[1]。鱼藤属植物大多为民间药用植物,如D.trifoliata以全株及根状茎入药,主要治疗散瘀止痛、杀虫止痒、跌打肿痛、关节疼痛、疥癣和湿疹。鱼藤属植物也是使用较广泛的植物源农药,主要以杀虫为主,也作为毒鱼剂使用。鱼藤属植物还具有抗氧化、抗菌、抗炎、抗癌等作用。本文针对鱼藤属植物的化学成分及药理活性研究现状进行综述。
1 化学成分
据国内外报道的文献,鱼藤属植物的化学成分主要以黄酮、异黄酮、鱼藤酮为主,还有萜类,单苯环类和脂肪族类化合物。主要对D.scandens,D.elliptica,D.trifoliata,D.robusta,D.laxiflora,D.indica,D.malaccensis,D.reticulata几种植物进行了深入的研究。其余几种研究较少。
1.1 酚性类成分
1.1.1 黄酮类化合物
该属植物中分离得到的黄酮类化合物大部分化合物在C-6位上或C-8位有异戊烯基取代,或C-6,C-8上的异戊烯基与C-7上的羟基形成吡喃环或呋喃环。
1.1.1.1 黄酮及其衍生物
由鱼藤属植物中发现的黄酮类化合物很多,其中黄酮及其衍生物就有63个(1~63),大多为从该属中得到的新化合物(图1)。
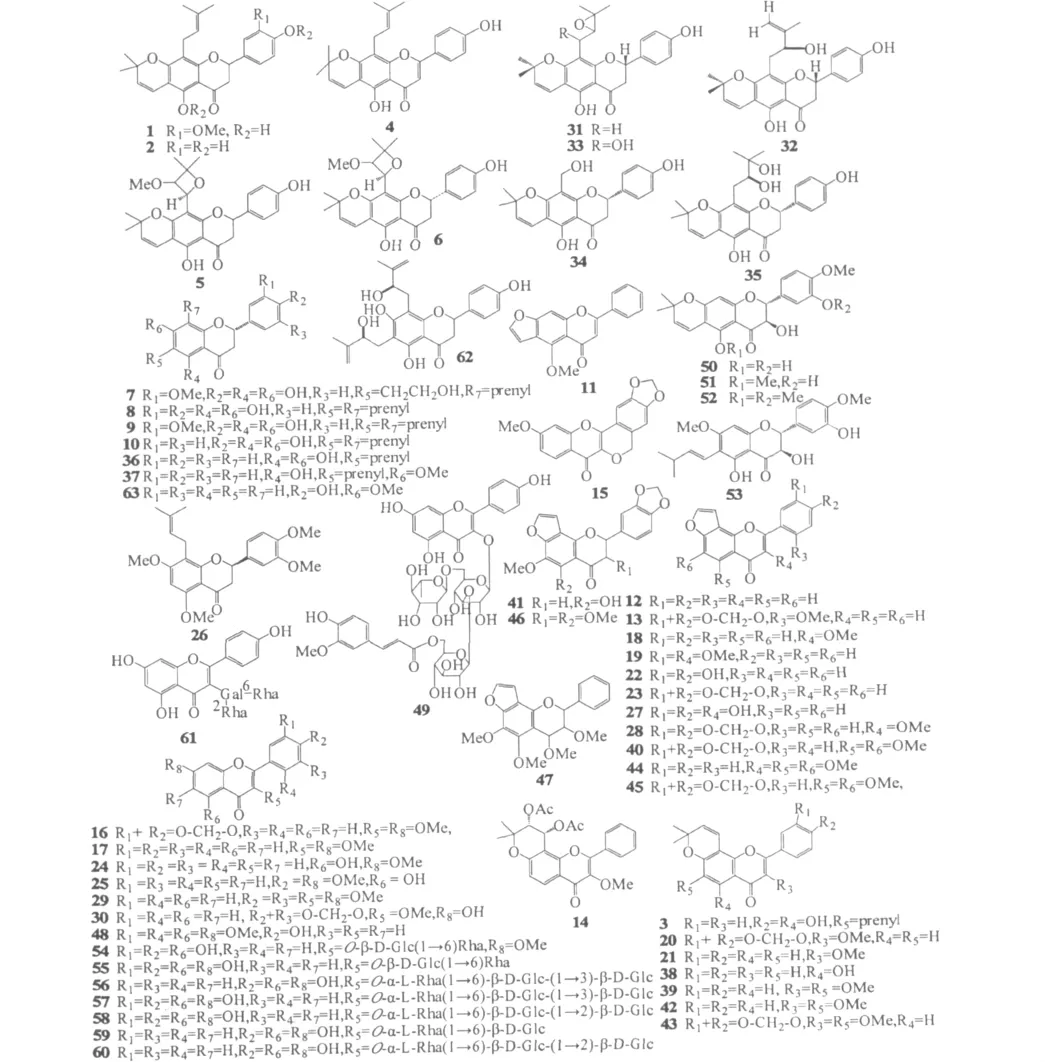
图1 鱼藤属植物中的黄酮及其衍生物Fig.1 Structures of flavonoids from Derris
D.laxiflora[2-4]中得到的3'-methoxylupinifolin(1)、lupinifolin(2)、laxifolin(3)、Isolaxifolin(4)、derriflavanone或 epi-derriflavanone(5或 6)、laxiflorin(7)、6,8-diprenyleriodictyol(8)、hiravanone(9)、senegalensein(10),其中化合物2和3分别也从D.reticulata[5]和 D.scandens[6]中分离得到。2006 年,Koysomboon S[7]等人从鱼藤属植物 D.indica 中得到11个黄酮类化合物,分别为pinnatin(11)、lacheolatin B(12)、2'-methoxy-4',5'-methylenedioxyfurano[7,8:4'',5'']-flavone(13)、3-methoxy-(3'',4''-dihydro-3'',4''-diacetoxy)-2'',2''-dimethylpyrano-(7,8:5'',6'')-flavone(14)、3,4-methylenedioxy-10-methoxy-7-oxo[2]benzopyrano[4,3-b]benzopyran(15)、desmethoxy kanugin(16)、3,7-dimethoxyflavone(17)、karanjin(18)、pachycarin D(19)、pongachromene(20)、karanjachromene(21),其中化合物 14 ~21为黄酮醇类化合物,化合物14和15是从该植物中得到的新化合物。2009年,Rao RR[8]等人也对该植物进行了研究,从中得到了9个黄酮类化合物,即3',4'-dihydroxy-4H-furo[2,3-h]chromen-4-one(22)、pongaglabrone(23)、7-O-methylchrysin(24)、7,4'-dimethoxy-5-hydroxyflavone(25)、pongapinone B(26)、3,3',4'-trihydroxy-4H-furo[2,3-h]chromen-4-one(27)、pongapin(28)、fisetin tetramethyl ether(29)、3-methoxy-7-hydroxy-3',4'-methylenedioxyflavone(30),其中化合物22和27是从该属中得到的新的黄酮类化合物。此外,D.reticulata[9,5,10]中得到的 2''',3'''-epoxylupinifolin(31)、dereticulatin(32)、1'''-hydroxy-2''',3'''-epoxylupinifolin(33)、4',5-dihydroxy-8-hydroxymethyl-6'',6''-dimethylpyrano[2'',3'':7,6]flavanone(34)、2'',3''-dihydroxylupinefolin(35);D.rariflora[11]中 的 (2S)-5,7-dihydroxy-6-prenylflavanone(36)、(2S)-5-hydroxy-7-methoxy-6-prenylflavanone(37);D.obtusa[12]中的 5-hydroxy-6'',6''-diethylchromeno-(7,8,2'',3'')-flavone(38)、3,6-dimethoxy-6'',6''-dimethylchromeno-(7,8,2'',3'')-flavone(39),其中化合物39为黄酮醇衍生物;D.araripensis[13]中的 methylenedioxy-(3',4')-5,6-dimethoxyfurano-(7,8,2'',3'')-flavone(40)、methylenedioxy-(3',4')-5-hydroxy-6-methoxy-furano(7,8,2'',3'')-flavanone(41)、3,6-dimethoxy-6'',6''-dimethylchromeno-(7,8,2'',2'')-flavone(42)、methylenedioxy-(3,4)-3,6-dimethoxy-6'',6''-dimethylchromeno-(7,8,2'',3'')-flavone(43)、3,5,6-trimethoxyfurano-(7,8,2'',3'')-flavone(44)、methylenedioxy-(3',4')-3,5,6-trimethoxyfurano-(7,8,2'',3'')-fravone(45)、3,5,6-trimethoxyfurano-(7,8,2'',3'')-flavanone(46)、3,4,5,6-tetramethoxyfurano-(7,8,2'',3'')-flavanone(47);D.robusta[14]中得到的 4'-hydroxy-5,7,3',6'-tetramethoxyflavone(48)。另外,还从 D.triofoliata[15]中得到了1个新的黄酮醇苷kaempferol 3-O-[(6''''-feruloyl)-β-D-glucopyranosyl-(1→3)]-[α-L-rhamnopyranosyl-(1→6)]-β-D-glucopyranoside(49);D.urucu[16]中得到的 urucuol(A-C)(50 ~ 52)、isotirumalin(53);D.trifoliata[17,18,19]中的 rhamnetin 3-O-β-neohesperidoside(54)、quercetin 3-O-β-neohesperidoside(55)、kaempferol-3-O-α-L-rhamnopyranosyl-(1→6)-β-D-glucopyranosyl-(1→3)-β-D-glucopyranoside(56)、quercetin-3-O-α-L-rhamnopyranosyl-(1→6)-β-D-glucopyranosyl-(1→3)-β-D-glucopyranoside(57)、quercetin-3-O-α-L-rhamnopyranosyl-(1 →6)-β-D-glucopyranosyl-(1 → 2)-β-D-glucopyranoside(58)、kaempferol-3-O-α-L-rhamnopyranosyl-(1 → 6)-β-D-glucopyranoside(59)、kaempferol-3-O-α-L-rhamnopyranosyl-(1 →6)-β-D-glucopyranosyl-(1→2)-β-D-glucopyranoside(60)、mauritianin(61)。2012 年,Cheng J[20]等人也对该植物进行研究,从中分离得到了1个新的化合物4',5,7-trihydro-xy-6,8-di-(2-hydroxy-3-methyl but-3-enyl)-flavanone(62)和已知化合物4'-hydroxy-7-meth-oxy-flavanone(63)。
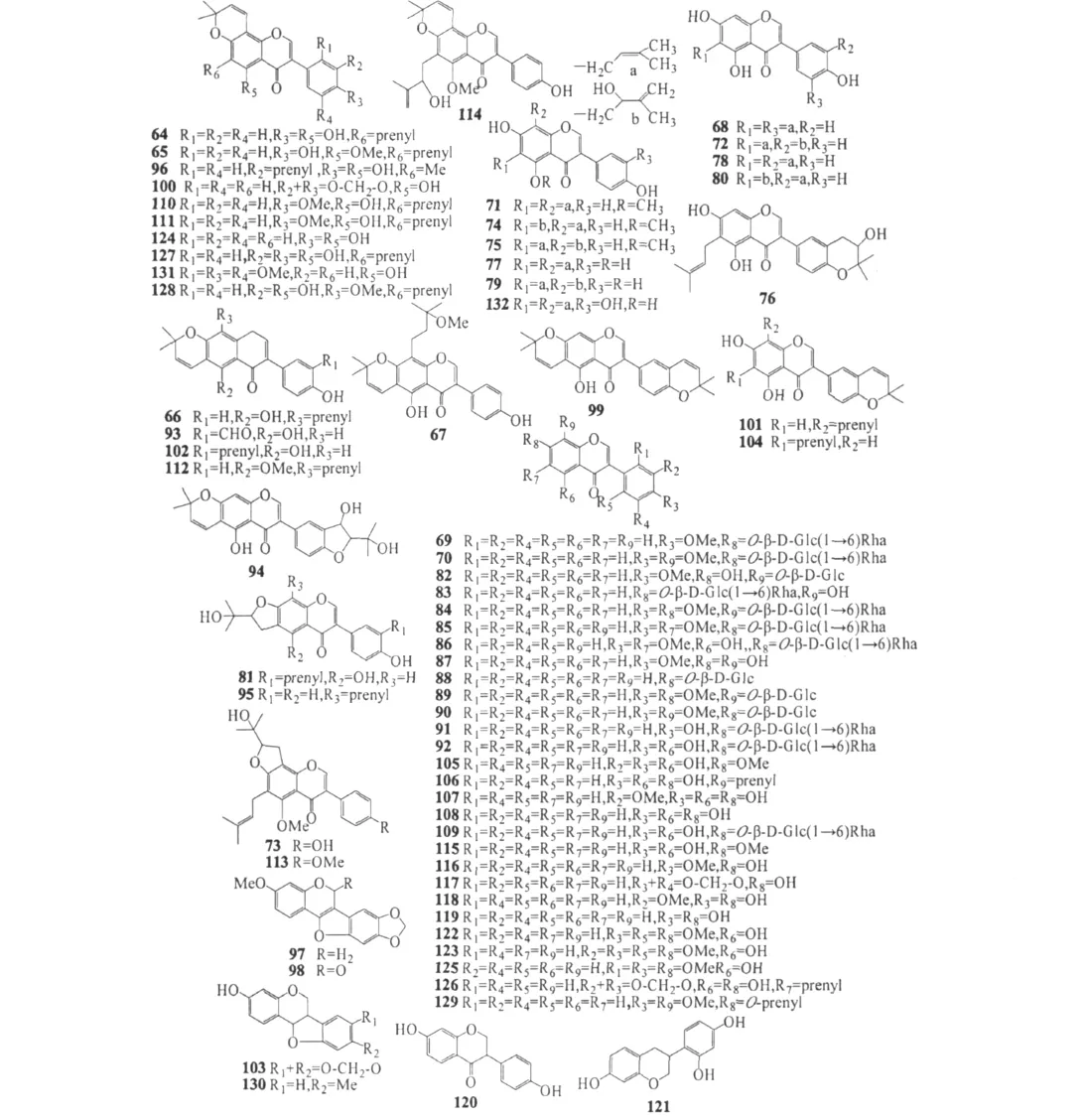
图2 鱼藤属植物中的异黄酮及其衍生物Fig.2 Structures of isoflavonoids from Derris
1.1.1.2 异黄酮及其衍生物
由鱼藤属植物中分离得到的异黄酮及其衍生物有69 个(64 ~ 132)(图 2),其中从 D.scandens[21-30]中就得到了51个。即osajin(64)、scandinone(65)、scandenone(66)、eturunagarone(67)、3'-γ,γ-dimethylallylwighteone(68)、derriscanoside(A-B)(69 ~70)、derrisisoflavone(A-F)(71 ~76)、5,7,4'-trihydroxy-6,8-diprenylisoflavone(77)、lupalbigettirt(78)、erysenegalensein E(79)、lupinisol A(80)、lupinisoflavone G(81)、derriscandenoside(A-E)(82-86)、7,8-dihydroxy-4'-methoxyisoflavone(87)、formononetin 7-O-β-glucopyranoside(88)、8-hydroxy-4',7-dimethoxyisoflavone 8-O-β-glucopyranoside(89)、diadzein 7-O-[α-rhamnopyranosyl-(1 → 6)]-β-glucopyranoside(90)、7-hydroxy-4',8-dimethoxyisoflavone 7-O-β-glucopyranoside(91)、genistein 7-O-[α-rhamnopyranosyl-(1→6)]-β-glucopyranoside(92)、3'-formylalpinumisoflavone(93)、2-(1-hydroxy-l-methylethyl)-3-hydroxy-2,3-dihydrofuranoal-pinumisoflavone(94)、senegalensin(95)、scanderone(96)、flemichapparin(B-C)(97-98)、isorobustone(99)、5-hydroxy-2'',2''-dimethylchromeno-[6,7:5'',6'']-2''',2'''-dimethylchromeno-[3',4':5''',6''']isoflavone(100)、ulexone A(101)、chandalone(102)、maackiain(103)、isochandalone(104)、santal(105)、lupiwighteone(106)、3'-methylorobol(107)、genistein(108)、7-O-α-rhamno(1→ 6)-β-glucosylgenistein(109)、4'-O-methylosajin(110)、4'-O-methylscandinone(111)、isoscandinone(112)、4'-O-methyl senegalensein(113)、scandinone A(114),其它植物 D.elliptica[31]中得到的 prunetin(115)、formononetin(116)、pseudoboptigen(117)、3'-methoxy-daidzein(118)、daidzein(119)、dihydrodaidzein(120)、demethylvestitol(121);D.robusta[32-34,14,35]中的 derrugenin(122)、robustigenin(123)、derrone(124)、6-hydroxy-7,2',4'-trimethoxyisoflavone(125)、derrubone(126)。D.malaccensis[36,37]中的 pomiferin(127)、pomiferin-4'-O-methyl ether(128),其中化合物128是从 D.malaccensis中得到的新化合物;D.indica[7]中 的 8,4'-dimethoxy-7-O-γ,γ-dimethylallylisoflavone(129)、medicarpin(130);D.ovalifolia[38]中的 toxicarol isoflavone(131);D.trifoliata[20]中的5,7,3',4'-tetrahydroxy-6,8-diprenylisoflavone(132)。
1.1.1.3 鱼藤酮及其衍生物
鱼藤酮类化合物在该属植物中比较常见,且含有此类成分的鱼藤属植物早被人们所利用。现已报道的鱼藤酮类化合物在 D.elliptica[39-43]中得到17个,即 elliptinol(133)、4',5'-dihydroxy-6a,12a-dehydrodeguelin(134)、11,4',5'-trihydroxy-6a,12a-dehydrodeguelin(135)、deguelin(136)、6a,12a-dehydroα-toxicarol(137)、6a,12a-dehydro-β-toxicarol(138)、villosol(139)、6-oxo-6a,12a-dehydrodeguelin(140)、rotenonone(141)、13-homo-13-oxa-6a,12a-dehydrodeguelin(142)、elliptoic acid(143)、7'-hydroxy-6a,12adehydrodeguelin(144)、6-hydroxy-6a,12a-dehydrode-guelin(145)、(6aR,12aR,4'R,5'S)-4',5'-dihydro-4',5'-dihydroxytephrosin(146)、6'-hydroxy-6a,12adehydrorotenone(147)、(-)-rotoic acid(148)、(-)-deguoic acid(149);D.trifoliata[44-48]中 的 rotenone(150)、elliptone(151)、6aα,12aα-12a-hydroxyelliptone(152)、α-toxicarol(153)、(-)-tephrosin(154)、7a-O-methyldeguelol(155)、7a-O-methyl-12a-hydroxydeguelol(156)、spiro-13-homo-13-oxaelliptone(157)、dehydrodeguelin(158)、13-homo-13-oxa-6a,12a-dehydrorotenone(159)、7a-O-methylelliptonol(160)、6a,12a-dehydrodeguelin(161)、12a-hydroxyrotenone(162)、6a,12a-dehydrorotenone(163)、Dehydrororenone(164)、12-hydroxyrot-2'-enonic acid(165);D.malaccensis[49,50]中 得 到 的 12a-hydroxyelliptone(166)、12-deoxo-12α-acetoxyelliptone(167)、derrisin(168)、trans-4',5'-dihydro-12aβ-4'β,5'α-trihydroxydeguelin(169)、rotenolone(170)。其中化合物143、148和149是12位上碳和12a位上碳断裂形成羧酸,而155、156和160是C环上6a位上碳和氧(O-7)开环的新颖鱼藤酮类化合物,157也是C环变形的新奇的鱼藤酮类化合物,见图3。

图3 鱼藤属植物中的鱼藤酮及其衍生物Fig.3 Structures of rotenones from Derris
1.1.1.4 查尔酮,橙酮及色酮类化合物
其它黄酮类化合物主要是查尔酮类和橙酮类化合物,其中查尔酮类化合物有8个(171~179)(图4)。在 D.laxiflora[51]中得到 2 个,即 laxichalcone(171)、derrichalcone(172);D.malaccensis[37,52]中的3'-(2-hydroxy-3-methylbut-3-enyl)-2',4'-dihydroxy-4-methoxychalcone(173)、2',4'-dihydroxy-4-methoxy-3'-prenylchalcone(heyneanachalcone,174);D.obtusa[12]中的 methylenedioxy-(3,4)-5'-hydroxy-2'-methoxy-furano-(4',3',2'',3'')-chalcone(175);D.araripensis[13]中的 methyfenedioxy-(3,4)-5'-hydroxy-2',3'-methoxyfurano-(3',4',2'',3'')-dihydro-chalone(176);D.robusta[53]中 的 rubone(177);D.indica[54,8]中的 pongamol(178)、ovalitenone(179)。橙酮类化合物从 D.obtusa[12]中得到 6 个,即 derriobtusone(A-B)(180 ~181)、furano-(6,7,2'',3'')-aurone(182)、4-hydroxy-fiuno-(6,7,2'',3'')-aurone(183)、4-methoxy-futano-(6,7,2'',3'')-aurone(184)、methylenedioxy-(3',4')-furano-(6,7,2'',3'')-aurone(185);D.trifoliata[45]中得到 1 个色酮 6,7-dimethoxy-4-chromanone(186)。

图4 鱼藤属植物中的查尔酮类和橙酮类化合物Fig.4 Structures of chalcones,aurones and a chromane from Derris
1.1.2 香豆素类化合物
该属植物中得到的香豆素类化合物不多,仅有7 个(187 ~ 193)(图 5)。在 D.scandens[55,22,21,29]中得到4 个,分别是 scandenin(187)、4,4'-di-O-methylscandenin(188)、robustic acid(189)、scandenin(AB)(190 ~ 191);D.spruceana[56]中的 3-methylenedioxy-(3', 4')-phenyl-4-hydroxy-5-methoxy-2'', 2''-dimethylchromeno-(5'',6'',7,8)-coumarin(192)、3-methylenedioxy-(3',4')-phenyl-4,5-dimethoxy-2'',2''-dimethylchromeno-(5'', 6'', 7, 8)-coumarin(193)。

图5 鱼藤属植物中的香豆素类化合物Fig.5 Structures of coumarins from Derris
1.1.3 芪类化合物
芪类化合物只有5个(194~198)(图6)。D.scandens[27,6]中的 scandione(194)、1-[6-hydroxy-2-methoxy-3-(3,3-dimethylallyl)-2'',2''-dimethylpyra-no-(5'',6'':5,4)]-2-(4'-hydroxyphenyl)-1,2-ethanedione(195)、derrisdione A(196);D.spruceana[56]中 的 2,4-dimethoxy-2'',2''-dimethylchromeno-(5'',6'',3',4')-stilbene(197);D.rariflora[11]中的 3,5-dimethoxy-4-prenylstilbene(198)。

图6 鱼藤属植物中的芪类化合物Fig.6 Structures of stilbenoids from Derris
1.1.4 其它酚性成分
从D.triofoliata[15]得到2个已知木脂素类化合物(+)-lyoniresinol-3α-O-β-D-glucopyranoside(199)和 (-)-lyoniresinol-3α-O-β-D-glucopyranoside(200);D.laxiflora[57]中得到化合物 2,3-(methylenedioxy)-4-methoxy-5-methylphenol(201)、2,3,6-trimethoxy-5-methylphenol(202);D.indica[54,8]中的 methylkarranjic acid(203)、piperonylic acid(204);D.trifoliata[19]中的 2,6-dimethoxy-p-hydroquinone 1-O-β-D-glucopyranoside(205)、tachioside(206)、isotachioside(207)、benzyl-β-D-glucopyranoside(208);D.scandens[25]中的4-hydroxy-3-methoxybenzoic acid(209)、4-hydroxy-3,5-dimethoxybezoic acid(210)。见图7。
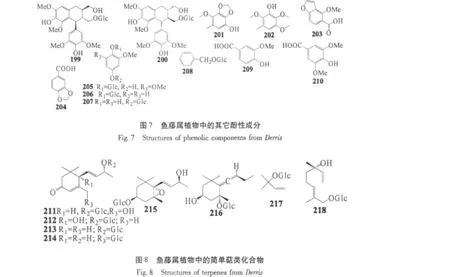
1.2 萜类化合物
1.2.1 简单萜类化合物
从D.trifoliata[19]中得到8个简单萜类化合物(图8),分别是 inamoside(211)、(6S,9R)-roseoside(212)、(6R,9R)-3-oxo-α-ionyl-β-D-glucopyranoside(213)、apocynoside I(214)、corchoionoside A(215)、citroside A(216)、2-methyl-3-buten-2-yl β-D-glucopyranoside(217)、betulalbuside A(218),该类化合物都是首次从该植物中分离得到。
1.2.2 三萜及其衍生物
从鱼藤属中得到的三萜类化合物不多,从D.laxiflora[2,57]中分离得到的 β-amyrin(219)、lupeol(220)、O-trans-cinnamoylglutinol(221)、22β-hydroxy-12-oleanen-3-one(222)、15α,16α-epoxy-12-oleanen-3-one(223)、29-hydroxy-12-oleanene-3,22-dione(224)、22β,29-dihyroxy-12-oleanen-3-one(225)、25-cycloartene-3,24-dione(226)、24ξ-hydroxy-25-cycloarten-3-one(227),从 D.eriocarpa How[58]中也得到了化合 物 219,D.triofoliata[59]中 的 taraxerol-3-β-O-tridecyl ether(228);D.eriocarpa How[58]中的 eriocarpin(A-C)(229 ~ 231)、2β,3β,28-trihydroxy-12(13)-en-olean(232)。除化合物 219、220、226、227和232外,其它的化合物都是从鱼藤属中分离得到的新的三萜类化合物(图9)。

图9 鱼藤属植物中的三萜类化合物Fig.9 Structures of triterpenes from Derris
1.3 生物碱类
从D.elliptica[42]中得到1个新的含N鱼藤酮2-hydroxy-5-aminorotenonone(233),也是鱼藤属中分离得到的第一个含N鱼藤酮,还从D.ovalifolia[38]中得到了1个新的生物碱7-methoxy-3-[1-(3-pyridyl)methylidene]-4-chromanone(234)和1个已知的生物碱 indole-3-carbaldehyde(235)(图10)。

图10 鱼藤属植物中的生物碱类化合物Fig.10 Structures of alkaloids from Derris
1.4 其它类成分
从 D.elliptica[60]中得到3 个(236 ~238)神经酰胺化合物,分别是(2S,3S,4R,8E)-2N-[(2'R)-2',3'-dihydroxy-hexacosanoyl]-1,3,4-trihydroxy-8-octadecene(236)、(2S,3S,4R,8E)-2N-[(2'R)-2'-hydroxyhexacosanoyl]-1,3,4-trihydroxy-8-octade-cene(237)、1-O-β-D-glucopyranosyl-(2S,3S,4R,8E)-2N-[(2'R)-2'-hydroxytetracosanoyl]-3,4-dihydroxy-8-oc-tadecene(238),其中化合物236为新化合物,是第一个C-3'上连有羟基的神经酰胺,237和238是首次从该属中分离得到(图11)。鱼藤属中还分离得到了一些烯烃、醇类、醌类、有机酸、苷类、氨基酸类等化合物,如多羟基十八烯酸[60]、octa cos-3-one[61]、23-hydroxy-octacos-5-ene-3-one[61]、二十七烷醇[12]、n-hexyl β-D-glucopyranoside[19]、maltol β-D-glucopyranoside[19]、 2S-carboxy-4R, 5S-dihydroxy- piperidine[62]、2S-carboxy-4S,5S-dihydroxypiperidine[62]、2,5-dihydroxymethyl 3,4-dihydroxypyrrolidine[63]。

图11 鱼藤属植物中的神经酰胺化合物Fig.11 Structures of ceramides from Derris
2 药理作用
2.1 抗氧化活性
Laupattarakasem P[28]等对 D.scandens中分离得到的化合物进行了抗氧化活性实验,其中化合物108、68、187具有和阳性对照没食子酸丙酯(PG)和秦皮素(Cou)相当的抗氧化活性,并且D.scandens的己烷和氯仿提取物具有温和的抗氧化活性[29],主要成分是化合物11、77、66、65和香豆素类化合物190、191。而从D.Malaccensis中得到的化合物127具有很强的抗氧化活性[36]。其它植物如 D.indica中得到2个黄酮22、27具有温和的抗氧化活性[8];从 D.urucu中得到的二氢黄酮醇50、51、52、53也具有较弱的抗氧化活性[16]。Tewtrakul S[64]等对 D.trifoliata中得到的鱼藤酮进行活性测定,其中化合物161和136具有清除DPPH活性。
2.2 抗癌活性
从 D.trifoliate[45]中得到鱼藤酮类化合物 160、136、153、150、162 对 KB,BC,和 NCI-H187 细胞株具有较强的细胞毒活性,而化合物155、161、163具有选择性抑制NCI-H187细胞株的活性,其中化合物136、153、150、166表现出较强的抗 KB和 BC细胞活性,化合物150对NCI-H187细胞株具有极其强的细胞毒活性,因此具有作为治疗肺癌的潜力,化合物136和153还具有显著的抑制皮肤癌细胞扩散的活性[44]。D.reticulata 中得到的黄酮类化合物 34、35、31、32 对 P-388 细胞株具有细胞毒活性[9,10]。鱼藤属植物中的鱼藤素对诱导乳腺癌MDA-MB-231细胞的增殖也具有显著的增殖抑制、诱导凋亡作用[65]。D.malaccensis[37]中分离得到的化合物 128、64、66、127、173 和 174 对癌细胞系 HuCCA-1、KB、HeLA、MDA-MB231、T47D和 H69AR均具有不同程度的细胞毒性。
2.3 抗菌活性
从D.malaccensis中得到鱼藤酮类化合物对幽门螺杆菌具有不同程度的抗菌活性[50],而从该植物中得到的化合物12具有很强的抗菌活性[35]。其它植物如D.indica中得到的酚性化合物203和178也具有抗菌活性[54]。2006 年,Khan MR[66]等对 D.elliptica、D.indica和 D.trifoliata三种植物的叶、茎、根、根皮或根心的石油醚、二氯甲烷、乙酸乙酯、正丁醇和甲醇提取液进行抗菌活性测定,其中活性显著的为D.indica的叶子和根心部分的甲醇提取液及其根皮的石油醚、正丁醇和甲醇提取液,还有D.trifoliata的石油醚和乙酸乙酯的提取液。另外,D.scandens茎的水提取物对金黄色葡萄球菌、大肠杆菌和表皮葡萄球菌的生长具有很好的抑制活性[67]。
2.4 杀虫活性
鱼藤属中的某些植物具有显著的杀虫和抗幼虫的活性,其主要活性成分是鱼藤酮类化合物。如现已报道的D.trifoliata的丙酮提取物具有较好的杀虫活性,主要活性成分是分离得到的鱼藤酮(150)和鱼藤素(136)[44,45];D.trifoliata[20]中分离得到的化合物 150、154、162、136、163、158、155、160、63 对Brine shrimp具有显著的毒性,而化合物62则毒性较弱;D.elliptica Benth中的鱼藤酮类或类鱼藤酮化合物具有杀蚜虫活性,可有效控制蚜虫类如甘蓝蚜等害虫[68,69]。此外,鱼藤酮对 Sitophilus grannarius和Tribolium confusum的成虫和Tribolium confusum和Trogoderma grannarium的幼虫具有较强的拒食活性[70]。D.indica Bennet的氯仿提取物对 Callosobruchus maculatus(F.)(以豆类植物为寄生食物的有害昆虫)的成虫具有毒性[71],还有 D.urucu的提取液具有杀埃及伊蚊的活性[72],D.scandens Benth中分离到的化合物 66、64、3、78、65、190、187、109 和 108对四种储存物害虫Callosobruchus chinensis L.,Sitophilus oryzae L.、Rhyzopertha dominica L.和 Tribolium castaneum H.具有不同程度的气相毒性[73]。
2.5 降血糖活性
D.scandens的己烷和氯仿提取物具有很强的抑制葡萄糖苷酶活性,从中得到的异黄酮类化合物113、77、66、65,香豆素类化合物 190 和 191 是主要活性成分[29]。从D.indica中得到的黄酮化合物22和27具有温和的抑制肠葡萄糖苷酶活性,而该植物中得到的查尔酮类化合物178具有很强的抑制肠葡糖苷酶活性[8],结果表明具有降血糖作用。
2.6 抗炎活性
从D.trifoliata中得到鱼藤酮化合物162、136、166、150 具有抑制NO 活性[64]。2011 年,Vilai Kuptniratsaikul MD[74]等对膝盖骨关节炎的人进行抽样D.scandens Benth的提取物治疗,通过数据和治疗结果分析,D.scandens Benth的提取物治疗膝盖骨关节炎具有很好的功效和安全性,且D.Scandens的水醇提取物对人类的免疫功能正常及免疫力低下的外周单个核细胞具有体外免疫刺激活性[75]。其它D.uliginosa叶子的乙醇提取物具有镇痛的活性[76],D.robusta中分离得到的异黄酮化合物126具有很强的抑制 Hsp90 活性[35]。
3 结论
对鱼藤属植物的利用和研究比较早,19世纪中叶中国民间就把含有鱼藤酮类物质的植物作为杀虫剂和毒鱼剂来使用,后来作为植物农药来使用。20世纪40年代开始对鱼藤属植物进行系统的研究,经查阅文献发现其杀虫谱比较广,其主要活性成分是鱼藤酮类化合物。鱼藤酮类化合物具有毒性,其毒性对农作物安全,对哺乳动物低毒的特点[77],是比较理想的植物源农药,应对其充分利用和控制。鱼藤属植物还具有抗氧化、抗癌、抗菌、降血糖、镇痛等功效。综上所述,鱼藤属植物具有很好的药用价值,应重视其栽培和种植,且对鱼藤属植物的化学成分进一步的研究,有利于合理开发和利用。
1 Delectis Florae Reipublicae Popularis Sinicae Agendae Academiae Sinicae Edita(中国科学院中国植物志编辑委员会).Flora Reipublicae Popularis Sin(中国植物志),Tomus 40.Beijing:Science Press,1994,193.
2 Lin YL,et al.Three new flavonoids,3'-methoxylupinifolin,laxifolin,and isolaxifolin,from the roots of Derris laxiflora Benth.Chem Pharm Bull,1991,39:3132-3135.
3 Lin YL,et al.Two new flavanones and two new chalcones from the root of Derris laxiflora Benth.Chem Pharm Bull,1992,40:2295-2299.
4 Kim YH,et al.Prenylated flavanones from Derris laxiflora.Nat Prod lett,1995,6:223-231.
5 Prawat H,et al.Reinvestigation of Derris reticulata.Pharmaceutical Biology,2000,38:63-67.
6 Sreelatha T,et al.A new benzil derivative from Derris scandens:Structure-insecticidal activity study.Bioorg Med Chem Lett,2010,20:549-553.
7 Koysomboon S,et al.Antimycobacterial flavonoids from Derris indica.Phytochemistry,2006,67:1034-1040.
8 Rao RR,et al.New furanoflavanoids,intestinal a-glucosidase inhibitory and free-radical(DPPH)scavenging,activity from antihyperglycemic root extract of Derris indica(Lam.).Bioorg Med Chem Lett,2009,17:5170-5175.
9 Mahidol C,et al.Prenylated flavanones from Derris reticulata.Phytochemistry,1997,45:825-829.
10 Milhidol C,et al.Two new pyranoflavanones from the stems of Derris reticulata.Heterocycles,2002,57:1287-1292.
11 Filho R B,et al.A stilbene and two flavanones from Derris rariflora.Phytochemistry,1975,14:261-263.
12 Nascimento MCD,et al.Flavonoids of Derris obtusa:aurones and auronols.Phyfochemistry,1976,15:1553-4558.
13 Nascimento MCD,et al.Flavonoids of Derris Araripensis.Phytochemisry,1981,20:147-152.
14 GuptaI A,et al.Flavone and isoflavone derivative from the seeds of Derris robusta with pods.Indian J Chem,1998,37B:419-421.
15 Xu LR,et al.A new acylated flavonol glycoside from Derris triofoliata.J Asian Nat Prod Res,2006,8:9-13.
16 Lobo LT,et al.Dihydrolavonols from the leaves of Derris urucu(Leguminosae):Structural Elucidation and DPPH Radical-Scavenging Activity.J Braz Chem Soc,2009,20:1082-1088.
17 Ramachandran NAG,et al.Rhamnetin-3-O-neohesperidoside,a new flavonoid from the leaves of Derris Trlfollata.J Nat Prod,1986,49:710-711.
18 Xu LR,et al.Three new flavonol triglycosides from Derris trifoliata.J Asian Nat Prod Res,2009,11:79-84.
19 Takeda Y,et al.Glycosidic constituents of the leaves of an Okinawan Leguminosae plant,Derris trifoliata Lour.J Nat Med,2008,62:476-478.
20 Cheng J,et al.A new prenylated flavanone from Derris trifoliata Lour.Molecules,2012,17:657-663.
21 Pelter A,Stainton P.The Extractives from Derris scandens.Part 11.The isolation of osajin and two new isoflavones,scandenone and scandinone.J Chem SocC,1966:701-704.
22 Rao MN,et al.Four isoflavones and two 3-aryl coumarins from stems of Derris Scandens.Phytochemistry,1994,37:267-269.
23 Li DP(李典鹏),et al.Two isoflavonoid glycosides from Derris scandens.Acta Pharm Sin(药学学报),1999,3 4:43-45.
24 Sekine T,et al.Six diprenylisoflavones,derrisisoflavonesA-F,from Derris scandens.Phytochemistry,1999,52:87-94.
25 Rukachaisirikul V,et al.Isoflavone glycosides from Derris scandens.Phytochemistry,2002,60:827-834.
26 Chuaukamnerdkarn M,et al.Prenylated Isoflavones from Derris Scandens.Heterocycles,2002,57:1901-1906.
27 Mahabusarakam W,et al.A benzil and isoflavone derivatives from Derris scandens Benth.Phytochemistry,2004,65:1185-1191.
28 Laupattarakasem P,et al.Anti-inflammatory isoflavonoids from the stems of Derris scandens.Planta Med,2004,70:496-501.
29 Rao SA,et al.Isolation,characterization and chemobiological quantiflcation of α-glucosidase enzyme inhibitory and free radical scavengingconstituents from Derris scandens Bent.J Chromatogr B,2007,855:166-172.
30 Babu TH,et al.A new prenylated isoflavone from Derris scandens Benth.J Asian Nat Prod Res,2010,12:634-638.
31 Lu HY(卢海英),et al.Isoflavones and their derivatives from the root of Derris elliptica(Roxb.)Benth.Chin J Nat Med(中国天然药物),2008,6:265-267.
32 Chibber SS,Sharma RP.Derrugenin,A new isoflavone from seed shells Derris robusta.Phytochemistry,1979,18:1583-1584.
33 Chirber SS,Sharma RP.Kobustigenin.A new isoflavone from Derris robusta Seed Shells.Phytochemistry,1979,18:1082.
34 Chibber SS,Sharma RP.Derrone,a new pyranoisoflavone from Derris robusta seeds.Phytochemistry,1980,19:1857-1858.
35 Hadden MK,et al.Derrubone,an inhibitor of the Hsp90 protein folding machinery.J Nat Prod,2007,70:2014-2018.
36 Svasti J,et al.Proteomic profiling of cholangiocarcinoma cell line treated with pomiferin from Derris malaccensis.Proteomics,2005,5:4504-4509.
37 Daranee C,et al.Prenylated flavonoids from the leaves of Derris malaccensis and their cytotoxicity.Nat Prod Commun,2011,6:1103-1106.
38 Shankar T,et al.A chromanone alkaloid from Derris ovalifolia stem.Nat Prod Res,2009,23:1652-1656.
39 Ahmed M,et al.A further rotenoid from Derris elliptica.Planta Medica,1989,55:207-208.
40 Lu HY,et al.Two new rotenoids from the root of Derris elliptica.Chin Chem Lett,2008,19:1218-1220.
41 Lu HY(卢海英),et al.Rotenoids from the root of Derris elliptica(Roxb.)Benth.J China Pharm Univ(中国药科大学学报),2008,39:108-110.
42 Lu HY,Liang JY.Novel N-containing rotenoid and seco-rotenoid from the root of Derris elliptica.J Asian Nat Prod Res,2009,11:58-62.
43 Lu HY,et al.Rotenoids from the root of Derris elliptica(Roxb.)Benth.Ⅱ.Chin J Nat Med Jan,2009,7:24-27.
44 Ito C,et al.Cancer chemopreventive activity of rotenoids from Derris trifoliata.Planta Med,2004,70:585-588.
45 Yenesew A,et al.7a-O-methyldeguelol,a modified rotenoid with an open ring-C,from the roots of Derris trifoliata.Phytochemistry,2005,66:653-657.
46 Yenesew A,et al.Two unusual rotenoid derivatives,7a-O-methyl-12a-hydroxydeguelol and spiro-13-homo-13-oxaelliptone,from the seeds of Derris trifolia.Phytochemistry,2006,67:988-991.
47 Cheenpracha S,et al.Cytotoxic rotenoloids from the stems of Derris trifoliata.Can J Chem,2007,85:1019-1022.
48 Xu LR(徐鲁荣),et al.Rotenoids from Derris trifoliate.J Chin Med Mater(中药材),2007,30:661-662.
49 Thasana N,et al.A new 12a-hydroxyelliptone from the stems of Derris malaccensis.Heterocycles,2001,55:1121-1125.
50 Takashima J,et al.Derrisin,a new rotenoid from Derris malaccensis Plain and anti-helicobacter pylori activity of its related constituents.J Nat Prod,2002,65:611-613.
51 Lin YL,et al.Two new chalcones,laxichalcone(I)and derrichalcone(II)from the roots of Derris laxiflora Benth.Chem Express,1991,6:747-750.
52 Siripaisarnpipat S,et al.Crystal structure of new prenylated chalcone from Derris Malaccensis.Anal Sci,2007,23:33-34.
53 Chibber SS,et al.Rubone,a new chalcone from Derris robusta Seed Shells.Phytochemisfry,1979,18:2056.
54 Baki MA,et al.Methylkarranjic acid and pongamol from Derris indica Seeds and their antibacterial activity.Dhaka Univ J Pharm Sci,2007,6:9-13.
55 Clark EP.Scandenin-A constituent of the roots of Derris Scandens.J Organic Chem,1943,8:489-492.
56 Garcia M,et al.Isoflavonoids from Derris spruceana.Phytochemistry,1986,25:2425-2427.
57 Chiu HL,et al.Triterpenoids and aromatics from Derris laxiflora.J Nat Prod,2008,71:1829-1832.
58 Zhang XM(张宪民),et al.Three new triterpenoids from Derris eriocarpa.Acta Bot Yunnan(云南植物研究),2002,24:787-791.
59 Xu LR,et al.A new triterpenoid:taraxerol-3-β-O-tridecyl ether from Derris triofoliata.Pharmazie,2004,59:655-656.
60 Lu HY,Liang JY.A novel ceramide from the roots of Derris elliptica.Chin J Nat Med,2011,9:94-97.
61 Gupta A,et al.New aliphatic compounds from the seeds with pods of Derris robusta.Indian J Chem,1999,38B:752-753.
62 Mawer M,et al.2S-carboxy-4R,5S-dihydroxypiperidine et 2S-carboxy-4S,5S-dihydroxy-piperidine a partir de Derris elliptica.Phytochemistry,1976,15:183-185.
63 Welter A,et al.2,5-dihydroxymethyl 3,4-dihydroxypyrrolidine dans les feuilles de Derris elliptica.Phytochemistry,1976,15:747-749.
64 Tewtrakul S,et al.Nitric oxide inhibitory principles from Derris trifoliata stems.Phytomedicine,2009,16:568-572.
65 Du J(杜佳),Deng HY(邓华瑜).Effect and pathway of induction of breast cancer MDA-MB-231 cell apoptosis by deguelin.Chin J Biologicals March(中国生物制品学杂志),2010,23:238-242.
66 Khan MR,et al.Antimicrobial activity of the Derris elliptica,Derris indica and Derris trifoliata extractives.Fitoterapia,2006,77:327-330.
67 Sittiwet C,Puangpronpitag D.Antimicrobial properties of Derris scandens aqueous extract.J Biol Sci,2009,9:607-611.
68 Moyo M.,et al.Efficacy of the botanical pesticides,Derris elliptica,Capsicum frutescens and Tagetes minuta for the control of Brevicoryne brassicae in vegetables.J Sustai Dev Africa,2006,8:216-222.
69 Hu MY,et al.Insecticidal activities of secondary metabolites of endophytic Pencillium sp.in Derris elliptica Benth.J Appl Entomol,2005,129:413-417.
70 Nawrot J,et al.Antifeeding activity of rotenone and some dedva ves towards selected insect storage pests.Biochem Syst Ecol,1989,17:55-57.
71 Mondal OA,Islam N.Toxicity of chloroform extracts of Derris indica Bennet.against Callosobruchus maculatus(F.)adults.Univ J Zool Rajshahi Univ,2008,27:95-96.
72 Biotecnologia L,et al.Derris(Lonchocarpus)urucu(Leguminosae)extract modifies the peritrophic matrix Structure of Aedes aegypti(Diptera:Culicidae).Mem Inst Oswaldo Cruz,Rio de Janeiro,2002,97:371-375.
73 Hymavathi A,et al.Vapor-Phase toxicity of Derris scandens Benth.,Derived constituents against four stored-product pests.J Agric Food Chem,2011,59:1653-1657.
74 Vilai Kuptniratsaikul MD,et al.Efficacy and Safety of Derris scandens Benth Extracts in Patients with Knee Osteoarthritis.J Alter Compl Med,2011,17:147-153.
75 Sriwanthana B,Chavalittumrong P.In vitro effect of Derris scandens on normal lymphocyte proliferation and its activities on natural killer cells in normals and HIV-1 infected patients.J Ethnopharmacol,2001,76:125-129.
76 Ahmed F,et al.Antinociceptive activity of Derris uliginosa.Fitoterapia,2007,78:377-378.
77 Zhang TY(张庭英),et al.Current status of rotenone utilization and existing concerns.Chin J Pestic(农药),2005,44:352-355.