α-丙二醇-水相中氯代二噁英的催化加氢脱氯降解
金士威,华 晔,李晨曦,邹 彬,Daniel Dianchen Gang,3
(1.马里兰大学土木与环境工程系,美国马里兰州 大学公园20742;2.武汉工程大学化工与制药学院,绿色化工过程教育部重点实验室,湖北 武汉 430074;3.路易斯安那大学拉法叶分校土木工程系,美国路易斯安那州 拉法叶 70504)
0 引 言
多氯二苯并二噁英polychlorinated dibenzop-dioxin简称 PCDDs)和多氯二苯并呋喃polychlorinated dibenzofuran(简称 PCDFs)是一类典型的持久性有机污染物(POPs),主要来源于人类活动,如市政垃圾焚烧、化工、冶金、造纸、汽车尾气排放等[1-4].PCDD/Fs的毒性随氯原子的取代数量和取代位置不同而有所差异,其中2,3,7,8-四氯代二苯-并-对二噁英(2,3,7,8-TCDD)是迄今为止人类已知的毒性最强的污染物,不仅具有三致毒性,还具有生殖毒性、发育毒性、免疫毒性以及内分泌干扰效应[4-6],因此受到国际社会的普遍重视.杜绝或尽量避免人类接触二噁英的最佳途径是源头控制,也就是说,严格控制工业过程,以尽可能减少二噁英的形成.但进入环境的二噁英,因其难生物降解,而可持久存在于环境中.近十年来,已经开发了许多降解二噁英的方法,如微生物降解法、光催化降解法、高温热解法等.近年来发展的催化加氢脱氯法,相比其他方法,具有简单、高效、反应条件温和、几乎不产生二次污染等优点[1-2].许多金属催化剂,包括 Pd/C,Pt/C,Rh/C等被用于氯代有机物的催化脱氯.
已开发的贵金属催化剂对二噁英类物质的催化还原脱氯方法可归为两类:一类用H2作为氢源[7-8],而另一类用2-丙醇作为氢源[9-14],两类催化系统都在水/有机溶剂中以多孔粉末为载体的贵金属催化下进行.Ukisu等[14-15]对2-丙醇为溶剂的氯代二噁英的催化脱氯进行了卓有成效的研究.Mitoma等[15-16]用钙催化剂降解醇溶液中的二噁英,取得了较好的结果.但二噁英的催化加氢脱氯研究,主要在低氯代方面,少数研究涉及高氯代二噁英,如 Zhang等[7,11]研究了乙醇-水溶液中八氯代二噁英以H2作为氢源的催化脱氯.
由于α-丙二醇是一种对人体无毒无害同时能够与水和多种有机溶剂混溶的溶剂,本研究选择以α-丙二醇与水按1∶1混合液作为溶剂,以实验室自制的质量分数5%Pd/C为催化剂,以1,2,7,8-四氯代二噁英(1,2,7,8-TCDD)为模型化合物,在碱性条件下研究了反应温度、反应物初始浓度和催化剂浓度等对二噁英催化加氢脱氯的影响.
1 实验部分
1.1 仪器与试剂
Agilent GC 7890/MS 5975气质联用色谱仪,以及 DB-5MS毛细管柱 (60m × 250μm×0.25μm),均购自美国Agilent公司.
标准样品:1,2,7,8-TCDD(质量分数98%)、内标物五氯苯(C6HCl5)(质量分数为98%)购自美国 Cambridge Isotope.Laboratories,Inc;1,2-丙二醇、氢氧化钠为分析纯;正己烷,二氯甲烷,甲苯,均为农残级 (J.T.Baker,USA);催化剂:质量分数为5%的Pd/C,粉末状(实验室合成);H2、He为高纯钢瓶气(四川天一科技股份有限公司武汉供气分公司),纯度大于99.999%.
1.2 方法与步骤
反应在装有玻璃通气管、温度计和回流冷凝管的250mL四口烧瓶中进行.将反应仪器搭建好后,在加料口处加入催化剂Pd/C,塞上磨口塞,通入氮气约5min,将烧瓶中空气置换掉,然后再通入氢气,置换氮气,约5min后,将四口烧瓶加热至200℃,保持40min,以活化催化剂.停止加热,使烧瓶在冰水浴中冷却,迅速加入1mol/L的氢氧化钠溶液和含有标准样品的丙二醇溶液.开启磁力搅拌器,控制反应温度,进行催化加氢脱氯反应,反应过程一直通入氢气.不同时间间隔取样1 mL,置于冰箱,避光冻存,便于后续的前处理和检测.
试验研究了不同反应温度,不同初始浓度和不同催化剂用量对催化加氢脱氯的影响.
1.3 样品前处理过程
在1mL二噁英样品溶液中加入5μL C6HCl5/甲苯 (10μg/mL)的内标液,混匀.然后以1 000r/min的转速离心15min,将小管中的上清液转入至另一小管,将原管中沉淀用正己烷超声提取5min,离心,取上清液,过程重复2次.将取得的上清液合并,超声10min,转移分层后的上层液体,对残余下层液体用正己烷超声提取2次,合并提取液,氮吹至1mL,用于GC-MS检测.
1.4 仪器分析
GC7890/MS 5975的气相条件:进样口温度为250℃,载气:He,流速为1.4mL/min,不分流进样.进样量:1μL.
气相色谱升温程序为:100℃保持4min,25℃·min-1至170℃,然后以5℃/min升至270℃,保持5min.
质谱条件:电离方式EI,电子轰击能量为70eV,离子源温度为:230℃,扫描方式为选择离子监测(SIM)模式.C6HCl5的特征离子为178,215,250;1,2,7,8-TCDD的特征离子为194,257,322.
2 结果与讨论
2.1 1,2,7,8-TCDD的色谱图和标准曲线
1,2,7,8-TCDD的 GC-MS图谱如图1所示,标准曲线如图2所示.1,2,7,8-TCDD的检测限为1ng/mL,样品回收率为98.9%~102.1%.

图1 1,2,7,8-TCDD及内标的色谱图Fig.1 GC-MS chromatogram of 1,2,7,8-TCDD and internal standard compound C6HCl5

图2 1,2,7,8-TCDD的标准曲线Fig.2 The calibration curve of 1,2,7,8-TCDD
2.2 温度对反应的影响
为了研究温度对催化加氢脱氯的影响,选取30、45、60℃三个不同反应温度进行实验,初始质量浓度为5μg/mL,反应时间150min,其实验结果如表1所示.
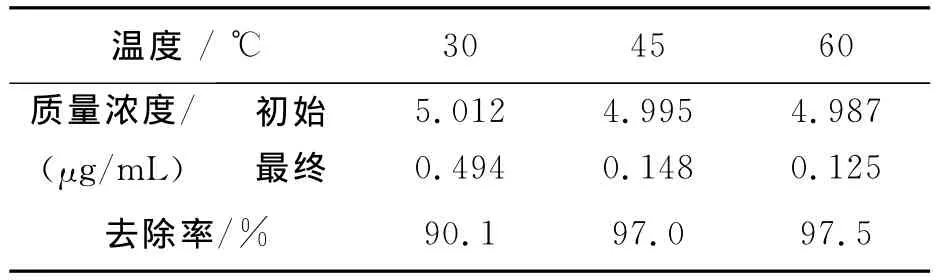
表1 不同反应温度对1,2,7,8-TCDD去除率的影响Table 1 Effect of reaction temperature on the removal of 1,2,7,8-TCDD
由表1可知,30℃时,其去除率已达90.1%,随着温度升高,其去除率逐渐增大,45℃时的去除率达97.0%,说明升高温度有利于催化加氢反应的进行.这可以从两方面解释,首先,根据阿伦尼乌斯方程,温度升高,反应速率常数增大.当反应物浓度保持不变时,反应速率与反应速率常数成正比,因此,反应温度升高,加氢反应速率加快;其次,由菲克定律可知,随着温度的升高,反应物和生成物的扩散速率加快,从而导致反应物与催化剂的接触频率增加,并可使生成物与催化剂较容易分离,从而使加氢反应速率加快.因此,适当地升高反应温度,反应速率会明显加快.但当反应温度过高时,反应速率的提高就不明显了,这可能是过高的温度,导致反应物和氢气不利于在催化剂表面上的吸附和活化,使反应速率的增加不明显.本实验中,温度继续升高到60℃时,去除率则为97.5%.表明温度继续升高,去除率已变化不大.从减少能耗方面考虑,反应温度以45℃为宜,故后面的实验选取45℃作为反应温度.
2.3 初始质量浓度对去除率的影响
为了研究初始质量浓度对去除率的影响,在反应温度为45℃时,对初始质量浓度分别为1,5,10,25μg/mL的1,2,7,8-TCDD丙二醇溶液进行了催化加氢反应,反应时间为150min,结果如表2所示.
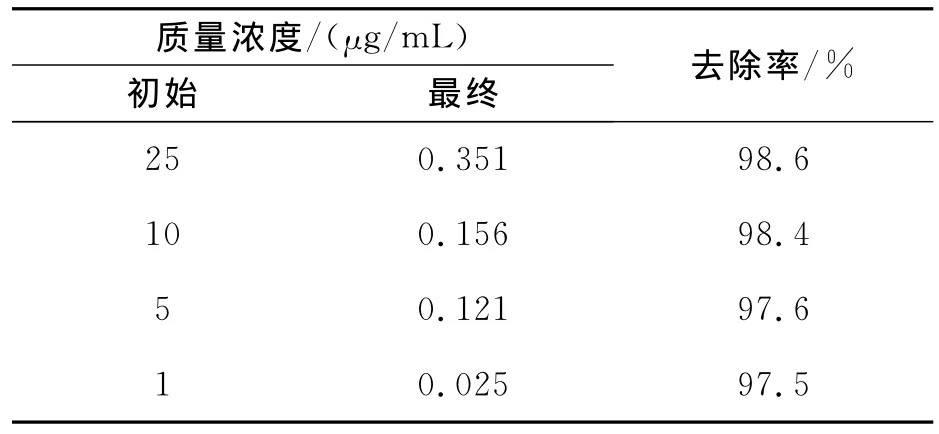
表2 初始质量浓度对1,2,7,8-TCDD去除率的影响Table 2 Effect of initial concentration on the removal of 1,2,7,8-TCDD
由表2可知,在用Pd/C催化1,2,7,8-TCDD的加氢脱氯反应中,1μg/mL的二噁英反应液在150min时能较好地发生加氢脱氯反应,其残余量为0.025μg/mL,去除率为97.5%,5μg/mL的二噁英在150min时的去除率为97.6%.当质量浓度增大到10μg/mL和25μg/mL时,去除率在98%以上.表明 1,2,7,8-TCDD的催化加氢反应与初始质量浓度变化关系较小.无论是较高初始质量浓度25μg/mL还是较低浓度1μg/mL条件下,丙二醇/水反应液中的1,2,7,8-TCDD均能实现较好的加氢脱氯反应.徐杰等[17]研究了初始质量浓度为30μg/mL和600μg/mL三氯新15min加氢脱氯反应,其去除率分别为100%和98%.当质量浓度增大到4 500μg/mL和10 000μg/mL延长反应时间也能够去除,表明无论是高浓度,还是低浓度,该类污染物均可以用催化加氢的方法脱氯去除.这是由于有机氯化物的催化加氢脱氯过程是一个不可逆过程,只要有足够的反应时间,有机氯污染物最终都可以完全反应而彻底去除.
2.4 反应时间对去除率的影响
本实验研究了反应时间对1μg/mL 1,2,7,8-TCDD催化加氢脱氯去除率的影响,结果如图3所示.

图3 反应时间对1,2,7,8-TCDD(1μg/mL)去除率的影响Fig.3 Effect of reaction time on the removal of 1,2,7,8-TCDD (1μg/mL)
由图3可知1,2,7,8-TCDD催化加氢反应主要发生在前15min内,反应5min时的去除率达到59.0%,15min时的去除率达到76.3%,其质量浓度下降较快.30min后的去除率变化不大.说明随着1,2,7,8-TCDD在丙二醇中浓度的降低,其加氢反应的速率也变得越来越慢.可能的原因是因为反应物的浓度随着反应进行而不断降低,其在丙二醇/水中的扩散和在催化剂上的吸附也将变得越来越难,使得吸附在催化剂Pd/C上的质量浓度减少,从而使1,2,7,8-TCDD催化加氢反应速率变慢.反应时间在150min时,去除率超过97%.
2.4 催化剂质量浓度对去除率的影响
在催化加氢脱氯反应中催化剂起着十分重要的作用,催化剂活性的高和低、稳定性的好与坏,催化剂的用量多少都会直接影响到脱氯反应的效果.本实验选取 Pd/C作为 1,2,7,8-TCDD加氢反应催化剂,通过调节催化剂的质量浓度来讨论其对去除率的影响.实验结果如图4所示.
图4表明,随着催化剂质量浓度的逐渐增加,催化加氢反应的去除率先增加后减少.催化剂质量浓度为0.125,0.25,0.5g/mL时的去除率分别为90.8%,95.1%,97.1%.表明增大催化剂的质量浓度有利于脱氯反应的进行.但当催化剂的质量浓度从0.5g/mL增加到1g/mL时,1,2,7,8-TCDD的去除率并未继续增加反而有所降低,其去除率为94.6%.可能由于催化剂用量的增加,导致了活性中心增多,但造成了每个活性中心反应物浓度下降,从而降低了反应速率.根据试验结果,确定催化剂的最佳用量为0.5g/mL.
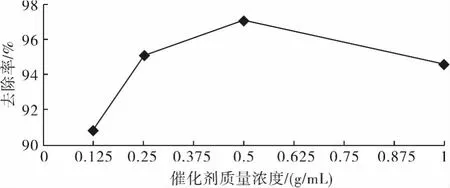
图4 Pd/C催化剂用量对去除率的影响Fig.4 Effect of Pd/C catalyst dosage on the removal of 1,2,7,8-TCDD
贵金属催化加氢脱氯反应由于反应条件温和、降解率高,而成为去除有机氯代化合物的有效手段.催化加氢脱氯反应,会生成HCl,而HCl会对催化剂造成中毒,因此催化加氢脱氯反应通常在碱性条件下进行.本试验中,加入NaOH的浓度为1mol/L,以保证HCl能被完全中和.二噁英的催化加氢脱氯产物是低氯代或不带氯的二噁英或呋喃.氯原子按一级动力学被一个接一个脱除,反应如图5所示.在本试验中,检测到了一些二氯代的二噁英以及不带氯的母体二噁英化合物.且随着反应时间的增加,母体化合物的浓度峰高也增大,表明脱氯的最终产物就是二噁英的母体化合物.
尽管当前的用贵金属催化还原脱氯方法修复PCDD/Fs污染是有效的,但也存在一些缺点,如降解不彻底时产生二次废液,复杂的催化剂回收/清洗过程及催化剂的使用寿命等.因此,还必须对催化加氢脱氯的去除二噁英的实际应用开展进一步的研究.

图5 氯代二噁英的催化脱氯反应式Fig.5 The equations of catalytic dechlorination of PCDD/Fs
3 结 语
催化加氢脱氯反应是一个去除有机氯代化合物的有效手段.通过使用氢气或是氢转移试剂作为氢源、利用加氢催化剂在碱性条件下与氯代化合物进行反应,从而消除氯代化合物上的氯原子达到去除的目的.本研究利用H2作为氢源,质量分数5%Pd/C作为加氢催化剂,α-丙二醇/水(1∶1)作为溶剂,在 NaOH 碱性条件下对1,2,7,8-TCDD催化加氢反应进行了探讨.结果表明,当反应温度为45℃,催化剂用量为0.5g/mL,反应时间为150min时,1,2,7,8-TCDD 的 去 除 率 达97.0%,1,2,7,8-TCDD 初始质量浓度对催化加氢脱氯的去除率没有影响.
[1]Weber R.Relevance of PCDD/PCDF formation for the evaluation of POPs destruction technologies-review on current status and assessment gaps [J].Chemosphere,2007,67:S109-S117.
[2]Kulkarni P S,Crespo J G,Afonso C A M.Dioxins sources and current remediation technologies—a review [J].Environ Int,2008,34:139-153.
[3]Altarawneh M,Dlugogorski B Z,Kennedy E M,et al.Mechanisms for formation,chlorination,dechlorination and destruction of polychlorinated dibenzo-pdioxins and dibenzofurans (PCDD/Fs)[J].Prog Energy Combust,2009,35:245-274.
[4]Stanmore BR.The formation of dioxins in combustion systems[J].Combustion and Flame,2004,136(3):398-427.
[5]McGregor D B,Partensky C,Wilbourn J,et al.An IARC evaluation of polychlorinated dibenzo-p-dioxins and polychlorinated dibenzofurans as risk factors in human carcinogenesis [J].Environ Health Perspect,1998,106(suppl 2):755-760.
[6]周莉菊,冯家满,赵由才.二噁英的毒性及环境来源[J].工业安全与环保,2006,32(11):49-51.ZHOU Li-ju,FENG Jia-man,ZHAO You-cai.The Toxicity of Dioxin and the Source in Environment.[J].Industrial Safety and Environmental Protection,2006,32(11):49-51.(in chinese)
[7]Zhang F,Chen J,Zhang H,et al.The study on the dechlorination of OCDD with Pd/C catalyst in ethanol-water solution under mild conditions[J].Chemosphere,2007,68:1716-1722.
[8]Ghattas A,Abu-Reziq R,Avnir D,et al.Exhaustive hydrodechlorination of chlorinated aromatic environmental pollutants to alicyclic compounds[J].Green Chem,2003(5):40-43.
[9]Ukisu Y,Miyadera T.Dechlorination of polychlorinated dibenzo-p-dioxins catalyzed by noble metal catalysts under mild conditions [J].Chemosphere,2002,46:507-510.
[10]Yang Z,Xia C,Zhang Q,et al.Catalytic detoxification of polychlorinated dibenzo-p-dioxins and polychlorinated dibenzofurans in fly ash[J].Waste Manage,2007,27:588-592.
[11]Zhang F,Chen J,Zhang H,et al.Dechlorination of dioxins with Pd/C in ethanol-water solution under mild conditions [J].Separation and Purification Technology,2008,59:164-168.
[12]Cobo M,Conesa J A,Correa C M D.Effect of the reducing agent on the hydrodechlorination of dioxins over 2wt%Pd/γ-Al2O3[J].Appl Catal B:Environ,2009,92:367-376.
[13]Ukisu Y,Miyadera T.Hydrogen-transfer hydrodechlorination of polychlorinated dibenzo-p-dioxins and dibenzofurans catalyzed by supported palladium catalysts[J].Appl Catal B:Environ,2003,40:141-149.
[14]Ukisu Y,Miyadera T.Dechlorination of dioxins with supported palladium catalysts in 2-propanol solution[J].Appl Catal A:Gen,2004,271:165-170.
[15]Mitoma Y,Uda T,Egashira N,et al.Approach to highly efficient dechlorination of PCDDs,PCDFs,and coplanar PCBs using metallic calcium in ethanol under atmospheric pressure at room temperature[J].Environ Sci Technol,2004,38:1216-1220.
[16]Mitoma Y,Tasaka N,Takase M,et al.Calciumpromoted catalytic degradation of PCDDs,PCDFs,and coplanar PCBs under a mild wet process[J].Environ Sci Technol,2006,40:1849-1854.
[17]徐杰,夏传海,梁鑫淼,等.一种多卤代苯氧基卤代苯酚类化合物的催化加氢脱卤的方法:中国, 02132909.5[P].2003-03-19.XU Jie,XIA Chuan-hai,LIANG Xin-miao,et al.A method about catalytic hydrodehalogenation of multi-halogenated phenoxy halogenated phenolic compounds:China, 02132909.5 [P].2003-03-19.(in Chinese)

