高含硫气田元素硫沉积及其腐蚀
范 舟 李洪川 刘建仪 欧阳旭 鲁柳利
1.西南石油大学材料科学与工程学院 2.“油气藏地质及开发工程”国家重点实验室·西南石油大学3.中国石油川庆钻探工程公司地质勘探开发研究院
高含硫气田在开发过程中,由于温度、压力等因素的改变,高腐蚀性的元素硫析出沉积并在沉积区引起严重的腐蚀[1-6]。硫沉积造成的管道堵塞和腐蚀引起的管道穿孔、设备的损毁失效,都会严重影响气田的正常生产,造成减产甚至是停产。虽然人类早就认识了硫的单质形式——硫磺并广泛应用于医药、冶金和火药制造,但面对高含硫油气运输过程中储罐的腐蚀和油气管道中的硫腐蚀,由于环境复杂、影响因素众多再加上元素硫活泼的化学性质,一直没能找出一种合理的腐蚀机理。
1 高含硫气田元素硫的来源
含硫气藏是指产出的天然气中含有H2S、CO2等非烃类气体以及硫醇、硫醚等杂质的气藏。国家矿产储量委员会对含硫气田的划分标准为硫化氢含量大于或等于30g/m3气田为高含硫气田。酸性气田硫沉积的现象早有报道,但是对元素硫的来源,科学家们的观点不一致。随着该领域的广泛研究,已证实酸性气藏中元素硫的含量主要决定于储层成岩变化与油气成藏演化过程中地质—地球化学作用[7-10],油气藏的温度、压力和气体组成、开采的技术手段也在一定程度上影响了气井中的硫含量。
基于广泛的研究,ASRL(Alberta Sulfur Research Ltd.)对于酸性气藏中元素硫的来源提出了一系列的机理[11]:
1.1 主要来源
烃类硫酸盐的热化学反应(TSR):
(A)2H2S+O2
(B)CaSO4+HC+H2SCO2+H2O
1.2 其他来源
1.2.1 高温高压下H2S的缩聚反应

1.2.2 硫烷的分解
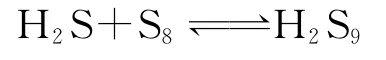
1.2.3 离子多硫化物的分解

1.2.4 氧气对 H2S的氧化
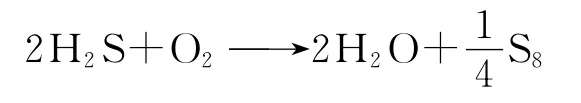
1.2.5 溶解在液态烃中的元素硫
现以普光气田为例说明元素硫的来源,其基本生产参数见表1。普光气田是四川盆地勘探过程中发现的我国最大的海相碳酸盐岩层系气藏。元素硫形成于第三纪区域抬升降温减压阶段,长期的烃类硫酸盐热化学反应(TSR)除了产生元素硫外还产生了方解石、H2S和CO2等,其中元素硫是其主要产物[12]。
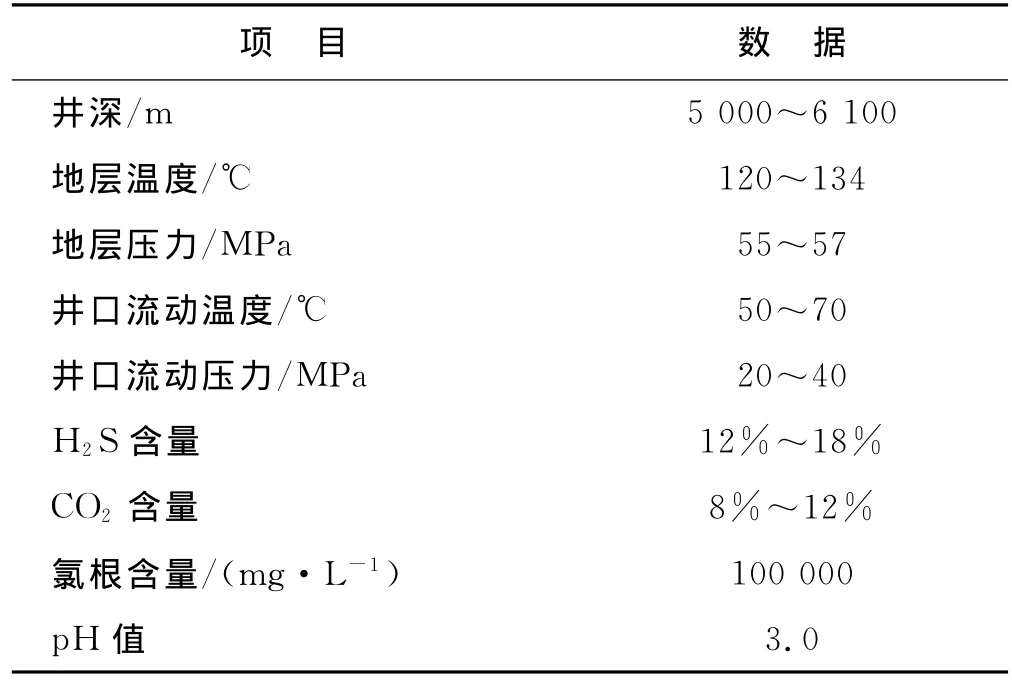
表1 普光气田的基本生产参数表
1)油气储层受沉降埋深和高温热流作用时期,H2S主要形成阶段。
CaSO4+HCH2S+CO2+CaCO2+沥青+气态烃
在此阶段,新生方解石中捕获的流体包裹体有含H2S的气态烃以及固体沥青。
2)储层后期抬升降温、减压时期,元素硫形成阶段。
在此阶段,储层裂隙和孔隙中不仅有元素硫产生,而且新生石膏和方解石晶体中常捕获有含元素硫和H2S等多种不混溶包裹体。产生的元素硫以3种不同的形式存在于油气藏中:①一部分以液相或作为游离的固相物理溶解在石油中,或化学溶解形成硫烷以气相的形式存在;②一些元素硫在长期的地热条件下被还原成H2S和其他硫化物;③大多数的元素硫作为孔隙填充物存在于普光气田白云岩储层中,这是气藏元素硫的主要来源。
此外,普光气田的H2S含量超过10%,属于特高含硫气藏,气藏中含有大量的H2S分子,这些H2S气体分子在高温高压的地热条件作用下将发生剧烈的热运动,当多个H2S分子发生有效碰撞时就会发生缩聚反应产生元素硫。随着温度和压力降低,管线中缩聚反应产生的硫烷和高温高压地热条件形成的硫烷(H2S+S8→H2S9)不断分解产生大量的元素硫,同时在CO2水解产生的的作用下,硫烷形成水溶性离子多硫化物()。当温度进一步降低,H2S和CO2在水中溶解度增加,水解产生的H+增多,将会发生分解产生元素硫。气藏中气体组成(尤其是H2S含量)、温度压力、地层深度和地质特征等因素都会影响上述方式产生的元素硫的数量。
研究者针对加拿大西部酸性气田的研究发现:设备和管线的不完全密封会产生氧气侵入,进而导致氧气对H2S的氧化也会产生少量的元素硫[13]。常发生氧气侵入的地方是:外壳通气孔、填料箱、清管操作的发送器/接收器、安全阀、贮水箱、油气回收设备和压缩机。在冬季使用天然气水合物抑制剂形成的甲醇,因其高溶解氧,持续注入也会产生氧气的侵入。此外,像钻井液、溶硫剂和缓蚀剂等在油气开发生产过程中注入的液体中也或多或少地溶解了一定量的氧气,也会产生一定量的元素硫。不过由于入侵的氧气总量很少,只会产生少量的元素硫,因而不是硫的主要来源。此外,当管线已产生腐蚀产物时,氧气对腐蚀产物的氧化也会产生元素硫:Fe9S8+6O2→3Fe3O4+S8。
2 元素硫沉积机理
研究发现元素硫能溶解在酸性气体中,主要是溶解在硫化氢中。元素硫在硫化氢中的溶解是指在一定的条件下,元素硫能分散在硫化氢气体中,使整个混合物呈现单一气相。元素硫在天然气中有两种溶解方式,分别是化学溶解和物理溶解[14]。
化学溶解指在高含硫气藏中,元素硫在地层条件下与硫化氢反应生成一种硫烷(图1)。当地层压力增加时,反应向生成硫烷的方向进行,使元素硫在天然气中的溶解度增大;反之,当地层压力降低时,反应向有利于多硫化氢分解生成硫化氢和元素硫的方向进行。
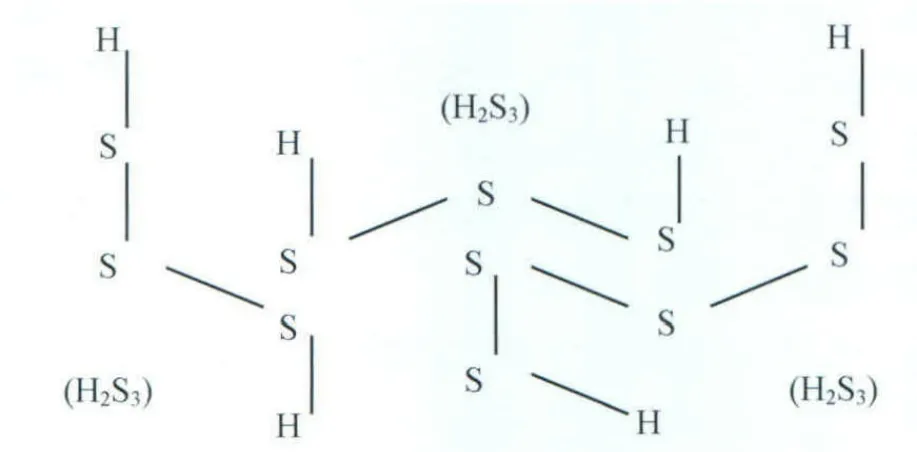
图1 硫的化学溶解结构式图
物理溶解指在超过临界温度、高压条件下,元素硫以物理方式溶解在酸气中(图2)。
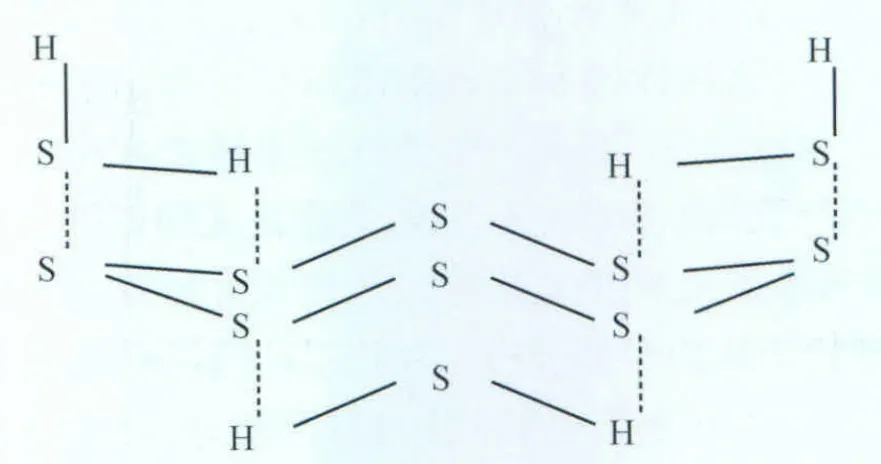
图2 硫的物理溶解结构式图
元素硫在高含硫气藏高温高压的储集层环境中的溶解度比较大。在高含硫气藏生产、开发过程中,气体中元素硫的溶解度达到临界饱和时,继续降低温度和压力,元素硫就会析出,并在一定条件下沉积。前人研究认为存在3种可能产生硫沉积的机理:化学反应[15-16]、水合物的形成和元素硫的凝华[17-20]。其中化学反应理论能很好地解释元素硫的来源,但无法解释管线、设备在下游压力迅速下降处发生的硫沉积。而水合物的形成可能导致元素硫的沉积,这是因为液态水合物能部分溶解气态的元素硫,当这些液态水合物蒸发后便会产生颗粒状的硫沉积。尽管这样,水合物机理只能发生在产生大量水合物的气井,但实际生产的含硫气井中在某位置的水合物生成量很低。而凝华作用指元素硫直接从气态到固态的转变,当气相趋于饱和时,进一步的温度或压力的下降都会产生热力学的不稳定,硫相态转变进而析出硫沉积。
显然,两种溶解机理导致的元素硫析出沉积的本质是不同的。从文献资料来看,大多数科学家认为元素硫在气井中的溶解以物理溶解为主。虽然溶解方式不同,但是过饱和析出的元素硫都以第3种沉积机理生产硫沉积,即气态的硫分子通过凝华作用产生固态硫分子,再在这些硫分子上成核结晶,最终产生硫沉积。
从上面的分析可以看出,硫沉积的发生主要与元素硫在酸性气体的溶解度相关,因而科学家进行了硫在酸性气体中溶解度的研究。Harris提出了如下元素硫在酸性气体中溶解度的表达式:
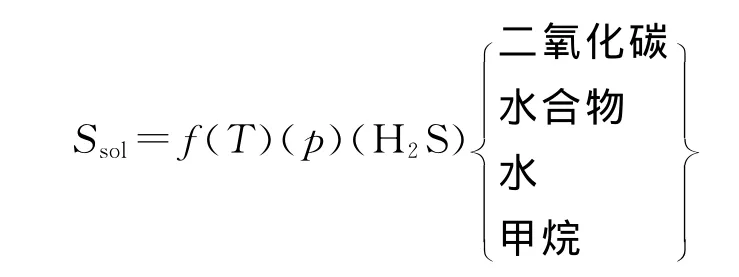
H2S含量、压力和温度是主要影响因素,而CO2和CH4的含量,气井中形成的水合物和凝析水的量也会影响硫的溶解度。
在充分考虑影响硫溶解的基础上,Roberts提出了地层中元素硫沉积的预测模型[21],而Hands提出了用于天然裂缝气藏和人工裂缝气藏硫沉积的预测模型[22],后人在这两种模型的基础上不断修正、改进,取得了一些较好的模拟预测模型。当然有些研究者根据最新的油气田研究成果,结合先进的数学、物理和化学模型,提出了自己的硫沉积预测模型[23-24],为模型的研究提供了新思路。但是由于影响硫沉积的因素众多,而且每个气井的地质特征不同、形成过程不同,很难找到一个能普遍适用的硫沉积的预测模型。因而开发针对不同特征并能很好模拟实际情况的硫沉积模型是发展的方向,这方面仍然需要大量的研究。
3 硫腐蚀及其影响因素
3.1 腐蚀机理
国外很早就开展了元素硫腐蚀机理研究,但到目前为止,元素硫腐蚀机理主要有以元素硫的水解为基础的催化机理、水解机理、电化学机理和近期进行了大量研究的直接反应机理。
3.1.1 催化机理
1978年Hyne J B等人做了厌氧和含氧环境下湿元素硫对碳钢的腐蚀实验。实验是测量盘绕成一圈圈的铁丝在不同pH值、不同气氛(厌氧或含氧)和大小不同的元素硫颗粒溶液中腐蚀速率的变化,实验得到了以下重要发现:① 严重腐蚀发生前存在一个诱导期,其时间长短取决于原始溶液的pH值,诱导时间随着初始pH值(3.88~5.79)的升高减小,有氧系统的诱导期比无氧系统的时间要短;诱导期随着元素硫粒径的减小而缩短,特别是在厌氧环境。②腐蚀产物为H2S和马基诺矿Fe1+xS(0≤x≤0.11)。③严重的腐蚀是自催化过程。④腐蚀开始后,腐蚀电位不断升高。⑤碳钢和元素硫的直接接触是严重腐蚀发生的必要条件。⑥pH值随反应时间的增加而升高。基于以上发现,他们提出了催化理论:
总的电化学反应:(x-1)Fe+Sy-1S2-+2H2
笔者指出虽然不知道附加反应的具体反应程度,但附加反应的加入使整个理论完整。附加反应成功解释了低碳钢在含硫化氢的水环境中发生的氢脆:产生的氢原子(Had)进入钢内部,在夹杂物或缺陷处聚集,进一步反应生成氢气,当压力超过钢断裂临界压力,产生裂纹,随着氢原子不断进入,裂纹不断扩展,最终产生氢脆(氢压理论)。反应式中Sy-1·S2-是由硫离子和固体硫颗粒的化学吸附作用产生的,S2-和吸附的多硫酸盐离子可能是元素硫与水反应生成的。生成马基诺矿中的硫铁比不是1∶1,其不完美结构使硫化亚铁具有半导体的性能,像一个导线连接了阴极和阳极,形成了无数腐蚀电池,催化了上述反应。
3.1.2 水解机理
1981年Maldonado等做了元素硫的水解实验[25-26],并研究了水解后的溶液对碳钢的腐蚀,发现在3 000r/m的转速下元素硫水解产生的溶液的pH值很低,随温度的升高pH值不断下降,并且水解后的溶液对碳钢片和铁粉都产生强烈的化学反应。基于这些发现和前人的研究结果,他们提出了潮湿的元素硫对碳钢的腐蚀是由元素硫与水反应产生的硫酸(H2SO4)和硫化氢(H2S)对碳钢的化学反应的理论,水解反应方程为:4S+4H2→O 3H2S+H2SO4。元素硫的表面形成扩散层,由于极性和吸附力的不同,使得H+聚集在硫颗粒的表面而HS-和SO42-堆积在硫颗粒的边缘(图3),元素硫扮演了氢离子载体的角色,固体硫颗粒表面物理吸附氢离子的堆积导致颗粒表面的pH值下降。从标准摩尔吉布斯自由能来看,ΔrGθm=157.833kJ/mol,说明常温常压下,反应不能自发形成,必需升温或者搅拌等方式促使反应进行。
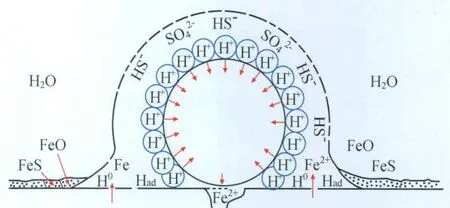
图3 可溶性离子在硫颗粒的分布和对碳钢表面的影响示意图
此外,他们在水解后溶液对碳钢腐蚀的过程中发现了两个有价值的现象:
1)诱导期的存在:刚把碳钢加入溶液中时,虽然碳钢的腐蚀电位在降低,但是腐蚀并没有马上发生,而是过了一段时间,严重的腐蚀反应才发生。他们认为这段时间硫酸根离子和HS-大量形成并到达一定稳定值,因此,这段时间pH值上升。
2)活性期的存在:实验中碳钢在水解后溶液中的腐蚀速率比含可溶性硫化物离子溶液或硫酸溶液的腐蚀速率高。这是由于碳钢和溶液中的H+反应导致溶液中的H+减少,硫的进一步水解补充溶液中的H+,使反应持续进行。
3.1.3 电化学腐蚀机理
Schmitt总结前人的研究成果结合自己关于阴离子对腐蚀影响的实验成果[27],在1991年提出了一个关于潮湿元素硫的电化学腐蚀机理。元素硫和水首先反应产生H2S,然后H2S和铁以及氧化亚铁反应在碳钢表面形成马基诺矿。因为这种腐蚀产物的结构缺陷,使得硫化亚铁膜具有高的导电性,因而充当了电子从金属表面传递到元素硫的载体。由于油气田生产中产出的地层水中含有大量的Cl-,而活性离子Cl-影响腐蚀产物膜的稳定性。因而Schmitt G提出了含有Cl-的电化学反应(图4):
阳极金属溶解:Fe+2Cl-+H2→O[Fe(OH)++Cl-]+HCl+2e-

图4 Cl-存在时的硫腐蚀机理图
阳极区的铁离子水解生成水合氢离子导致pH值下降,从而提高了阳极区域的腐蚀速度。在阴极区域形成了氢氧根离子,pH值增加。因此,钢铁的硫腐蚀类似于氧浓差电池,并形成局部pH值变化。这种机理完美地解释了钢在湿硫环境下的局部缝隙腐蚀。加入下面的3个反应,使得腐蚀机理得以完善:
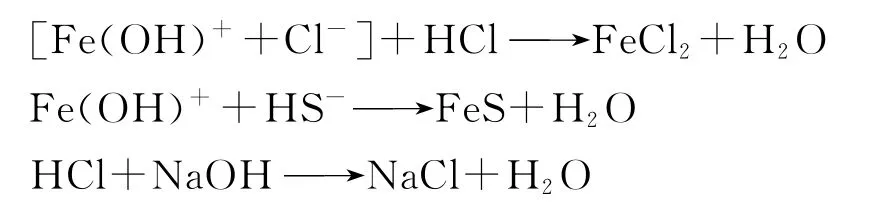
通过X射线衍射(XRD)对含硫气井的硫化物膜成分进行检测,证实了氯化亚铁(FeCl2)的存在。
关于阴离子效应的研究发现阴离子(F-、Cl-、Br-、I-、SO4-)大幅度降低了反应的活化焓(纯水活化焓为28kJ/mol,而阴离子水溶液的活化焓降低到13~18kJ/mol),腐蚀速率并按照 F-、Cl-、Br-、I-、SO4-的顺序不断增大,表明阴离子效应是熵控制而非焓控制[27]。阴离子通过特性吸附和催化作用加速元素硫对钢的腐蚀。
3.1.4 直接腐蚀机理
以上以元素硫水解为基础的腐蚀机理,都指出水解产物中有SO4-的存在,但腐蚀实验的最终产物都是铁的硫化物和氧化物,而没有硫酸亚铁(FeSO4)或者硫酸铁[Fe2(SO4)3]。Zhang Lei等人做了熔融元素硫在3.5%NaCl溶液环境下的碳钢腐蚀实验,腐蚀产物的X射线衍射(XRD)分析证实没有硫酸亚铁或硫酸铁的存在,产物只有磁黄铁矿、黄铁矿和马基诺矿。因而不少科学家产生了对以元素硫水解为基础的腐蚀机理的质疑,认为硫原子和铁原子的直接反应更加可能。基于严重腐蚀的发生需要潮湿环境中碳钢与元素硫的直接接触,结合自己的研究结果,Norman Dowling提出了直接腐蚀机理(图5)。
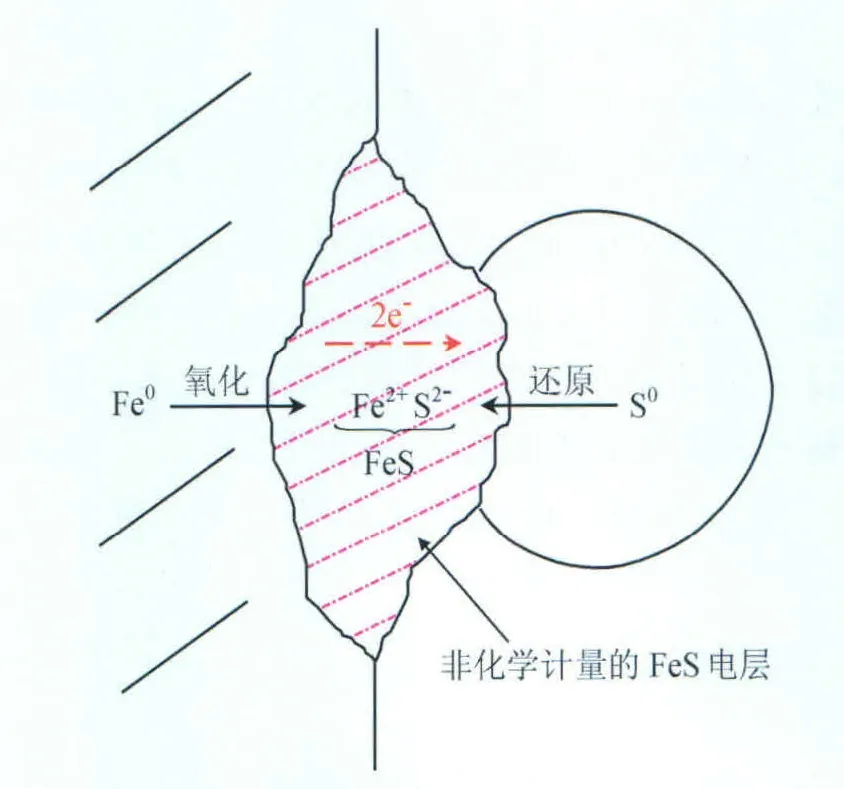
图5 硫与铁直接反应原理图
诱导期主要发生:铁在水中的腐蚀、包裹在固体硫中的硫化氢(H2S)的释放或在元素硫表面SxOy2-类型的硫化物在水中的歧化反应生成硫化氢(H2S),进而发生硫化氢的水解。腐蚀产生的Fe2+和水解出的HS-(硫化氢的水解以一级水解为主)达到一定浓度时,FeS产生(Fe2++HS→-FeS+H+)。腐蚀产物FeS由于其结构缺陷,催化了腐蚀的进一步发生。Norman Dowling通过电化学手段研究了固体硫的还原反应(图6),通过外加电流给放置在FeSO4溶液中覆盖着元素硫的铂片进行腐蚀,其产物通过X射线发射谱(XES)证明了FeS的存在,从而证明了上述腐蚀机理的可能性。
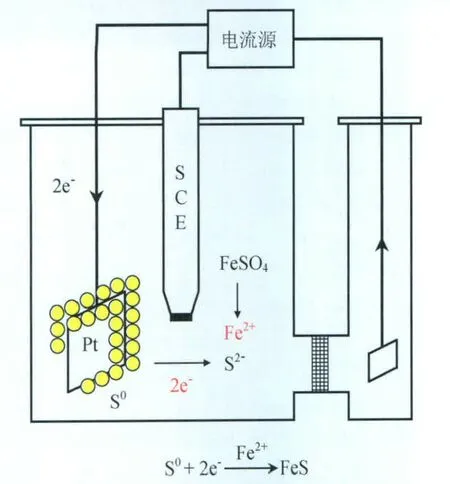
图6 硫的还原反应电化学图
3.2 影响硫腐蚀的环境因素
影响元素硫对碳钢腐蚀的环境因素较为复杂,主要包括温度、压力、氯离子、硫的存在形式和流速等。
3.2.1 温度和压力
温度和压力对碳钢硫腐蚀的影响主要体现在以下3个方面:①影响元素硫在酸性气体(硫化氢为主)中的溶解度,硫的溶解度随着压力和温度的升高而增加[28],温度压力的升高减少了元素硫的沉积量进而抑制了腐蚀的进行,反之将增加硫沉积,促进腐蚀;②温度和压力的升高,加快了硫、硫化氢与金属的反应速率,促进了腐蚀的进行;③影响腐蚀类型,硫悬浮存在且溶解度低于10g/L时,碳钢腐蚀速率随温度的升高而增加并且腐蚀类型从全面腐蚀变为局部腐蚀[29]。
3.2.2 氯离子
天然气生产过程中多会产出地层水,而地层水中富含氯离子,由于u-氯离子的半径小,将会对腐蚀产生下列影响:
1)降低试样表面钝化膜形成的可能性或加速钝化膜的破坏,促进局部腐蚀。
2)使得CO2和H2S在液体介质中的溶解度降低,增加酸性气体的含量,从而增加溶解的元素硫含量,减少硫沉积,减缓硫腐蚀。
3)影响腐蚀产物的形成位置。无Cl-时,腐蚀产物形成于与元素硫直接接触的碳钢表面;而在10%的氯化钠溶液中,腐蚀产物形成于未与硫直接接触的碳钢表面[30]。
4)Sato认为,Cl-的自催化效应对基体金属的溶解还具有加速作用[31],导致金属一直处于活化态。Cl-能优先吸附于腐蚀产物膜中金属内应力产生的各种缺陷处,或者挤掉吸附的其他阴离子,或者穿过膜的孔隙直接与金属接触后发生作用,形成可溶性的化合物,引起金属表面的微区溶解而产生点蚀核心;Cl-会在点蚀坑内富集,造成局部pH值下降,Cl-在蚀坑内外的浓度差导致局部的电偶腐蚀,形成大阴极、小阳极的腐蚀特征,最终导致很高的局部腐蚀速率。
3.2.3 硫的存在形式
实验室研究了硫的4种存在形式:悬浮、沉积、黏贴覆盖和熔化覆盖,硫与碳钢表面接触越紧密,腐蚀速率越高。其中沉积和黏贴覆盖以均匀腐蚀为主,而悬浮和熔化覆盖以局部腐蚀为主[29]。
硫悬浮存在时,碳钢的腐蚀速率随元素硫的含量增加而加大,元素硫含量10g/L时碳钢的腐蚀速率达到最大值,而后随元素硫含量的增加而减小。这主要是由于增加悬浮硫含量,就增加了硫与样本表面接触的面积,促进了腐蚀的发生。当继续增加悬浮硫含量时,更多硫粒子集聚成团阻碍了硫与样品表面的有效接触,从而降低了腐蚀速率。
3.2.4 流速
研究发现气体在管内的流速直接影响到气流携带元素硫的效率,流速越高,则愈能有效地使元素硫悬浮于气体中带出。但高流速影响缓蚀剂的效果,当气体流速高于10m/s时缓蚀剂就不再起作用。而且高流速还会加剧冲刷腐蚀,因而必须控制气体流速的上限。为有效地带出元素硫且不增加腐蚀,气体的流速应大于3m/s、小于5m/s。
此外气体组成、地层水矿化度、使用的缓蚀剂和溶硫剂,以及注入的甲醇和侵入的氧气都会影响管道中的硫腐蚀。
4 结论与建议
1)研究温度、压力、气体组分以及H2S和CO2分压对元素硫溶解度的影响,特别是主要组分物理性质剧烈变化对元素硫溶解的影响。
2)结合高含硫气田的地质特征和气体组成,提出适合其实际情况的硫沉积预测模型,研发经济、高效、环保、能循环使用的溶硫剂。
3)研究产层中超临界态流体的腐蚀机理和主要组分临界点附近的腐蚀机理。
4)针对硫沉积区的特殊环境,开展多介质多相混合流体中管线的硫腐蚀机理研究,并建立其腐蚀模型。
[1]BRUCKHOFF W.New results in corrosion control in sour gas wells[J].Erdoel,Erdgas Zeitschrift,1979,95(3):82-89.
[2]OCKELMANN H,BLOUNT F.Ten years′experience with sour gas production in Germany[C]∥paper 4663-MS presented at the Fall Meeting of the Society of Petroleum Engineers of AIME,30September-3October 1973,Las Vegas,Nevada,USA.NewYork:SPE,1973.
[3]刘志德,路民旭,肖学兰,等.高含硫气田元素硫腐蚀机理及其评价方法[J].石油与天然气化工,2012,41(5):495-498.LIU Zhide,LU Minxun,XIAO Xuelan,et al.Elemental sulfur corrosion mechanism and evaluation methods for high sour gas fields[J].Chemical Engineering of Oil & Gas,2012,41(5):495-498.
[4]潘光成,李涛,吴明清.加氢型喷气燃料元素硫腐蚀性研究[J].石油与天然气化工,2012,41(5):464-468.PAN Guangcheng,LI Tao,WU Mingqing.Study on element sulfur corrosion of hydrogenation jet fuel[J].Chemical Engineering of Oil & Gas,2012,41(5):464-468.
[5]李时杰,杨发平,刘方俭.普光气田地面集输系统硫沉积问题探讨[J].天然气工业,2011,31(3):75-79.LI Shijie,YANG Faping,LIU Fangjian.A discussion on the sulphur deposition in the ground surface gathering and transmission system of the Puguang Gas Field[J].Natural Gas Industry,2011,31(3):75-79.
[6]杜志敏.高含硫气藏流体相态实验和硫沉积数值模拟[J].天然气工业,2008,28(4):78-81.DU Zhimin.Phase behavior experiments of gas reservoir fluid with high sulfur content and numerical simulation of sulfur deposition[J].Natural Gas Industry,2008,28(4):78-81.
[7]ZHANG Xuefeng.Special elemental sulfur in the dolomite reservoirs of the giant Puguang Gas Field:Proof of crude oil involved thermochemical sulfate reduction[J].Procedia Earth and Planetary Science,2011(2):229-234.
[8]王一刚,窦立荣,文应初,等.四川盆地东北部三叠系飞仙关组高含硫气藏 H2S成因研究[J].地球化学,2002,31(6):517-524.WANG Yigang,DOU Lirong,WEN Yingchu,et al.Origin of H2S in Triassic Feixianguan Formation gas pools,northeastern Sichuan Basin,China[J].Geochimica,2002,31(6):517-524.
[9]朱光有,张水昌,梁英波,等.川东北地区飞仙关组高含H2S天然气TSR成因的同位素证据[J].中国科学:D辑地球科学,2005,48(11):1037-1046.ZHU Guangyou,ZHANG Shuichang,LIANG Yingbo,et al.Isotopic evidence of TSR origin for natural gas bearing high H2S contents within the Feixianguan Formation of the northeastern Sichuan Basin,southwestern China[J].Science in China:Series D-Earth Sciences,2005,48(11):1960-1971.
[10]张水昌,朱光有,梁英波.四川盆地普光大型气田H2S及优质储层形成机理探讨——读马永生教授的“四川盆地普光大型气田的发现与勘探启示”有感[J].地质论评,2006,52(2):230-235.ZHANG Shuichang,ZHU Guangyou,LIANG Yingbo.Probe into formation mechanism of H2S and high-quality reservoirs of Puguang large gas field in Sichuan Basin—the new cognition after reading professor Ma’s paper“Discovery of the large-scale gas field in the Sichuan Basin and its enlightenment for exploration[J].Geological Review,2006,52(2):230-235.
[11]BOJES J.Sulfur deposition and other aspects of the chemistry and technology of sour gas production[C]∥Conjunction with ASRL’s Sulfur Deposition Forum.Calgary:U-niversity Research Centre,2006.
[12]BOJES J,LERBSCHER J,WAMBURI W.Elemental sulfur in 3-phase sour gas systems is conderstate really your ally[C]∥Northern Area Western Conference,15-18 Februrary,2010Calgary,Alberta,Canada.Houston:NACE International Publications,2010.
[13]刘德汉,肖贤明,熊永强,等.四川东部飞仙关组鲕滩气藏储层含自然硫不混溶包裹体及硫化氢成因研究[J].中国科学:D辑 地球科学,2006,36(1):1-13.LIU Dehan,XIAO Xianming,XIONG Yongjiang,et al.Eastern Sichuan group of oolite beach Feixianguan gas reservoir containing immiscible inclusion of natural sulfur and hydrogen sulfide formation research[J].Science in China:Series D-Earth Sciences,2006,36(1):1-13.
[14]BOIVIN J,OLIPHANT S,LIMITED C,et al.Sulfur corrosion due to oxygen ingress[C]∥paper 11120presented at NACE International Corrosion Conference and EXPO,13-17March 2011,Houston,Texas,USA.Houston:NACE,2011.
[15]唐力,陈铭奇.高含硫气体中元素硫溶解、沉积的机理分析[J].新疆石油科技,2009,19(1):39-40.TANG Li,CHEN Mingji.The elemental sulfur in high sulfur gas dissolving and deposition mechanism analysis[J].Xinjiang Petroleum Science & Technology,2009,19(1):39-40.
[16]CHESNOY A B,PACK D J.S8threatens natural gas operations,environment[J].Oil and Gas Journal,1997,95(17):74-79.
[17]PACK D J.Elemental sulphur formation in natural gas transmission pipelines[D].Perth:University of Western Australia,2005.
[18]KARAN K,HEIDEMANN R A,BEHIE L A.Sulfur solubility in sour gas:Predictions with an equation of state model[J].Industrial & Engineering Chemistry Research,1998,37(5):1679-1684.
[19]HEIDEMANN R A,PHOENIX A V,KARAN K,et al.A chemical equilibrium equation of state model for elemental sulfur-containing fluids[J].Industrial & Engineering Chemistry Research,2001,40(9):2160-2167.
[20]GIRGIS MAGDY.Challenges in highly sour gas environment containing elemental sulphur[C]∥paper 117951-MS presented at the Abu Dhabi International Petroleum Exhibition and Conference,3-6November 2008,Abu Dhabi,UAE.New-York:SPE,2008.
[21]ROBERTS B E.The effect of sulfur deposition on gas well inflow performance[J].SPE Reservoir Engineering,1997,12(2):118-123.
[22]HANDS N,OZ BORA,ROBERTS B,et al.Advances in the prediction and management of elemental sulfur deposition associated with sour gas production from fractured carbonate reservoirs[C]∥paper 77332-MS presented at the SPE Annual Technical Conference and Exhibition,29 September-2October 2002,San Antonio,Texas,USA.NewYork:SPE,2002.
[23]DU Zhimin,GUO Xiao,ZHANG Yong,et al.Gas-liquidsolid coupled flow modeling in fractured carbonate gas reservoir with high H2S-content[C]∥paper 103946-MS presented at the First International Oil Conference and Exhibition,31August -2September 2006,Cancun,Mexico.NewYork:SPE,2006.
[24]ZHU Zhenjin,TAJAILLIPOUR N,PATRICK J,et al.Modeling of elemental sulfur deposition in sour-gas petroleum pipelines[C]∥NACE International 11124,Corrosion 2011,13-17March 2011Houston,Texas,USA.Houston:NACE,2011.
[25]MACDONALD D D,ROBERTS B E,HYNE J B.The corrosion of carbon steel by wet elemental sulfur[J].Corrosion Science,1978,18(5):411-425.
[26]MALDONADO S B,BODEN P J.Hydrolysis of elemental sulphur in water and its effect on the corrosion of mild steel[J].British Corrosion Journal,1982,17(3):116-120.
[27]SCHMITT G.Effects of elemental sulfur on corrosion in sour gas systems[J].Corrosion,1991,47(4):285-308.
[28]DOWLING N.Sulfur-related corrosion mechanisms[C]∥Corrosion Society,Calgary Section Elemental Sulfur Corrosion &its Mitigation,8October,2010,Calgary,Alberta,Canada.Houston:NACE,2010.
[29]BRUNNER E,PLACE JR M C,WOLL W H.Solubility of sulfur in sour gas[J].Journal of Petroleum Technology,1988,40(12):1587-1592.
[30]FANG Haitao,YOUNG D,NE I S.Corrosion of mild steel in the presence of elemental sulfur[C]∥NACE International 08637,Corrosion 2008Conference and EXPO,16-20March 2008,New Orleans,Louisiana,USA.Houston:NACE,2008.
[31]SATO N.Toward a more fundamental understanding of corrosion processes[J].Corrosion,1989,45(5):354-368.

