盐酸作吸收剂用于气态膜法从废水中脱除/回收氨氮
解利昕,王元喜,秦英杰,郝兴阁,李海庆,刘立强
(1天津大学化工学院,天津 300072;2天津市膜科学与海水淡化技术重点实验室,天津 300072;3天津凯铂能膜工程技术有限公司,天津 300308)
水体中的氨氮是导致水体富营养化的主要因素之一[1-2],国家对氨氮的排放制定了严格的标准。膜接触器用作气态膜法脱氨装置已经得到广泛研究并已得到工业化应用,它相当于把传统解吸塔和化学吸收塔微观上合二为一,同时克服了传统吸收塔雾沫夹带、沟流、液泛、返混等缺点,并具有投资少、能耗低、高效、操作简单、无二次污染等优点[3-7]。
气态膜脱氨过程一般以稀硫酸作吸收剂并得到副产品硫酸铵。然而在许多处理氨氮废水的场合,硫酸铵并非是理想回收产品。例如氯化铵焙烧法提取稀土金属过程中产生的含氨氮废水;化工厂氯化铵料液用多效蒸发浓缩结晶由于雾沫夹带产生的氨氮废水。在这些情况下,如果使用盐酸作吸收剂,回收的氨氮为氯化铵溶液,可以再回用到生产工艺中。因此,选择盐酸用于气态膜法脱氨具有重要意义。
王建黎等[8]考察了盐酸作吸收剂用膜接触器从废气中脱除回收氨的效果。但迄今为止还没有盐酸-气态膜法废水脱氨的研究报道。这有可能是因为盐酸被视为挥发性酸,研究者担心来自料液的挥发性氨和来自吸收液的挥发性氯化氢在膜壁微孔中的气相相遇生成氯化铵固体,进而破坏膜结构、导致膜孔润湿[9],破坏气态膜分离过程的顺利进行。但实际上,由于氯化氢与水强烈的缔合作用,低浓度盐酸中的氯化氢的饱和蒸气压极低[10],这使得HCl/H2O的相对挥发度远远小于NH3/H2O的相对挥发度;另一方面,膜蒸馏用于稀盐酸浓缩处理的结果发现,在低盐酸浓度下,氯化氢可以视为非挥发性组分[11]。这使得在一定适合的操作条件下,把氨和盐酸的反应严格控制在吸收液中,盐酸作吸收剂用气态膜法从废水中脱除回收氨氮是可行的。本文作者用气态膜过程从含氨水溶液中脱除/回收氨,探讨稀盐酸作为吸收剂的可行性,并研究各操作因素对传质性能和操作稳定性的影响。本研究将为盐酸法气态膜过程脱除废水中氨氮提供实验数据和理论基础。
1 实验部分
1.1 实验材料
本实验用的5个完全相同的微孔疏水性聚丙烯中空纤维膜组件(膜接触器)由天津凯铂能膜工程技术有限公司提供,膜丝及膜组件的具体参数见表1。
表1中,n为膜丝根数;di为膜丝内径;do为膜丝外径;Dm为膜组件外壳内径;L为膜组件有效长度;ζ为膜丝孔隙率;A为基于膜丝内径计算的膜组件有效面积;τ为膜丝曲率因子;dm为膜丝微孔最大直径;Pm为膜组件的测漏压力。
试剂:浓氨水、浓盐酸、硝酸汞、氢氧化钠、浓硫酸、氯化钠、二苯偶氮碳酰肼、纳氏试剂、溴酚蓝、乙醇,均购于天津江天化工试剂有限公司,所用试剂均为分析纯。
1.2 仪器设备
恒流泵,HD68型,上海青沪西仪器厂;电子天平,AL204-IC型,Mettler Toledo;紫外可见分光光度计,DL28型,Mettler Toledo;pH计,PB-106型,Sartorious;超级恒温槽,JD-3015型,宁波新芝生物科技有限公司。
1.3 实验流程及操作
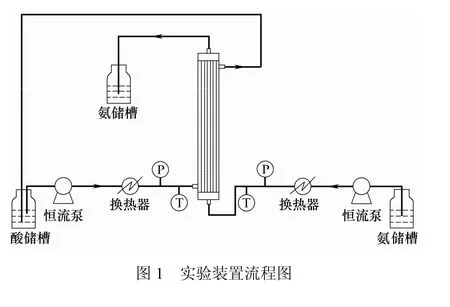
实验装置及流程如图1所示,含氨料液(氨氮浓度精确值由纳氏试剂测定)被泵出料液储槽,经恒流泵调节流速后流过换热器使温度控制在预定值,再流过膜组件管程,出口处料液氨浓度和氯离子含量被分别测定(氯离子含量由GB/T 13025.5—91测定);吸收液在壳程与料液呈顺流或逆流流动,料液采取一次性通过操作方式,吸收液采取循环操作方式。
新制的膜组件要先通过渗漏测试,使用中的膜组件也时常进行渗漏测试。渗漏测试的具体方法为:膜组件的壳程充满去离子水,在 2.5 atm(1 atm=101325 Pa)压力下压缩壳程水并持续2 h以上,只有管程两端出口处没有水渗出才表明膜组件完好。

表1 中空纤维膜及膜组件参数
2 实验数据分析处理方法
2.1 传质系数
盐酸是具有挥发性的强酸,盐酸(或氯化氢)与氨的反应是瞬间不可逆反应,因而 NH3分子和HCl分子之间的反应可认为发生在一个界面上。在气态膜法脱氨过程中,存在3种反应界面情况:盐酸与氨的反应界面在壳层吸收液中;盐酸(实质上是气态氯化氢)与氨的反应界面在膜壁微孔气相中;盐酸与氨的反应界面在管程料液中。只有反应界面在壳层吸收液中的情况才是人们期待的气态膜法脱氨过程。此时盐酸吸收氨的传质过程如图2所示,管程料液中的游离氨挥发透过膜壁微孔后在壳程壁面处被吸收液溶解吸收,壳程壁面处气相氯化氢的分压为零,不存在由于盐酸挥发性导致的膜渗漏问题。这种情况下氨氮脱除的总传质系数K与流入和流出膜组件的料液中氨浓度C0、C1及进料流量Q和有效膜面积A之间的关系可描述为式(1)[12-13]。

吸收过程的总传质阻力可以表示为壳程传质阻力、跨膜传质阻力与管程传质阻力之和,即式(2)。

式中,kS、kM、kL分别为膜壳程传质系数、跨膜传质系数、膜管程传质系数。
壳程传质系数可以表示为式(3)。

式中,D为游离氨在壳程中的扩散系数;d为游离氨在壳程扩散距离。

氨氮脱除率定义为式(4)。

2.2 膜渗漏表征
当吸收液中盐酸的浓度相对于料液中氨的浓度比较大时,氨与氯化氢的反应界面可能会在膜孔中,这会造成膜渗漏。如果吸收液中盐酸的浓度足够大,进料氨水中氨的浓度足够小,氯化氢就能气化、扩散通过微孔膜、溶解到管程料液中与氨反应,此时氨与氯化氢的反应界面在管程中,这相当于氨水吸收氯化氢。基于膜吸收法盐酸脱氨的考虑这两种情况都要避免。任何情况下,用盐酸作吸收剂的气态膜法脱氨过程的操作稳定性可由氯离子的渗漏量来表示,定义为式(5)。

式中,CClo为管程出口料液中氯离子浓度;CCli为管程进口料液中氯离子浓度。理想情况下,氯离子渗漏量为0,当氯离子渗漏量明显大于0时可以认为膜孔出现润湿问题。
3 实验结果与讨论
3.1 可行性研究
实验条件为:使用膜组件1#,料液氨浓度5000 mg/L,流速0.02 m/s,温度25 ℃;盐酸吸收液流速0.0424 m/s,温度25 ℃,顺流操作。

实验中定时向酸槽中添加盐酸以维持吸收液中酸的浓度基本恒定。每组实验持续进行 9 h,每隔1.5 h测量一次总传质系数与氯离子渗漏量。传质系数测量的结果如图3所示,使用低浓度盐酸作吸收液时的总传质系数基本不随时间变化,同时测量氯离子渗漏量基本为 0,说明膜组件性能保持完好;吸收液中盐酸浓度较低时,总传质系数K随吸收液中酸浓度增大而增大,这是因为低酸浓度时壳程存在明显的游离氨传质阻力,吸收液中盐酸浓度越大游离氨在吸收液中需要扩散的距离越小,壳程传质阻力越小,因之总传质系数越大;质量浓度 6%的盐酸作吸收液时总传质系数随时间延长而降低,实验最后测得管程出口料液中氯离子浓度为 415.7 mg/L。试验后对膜组件进行渗漏测试,膜组件渗漏严重。渗漏后的膜组件不能用去离子水清洗、碱溶液和酸溶液依次清洗并随后干燥等手段恢复疏水性能,即膜组件遭到严重损坏。这证明了低浓度盐酸用于气态膜法脱氨的可行性,而高浓度盐酸溶液用作吸收剂时挥发性的氯化氢和氨分子在膜微孔内反应生成的氯化铵固体会使膜组件不可逆地损坏。
3.2 盐酸临界浓度
实验条件:使用膜组件2#,料液流速0.02 m/s,温度25 ℃;盐酸吸收液流速0.0424 m/s,温度25℃,顺流操作。
如前面讨论在一定操作条件下某一浓度的含氨进料液对应一个盐酸吸收液的最大允许浓度,这个最大浓度定义为盐酸临界浓度。只有吸收液中盐酸浓度小于临界浓度时氯化氢才不会扩散到膜壁微孔中,膜组件才可以长期稳定地运行。在上述实验条件下,以管程出口料液中氯离子浓度大于10 mg/L时的吸收液中盐酸浓度视为临界浓度。如图4所示,盐酸临界浓度随着进料氨浓度增大而近似对数增加。这可能是因为在考察的浓度范围内与氨水料液呈气液平衡的气相中氨气分压符合亨利定律[14],而与盐酸水溶液呈气液平衡的气相中氯化氢分压不符合亨利定律而随盐酸浓度增加呈指数增加[10]。
3.3 操作方式对膜稳定性的影响

实验条件为:使用膜组件 3#,料液流速 0.02 m/s,温度25 ℃;吸收液盐酸质量浓度2%,流速0.0424 m/s,温度25 ℃。
总传质系数K随进料氨浓度变化如图5所示。在高氨浓度下逆流操作时的总传质系数大于顺流操作时的总传质系数,这可能是逆流操作时传质推动力大的原因。由图5可见,当顺流操作时进料氨水浓度从2000 mg/L增加到5000 mg/L,总传质系数减少了 27.6%,同时检测氯离子扩散渗漏量基本为零,实验后对膜组件进行渗漏测试,没有观察到膜组件渗漏。这是因为随着进料氨浓度增加氨扩散通量增加,造成壳程靠近膜壁处酸吸收液局部不足,氨和盐酸的反应界面向远离膜壁面的吸收液深处推进,使游离氨在壳程的传质阻力增大,其结果是造成基于管程料液进出口浓度变化计算的总传质系数降低。

逆流操作时,首先用高浓度氨水作料液,依次做低浓度氨水实验。如图5所示,总传质系数随氨进料浓度减少而增大,当使用2000 mg/L的氨水作料液时总传质系数突然降低,同时测得出口料液中氯离子浓度为178.5 mg/L。实验后对膜组件进行渗漏测试,测试持续5 min后膜组件出现渗漏。这可解释为:①逆流操作时管程出口处氨浓度最低而与之对应的壳程进口酸浓度最高,如果管程进料中氨浓度过低而壳程膜壁处吸收液相中盐酸浓度过高,高浓度的盐酸造成氯化氢汽化进入膜壁微孔中,随之与气态氨相遇生成固体氯化铵,固体氯化铵有可能堵塞部分膜壁微孔通道,减少膜有效面积,减少氨的扩散传递。②膜壁微孔中生成的氯化铵固体造成微孔内表面亲水化,而此管程出口处为管程压力最小而壳程压力最大的地方,亲水化的微孔可能造成吸收液穿透微孔膜进入管程从而把部分游离氨转化成铵根离子,减少了氨氮气态膜法脱除的推动力,从而造成基于管程料液进出口浓度变化计算的总传质系数的降低。③甚至过高浓度的盐酸吸收液造成氯化氢扩散到低氨浓度的管程料液侧,使得膜组件管程出口端脱氨过程变为脱氯化氢过程,这也大大减少据实验数据计算得到的总传质系数值。实验结束后对膜组件的渗漏测试表明氨和氯化氢在膜壁微孔中形成的固体氯化铵已经对疏水微孔膜造成损坏。由此可以得出,顺流操作比逆流操作稳定,故用盐酸-气态膜法脱除废水中的氨氮时建议采用顺流操作。
3.4 料液pH值对传质性能的影响
实验条件为:使用膜组件4#,料液氨浓度3000 mg/L,流速0.02 m/s,温度25 ℃;吸收液盐酸质量浓度 2%,流速 0.0424 m/s,温度 25 ℃,顺流操作。
实验过程中进料液的pH值通过添加氢氧化钠溶液或稀硫酸溶液来调节。料液pH值对总传质系数与氨脱除率的影响如图6所示,随着料液pH值上升,总传质系数与脱除率先是显著上升,当 pH值增大到11以后,总传质系数与脱除率上升缓慢。料液pH值从9.0升高到12.0总传质系数提高了一倍,脱除率从 24.7%提高到 42.7%。这是因为在氨水溶液中存在氨的水解平衡,pH值越大越有利于游离氨的生成,当pH值大于11时,氨在料液中几乎完全以游离氨的形式存在,传质推动力达到最大。故在气态膜法脱除废水中氨氮的过程中,进料 pH值应调节在11以上。
3.5 料液流速对传质性能的影响
实验条件为:使用膜组件4#,料液氨浓度3000 mg/L,温度25 ℃;吸收液盐酸质量浓度2%,流速0.0424 m/s,温度25 ℃,顺流操作。

总传质系数与脱除率随含氨料液流速的变化如图7所示。含氨料液流速从0.013 m/s增加到0.033 m/s,总传质系数略有下降,降低了5.9%。这是因为总传质系数是由管程传质系数、跨膜传质系数和壳程传质系数三部分构成的。经过很短的一段入口长度后,料液在管程的流动及传质边界层达到充分发展,管程的传质系数基本不随料液流速变化;跨膜传质系数与料液流速无关,只是温度的函数[15];而壳程传质情况比较复杂。可以设想,如果料液中氨浓度相对较大,部分游离氨扩散溶解进入壳程吸收液中才能遇见盐酸反应生成氯化铵的情况下,氨在壳程的传质阻力不能忽略。由实验数据计算可知由于料液进料速度的增加氨透膜通量增加了19.8%,在壳程酸不足的情况下这将增加壳程传质阻力,使总传质系数略微下降,由式(3)知壳程阻力增加使氨在壳程扩散距离增加,有利于膜组件稳定操作。
由图7知氨脱除率η从57.2%减少到26.8%,这是因为料液流速增加减少了料液中氨在管程中的停留时间,使游离氨的扩散时间减少,脱除率降低。实验过程中检测氯离子渗漏量基本为零,实验后对膜组件进行渗漏测试,膜组件完好。
3.6 盐酸流速对传质性能的影响
实验条件为:使用膜组件4#,料液氨浓度3000 mg/L,流速0.02 m/s,温度25 ℃;吸收液盐酸质量浓度2%,温度25 ℃,顺流操作。
由图8可知,盐酸流速从0.016 m/s增加到0.043 m/s,总传质系数增加了56%,脱除率从30.4%增加到43.2%。这是因为用2%的盐酸吸收3000 mg/L的氨水时壳程存在明显的传质阻力,在其它操作条件不变的情况下增大酸流速降低了壳程传质边界层,游离氨扩散距离d减小,壳程传质阻力降低,总传质系数与脱除率因之增加。但过薄的壳程边界层厚度有可能不利于膜组件长期稳定操作,所以不宜采用过高的壳程盐酸吸收液的循环速率。实验过程中检测氯离子渗漏量为零,实验后对膜组件进行渗漏测试,膜组件保持完好。
3.7 操作温度传质性能的影响
实验条件为:使用膜组件4#,料液氨浓度3000 mg/L,流速0.02 m/s;吸收液盐酸质量浓度2%,流速0.0424 m/s,顺流操作。
实验过程中保持管程与壳程进料温度一致。由图9可知,温度显著影响氨传质,操作温度从11 ℃升到到 35 ℃总传质系数增加了 79%,脱除率从33.8%增加到了 52.2%。这是因为随着操作温度升高,氨的亨利系数、液相扩散系数及在膜孔中的气相扩散系数都相应增大,所有这些因素使得K值增大[16]。实验过程中检测氯离子渗漏量为 0,实验后对膜组件进行渗漏测试,膜组件保持完好。
3.8 废水中氨氮脱除达标实验
实验条件为:使用膜组件4#,氨水料液体积5 L,氨浓度1000 mg/L,流速0.02 m/s,温度25 ℃;吸收液体积3 L,盐酸质量浓度0.5%,流速0.0424 m/s,温度25 ℃,顺流操作。


实验过程中氨水料液与盐酸吸收液均循环操作。氨储槽中氨氮浓度随时间的变化如图10所示,在实验进行120 min后,氨储槽中氨氮浓度降为13.2 mg/L,氨氮脱除率达到98.7%,测量此时盐酸吸收液的pH值为1.4,计算可知吸收液中盐酸质量浓度为0.145%。由文献可知此时的盐酸吸收液几乎不具有挥发性[10],而进料氨水中氨气的饱和蒸汽压仍然相对很大(由亨利定律计算可知)。检测氯离子渗漏量为 0,实验后对膜组件进行渗漏测试,膜组件保持完好。实验结果表明,用低浓度的盐酸吸收液脱除废水中的氨氮能达到很高的脱除率,处理后的废水能达到国家环保标准。
3.9 长期稳定性试验
实验条件为:使用膜组件5#,料液氨浓度3000 mg/L,流速0.02 m/s,温度25 ℃左右;吸收液盐酸质量浓度2%,流速0.0424 m/s,温度25 ℃左右,顺流操作。
本研究对一个新的膜组件进行了长期稳定性试验。定时向酸槽中添加浓盐酸维持酸吸收液浓度基本恒定,每天持续运行9 h,每3 h测量一次数据,当吸收液中氯化铵质量浓度大于15%时用新的稀盐酸替换吸收液,实验持续近3个月。实验结果如图11所示,总传质系数基本维持在 4.25×10−6m/s左右。氯离子渗漏量基本为0,实验过程中膜组件表现出了良好的稳定性。因此,用稀盐酸用于气态膜法脱除废水中的氨氮是可行的。

4 结 论
本文研究了稀盐酸作为吸收剂时气态膜法脱除废水中的氨氮的可行性,研究了影响气态膜传质性能的各种因素并考察了该工艺的操作稳定性,得到了如下主要结论。
(1)实验测定了一定操作条件下吸收液中盐酸临界浓度,用小于盐酸临界浓度的吸收液进行稳定性试验,膜组件稳定运行了650 h,表明盐酸用于气态膜吸收法脱氨是可行的。
(2)操作方式对膜传质性能与稳定性有较大的影响,逆流操作比顺流操作有利于传质,顺流操作比逆流操作稳定,建议采用顺流操作方式。
(3)实验发现含氨料液流速、浓度、pH值和盐酸吸收液浓度、流速及操作温度对氨的传质性能具有较大的影响。在考察范围内,料液流速和浓度增加使总传质系数降低了5.9%与27.6%;料液pH值与操作温度增加使总传质系数提高了一倍与79%;盐酸吸收液流速增加使总传质系数提高了56%。
(4)低浓度的盐酸吸收液在一定时间内将含氨废水中的氨氮脱除 98.7%以上,处理后的废水达到国家排放标准。
符 号 说 明
A——膜接触器有效表面积,m2
C0——料液进口浓度,mg/L
C1——料液出口浓度,mg/L
D——NH3在水中的扩散系数,m2/s
Dm——膜壳内径,cm
di——膜丝内径,m
dm——膜丝微孔最大直径,m
do——膜丝外经,m
K——总传质系数,m/s
kS——膜壳程传质系数,m/s
kL——膜管程传质系数,m/s
kM——跨膜传质系数,m/s
L——膜组件有效长度,m
n——膜丝根数
Pm——膜组件测漏压力,MPa
Q——料液流量,m3/s
ζ——膜丝孔隙率
τ——膜丝曲率因子
η——氨氮脱除率
[1]Dachs J,Eisenreich S J,Hoff R M.Influence of eutrophication on air-water exchange,vertical fluxes,and phytoplankton concentrations of persistent organic pollutants[J].Environmental Science and Technology,2000,34(6):1095-1102.
[2]Moazed H.Ammonium ion removal from wastewater by a natural resin[J].Journal of Environmental Science and Technology,2008,1(1):11-18.
[3]张秀芝,王静,张雨山,等.气态膜吸收法脱除水中氨的传质效果[J].化工进展,2011,30(2):438-442.
[4]齐麟,吕晓龙,贾悦.膜吸收从废水中脱氨的研究[J].水处理技术,2008,34(5):7-10.
[5]Shao Jiahua,Fang Xuliang,He Yiliang,et al.Emergency membrane contactor based absorption system for ammonia leaks in water treatment plants[J].Journal of Environmental Sciences,2008,20(10):1189–1194.
[6]徐又一,徐红,王红军,等.聚丙烯中空纤维膜结构与氨水分离性能研究[J].环境化学,1994,13(2):157-162.
[7]李玲,王冠平,施汉昌.膜吸收法应用于氨氮废水净化的研究[J].膜科学与技术,2006,26(3):74-78.
[8]王建黎,徐又一,徐志康,等.膜接触器从混合气中脱氨性能的研究[J].环境化学,2001,20(6):588-594.
[9]Gryta M.Fouling in direct contact membrane distillation process[J].Journal of Membrane Science,2008,325(1):383-394.
[10]Fritz J J,Fuget C R.Vapor Pressure of aqueous hydrogen chloride solutions,0 ℃ to 50 ℃[J].Journal of Chemical and Engineering Data,1956,1(1):10-12.
[11]Liu Rongling,Qin Yingjie,Li Xiaojun,et al.Concentrating aqueous hydrochloric acid by multiple-effect membrane distillation[J].Frontiers of Chemical Science and Engineering,2012,6(3):211-321.
[12]Wang S C,Xu S C,Qin Y J.Mass transfer in membrane absorption-desorption of ammonia from ammonia water[J].Chinese Journal of Chemical Engineering,1993,1(3):160-170.
[13]Qin Y J,Cabral J M S.Lumen mass transfer in hollow-fiber menbrane process with constant external resistances[J].AIChE Journal,1997,43(8):1975-1987.
[14]Hasanoglu A,Romero J,Perez B,et al.Ammonia removal from wastewater streams through membrane contactors;Experimental and theoretical annlysis of operation parameters and configuration[J].Chemical Engineering Journal,2010,160(2):530-537.
[15]Qin Y J,Cabral J M S,Wang S C.Hollow-fiber gas-membrane process for removal of NH3from solution of NH3and CO2[J].AIChE Journal,1996,42(7):1945-1956.
[16]张慧峰,王国强,张淑芬,等.温度对气态膜过程传质性能影响[J].水处理技术,2007,33(1):16-19.

