红霉素自乳化制剂处方研究
匡 扶 ,肖廷超 ,朱照静 ,钱 妍
(1.重庆医科大学附属第二医院药剂科,重庆 400010; 2.重庆医科大学图书馆,重庆 400016; 3.重庆医药高等专科学校,重庆 400030)
自微乳化给药系统(self-microemulsifying drug delivery system,SMEDDS)由药物、油相、非离子型乳化剂和助乳化剂组成,在温和搅拌下可自发形成O/W型微乳,其粒径小于100 nm。SMEDDS可显著提高水难溶性药物的溶出度、口服吸收率和生物利用度[1],是近年来药剂学研究的热点领域之一。SMEDDS口服后在胃肠道内迅速乳化,药物可直接进入小肠淋巴系统,后经胸腺淋巴管转运,不进入肝门静脉[2],因此可避免或减小药物的肝首过效应,提高药物的生物利用度。SMEDDS一般分装于软胶囊中,制备工艺简单,性质稳定,剂量准确且服用方便。红霉素是大环内酯类抗生素,近年来,临床报道其在各种感染和某些非感染性疾病治疗中的应用越来越多,如红霉素可抑制一些抗癌药从癌细胞内的主动外排,增强抗癌效果,并能逆转某些恶性肿瘤对抗癌药的耐药性[3];能抑制肺间质纤维化的形成[4];对于假单胞菌感染治疗有特殊用途[5]。但由于红霉素为水难溶性药物,其口服制剂存在不耐酸、溶出难、口服吸收率为18%~45%、生物利用度差等问题[6],极大地限制了临床应用,将红霉素制成SMEDDS有望解决上述问题。
1 仪器与试药
DF-101B型集热式恒温加热磁力搅拌器(郑州长城科工贸有限公司);AB204-E型分析天平(瑞士Mettler Toledo公司);800型离心机(上海手术器械厂);KQ2200B型超声波清洗器(昆山市超声仪器有限公司仪);Zetasizer Nano纳米粒度/zeta电位仪(英国马尔文仪器有限公司);UV-3150型紫外分光光度计(日本岛津株式会社);ZRS-8G型智能溶出仪(天津大学无线电厂)。橄榄油(OLIVE-OIL,盛隆天然药油有限公司,批号为090535);十四酸异丙酯(isopropyl myristate,IPM,美国Fluka公司,批号分别为1216171,21106124);吐温80(Tween 80,上海申宇医药化工有限公司,批号为090535);聚乙二醇400(PEG400),天津天泰精细化学品有限公司,批号为20090120);聚氧乙烯蓖麻油(polyoxyethylene castor oil,Cremophor EL,Fluka,批 号 分 别 为1210306,44506130);聚乙二醇 -8-甘油辛酸 /葵酸酯(Labrasol,LAS,法国Gattefosse公司,Lot 33347);红霉素原料药(内江山山制药厂,批号为090301,纯度为99.0%);红霉素标准品(中国药品生物制品检定所,批号为30307-200815纯度不低于98%)。
2 方法与结果
2.1 红霉素溶解度测定
在预试验基础上选取可形成微乳的油相(IPM,OLIVEOIL)、乳化剂(Tween 80,Cremophor EL)、助乳化剂(LAS,PEG400)进行研究。取上述6种液体各2 mL,分别置10 mL试管中,逐步加入红霉素原料药约10 mg(以减量法计量),每次超声溶解20 min,溶解平衡室温25℃静置30 min,观察溶解情况,直至饱和,根据《中国药典》近似溶解度的概念,判断出各种溶剂中药物的溶解能力级别。结果见表1。

表1 红霉素在不同溶剂中的溶解性(n=3)
根据表1结果,可选取溶解度大的IPM作为油相,LAS作为乳化剂。但红霉素在Cremophor EL和Tween80中溶解度差别不大,试验中发现超声溶解过程中体系温度上升时药物均溶解,当红霉素质量浓度大于20~30 g/L时室温下静置过夜后OLIVEOIL中的药物析出。应进一步通过空白伪三元相图进行比较,确定EM-SMEDDS处方组分以及各组分的比例。
2.2 EM-SMEDDS处方构成确定[7-9]
以 IPM为油相、LAS为助乳化剂,比较Tween 80与Cremophor EL为乳化剂时成乳情况,并确定各组分的最佳比例。通过滴定法绘制出油相-乳化剂/助乳化剂(混合乳化剂)-水体系的伪三元相图,先将乳化剂与助乳化剂按照Km值为1∶1,2∶1和3∶1(W/W)的比例混合,在三元相图中记为混合乳化剂(S-cos),再与油相 IPM 按 Km 值 1 ∶9,2 ∶8,3 ∶7,4 ∶6,5 ∶5,6 ∶4,7 ∶3,8 ∶2,9∶1(W/W)比例混合,37℃水浴,逐滴加入蒸馏水,搅拌混匀,记录系统状态变化并用Origin 7.5软件绘制伪三元相图。结果见图1和图2。可知,Cremophor EL成乳效果优于 Tween80,当 Km相同时,Cremophor EL体系自微乳化区域更大,试验还发现Cremophor EL体系黏度更小、分散时间更短,有利于在胃肠道内成乳。在油、混合乳化剂和水三者比例固定的情况下,当Cremophor EL含量增加,Km值增大,虽自微乳化区域增大,但伪三元体系的黏度增加,易形成难以分散的稠厚凝胶;当LAS含量增加,Km减小,体系黏度可有效降低,减少凝胶形成;同时提高LAS的比例还可提高载药量,促进药物在胃肠体内的吸收。因此,Cremophor EL成乳效果优于Tween 80,选用Cremophor EL为EM-SMEDDS乳化剂,当油相IPM与混合乳化剂比例在2∶(3~8)的范围内可形成微乳,其中混合乳化剂中Labrasol与Cremophor EL比例在11∶(21~33)的范围即可。

图1 以IPM为油相、Tween 80与Labrasol为混合乳化剂的伪三元相图
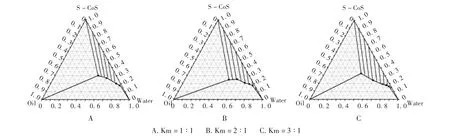
图2 以IPM为油相、Cremophor EL与Labrasol为混合乳化剂的伪三元相图
2.3 制备方法对制剂粒径的影响
2.3.1 处方组成和制备温度
在单因素试验基础上,选择载药量(X1)、体系中油相比例(X2)、混合乳化剂中Cremophor EL比例(X3)和制备温度(X4)四者为自变量,自微乳的平均粒径为因变量(Y),方案设计成4因素3水平,为使结果更准确,采用拟水平处理成9个水平[10-11]。用U9(95)均匀表设计试验,见表2。
按表2设计,精密称取相应油相、乳化剂助、乳化剂和药物,置西林瓶中,并在对应的水浴温度下搅拌混合20 min,冷却至室温备用。各组取0.05 mL EM-SMEDDS滴入50 mL、37℃恒温的分散介质(pH=6.8磷酸缓冲液)中,以转速50 r/min搅拌20 min,取5 mL,用Zetasizer Nano纳米粒度仪测定微乳的粒径和粒径分布范围。测定条件为He-Ne激光,测量角度135°,温度25℃,黏度0.933 cP,反射指数 1.43,波长 632.8 nm。微乳粒径测量结果见表2。以各组平均粒径为因变量,用SAS软件包对各因素进行多元非线性回归二项式拟合模型,Y=b0+b1X1+b2X2+b3X3+b4X4+b5X21+b6X1X2+b7X22+b8X3X1+b9X3X2+b10X23+b11X4X1+b12X4X2+b13X4X3+b14X24。通过拟合方程的回归系数r2对方程进行准确性检测。处理结果可得以下模型,Y=90.390 833 - 0.283 067X1-0.983 000X2-0.451 667X3+0.032 917X4- 0.000 457X21+0.009 173X2X1(r2=0.999 9,P<0.000 5)。

表2 均匀设计因素与水平U9(95)及实验结果
从模型可知4个因素对微乳平均粒径的影响:当制备温度(X4)在30~70℃范围内升高,乳滴平均粒径变大,故温度为30℃时平均粒径最小;混合乳化剂中Cremaonophor EL的比例(X3)在65% ~75%范围内增大,乳滴粒径减小,故Cremophor EL占混合乳化剂的75%时粒径最小;体系中油相所占比例(X2)和载药量(X1)有交互影响,X3和X4与其他因素间没有交互影响。为直观地判断X2和X1对粒径的影响,可以固定X3为75%和X4为30℃后,通过ORING75软件绘制曲面图,见图3。可见,当载药量(X1)为10%、体系中油相所占比例(X2)为20%时,乳滴的平均粒径最小;固定载药量10%、制备温度为30℃时,体系中油相所占比例(X2):20%~40%范围内,混合乳化剂中Cremophor EL的比例(X3)在65% ~75%范围内的任意组合均可形成粒径小于100 nm的微乳。
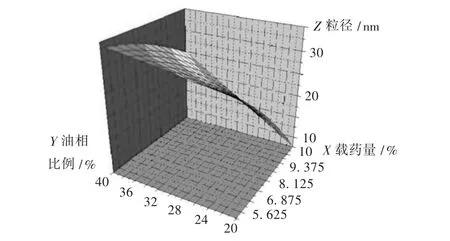
图3 固定 X3及 X4时,X1及 X2对平均粒径作效应曲面图
综合考虑到油相IPM是含17个碳的长链脂肪酸,在处方中适当增加比例可促进药物的淋巴转运吸收,减少红霉素的首过效应,提高生物利用的目的。从伪三元相图的绘制过程中也发现,乳化剂Cremophor EL含量增大时体系黏度增大、分散时间延长,助乳化剂LAS比例增加可以促进微乳迅速分散并促进药物的吸收。因此确定,EM-SMEDDS处方为体系中油相与混合乳化剂比例为3:7,混合乳化剂中LAS与Cremophor EL质量比为7∶13,载药量为10%,红霉素自微乳化制剂的乳化后粒径较小,粒径分布均匀且分散迅速。
2.3.2 加料顺序
水浴30℃时,以IPM为油相、油相与混合乳化剂质量比为3∶7、混合乳化剂中 LAS与Cremophor E质量比为7∶13、载药量为10%,分别按以下方式加料:油相、乳化剂和助乳化混合均匀后再加入药物(Ⅰ);药物溶解于油相后,再与乳化剂和助乳化混合均匀(Ⅱ);药物溶解于乳化剂后,再加入油相和助乳化混合均匀(Ⅲ);药物溶解于助乳化剂后,再加入乳化剂和油相混合均匀(Ⅳ);4种物质全部加入后再混合(Ⅴ);油相、乳化剂混合均匀,为空白SMEDDS(Ⅵ)。取上述配制的 EM-SMEDDS 0.5 mL滴入 50 mL、恒温37℃的水相中,以转速 50 r/min搅拌 20 min,取5 mL,用Zetasizer Nano纳米粒度仪测定微乳的粒径和粒径分布范围。测量条件见 2.3.1 项。结果见表3。
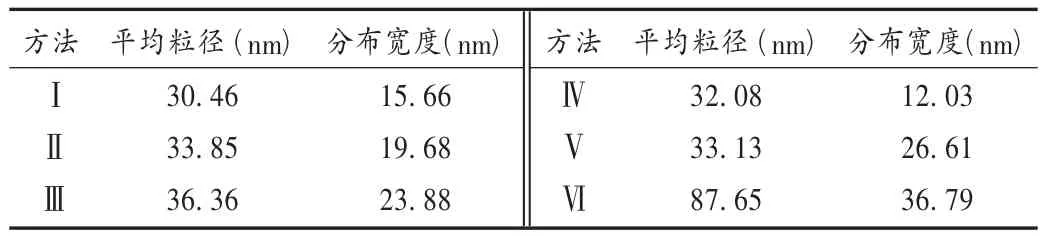
表3 加料顺序对微乳粒径、粒径分布的影响
可见,加料顺序对乳滴平均粒径和粒径分布有影响,第Ⅰ和第Ⅳ种方法的微乳粒径最小,粒径分布也相对较窄,原因可能是单独的每一种组份对红霉素的溶解能力均有限,这两种方法的混合体系能有效提高对红霉素的溶解能力;药物的加入使其形成的微乳粒径变小。第Ⅰ和第Ⅳ种方法都可制得粒径小且粒径分布也相对较窄的EM-SMEDDS,但考虑到后期试验中需要空白基质与对照,故本试验中选取第Ⅰ种方法。
2.3.3 自乳化效率
确定EM-SMEDDS处方构成,即以IPM为油相,油相与混合乳化剂质量比为3∶7,混合乳化剂中LAS与Cremophor E质量比为7:13,载药量为10%。制备方法是30℃水浴,先将油相、乳化剂和助乳化剂混合均匀,然后加入原料药,溶解混匀即得。用此方法制备3组EM-SMEDDS,采用溶出度测定方法中的小杯法,加入蒸馏水250 mL、37℃恒温的分散介质(pH=6.8磷酸盐缓冲液),精密量取 EM -SMEDDS 0.5 mL,注入杯底部,37 ℃恒温,以50 r/min搅拌分散,搅拌开始时计时,测定处方的分散时间,并测定所成微乳的平均粒径和粒径分布情况[12]。结果见表4。可见,该处方组成的EM-SMEDDS所成微乳平均粒径小于50 nm,粒径分布窄,且成乳迅速。

表4 EM-SMEDDS微乳的平均粒径和分布
2.4 EM-SMEDDS处方构成确定
以IPM为油相,油相与混合乳化剂质量比为3∶7,混合乳化剂中LAS与Cremophor E质量比为7∶13,载药量为10%,该红霉素自微乳化制剂的乳化后粒径较小,粒径分布均匀且分散迅速。EM-SMEDDS的制备方法先将油相、乳化剂和助乳化剂混合均匀,然后加入原料药,溶解混匀即得。
3 讨论
3.1 处方组成选择
油相:IPM是天然植物油提取物,对人体无影响,且可与多种乳化剂混合形成微乳,是制备微乳和自微乳的良好油相,而在预试验中以橄榄油为油相却难以形成微乳;微乳区面积的大小与油相分子量有关,分子量大的油相难以形成微乳,小分子油相的作用类似于助化剂,易嵌入到乳化剂中,与之形成界面膜,乳化剂对小分子油相的增溶量大于大分子油相。乳化剂:制备O/W微乳一般采用HLB值为10~15的非离子型乳化剂,比离子型乳化剂毒性低,但也会引起胃肠道壁渗透性的可逆性转变[11];本试验选取口服安全的乳化剂Cremophor EL,比Tween 80所形成微乳区域较大,不易形成凝胶,容易分散,长期放置较稳定。助乳化剂:助乳化剂的分子嵌入乳化剂分子中共同形成胶束的界面膜,起降低界面张力、增加界面膜的流动性、调节HLB值的作用,由此形成的微乳粒径较小,口服常用助乳化剂有乙醇、异丙醇、甘油、聚乙二醇、Transcutol(乙二醇单乙基醚)等,因乙醇等挥发性助乳化剂能迁移入明胶胶囊壳中,有可能导致药物析出,在预试验中选择LAS和PEG400作为辅助表面活性剂来考察对微乳形成的影响,结果PEG400作助乳化剂虽能形成微乳,但容易形成凝胶而难以分散,而LAS能明显降低体系的黏度而容易分散。
3.2 匀设计试验
因素水平选择时,载药量主要依据2.1项下的红霉素溶解度试验,体系中油相比例、混合乳化剂中组分比例两个因素主要是依据2.2项下的空白伪三元相图。而预试验中发现,制备温度对SMEDDS成乳的粒径有影响,温度越低,所成微乳的粒径越小,当温度高于70度时成乳粒径大于100 nm,考察无意义。考虑到实际操作过程一般为常温(25~40)℃,但因混合过程以及搅拌过程都能产生热量故考察温度定为30~70℃。匀设计试验的考察指标为粒径大小和粒径分布宽度,没有将剂型分散时间作为考察指标。因为在预试验中发现,Km在1∶1~1∶4时之间,油相与混合乳化剂比例为1∶4~1∶1均可在10 min内迅速分散形成微乳符合药典要求,再以剂型分散时间作为考察指标没有实际意义。
[1]李国栋.自微乳释药系统研究开发[J].国外医药:合成药生化药制剂分册,2001,22(5):304 -305.
[2]寇 欣.微乳给药系统的研究进展[J].天津药学,2005,17(6):49-52.
[3]葛成华,王世伟.红霉素逆转人胃癌细胞株多药耐药性的研究[J].外科理论与实践,2003,8(5):391 -393.
[4]Desaki M,Okazaki H,Sunazuka T,et al.Molecular mechanisms of antiinflammatory action of erythromycin in human bronchial epithelial cells:possible role in the signaling pathway that regulates nuclear factor-kappaB activation[J].Antimicrob Agents Chemother,2004,48(5):1 581 - 1 585.
[5]Amsden GW.Anti-inflammatory effects of macrolides-an underappreciated benefit in the treatment of community-acquired respiratory tract infections and chronic inflammatory pulmonary conditions?[J].Journal of Antimicrobial Chemotherapy,2005,55(1):10 -21.
[6]顾觉奋,王鲁燕.红霉素制剂的研究概述[J].中国医药情报,1997,3(4):248-252.
[7]胡 玮,曹红燕,李建平.用Origin绘制氯仿-醋酸-水三元液相图[J].实验技术与管理,2007,24(3):46 -48.
[8]汪 杨,吴 伟,阙 俐.油-吐温/醇-水体系伪三元相图在自微乳化制剂研究中的应用[J].中国医药工业杂志,2005,36(6):345-349.
[9]陆 彬,张正全.用三角相图法研究药用微乳的形成条件[J].药学学报,2001,36(1):58 -62.
[10]吴钟琪,周宏灏,许树梧.全科医学临床药物学[M].北京:科学出版社,2001:816-819.
[11]陆 彬.药剂学实验[M].北京:人民卫生出版社,1994:5-9,177-187.
[12]王思玲,苏德森.胶体分散药物制剂[M].北京:人民卫生出版社,2006:176-177.

