浊点萃取法提取青蒿中青蒿素的工艺研究
况 刚 ,杨 林 ,郑小平 ,何 丹
(1.重庆市食品药品检验所,重庆 410021; 2.重庆医科大学药学院,重庆 400016)
青蒿Artemisia annuaL.是菊科1年生草本植物,是唯一含青蒿素的蒿属植物,又名黄花蒿,为重庆道地药材,主要药效成分青蒿素(artemisinin)是非常有效的疟疾治疗药物[1]。青蒿素的传统提取生产工艺主要有有机溶剂萃取、超亚临界流体萃取、微波萃取等方法[2],但都存在提取率有限、杂质多、能耗高、试剂回收率低、资源严重浪费等不足。因此,寻找一种高效、低毒、稳定、适合工业化的青蒿素提取工艺对于重庆道地药材的利用开发尤为重要。本研究中采用浊点萃取技术提取青蒿中的青蒿素,以正交试验优化提取工艺,为青蒿素的高效、环保提取提供新方法。
1 仪器与试药
UV 240型紫外分光光度计(日本岛津公司);Model 800型超速离心机(上海优浦科学仪器有限公司);KQ2200B型超声波清洗器(昆山市超声洗器有限公司);电子恒温水浴锅(上海亚荣生化仪器厂)。青蒿素对照品(批号为100202-201004,中国食品药品检定研究院);青蒿药材采集于重庆各青蒿种植区县,由重庆市食品药品检验所中药室郑小平主管中药师鉴定为菊科植物黄花蒿Artemisia annuaL.干燥地上部分;其他试剂均为分析纯。
2 方法与结果
2.1 青蒿的提取
将青蒿粉末干燥,过60目,取约10.0 g,精密称定。向其中加入20 mL Genapol-X 80(10%),磁力搅拌混合均匀,300 W超声处理40 min后,4 000 r/min离心15 min,取上清液,加入适量盐溶液,再次混合均匀,60℃恒温水浴30 min,再4 000 r/min离心15 min,至溶液清晰地分为两层,上层为表面活性剂富集相,下层为水相。分液漏斗中分离去水相,上层表面活性层中加入2 mL甲醇,以降低黏度,用超滤膜过滤,回收表面活性剂,滤液旋干,得青蒿提取物。
2.2 青蒿素的含量测定[3]
2.2.1 溶液制备
精密称取浊点萃取得到的青蒿提取物0.88 g,溶解至25 mL容量瓶中,加入 0.2%NaOH溶液7 mL,于(50±1)℃水浴加热 30 min,进行衍生,取出,冷水快速冷却,0.22 μm 纤维素滤膜滤过,得供试品溶液。精密称取青蒿素对照品50.0 mg,无水乙醇溶解,50 mL容量瓶定容,得质量浓度为1 g/L的对照品溶液。
2.2.2 方法学考察
标准曲线绘制:精密吸取对照品溶液 1,2,3,4,5 mL,置 25 mL容量瓶中,按供试品溶液同法处理,以无水乙醇为空白,在292 nm波长处测定吸光度值,以吸光度(A)为纵坐标、质量浓度(C)为横坐标绘制回归曲线,回归方程为A=0.015 30C+0.001 6,r=0.999 6(n=5)。结果表明,青蒿素质量浓度在 0.04 ~0.2 g/L 范围内与吸光度线性关系良好。
精密度试验:取同一对照品溶液,依法在292 nm波长处测定吸光度。结果平均吸光度为 0.168,RSD为 0.56%(n=5),表明仪器精密度良好。
稳定性试验:取同一供试品溶液,于12 h内隔1 h测定1次吸光度。结果平均吸光度为 0.165,RSD为 1.1%(n=5),表明供试品溶液在12 h内基本稳定。
重复性试验:取青蒿提取物,依法制备供试品溶液并测定吸光度。结果青蒿素平均含量为15.34 mg/g,RSD为0.72%(n=5),表明方法重复性好。
回收率试验:取已知含量的青蒿提取物,加入适量青蒿素对照品,按供试品溶液制备方法制备待测溶液,依法测定吸光度,计算回收率。结果平均回收率为100.3%,RSD为1.45%(n=5),表明方法回收率较好。
2.2.3 样品含量测定
以无水乙醇作为空白参比,取青蒿提取物,依法制备供试品溶液,在292 nm波长处测定吸光度,计算含量。
2.3 提取工艺条件的优化
采用正交试验,以液固比(因素A)、平衡时间(因素B)、盐溶液离子强度(因素C)、聚氧乙烯脂肪醇醚(Genapol-X 80浓度,因素D)为考察因素,每因素取3水平,选用L9(34)正交表进行试验。因素水平见表1,结果见表2。可见,在影响浊点萃取法提取青蒿素的4个因素中,影响的大小次序为液固比、Genapol-X 80浓度、离子强度、平衡时间。各因素的优化工艺参数为A2B3C1D2,即液固比为 100∶1,平衡时间为 40 min,离子强度为 2.0 mol/L,Genapol-X 80浓度为 15.0%。此时青蒿素提取率最高,为15.33%。
2.4 最佳工艺验证试验
按优选的最佳工艺进行3次平行试验,结果青蒿素平均提取率为15.32 mg/g,RSD为1.1%(n=3),表明该工艺合理可行。
3 讨论
浊点萃取技术(cloud point extraction,CPE)以水代替有机溶剂作为萃取剂,通过加入少量表面活性剂产生浊点现象,从而实现高效提取[4]。其原理是,表面活性剂结构上的亲水基团与疏水基团分别与水和待提取的有效成分结合,形成疏水基团在内、亲水基团在外的胶束,从而显著提高水溶性不佳的有机物水提时的溶解度[5];同时,表面活性剂水溶液加热到一定温度(浊点温度)后,溶液变浑浊并出现分相,通过改变试验参数(如溶液的离子强度、温度等)引发相分离,最终实现溶质的高效富集和分离[6-7]。

表1 浊点萃取的因素水平表
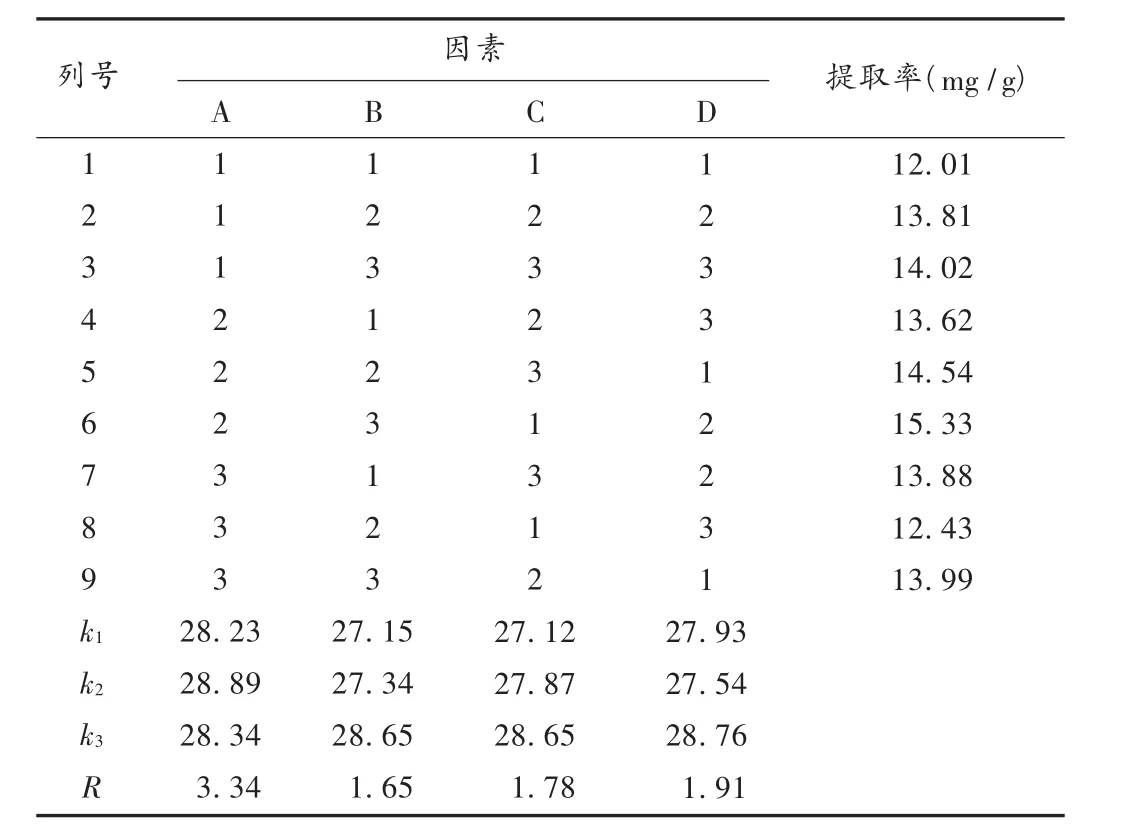
表2 浊点萃取条件的正交试验结果
用浊点萃取法提取青蒿中青蒿素,具有操作简单、绿色环保、避免高温破坏和提取率高等优点,试验中优化了液固比、平衡时间、盐溶液离子强度、表面活性剂浓度等影响萃取效率的各种因素,得到最佳工艺,为青蒿素的提取提供了一种新的方法。
[1]谢德玉,叶和春.青蒿素的研究进展——生物技术的应用前景[J].植物学报,1995,12(4):28-31.
[2]李子颖,李士雨,齐向娟.青蒿素提取技术研究进展[J].中药研究与信息,2002,2(4):17 -20.
[3]左巨波,代广会,杨俊卿,等.现场快速检测青蒿药材质量的方法研究[J].重庆医科大学学报,2009,34(2):206 -209.
[4]申进朝,邵学广.浊点萃取技术及其在有机化合物分离分析中的应用[J].化学进展,2006,18(4):482.
[5]王志龙.非离子表面活性剂为溶媒的浊点萃取技术[J].化学工程,2006,34(4):9.
[6]J Zhou,SW Wang,LX Sun.Determination of Osthole in rat plasma by high- performance liquid chromatograph using cloud-point extraction[J].Anal Chim Acta,2008,608(2):158.
[7]J Zhou.LX,Sun,SW Wang.Micelle -mediated extraction and cloud -point preconcentration of Osthole and imperatorin from Cnidium monnieri[J].J Chromatogr A,2008,1200(2):93.

