喹诺酮类药物不良反应的统计分析
王玉娟 梁 竹 陶 利
(济南军区总医院药剂科,山东 济南 250031)
喹诺酮类药物不良反应的统计分析
王玉娟 梁 竹 陶 利
(济南军区总医院药剂科,山东 济南 250031)
目的 通过对喹诺酮类药物不良反应的特点及成因的分析,为临床合理药物提供参考。方法 利用中国知网期刊数据库,统计 2012年最新发表的喹诺酮类不良反应报告。根据患者性别、年龄、给药途径、喹诺酮药物种类及 ADR 的临床表现等对收集的 2006 例喹诺酮类不良反应逐项进行统计分析。结果 药物不良反应(ADR)的规律和特点主要表现为:不良反应发生的年龄分布中老年人居首位,占59.36%;药物种类中左氧氟沙星居首位,占 35.33%;静脉滴注 63.14% 远高于其他给药途径;ADR 所累及的主要器官是神经系统(23.37%)、消化系统(21.19%)和皮肤及附件(19.35%)。结论 喹诺酮类不良反应多发生于老年人;静脉给药途径引起的不良反应高于口服给药途径;引起不良反应的主要药物是左氧氟沙星;不良反应所累及的器官-系统主要为神经系统、消化系统和皮肤及其附件。
喹诺酮类;药物不良反应;统计分析
1 文献综述
喹诺酮类(quinolones),又称吡酮酸类或吡啶酮酸类,是人工化学合成的抗菌药,母核为4-喹酮。随着医药科学技术的快速发展,喹诺酮类药物经过了不断的结构修饰,抗菌谱越来越广,抗菌活性越来越强。诺氟沙星、氧氟沙星、培氟沙星等是国内现阶段常用的主要品种。
喹诺酮类药物发展至今已开发出四代,第一代为萘啶酸,因其抗菌谱窄,口服吸收差,不良反应多已被淘汰;第二代为吡喹酸,口服后血药浓度低,尿中浓度高,主要用于尿道或肠道感染;第三代为氟喹诺酮,因抗菌谱广,高效,不良反应少,临床应用较广泛[1];第四代抗菌谱更广、药效更强、口服吸收快、血浆半衰期长、体内分布广,可以每天一次给药。
喹诺酮类因抗菌谱广、抗菌活性强,且使用方便而在临床上被广泛使用。因临床疗效确切,近年来该类药物不断在临床上广泛应用,其药物不良反应(adverse drug reaction,ADR)报道逐渐增加,有的甚至造成严重后果[2]。统计近四年来喹诺酮类抗菌药物的不良反应报告,探讨喹诺酮类不良反应的规律及特点,为临床合理用药提供参考,提高用药的安全性。
2 喹诺酮类的不良反应
2.1 皮肤过敏及光毒性
喹诺酮类药物较为常见的不良反应之一是过敏反应。其发生率为0.2%~3.0%[3]。文献分析表明喹诺酮类药物导致的过敏性休克[4],以环丙沙星、诺氟沙星、氧氟沙星发生率最高。光敏反应包括光毒反应和变态反应两类。这类药物在使用时,应避免暴露在阳光下。
2.2 消化系统不良反应
胃肠道反应也是喹诺酮类药物较为常见的不良反应之一。其中最为突出的是以环丙沙星所导致的不良反应,其次为诺氟沙星、氧氟沙星、氟罗沙星。临床症状为上腹部隐痛、呕吐、恶心,剂量越大,发生率越高。因此该类药物在使用时疗程不宜过长、剂量不宜太大。
2.3 神经系统不良反应
神经系统不良反应症状主要为头痛、眩晕、视力下降、耳鸣、听力下降、烦躁、抽搐及癫痫发作等。不良反应发生的原因推测为具有一定脂溶性的喹诺酮类药物透过血脑屏障进入脑组织,从而使中枢神经系统兴奋性增高[5]。因此服药时间在进餐后和睡觉前可明显降低头痛和眩晕的发生率[6]。
2.4 心血管系统不良反应
心血管系统表现为心慌、心悸、血压升高、心肌缺血、心肌炎、有时伴有心律失常,对心脏有一定的毒性[4]。因此,临床上在喹诺酮类药物使用时,应尽量避免与洋地黄等有心脏毒性的药物一起使用,同时也要避免与普萘洛尔等引起心动过缓的药物联合使用,使对心脏的毒副作用尽可能降低[7]。
2.5 泌尿系统不良反应
泌尿系统不良反应的表现为肾毒性,引起结晶尿、血尿、尿素氮升高,可发生肾炎、急性肾功能衰竭等[8]。
2.6 骨骼系统不良反应
软骨损伤是氟喹诺酮类对人体骨骼系统的不良反应,主要对未成年人的软骨组织产生损害。因而对尚未发育完全的18 岁以下的人群尽量不要使用喹诺酮类药物。此外,喹诺酮类还可引起用药部位、呼吸系统、全身反应性、代谢与营养系统等损害。因此,临床应用此类药物时必须合理,医师严格掌握喹诺酮类药物的适应证、合理选择药物及用药的剂量和方法,防止滥用[9]。提高患者用药的安全性、有效性。
3 资料与方法
3.1 资料来源
利用中国知网期刊全文数据库(CNKI),以喹诺酮和不良反应为检索主题对2012年1月1日至2012年11月30日发布的喹诺酮类抗菌药物的不良反应文献进行检索,共有文献133篇,其中18篇文献对该类药物不良反应做了详细的报道[10-27],其中统计不良反应报告2006例。
3.2 方法
按照患者性别、年龄、喹诺酮药物种类、给药途径、ADR的临床表现等对所收集的2006例喹诺酮类不良反应逐项进行统计分析。
4 结 果
4.1 ADR患者性别及年龄分布情况
对所收集的972例喹诺酮类抗菌药物不良反应病例,根据患者性别及年龄进行统计。而ADR多发生于中老年人,占59.36%。ADR的年龄分布如表1所示。
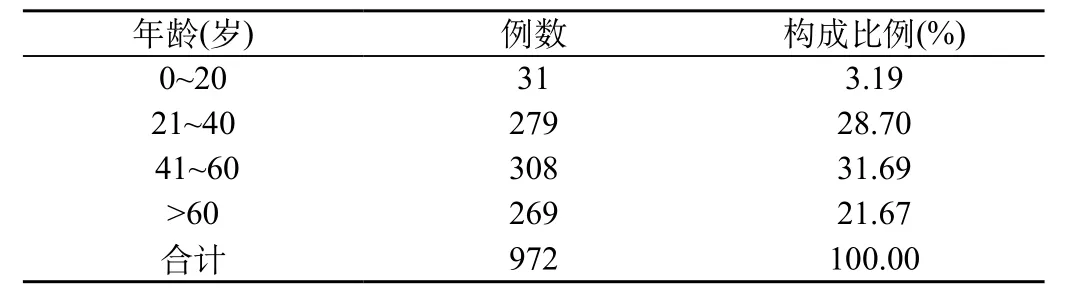
表1 ADR患者的年龄分布及构成比例
4.2 喹诺酮类药物品种分布
对所收集的1466例喹诺酮类抗菌药物不良反应病例,根据患者所用的喹诺酮药物种类进行统计,其中涉及到的喹诺酮类抗菌药物有左氧氟沙星、环丙沙星、加替沙星、诺氟沙星、氧氟沙星等14种。其中左氧氟沙星所导致的不良反应居首位,其次是环丙沙星、诺氟沙星和加替沙星等。患者所用的喹诺酮药物种类见表2。

表2 ADR病例的喹诺酮类药物品种及所占比例
4.3 喹诺酮类药物给药途径与ADR的关系
对所收集的1389例喹诺酮类抗菌药物不良反应病例,根据喹诺酮类药物给药途径进行统计,常用的给药途径为静脉滴注、口服、肌内注射、局部用药四种。ADR患者用量均为常规剂量。其中ADR患者最常用的给药途径是静脉滴注和口服。其给药途径与ADR发病率的关系见表3。
4.4 不良反应累及的系统-器官及临床表现

表3 喹诺酮类药物给药途径与ADR的构成

表4 ADR累及的系统-器官、临床表现及构成比
对所收集的1416例喹诺酮类抗菌药物不良反应病例,根据ADR所累及的系统-器官及临床表现进行统计。其中喹诺酮类药物的不良反应主要表现在神经系统、消化系统、皮肤过敏及其附件、心血管系统、泌尿系统等[28]。其中ADR主要表现在神经系统(居首位,占23.38%)、消化系统和皮肤及附件。ADR累及的系统—器官比例以及临床表现见表4所示。
5 讨 论
5.1 年龄与ADR的关系
ADR在各年龄段均有发生。由表1可以看出,大于40岁的中老年患者较多,占59.36%。老年人的肾脏、肝脏随着机体的衰老功能急剧下降、血浆蛋白输送药物的能力也在显著降低。另外,老年人常有合并用药的情况也使他们成为药物不良反应的高发人群[29]。鉴于老年人群药物代谢的特点,临床医师应考虑酌情慎用和减量使用此类药物,尽量降低不良反应的发生。
5.2 药物种类与ADR的关系
表2的数据显示,左氧氟沙星发生不良反应比例为35.33%,ADR例数较多可能与其在临床应用较广泛有关,临床应对过敏体质者慎用。环丙沙星为其次,为21.35%。
5.3 给药途径与ADR的关系
在四种给药途径中,静脉滴注引起的不良反应最多,占64.94%。这主要是由于静脉给药途径较直接、作用时间较快。另外,静脉注射液的pH、渗透压、注射液中的微粒、内毒素等都有可能引发ADR。而且,静脉给药时联用药物种类越多越容易引发ADR[30]。所以建议临床医师对患者用药时多首选口服给药,尽量不要使用静脉滴注的方案。静脉给药的方式只在急救时口服困难或无效时采用。必须静脉给药时,医师应询问患者ADR史,在安全有效剂量内合理使用。
6 结 论
喹诺酮类不良反应多发生于中老年人;不良反应所累计的器官-系统主要为皮肤及其附件;静脉给药途径引起的不良反应高于口服给药途径;引起不良反应的主要药物是左氧氟沙星。患者的年龄喹诺酮类抗菌药物的给药剂量、给药途径、药品种类及给药周期等均能影响ADR发生率,因此临床上应谨慎、合理地使用喹诺酮类抗菌药物。
[1]向绪彦.喹诺酮类药物的未来发展[J].医护论坛,2010,17(5):142-143.
[2]殷娟英.喹诺酮类药物的不良反应及防治对策[J].海峡药学,2009, 21(2):133-134.
[3]乔丽曼,楼旦,崔虓.浅谈喹诺酮类药物的不良反应[J].药物与临床,2010,48(32):53-54.
[4]杨晓,杨烨.喹诺酮类药物致过敏性休165 例文献分析[J].中国药房,2006,17(5):372- 374.
[5]李强,朱雄,王尔华.喹诺酮类抗菌剂结构与不良反应之间的关系[J].药学进展,2003,27(1):29-33.
[6]刁菱燕.喹诺酮类药物不良反应分析及注意事项[J].中国医院用药评价与分析,2008,8(2):143-144.
[7]Robinstein E,Camm J.Cardiotoxicity of fluoroquinolones[J].J Antimicrob Chemother,,2002,49(4):593-596.
[8]王玉满.喹诺酮类药物的不良反应及安全应用探讨[J].中外医疗,2009,29(1):85.
[9]黄玫,王丹丹.氟喹诺酮类药物不良反应与发生机制的研究进展[J].长春医学,2009,7(4):60-62.
[10]王琴.30例氟喹诺酮类药物致不良反应讨论[J].大家健康,2012, 6(6):57-59.
[11]虞玲芳,刘协萍.88例喹诺酮类药品不良反应报告分析[J].亚太传统医药,2012,8(8):84-85.
[12]兰敏.92例氟喹诺酮类药物不良反应临床分析报告[J].中国实用医药,2012,7(16):198-199.
[13]徐红冰.191例氟喹诺酮类药物不良反应分析[J].上海医药,2012, 33(3):36-38.
[14]刘瑞.对我院94 例氟喹诺酮类药物致胃肠道不良反应的回顾性分析[J].贵阳中医学院学报,2012,34(3):58-59.
[15]马进.氟喹诺酮类抗菌药物不良反应分析[J].实用医院临床杂志,2012,9(2):115-117.
[16]李福长,曾明辉.氟喹诺酮类抗菌药物致药物不良反应205例调查分析[J].临床合理用药,2012,5(3B):40-41.
[17]何佩莹.氟喹诺酮类抗生素不良反应65例临床分析[J].中外医疗,2012,32(11):109-110.
[18]薛周山.氟喹诺酮类药品不良反应的临床表现特点及其分布规律[J].中国药物经济学,2012,7(4):117-38118.
[19]杨汶刚氟喹诺酮类药物不良反应的临床特点分析[J].中国医药指南,2012,10(5):191-192.
[20]王树诚,王艳春.氟喹诺酮类药物不良反应分析[J].中国现代医药杂志,2012,14(6):27-29.
[21]蔺以啟.氟喹诺酮类药物临床应用的不良反应与用药原则[J].中国医药科学,2012,2(1):102-104.
[22]张丽萍.氟喹诺酮类药物致不良反应56例分析[J].中国乡村医药杂志,2012,19(6):60.
[23]丘志光,范雪燕.氟喹诺酮药物不良反应分析及合理应用[J].临床合理用药,2012,5(5C):42-43.
[24]邢海燕.喹诺酮类药物不良反应72例分析[J].现代医药卫生, 2012,28(7):1052-1053.
[25]李盛姿.喹诺酮类药物不良反应回顾性分析[J].现代医药卫生, 2012,28(17):2664-2665.
[26]黄洪波.喹诺酮类药物的耐药、联合用药及不良反应分析[J].中国当代医药,2012,19(4):57-58.
[27]陈玲.我院179例喹诺酮类药物不良反应情况分析[J].中国当代医药,2012,19(6):174-175.
[28]刘云霞,宋志伟.浅谈喹诺酮类药物不良反应[J].实用医药杂志, 2008,15(33):4787.
[29]滕永和.66例喹诺酮类药物不良反应分析[J].沈阳药科大学学报,2009,53(26):51-52.
[30]杨世春、陈明.116例喹诺酮类药物不良反应分析[J].广东医学院学报,2010,28(4):446-447.
Statistical Analysis of Adverse Drug Reaction Induced by Quinolones
WANG Yu-juan, LIANG Zhu, TAO Li
(Department of Pharmacy, Jinan Military General Hospital, Jinan 250031, China)
ObjectiveTo investigate the characteristics and causes of adverse drug reaction induced by quinolones so as to promote their rational applications in clinic.Methods2006 ADR(Adverse Drug Reaction) cases were collected from CNKI (China National Knowledge Infrastructure) in 2012. Term by term, these cases were analysised statistically in respect of patients’ ages, administration route, drug species,clinical manifestation,etc.ResultsThe old people composed most of the cases of ADR(59.36%).35.33% of ADR cases were induced by levofloxacin. The incidence of ADR induced by intravenous drip(63.14%)was very higher than other administration route.The lesions of ADR involved primarily nervous system (23.37%), digestive system(21.19%) and skin or its accessories (19.35%).ConclusionQuinolones ADR occurs more often in the elderly; In terms of incidence,intravenous administration was significantly higher than oral administration; ADR was primarily caused by levofloxacin; Adverse drug reaction mainly involved nervous system,digestive system and the skin and its accessories.
Quinolones; Adverse drug reactions; Statistical analysis
R969.3
:B
:1671-8194(2013)04-0027-03

