罗丹明类荧光探针的合成及在铜离子测定中的应用
王尚芝,郭 永,冯 锋,梁俊杰,李 平,孟双明*
(山西大同大学化学与化工学院,山西大同037009)
人体中微量元素铜,在生命过程中具有非常重要的作用,对肿瘤血管生长因子也起着重要调节作用[1],但高浓度的铜可能有害健康[2]。因此,检测铜元素的含量是非常有必要的。
目前,检测Cu2+的主要方法有原子吸收光谱法[3]、原子发射光谱法[4]、电化学法[5]、荧光光谱法[6]等。其中荧光法因检出限低、操作简单和高选择性,已得到了广泛的关注[7-8]。由于二价铜离子是d9结构顺磁性离子,对荧光具有较强的猝灭性,大多数报道的铜离子荧光分子探针都是猝灭型的,由于在探针识别客体时荧光猝灭不利于高通量信号输出,所以开发高灵敏、高选择性的荧光增强型铜离子荧光分子探针具有重要意义。
我们合成了一个新的苯甲醛-罗丹明类铜离子荧光增强型分子探针,并就探针的光谱特性及对铜离子的选择性识别作用进行了研究。
1 实验部分
1.1 试剂与仪器
试剂主要有罗丹明B、乙腈、80%水合肼、无水乙醇、3,4-二甲氧基苯甲醛等。实验用水为超纯水(18 MΩ·cm),其他试剂均为分析纯。

图1 化合物2和1的合成
金属离子标准溶液:均由其硝酸盐以水溶解制备。
化合物1的标准溶液:准确称取一定量的化合物1溶于乙腈中,配制成1.0×10-3mol/L化合物1储备液。
实验仪器主要有:SHZ-D(Ⅲ)循环水式真空泵(巩义市予华仪器有限公司),ADP31型真空烘箱 (日本yamato公司),精密烘箱 (DX-400型,日本yamato公司),RE200型旋转蒸发仪,ZF-20C暗箱式紫外分析仪(上海宝山顾村电光仪器厂),LS-55型荧光/磷光/发光分光光度计(美国PerkinElmer公司)。
1.2 实验过程
1.2.1 化合物 1 和 2 的合成
化合物1的合成过程见图1。中间体化合物2是根据文献[9]报道的方法合成。在50 mL容量瓶中,加入0.456 g(1 mmol)中间体化合物2并用20 mL 无水乙醇溶解。然后加入 0.159 g(1.5 mmol)3,4-二甲氧基苯甲醛。将混合物加热回流约8 h后,冷却溶液,加入20 mL水,有沉淀生成,过滤并用10 mL体积比为1∶1的水和无水乙醇的水溶液洗涤3次。减压干燥后,得到棕色固体。
1.2.2 荧光光谱的测定
在10 mL容量瓶中加入5.0 mL乙腈、0.5 mL储备液和一定体积的Cu2+溶液,用水稀释至刻度,摇匀,将溶液放置1.5 h后,用1 cm的石英比色皿,以550 nm为激发波长,记录溶液在555~640 nm波长范围内的荧光光谱。
2 结果与讨论
2.1 荧光光谱
按照1.2.2配制含不同铜离子的溶液,对化合物1进行荧光和紫外光谱测定。图2显示在未加入铜离子时荧光强度很弱,表明在这种情况下化合物1的螺酰胺环处于关闭状态[10]。当加入Cu2+后,荧光强度增大,并随铜离子浓度的增加增大,最大发射荧光波长由571 nm红移到584 nm。溶液由无色变为桃红色。铜离子浓度在2.8×10-7~2.8×10-5mol/L与荧光强度呈良好的线性关系。线性回归方程为ΔF=241.75 C + 1.39 (C 的单位是 10-6mol/L),相关系数 R=0.999 4。

图2 Cu2+与化合物1络合物的荧光光谱

图3 Cu2+与化合物1络合物在CH3CN中的紫外吸收
2.2 反应时间的影响
对含 5 μmol/L 化合物 1 和 28 μmoL/L Cu2+的10 mL的乙腈溶液(CH3CN/H2O体积比1∶1),在室温下测定荧光强度随反应时间的变化情况,图4显示化合物1与铜离子的反应在1.5 h后趋于稳定。
2.3 pH 值的影响
介质酸度对化合物1乙腈体系的荧光强度有很大的影响。如图5所示,在强酸性介质中,由于罗丹明的强质子化,罗丹明衍生物发生开环并造成化合物1在555 nm处荧光强度增加。当pH值大于5.33时,溶液变为无色又几乎无荧光,实验选择CH3CN/H2O(体积比1∶1)体系进行测试。
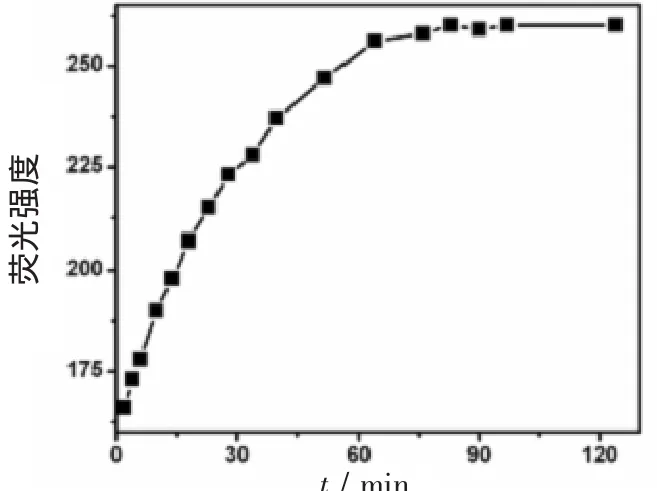
图4 Cu2+和化合物1的络合物的荧光强度随时间的变化
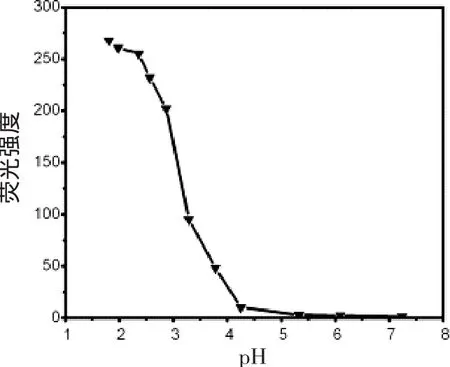
图5 pH值对探针荧光强度的影响
2.4 选择性研究
将5.0 mL乙腈和0.5 mL化合物1加到10 mL的容量瓶中,然后分别加入2.8×10-6moL/L Na+,K+,Ca2+,Mg2+,Zn2+,Ag+,Cd2+,Hg2+,Al3+,Co2+,Ni2+,Pb2+,Fe3+和 Cu2+。发现加入 Cu2+后溶液立刻变为红色。其他金属离子对化合物1影响很弱,该荧光试剂对铜离子有很高的选择性(图6)。

图6 化合物1的离子选择性
2.5 化合物1与铜离子的反应机理
根据文献[10]推测,探针与Cu2+的反应机理应该如图7所示。
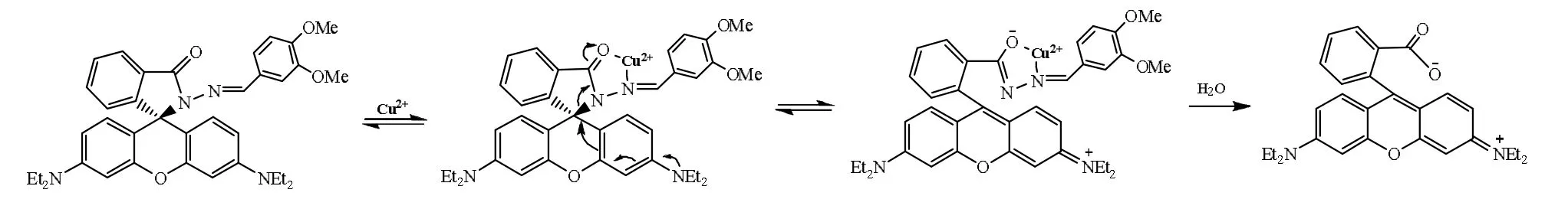
图7 Cu2+与化合物1的反应方程式
3 结论
合成的新型的罗丹明类衍生物,作为荧光试剂在乙腈/水溶液中呈现出对Cu2+很好的选择性,可以作为检测Cu2+的化学传感器,同时,利用此性质可以建立检测罗丹明衍生物的新方法。
[1]Blair B G,Larson C A,Adams P L,et al.Copper transporter 2 regulates endocytosis and controls tumor growth and sensitivity to cisplatin in vivo[J].molecular pharmacol,2011,79(1):157-166.
[2]Bertinato J,Zouzoulas A.Considerations in the Development of Biomarkers of Copper Status[J].J AOAC International,2009,92(5):1541-1550.
[3]王瑜.壳聚糖富集火焰原子吸收法测定水中痕量铜[J].分析化学,2005,33(6):872-874.
[4]Otero-Romanl J,Moreda-Pin~eiro A,Bermejo-Barrera P A.Evaluation of commercial C18 cartridges for trace elements solid phase extraction spectrometry determination[J].Anal Chim Acta,2005,536(1-2):213-218.
[5]Beni V,Ogurtsov V I,Bakunin N V,et al.Development of aportable electroanalytical system for the stripping voltammetry ofmetals:determination of copper in acetic acid soil extracts[J].Anal Chim Acta,2005,552:190-200.
[6]Yu M,Shi M,Chen Z,et al.Highly Sensitive and Fast Responsive Fluorescence Turn-On Chemodosimeter for Cu2+and Its Application in Live Cell Imaging[J].Chemistry,2008,14(23):6892-6900.
[7]Ha N K,Seong W N,Swamy K M K,et al.Rhodamine hydrazone derivatives as Hg2+selective fluorescent and colorimetric chemosensors and their applications to bioimaging and microfluidic system[J].Analyst,2011,136:1339-1343.
[8]王晓春,刘晓端,杨永亮,等.罗丹明类荧光探针在重金属和过渡金属离子检测中的应用[J].光谱学与光谱分析,2010,30(10):2693-2699.
[9]Zeng X,Wu C,Dong L,et al.A new tripodal rhodamine B derivative as a highly selective and sensitive fluorescence chemosensor for copper(II)[J].Sience in China Series B:Chemistry,2009,52(4):523-528.
[10]袁跃华,冯锋,田茂忠,等.罗丹明类荧光探针的合成及对铜离子的检测[J].高等学校化学学报,2011,32(1):62-66.

