先天性心脏病手术后并发多脏器功能障碍综合征的临床分析
周智恩,孙小圣,熊霞霞,冯 君,陈红英,何伦德,王道庄,邓硕曾
·临床研究·
先天性心脏病手术后并发多脏器功能障碍综合征的临床分析
周智恩,孙小圣,熊霞霞,冯 君,陈红英,何伦德,王道庄,邓硕曾
目的总结小儿心脏手术后多脏器功能障碍综合征(MODS)病例的临床特点,探讨发生MODS患者中导致死亡的危险因素和防治措施。方法收集2001年1月至2010年12月本科先天性心脏病术后并发MODS患者35例,男21例,女14例;年龄(6.43±4.65)岁;体重(16.52±9.12)kg。将其中并发MODS的患者分为死亡组与存活组,进行比较,回顾性分析导致死亡的高危因素,总结脏器衰竭数目及MODS评分与病死率的关系。结果本组病死率为51.4%(18/35)。①受累器官的发生率依次为心脏100.0%(35/35)、肺脏80.0%(28/35)、肾脏60.0%(21/35)、肝脏14.3%(5/35)、血液系统11.4%(4/35)及中枢神经系统5.7%(2/35),其中心、肺出现受损的时间最早。②脏器衰竭数目在2、3、4、≥5个时对应的病死率分别是25.0%、45.5%、77.7%、100.0%;MODS评分与本组病死率亦呈显著正相关。③与存活患者相比,死亡患者体外循环时间、主动脉阻断时间明显延长,二次转机、围术期意外事件发生率显著增高(P<0.01)。结论心肺功能受损是导致小儿心脏术后MODS的原发病,MODS死亡率随脏器衰竭数目和MODS评分的增加而递增,死亡的高危因素为体外循环时间及二次转机、围术期意外事件,重在预防。
小儿;体外循环;多脏器功能障碍综合征;临床分析
多脏器功能障碍综合征(multiple organ dysfunction syndrome,MODS)是指发病在24 h以上,两个或两个以上的器官或系统序贯性、渐进性发生的功能衰竭[1],一旦发生,病情十分凶险,病死率极高,国外报道病死率高达30%~60%[2]。笔者总结了2001年1月至2010年12月本院在体外循环(cardiopulmonary bypass,CPB)下进行手术的先天性心脏病患者的临床资料,对CPB术后并发MODS的临床特点及MODS患者死亡的高危因素进行回顾性分析,以期为指导合理的防治策略提供依据。
1 资料与方法
1.1 MODS诊断标准 本组病例各脏器功能衰竭均参考儿童MODS的诊断标准[3],评分高于3分的脏器。术后48 h内死亡者除外。
1.2 一般资料 各类先天性心脏病1 899例,术后符合MODS诊断的患儿共35例,发生率1.84%。其中男21例,女14例;年龄3个月~12(6.43±4.65)岁;体重6.5~28.0(16.52±9.12)kg。术前诊断室间隔缺损(VSD)合并重度肺动脉高压(PH)6例,主动脉缩窄(COA)、VSD合并重度PH 4例,重度肺动脉狭窄(PS)合并左心室发育不良2例,法洛四联症(TOF)12例(其中重症6例),完全性心内膜垫缺损(TECD)合并PH 4例,右心室双出口(DORV)5例,完全性大动脉转位(TGA)、肺动脉闭锁(PA)各1例。
1.3 手术方法与围术期监测 全部手术均采用静脉复合麻醉,常规建立CPB,应用膜式氧合器,预充液选用胶体(万汶及人血白蛋白)和晶体液(乳酸林格氏液或复方氯化钠溶液,碳酸氢钠)。根据术中情况进行改良超滤。
返回ICU后联合应用多巴胺、多巴酚丁胺、米力农、肾上腺素等小剂量多种类正性肌力药物,严格控制水、电解质平衡,少尿者早期行腹膜透析术。所有患儿行床旁心脏多普勒超声心功能检查评价解剖修复情况和心功能。根据各器官受损伤程度进行临床评分,见表1。
1.4 统计学方法 应用SPSS 11.5统计软件进行资料分析。计量资料以均数±标准差(±s)表示,计数资料以百分比表示,脏器衰竭数目及MODS评分与病死率之间的关系采用卡方检验。P<0.05为差异有统计学意义。

表1 多器官功能障碍的临床评分
2 结 果
1 899例患者中,术后发生MODS 35例,发生率1.84%。35例MODS患者中,死亡18例,病死率51.4%。总计发生衰竭脏器95个,平均2.71个。围术期发生意外情况6例,其中鱼精蛋白过敏致低血压3例,麻醉诱导时心脏骤停3例(2例因麻醉诱导时给药速度过快,发生低血压而引起心脏骤停;1例因颈内深静脉置管时,出现多源性室性早搏而引起心室颤动)。二次转机3例(2例因心内畸形矫治不满意,1例因Ⅲ°房室传导阻滞,需重新缝合而二次转机),占MODS患者的8.57%(3/35),显著高于非MODS患者的0.15%(4/1 864)(P<0.01)。术后感染4例,其中肺部感染3例,腹膜透析致腹腔感染1例。
2.1 MODS和病死患者的疾病构成比 MODS患者疾病构成中以复杂先心病最多,占MODS的65.71%(23/35),明显高于非MODS的6.22%(116/1 864)(P<0.01),且病死率亦最高,占MODS患者死亡例数的72.22%(13/18),复杂先心病是发生MODS和死亡的主要原因之一,见表2。
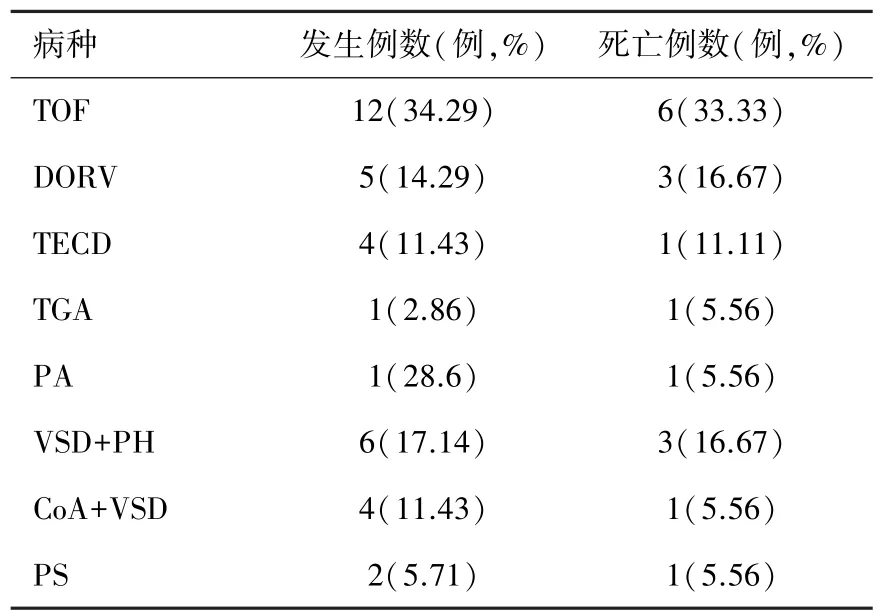
表2 MODS和病死患者的疾病构成比
2.2 术后衰竭脏器发生的概率及发生该脏器衰竭患者的病死率 术后衰竭器官或系统的发生率从高到低依次为心脏、肺部、肾、肝、血液系统和中枢神经系统,其中以心脏出现受损的时间最早,肺脏次之,见表3。
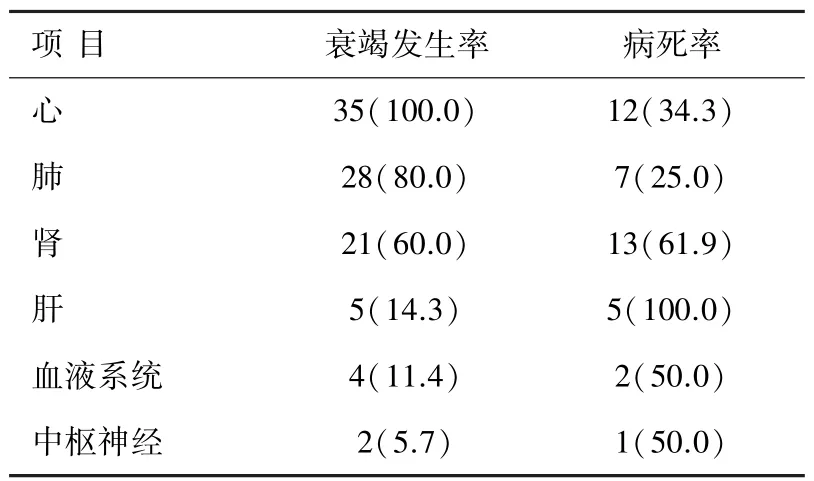
表3 脏器衰竭发生概率及病死率[例,(%)]
2.3 器官衰竭数目、临床评分与病死率的相关性随着器官衰竭数目的增多及临床评分分值的增加,病死率有升高的趋势,见表4。
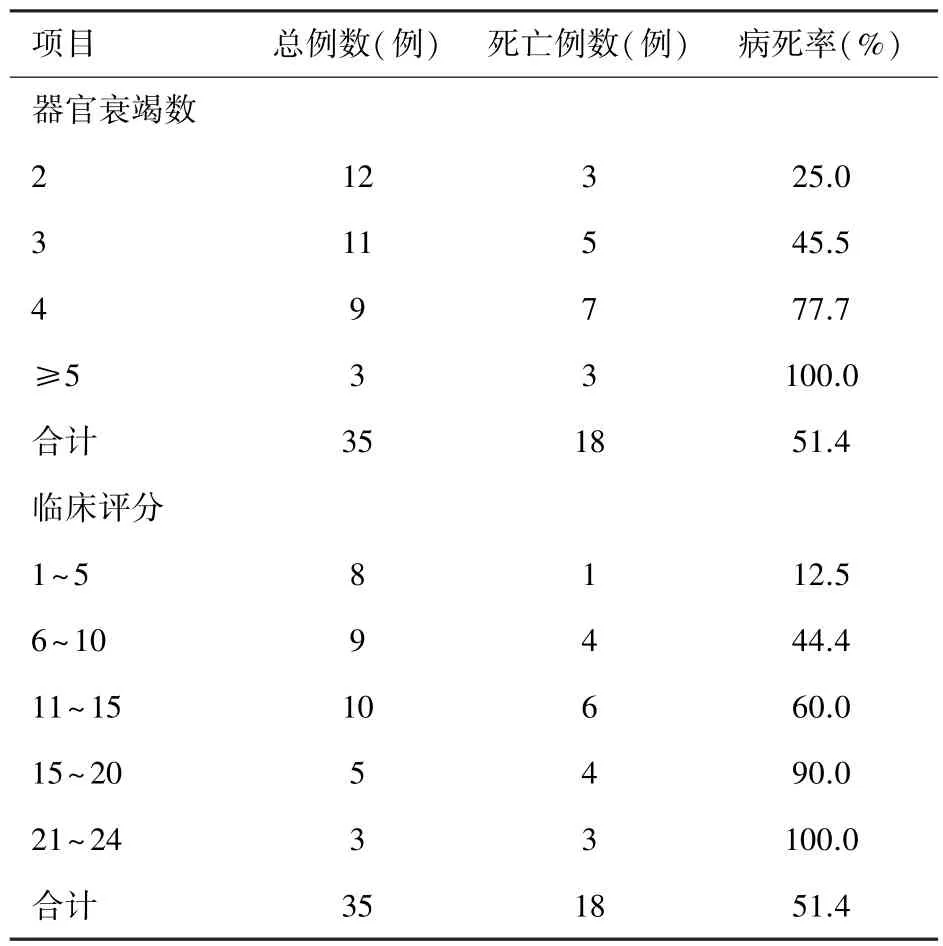
表4 器官衰竭数目、临床评分与病死率的关系
2.4 影响MODS死亡的围术期高危因素 本组中死亡患者与存活患者相比,CPB时间、主动脉阻断时间显著延长,二次转机、围术期意外事件显著增高,而年龄、术后感染、机械通气时间两者差异无统计学意义,见表5。
表5 影响MODS的围术期高危因素比较(±s)

表5 影响MODS的围术期高危因素比较(±s)
注:与死亡组比较∗P<0.05;∗∗P<0.01。
3 讨 论
MODS是小儿体外循环术后造成死亡的重要原因,由于目前尚无统一的诊断标准,且有多个器官的损害,病情错综复杂,纵横交错,涉及多学科,常常观点不一,救治中矛盾重重,往往顾此失彼,造成临床医生的困惑。因此,迫切需要找到心脏术后发生MODS的临床特征,为提高抢救成功率提供帮助。
3.1 先天性心脏病患儿临床特点 ①体重轻、年龄小;②术前合并症多:肺部感染、肺动脉高压、心力衰竭等;③各器官发育不完善,耐受CPB能力低下;④病情变化快,突发事件多,如肺动脉高压危象、缺氧、心律失常及心脏骤停等;⑤对器官衰竭的耐受性差,短时间内的低血压就可能出现肾或其他器官功能的衰竭,并会导致病死率增加;⑥心脏泵血是为全身脏器提供有效生理代谢的基础,当心脏发生功能不全或衰竭时,身体其他脏器将面临缺血缺氧的威胁[4]。基于上述特点,心脏术后发生MODS除了具有综合ICU的MODS发病特点外,还与其自身发病因素有关的影响因素,需要加以重视。
3.2 病种与MODS的关系 复杂先心病是心脏术后发生MODS最主要的因素。本组复杂先心病占MODS总例数的65.71%,明显高于非MODS者的复杂先心病比例且病死率高,占MODS患者总死亡例数的72.22%。这可能是由于复杂先心病往往病情重,术前心肺功能甚至其他脏器均可累及,尤其是发绀患儿长期慢性缺氧,即存的缺氧状态可使各器官生理储备受限,一旦遭受打击,更易诱发MODS,甚至死亡[5]。另外,复杂先心病手术时间和CPB时间较长,MODS发生率较高。
3.3 各器官系统与MODS的关系 本组资料显示,小儿CPB术后MODS患者各器官衰竭的发生率以心脏和肺功能衰竭发生居首位,其发生率分别为100%和80%,同时也是心内直视手术后MODS的首发脏器,其次分别是肾、肝、血液系统及中枢神经系统。这可能是由于心脏病患者术前大部分合并有不同程度的心肺功能不全,增加了术后心脏和呼吸功能衰竭的发生率;另一方面,心脏手术本身均有不同程度的心肺功能损害,特别是CPB转流时间长者,肺组织和循环白细胞激活,细胞因子大量释放,心肺作为首个靶器官,损伤出现早,损伤重;另外,循环和呼吸系统是保证其他脏器生理代谢正常进行的必要条件,一旦心肺功能损害,其他器官极易继发受损。本研究显示肝衰竭虽然在心脏术后发生率较低,但一旦发生多已是终末期,死亡风险却是最高的(本研究中5例肝衰竭患者均死亡),病死率100%,提示肝功能衰竭一旦发生,预后不良。因此,心肺功能受损是导致心脏术后MODS的原发病,控制原发病,改善组织血供是心脏术后防治MODS的关键。该结果与Johnston[6]所报道的以肺衰竭为首发或高发脏器存在明显差异,推测与二者不同的病源,基础疾病以及致病因素有关。
3.4 脏器衰竭数目及MODS评分与病死率的关系本研究发现MODS病死率随着脏器衰竭个数的增加和MODS评分分值的增加而显著升高,而随着病情的不断进展、恶化,死亡的风险也是增高的。脏器衰竭数目在2、3、4、≥5个时对应的病死率分别是25%、45.5%、77.7%、100%。脏器衰竭数目≥4的病死率为83.3%,是脏器衰竭数目≤3的2.4倍。参考儿童MODS评分标准,评分≥15的患者病死率高达87.5%,是评分≤15的2.1倍。由此可见,器官衰竭数目或程度的增加均可导致MODS死亡风险的上升,这与以前报道的结果相符[3,7]。因此,早发现,早诊断,早期给予脏器功能支持治疗,让病情尽量控制在早期,减少脏器受损数目,降低病死率是最终改善预后的关键。
3.5 体外循环、二次转机及围术期意外事件与MODS病死率的关系 CPB转流可导致机体内环境紊乱,机体免疫功能明显降低,释放和激活多种体液介质。CPB转流特别是转流时间过长是心脏术后发生MODS的重要基础[2]。笔者发现MODS死亡患者CPB转流时间和主动脉阻断时间明显延长,围术期意外事件、二次转机发生率显著增高,表明CPB转流引起全身炎症反应的强度以及二次打击是决定是否发生MODS的高危因素。这是因为早期创伤、休克等致病因素引起的第一次打击使机体炎性细胞被激活处于一种“激发状态”,如损伤持续存在,再度遭受第二次打击,即使强度不大,已一触即发的免疫内皮系统便会激发炎性介质和细胞因子,形成“瀑布样反应”而失去控制,加重原有组织损伤和器官功能障碍[8-9]。因此,尽量缩短CPB转流时间,避免二次转机、围术期意外事件的“第二次”打击亦是防治MODS的重要环节。
综上所述,心肺是小儿心脏术后发生MODS的首发衰竭器官,当其发生功能不全或衰竭时,应及时考虑到其他系统也有发生功能不全或衰竭的可能;脏器衰竭数目,MODS评分,CPB时间、二次转机及围术期意外事件是影响MODS患者病情和预后的因素。应密切监测各器官功能状况,积极治疗原发病,防止和减轻其他器官损伤,以减少MODS发生率及病死率。
[1] 刘大为.实用重症医学[M].北京:人民卫生出版社,2010.387.
[2] Combes A,Troullet JL,Bandot J,et al.Is it possible to cure mediastinitis in patients with major postcardiac surgery complication[J].The Ann of Thoracic Surgery,2001,72(5):1592-1597.
[3] Graciano AL,Balko JA,Rahn DS,et al.The pediatric Multiple Organ Dysfunction Score(p-MODS):development and validation of an objective scale to measure the severity of multiple organ dysfunction in critically ill children[J].Crit Care Med,2005,33(7):1484-1491.
[4] 陈英,毛斌,许春雷,等.冠状动脉搭桥术后并发多脏器功能障碍综合征的临床分析[J].心肺血管病杂志,2011,30(3):232-236.
[5] 周智恩,孙小圣,严善秀,等.婴幼儿体外循环手术后呼吸功能衰竭的危险因素分析.中国体外循环杂志,2009,7(3):129-131.
[6] Johnston JA,Yi MS,Britto MT,et al.Importance of organ dysfunction in determining hospital outcomes in children[J].J Pediatr,2004,144(5):595-601.
[7] 北京市科委重大项目MODS课题组.452例多器官功能障碍综合征患者基础疾病的临床分析[J].中国危重病急救医学,2009,21(3):164-167.
[8] Wang H,Ma S.The cytok ine storm and factors determining the sequence and severity of organ dysfunction in multiple organ dysfunction syndrome[J].Am J Emerg Med,2008,26(6):711-715.
[9] Ciesla DJ,Moore EE,Johnson JL,et al.Multiple organ dysfunction during resuscitation is not postinjury multiple organ failure.Arch Surg,2004,139(6):590-594.
Clinical analysis of multiple organ dysfunction syndrome in children after cardiac surgery
Zhou Zhi-en,Sun Xiao-sheng,Xiong Xia-xia,Feng Jun,Chen Hong-ying,He Lun-de,Wang Dao-zhuang,Deng Shou-zeng
Department of Critical Care Medicine,Chengdu Cardiovascular Hospital,Chengdu 630031,China
ObjectiveTo investigate the high risk factors and methods for prevention and treatment of multiple organ dysfunction syndrome(MODS)in children after cardiopulmonary bypass(CPB).MethodsFrom Jan.2001 to Dec.2010,there were total 35 children(21 males and 14 females)complicated with MODS after cardiac surgery in our department,and these cases were divided into two groups:death group and survival group.The high risk factors results in death,and the relationship between the MODS score and the fatality rate were compared and analyzed.ResultsThe overall mortality rate was 51.4%(18/35).(1)The incidence rate of cardiovascular,respiratory,renal,hepatic,hematologic and neurologic dysfunction was 100.0%(35/35),80.0%(28/35),60.0%(21/35),14.3%(5/35),11.4%(4/35)and 5.7%(2/35)respectively.Cardiac and respiratory injury appeared much earlier than other organs.(2)The more dysfunction organ systems presented,the higher mortality rate of patients would be.Furthermore,there was a significant positive correlation between clinic score and mortality rate.(3)Compared with survivals group,the death group had longer CPB time,longer aortic clamping time and higher incidence of repeat CPB support during surgery and perioperative unexpected events(P<0.01).ConclusionCardiac and respiratory dysfunction are the primary diseases in children with MODS after CPB.Mortality associated with MODS is highly correlated with the number of organ failing and clinical score.The high risk factors for the death of patients with MODS are the CPB time,incidence of repeat CPB support during surgery and perioperative unexpected events.
Children;Cardiopulmonary bypass;Multiple organ dysfunction syndrome;Clinical analysis
R654.1
A
1672-1403(2013)02-0071-04
2012-1-06)
2012-06-06)
610031成都,成都心血管病医院重症医学科(周智恩、孙小圣、熊霞霞、冯 君、陈红英、何伦德、王道庄);610017成都,成都市中西医结合医院重症医学科(周智恩);100037北京,阜外心血管病医院麻醉科(邓硕曾)

