石墨烯制备新技术及其在燃料电池催化剂中的应用
谭习有,黎华玲,彭洪亮,钟轶良,廖世军
(1 华南理工大学化学化工学院,广东广州510641;
2 广州军区联勤部油料监督处,广东广州510500)
碳纳米材料由于具有高的比表面积、电化学稳定性以及表面易修饰等独特的物理化学性质,使其在催化领域的应用研究变得越来越重要,并且一直位于纳米科学研究的前沿。继富勒烯和碳纳米管(CNTs)发现之后,2004年,英国曼切斯特大学的Geim教授等首次制备出二维原子晶体结构的石墨烯,推翻了经典的 “热力学涨落不允许二维晶体在有限的温度下自由存在”的认知[1],引发了石墨烯的研究热潮[2]。理想的石墨烯结构是由碳原子以SP2杂化方式连接而成的蜂窝状单原子层厚的材料。这种特殊的结构被认为是其它碳族材料的基本单元。如12个五角形石墨烯翘楚形成零维的富勒烯,而六角形的石墨烯通过卷曲成圆桶状则可形成一维的碳纳米管,通过堆垛成层状则可形成三维的石墨晶体[2]。这种特殊的结构使石墨烯表现出众多独特的性质,如石墨烯是世界上最薄最硬的材料[3],其导热系数高达5300 W/(m·K),高于碳纳米管和金刚石[4],常温下其电子迁移率超过20000 cm2/(V·s),又比纳米碳管或硅晶体高,而电阻率约10-6Ω·cm,比铜或银更低,为目前世上电阻率最小的材料[5]。石墨烯还具有高的理论比表面、独特的化学和电化学活性以及室温量子霍尔效应[6-7]等特殊性质。
石墨烯具有众多特殊的性质,它可以作为基体与其他物质发生协同作用,在电子信息、储能、超级电容、生物医药和催化等领域具有巨大的应用前景。近年来,石墨烯在燃料电池领域的应用受到了极大的关注。2004年以来,先后有400多篇相关文献进行了报道。石墨烯巨大的比表面积具有更多的吸附容量,而良好的导电、导热性,通过石墨烯负载催化剂粒子可明显降低催化反应的过电势,利于催化反应的进行。通过掺杂后的石墨烯基负载贵金属,可以增加贵金属与石墨烯间的协同作用,减少贵金属溶出的同时提高抗CO中毒能力[8]。本文将对石墨烯制备的新技术进行介绍,并从以下两个方面对石墨烯在燃料电池中的应用研究进展进行述评:①石墨烯作为载体应用于燃料电池的研究;②改性石墨烯直接用于燃料电池阴极催化剂的研究。
1 石墨烯制备新技术
石墨烯制备方法一般方法有微机械剥离法、单晶SiC外延生长法、化学气相沉积法、氧化还原法等,这些方法大都存在这样或者那样的不足,如使用有毒害试剂、制备过程复杂、产品性能均一性差、废弃物排放高等。为了克服这些不足,近年来国内外开展了大量的探索制备石墨烯的绿色、简便的新技术的研究工作,其中较为吸引人的方法有电化学制备、微波固相制备等。
1.1 微波制备技术
微波制备技术是近年来提出的一种制备石墨烯的新技术,可分为固相微波法和液相微波法两种方法。这种技术相对于传统制备技术而言,最大的特点是快速、高效,且制备的石墨烯能最大程度保持其本质特点,在燃料电池催化方面有出色的表现。
1.1.1 固相微波法
固相微波法是指通过对氧化石墨 (GO)或膨胀石墨等前体进行固相微波快速加热,含氧官能团在加热过程中形成气体产生的瞬间压力大于前体层间的范德华力,使之发生剥离,形成单层或多层的石墨烯(RGO)。
Li等[9]通过直接微波加热GO固体粉末,在小于5 s的超短时间内制备出石墨烯。研究发现:GO与RGO都能有效吸收微波,但是在一定频率下,如6.425 GHz,RGO对微波的吸收要比GO强得多。Park等[10]在氢气气氛下对石墨烯和GO混合的固体粉末进行1600 W微波加热1 min,通过石墨烯快速吸收微波并将能量传递给GO,有效快速地加热GO进而使之膨胀并剥离,氢气气氛则提高了GO的还原程度,阻止石墨烯缺陷,得到高质量的石墨烯。Sheng等[11]用800 W微波溅射在混合均匀的GO和碳酸铵固体粉末60 s,一步还原得到少层的RGO,在N,N-二甲基甲酰胺溶剂中超声剥离后即可得到单层石墨烯,其厚度大多在1.2 nm以下 (图1)[11]。这种方法相对于相同条件下单独微波溅射在GO固体粉末制备的石墨烯有了很大的改进。在研磨的过程中,碳酸铵盐插入到GO的层间,在微波加热中,当温度超过了GO(150200℃)和碳酸铵(150℃)的分解温度时,由于碳酸铵的分解的大量气体产生瞬间压力,破坏了GO层间的范德华力,加速了GO的剥离,而随着GO含氧官能团的分解的同时GO被还原,其层内的六元环共轭结构得到恢复。反应原理如图2所示[11]。
1.1.2 液相微波法

图1 RGO原子力显微镜(AFM)图片
液相微波是指在液相条件下,利用溶剂插层到层间,通过微波快速加热原理,使溶剂快速膨胀或发生热解产生大量气体克服层间作用力将氧化石墨剥离成石墨烯的方法。

图2 固态微波法制备RGO的原理图
液相微波法近年来也有较多的研究报道,Wang等[12]在N-甲基-2-吡咯烷酮溶剂中对GO进行微波得到25层分散均匀的石墨烯。Janowska等[13]在水合氨溶液中用膨胀石墨微波合成产率8%,厚度在0.20.5 mm的少层石墨烯,样品如图3[13]。研究表明,石墨剥离程度和产物的横向尺寸会受到氨水的浓度的影响。氨水浓度越高,石墨的剥离程度越高,石墨烯的横向尺寸越大,最大者达上百微米。剥离后的石墨烯在温和的温度下用氢气还原后制备的材料具有良好的电子传导性。该方法中未剥离的石墨可以回收用作反应的原料,过滤后的氨水也可以重复使用,很大程度地减少了化学试剂的使用,是一种环境友好绿色合成方法。

图3 石墨烯TEM图
鉴于使用GO或膨胀石墨作为前体会引入大量的含氧官能团,并且会产生较多的缺陷,降低石墨烯的电子传导性能等。Sridhar等[14]对液相微波法做了改进,不使用GO或膨胀石墨作为前驱体,而是将天然石墨与过硫酸铵和H2O2按一定比例装入玻璃管超声混合3 min,然后用家用微波炉用500 W微波90 s,在乙醇中超声30 min得到产率为5%,直径为几个微米,厚度为2 nm的石墨烯,如图4[14]。该研究表明:石墨粉∶H2O2∶过硫酸铵的质量比为2∶1∶0.1时得到的石墨烯质量最好,其BET比表面积高达590 m2/g。

图4 石墨烯SEM(a)和TEM(b)图
Chui等[15]则将石墨鳞片和体积比为1∶1的浓H2SO4和浓HNO3充分混合后,在300 W微波照射30 S,经中和、洗涤超声30 min后,得到大面积(400900μm2)、低缺陷、产率高达50%并能均匀分散于水溶液和有机溶液的低氧石墨烯。该研究表明,石墨烯的氧化程度与微波时间和微波功率有关,微波时间越长、微波功率越大,氧化的程度越高,石墨烯的缺陷也越大。该方法在微波条件下能够制备大面积高质量的石墨烯,是因为浓H2SO4与浓HNO3发生反应产生硝基自由基(NO),NO与石墨烯表面的芳环相互作用,通过单电子转移形成多芳香环自由离子对。在高温下,氧气转移到芳香自由基上就能形成多羟基或环氧基官能团,从而避免了因KMn O4氧化破坏芳香环结构而造成石墨烯的大量缺陷。其原理如图5[11]。
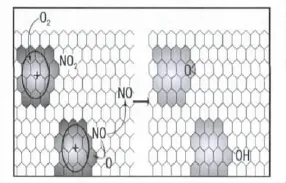
图5 固态微波法制备RGO的原理示意图
Murugan等[16]用微波溶剂热法还原GO制备聚苯氨/石墨烯用于能源储存。研究表明石墨烯晶面间距与溶剂和微波还原温度有关。溶剂不同,晶面间距也不同。在180300℃,晶面间距随着温度的升高而减少。
Hassan等[17]分别用不同的还原剂 (水合肼、乙二胺、胺水)在水相或有机相中1000 W微波还原GO后经离心干燥得到石墨烯。热重分析表明微波法合的石墨烯的氧官能团比传统方法合成要少得多。同时,他们还把各种金属前体与GO、还原剂充分混合后微波一步还原得到颗粒分布均匀的金属/石墨烯功能化合物。
与传统的石墨烯制备方法相比较,微波法制备石墨烯具有十分明显的优势,如制备条件简单、制备时间短、不需使用化学试剂还原等;尤其是固相微波一步制备石墨烯的方法,具有快捷、简便、完全不使用溶剂和化学试剂、产率高、石墨烯质量好等重要优点,是一项极其具有发展前景的制备技术。
1.2 电化学制备技术
除微波法外,近年来备受关注的石墨烯制备技术是电化学制备技术,包括电化学氧化剥离和电化学还原。与传统方法相比,电化学技术不需要使用还原或者氧化试剂,合成步骤少、能耗低、生产条件简单可控、易重复,可以有效降低因传统的氧化还原法带来的石墨烯缺陷。因此,近年来人们已开展了大量的探索和研究工作。
1.2.1 电化学还原技术
电化学还原制备技术是指通过调节外部电压使得氧化石墨烯在阴极得到还原,通常认为是电极表面材料的费米能级发生改变,使得材料的电子状态改变,最后腐蚀剥离的物质与电解质结合形成离子功能化的氧化石墨烯。
Liu等[18]首次采用电化学还原制备技术一步合成在极性溶剂中稳定存在的离子功能化石墨烯。在15 V电压下,阳极石墨棒在电解液中 (如甲基咪唑六氟磷酸盐)腐蚀,离子液体中的阳离子在阴极还原形成自由基,与石墨烯片中的π电子结合,形成离子液体功能化的石墨烯片。这种方法合成的石墨烯复合物缺陷较少,电子传导性比传统方法合成的要好。在适温下电子的渗流阀值为4.19%(体积分数),高于液相混合方法合成的渗流阀值(0.1%,体积分数),其电子传导率为13.84 S/m,是单壁碳纳米管/聚苯乙烯复合物的35倍。研究表明,电解质的种类和浓度的不同对合成的石墨烯性能会有一定的影响。如在氯化咪唑嗡盐电解质中,电解质:水的最佳质量比为1∶5;而在纯电解质或电解质:水的质量比为1∶1的六氟磷酸咪唑嗡盐、四氟硼酸磷酸咪唑嗡盐体系中,在电解质:水质量比为1∶1的六氟磷酸咪唑嗡盐电解质中合成的石墨烯的渗流阀值最大,电子传导性能最好。
Guo等[19]在-1.5 V电压条件下,以石墨棒为阳极,Pt为阴极,在GO悬浮液中电化学还原得到石墨烯。该方法不需要使用还原试剂,利用高的电负性克服GO氧官能团的能垒,达到还原GO的目的。这种电化学快速还原方法得到的石墨烯依然存在一定的缺陷,但是通过提高电化学还原温度或退火可以避免。用其修饰电极,经CV测试,其性能比化学还原石墨烯、氧化石墨、玻碳电极都要好。如图6[19]。
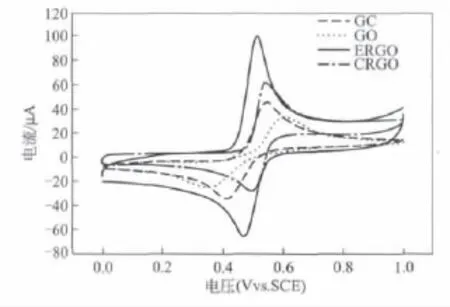
图6 玻碳电极GC、氧化石墨修饰电极GO、电化学还原石墨烯修饰电极ERGO、化学还原修饰电极CV图
Shao等[20]利用电化学工作站三电极体系循环伏安法在0.1 mol/L Na2SO4电解质中从1.0-1.0 V扫描还原GO悬浮液得到石墨烯,通过调节还原电位可以有效监控GO的还原程度。各种测试表明,这种方法制备的石墨烯电化学稳定性、对ORR和H2O2还原以及应用在电容上都要优于碳纳米管。Chen等[21]用循环伏安法一步电沉积还原GO磷酸胶体悬浮液,石墨烯直接沉积在玻碳电极表面,直接制备的电极可以有效鉴定邻、间、对苯二酚三种异构体。
1.2.2 电化学氧化剥离技术
电化学氧化剥离技术是指通过调节外部电压使得石墨能够在阳极腐蚀剥落而得到氧化石墨烯,然后通过超声剥离成少层石墨烯。
Wang等[22]使用两根石墨棒作电极,通入5 V电压,通过腐蚀阳极剥落,在聚苯乙烯磺酸钠溶液中得到厚度少于1 nm的石墨烯片层。Su等[23]在以高定向热裂解石墨棒为阳极,Pt丝为阴极,在电解质溶液中电化学剥落石墨棒得到大多数为2层、直径为30μm大面积、缺陷较少的高质量石墨烯。研究表明,工作电压、电解质对电化学剥离有着很大的影响。在HCl、HNO3、HBr和H2SO4的电解质中,只有H2SO4溶液可以有效电化学剥离得到高质量的石墨烯。而通过调节溶液的p H值以及电压,在0.5 mol/L H2SO4溶液,初始电压为2.5 V,保持1 min,然后电压加大到10 V制得的石墨烯质量最好。其光透性高达96%,HNO3处理后电阻<1 kΩ/sq,比传统方法制得的要好。
Wang等[24]用HOPG作为负极,石墨棒作正极,通入20 V电压,在含有LiCl O4的丙烯碳酸盐电解液中剥离膨胀石墨,通过强力超声10 h以上,纯化制备产率高达70%的少层的石墨烯。其合成原理示意如图7[24]。Alanyalloglu等[25]用表面活性剂辅助电化学法制备石墨烯。他们以石墨棒为阳极,Pt为阴极,在0.1 mol/L十二烷基硫酸钠(SDS)水溶液中通入电压,SDS先插入到石墨电极的层间,然后在电压的作用下剥离。石墨烯的厚度与插层SDS的量有关,通过调节电压控制插层石墨烯SDS的量,进而达到石墨烯厚度可控的目的。

图7 锂盐辅助电化学剥离石墨棒原理示意图
Shinde等[26]用多壁碳纳米管为原料先电化学氧化,然后电化学还原氧化后的多壁碳纳米管,超声后得到石墨烯。Shi等[27]用超声电化学方法制备PDDA-RGO-PdPt功能材料。由于PDDA的存在,很好的解决了石墨烯的亲水性问题,Zhou等[28]通过模板法电化学还原GO制备少层有图案大面积的石墨烯。他们在基底上蚀刻出形状,然后将泥桨状的GO喷涂在蚀刻的基底上,用红外照射烘干成膜,通过调节GO的浓度和喷涂的次数控制电化学还原石墨烯的层数,最后放入电解质溶液中电化学还原成石墨烯。其工艺流程如图8[28]。
电化学氧化剥离及电化学还原制备高性能石墨烯具有操作、少使用化学试剂等重要优点,是一种环境友好的制备石墨烯的新技术。同时,电化学氧化剥离技术制备的石墨烯含氧官能团较少,缺陷度较低,能够很好地保持其原有的电化学性能,在燃料电池催化剂的应用方面有很大的潜力。
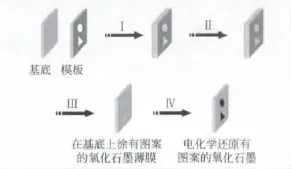
图8 模板法电化学还原石墨烯流程图
1.3 其它新方法
除电化学制备技术、微波技术外,近年来报道的制备石墨烯的新技术还包括等离子体技术、激光辐照技术等等。
Dato等[29]用微波等离子辅助CVD法,在常压无基底的条件下,将乙醇液滴与Ar输送到微波等离子区,经过冷却在过滤膜上沉积生成单层或双层的石墨烯片,而微波等离子辅助CVD法的最低温度可达到450℃。Liu等[30]在室温的条件下,将氨水、Zn粉、GO混合后超声得到石墨烯。超声时间与石墨烯的含氧官能团数量有关,超声10 min和60 min分别得到C/O比为8.09和8.59的石墨烯。这种材料在KOH电解液中其最大容量达到116 F/g。fan等[31]在90℃强碱性条件下超声还原氧化石墨溶液得到石墨烯,并且指出p H值越大,反应越快,在一定高的浓度下,即使在15℃也能反应。Shi等[27]用超声电化学方法一步合成PDDA-RGO-Pd Pt石墨烯功能材料。Yang等[32]在烷醇修饰电极表面吸附GO,通过自组装法制备石墨烯。Zhang等[33]在水-苯两相中用表面照射共振法一步合成Ag/石墨烯复合物。他们先将GO在去离子水中超声2 h分散,然后与油醇氨包覆的Ag纳米颗粒的甲苯溶液混合,在室温下用模拟太阳光照射2 h即可制成。Wei等[34]用激光照射法制备石墨烯。他们将光刻胶上涂在石英基底上的于120℃干燥5 min,用另一片石英盖上,置于真空箱里,用激光照射在石英上,光刻胶上碳分解,溶解在熔融的石英里,冷却石英后析出石墨烯。合成路线如图9[34]。
Wang等[35]通过电弧放电的方法在空气气氛下大量制备210层的石墨烯。在维持高电压、大电流、空气氛下,当两个石墨电极靠近到一定程度时会产生电弧放电,阳极石墨棒受到腐蚀,在反应室内壁得到石墨烯。研究表明,在高压(1000 Torr,1 Torr=133.322 Pa)下较容易得到石墨烯,而在低压下(400 Torr)则较容易得到其他形式的碳材料。该方法每天可得到几十克的石墨烯,同时使用空气使用H2/He的电弧放电法要便宜和安全,为规模化生产石墨烯提供了可能。

图9 激光照射法合成石墨烯示意图
等离子体技术等新技术目前的研究报道不多,但是这些方法无疑具有十分重要的价值,这些新技术对于高效和环境友好地制备出石墨烯具有重要价值。其研究工作将会受到越来越多的关注。
2 石墨烯在燃料电池催化剂中的应用
燃料电池由于具有能量转化效率高、对环境影响小 (零排放或者低排放)、燃料多样化、快启动、无机械运动部件等重要优点,被认为是21世纪能源之星,也是21世纪首选的清洁、高效的发电技术。然而,受制于其关键材料之一——Pt电催化剂成本高昂,在使用过程中催化剂发生团聚、CO中毒而失效等原因,使燃料电池商业化存在着一定的困难[36]。
目前,各种碳材料,如商业炭黑、XC-72、CNTS、C纳米纤维等,因其较高的比表面积和良好的电子传导率,被广泛应用于燃料电池电催化载体,但仍然存在总体性能较低、寿命较短、容易腐蚀、抗CO中毒能力较差问题。石墨烯作为新型的碳材料,由于其特殊的物理化学特性,如巨大的比表面、高的电子传导速率以及电化学稳定性等,在燃料电池应用上有独特的优势:①石墨烯上的大π键使其与贵金属催化剂之间有较强的相互作用,可以有效阻止贵金属粒子的迁移、聚集,提高催化剂的稳定性;②石墨烯良好的导电性使其在催化反应中电子容易传导而降低电池的内阻,提高电池的性能。石墨烯这些特性使其在燃料电池方面应用潜力巨大。
2.1 石墨烯用作燃料电池催化剂载体
石墨烯或功能化的石墨烯由于其巨大的比表面、优异的电子传导性能、独特的石墨平面结构以及良好的化学稳定性等特征使之有可能成为燃料电池催化剂的最佳载体。
石墨烯作为催化剂的载体担载金属一般合成路线有同步和分步还原GO和金属前体。负载在石墨烯上的金属纳米颗粒不仅仅是催化剂的活性粒子,同时也有效地防止了石墨烯的团聚和堆叠[37]。而金属功能化的石墨烯由于官能团为金属粒子提供了固定位置,增强了金属粒子与石墨烯之间的相互作用,有效地防止了金属纳米颗粒的团聚溶出,同时也为反应提供了催化活性点位,提高了其催化活性[38]。
一步还原法是将金属前驱体分散于GO水溶液中,通过不同的还原方法,如NaBH4还原法[39]、水合肼还原法[40]、柠檬酸盐还原法[41]、微波多羟基化合物[42]合成等还原得到金属/石墨烯基催化剂。Li等[43]采用NaBH4同时还原H2PtCl6和GO悬浮液的方法制备了Pt/石墨烯催化剂,Pt颗粒大小约为56 nm,与Pt/Vulcan XC72R相比,电化学活性比表面较大,对甲醇的氧化活性较好。由于传统的干燥方法容易引起石墨结构的堆叠导致纳米粒子的团聚,Xin等[44]采用了冻干法来干燥催化剂,水分直接从固态到气态,有效防止石墨烯片层的不可逆团聚。Kundu等[42]用微波快速法一步还原乙二醇、GO和H2PtCl6的方法制备了Pt颗粒大小约为23 nm的Pt/石墨烯催化剂。其电化学比表面为90.9 m2/g Pt,对甲醇的氧化有着良好的催化活性。
分步还原法是指先还原GO,然后再把金属前驱体沉积在石墨烯上进行还原。然而,由于没有功能化的石墨烯具有非亲水性,很难把金属前驱体沉积上去。因此,分步法一般都是先用环氧基、羟基、羧基官能团功能化石墨烯[38](FGS)或用PVP、聚二烯丙基二甲基铵 (PDDA)[27]等修饰石墨烯,然后再进行前驱体的还原。Kou等[38]通过热膨胀GO得到FGS,然后在100℃下用H2还原Pt前驱体和FGS混合液,最后得到Pt颗粒在2 nm左右的Pt-FGS。其电化学表面积(108 m2/g)比E-TEK商业催化剂(75 m2/g)大得多、稳定性要好。在CV扫描5000圈以后,其活性衰减了50%左右,而商业催化剂衰减了70%左右。该催化剂对甲醇的氧化以及氢燃料电池的催化比商业催化剂E-TEK和Pt-MWCNT要好。Shao等[45]用PDDA与石墨烯共混超声3 h制得PDDA-石墨烯。然后再将Pt负载上去制成Pt/石墨烯。Pt颗粒在3.5 nm左右。其ORR活性和稳定性都要优于Pt/CNT、Etek Pt/C。在稳定性测试中,44 h后,Pt/CNT、Etek Pt/C的ORR活性的衰减速率是Pt/石墨烯的23倍。
近年来,科学家们对分步还原法进行了改良,他们用通过表面活性剂包裹金属颗粒定向合成双金属/石墨烯催化剂,提高了催化活性的同时大大降低了催化剂的Pt载量。不仅如此,在催化剂设计上可实现尺寸和形貌的可控,具有很大的现实意义。Guo等[40]首次用湿化学法合成了高质量的3D Pt-Pd/石墨烯。他们先用PVP、氨水与GO共回流制备PVP-GN,然后将Pd前驱体沉积在PVPGN表面,在室温下用甲酸还原得到Pd/石墨烯,最后通过在Pd上链接PVP,快速度将Pt前驱体沉积上去进行还原得到3D Pt-Pd/石墨烯。由于单晶Pt长在多孔结构支撑的Pd上,双金属形成纳米树突,直接生长在石墨烯的表面,呈现出新型的金属/石墨烯异晶结构,且具有高电化学活性面积。另外,石墨烯片层表面的Pt-Pd双金属树突的数量,可通过简单地改变合成参数来控制,因此具有催化性质可调节性。这种催化剂在MOR中具有很高电化学活性,比铂黑催化剂高9.5倍,比商业催化剂E-TEK Pt/C高3.0倍。
Shi等[27]用超声电化学方法制备PDDA-RGOPd Pt纳米颗粒用于直接甲醇燃料电池催化。与传统的电化学方法相比,该方法以PDDA-RGO为导向剂,通过改变两者前体的比例合成不同比例的合金纳米催化剂。由于PDDA的存在,很好的解决了石墨烯的亲水性问题,金属纳米颗粒以合金的形式沉积在PDDA-RGO纳米颗粒上,同时具备2维结构的石墨烯的优异性能和合金的特性。与PDDA-Pd Pt相比,前者的ECSSA、电流密度约为后者的1.5倍,并且具有较好的抗CO中毒能力。研究表明,PDDA-RGO-Pd1Pt3的性能最好。该反应不需要使用强还原剂,通过超声电化学反应器,使用超声电极作为阴极和声音脉冲发生器,利用产生声音脉冲的同时引发电流脉冲,将金属前驱体PdCl2和H2PtCl6溶液共沉在PDDA-RGO,达到环保的目的。
2.2 改性石墨烯直接用作阴极催化剂
近年来,随着各种新型碳材料如富勒烯、碳纳米管、碳纳米纤维、石墨烯等的发现以及低金属含量在催化应用研究的深化,使非金属碳材料在燃料电池ORR过程中代替金属-载体催化剂成为可能。石墨烯作为新型的碳材料,在燃料电池催化领域上存在巨大的应用前景。功能化的石墨烯 (如掺O、N或其它表面官能团)的ORR催化活性比非功能化的要高。原始的石墨烯没有缺陷,在基面上的活性不是很高,只可以通过C环上π电子的离域或在石墨层边缘的不饱和C原子的活性位点才具有催化活性。富含高反应活性的官能团的材料,如N掺杂石墨烯,N原子上的孤对电子与sp2杂化的碳骨架形成离域的共轭系统,带正电荷C原子起着活性点位的作用,使之进攻O2变得容易,大大提高了ORR活性,而非功能化的石墨烯由于活性点位的不足使其催化效果不理想。而双掺杂石墨烯比单掺杂石墨烯的活性要好,这是因为通过DMF理论计算,两种物质的协调效应使自旋电荷密度重新分配,大大提高了石墨烯平面的电子转移,可以提供大量的C原子活性位点,从而提高ORR催化活性[46]。另一个原因是,双掺杂后,HOMO轨道和LUMO轨道能垒的降低有助于提高任何反应的活性,包括ORR[36]。
Lee等[47]用水合肼还原GO制备N掺杂石墨烯,其BET比表面为466 cm2/g,是商业XC-72R和GO的二倍多,而其电容为212.3 F/g,远远大于商业XC-72R(18.5 F/g)和GO(4.1 F/g)。在酸性条件下,GO不存在ORR活性,而N掺杂石墨烯的ORR活性远大于商业XC-72R和N掺杂阵列CNT,在0.7 V电压处,其电流密度是商业XC-72R的35倍,是N掺杂阵列CNT的2倍。
Zhou等[48]通过两步电还原法制备蒽醌/石墨烯玻碳电极,其ORR的活性要比蒽醌/玻碳电极好。他们预先制好的GO/GC电极浸入p H=7的磷酸缓冲液中,通入N2,以50 m V·s-1的速度从0.41.4 V扫描,得到电还原氧化石墨/玻碳电极;然后以此电极作为工作电极,在0.1 mol/L的四氟硼酸四丁基铵盐和10 mmol/L固红铝盐的混合溶液中还原得到电还原氧化石墨/玻碳电极(AQ/ER-GO/GC)。AQ/GN对ORR的催化分两步骤进行:①在-0.56 V时,醌官能团先进行还原;②在-0.75 V时,对ER-GO表面吸附的O2进行2 e还原。
Ma等[49]用热还原法还原GO溶液得到高分散的石墨烯,然后将聚吡咯涂于石墨烯薄膜上制得聚吡咯/石墨烯复合物,最后通过高温碳化得到N含量为10%左右的CNx/GN催化剂。该催化剂具有较好的稳定性、高的ORR活性、强的抗甲醇渗透和CO中毒能力。
Sheng等[50]在没有催化剂的前提下,以三聚氰氨为N源,通过热处理GO得到N-GN,在碱性条件下用于ORR反应。这种方法掺杂的N含量高达10%,N原子主要以类嘧啶的键合的方式存在。这种热处理方式也可以合成其它元素掺杂 (Si,S,B,P)的功能化石墨烯。Ahmed等[51]在三十二烷基甲基溴化铵(TDMAC)和GO混合的悬浮液中用NaBH4还原得到N掺杂的TDMAC-GRO功能化石墨烯。该功能石墨烯在碱性条件下对燃料电池的ORR催化有较好的活性。LSV测试表明,其起始电位 (0.24 V),远高于未掺杂石墨烯(-0.3 V)。动力学研究表明,该反应为四电子反应机理,在碱性条件下的ORR反应中,有着良好的稳定性、强的抗甲醇和乙醇腐蚀性。
Liang等[46]首次用简单易行的一步合成法制备介孔N-S掺杂石墨烯。他们先把GO分散在水中,然后用胶状的硅酸作模板加入到分散液中,通过旋转蒸发水分,得到GO/SiO2复合物。然后用三聚氰铵和二苄基二硫醚(BDS)作N和S的前驱体,在900℃的Ar氛围下加热GO/SiO2和前驱体三者的混合物得到N-S-G/SiO2。最后在HF酸下脱去SiO2纳米颗粒得到孔径为1040 nm的介孔N-S-G。当电极在N2氛围下,由于介孔碳材料的特征在伏安图上观察不到明显的还原峰;而在O2氛围下,在-0.24 V其峰电流为-3.3 m A/s。作者还指出,N-S-G的ORR活性与商业Pt/C相当,比N-G、S-G、g-C3N4/C或单纯石墨烯则要好得多。在电池测试中,N-S-G催化剂的稳定性要高于Pt/C,经历了60 h后前者衰减了19%,而Pt/C则衰减了40%。由于该制备方法简单、原料易得、活性高、稳定性好、成本低廉等优点,有可能进行规模生产,应用于燃料电池、锂电池、光催化等领域。
Choi等[52]合成B,N-GN和P,N-GN在酸性条件下用于ORR反应催化。经B,P掺杂后,LSV扫描,其起始电压大幅提高,尤其是P掺杂后,其起始电压约为0.9 V。他们ORR催化活性依次为N-GN<B,N-GN<P,N-GN,如图10。在RHE测试,P,N-GN的ORR活性要比其它石墨烯的衍生物活性要好,与制备出在酸性条件下所有石墨烯基材料活性最好的Shao-Horn课题组报道的相当((1.5 m A/mg)。他们用hummers法合成GO,然后用水合肼还原得到RGO,再与少量FeCl2·4 H2O和CoCl2·6 H2O、双氰胺(DCDA)水溶液混合超声1 h,蒸发水分后得到的粉末在900℃的Ar气氛下热处理,最后把热处理粉末用硫酸溶液浸泡滤出后,再次重复热裂解N-GN。他们用同样的方法在蒸发前分别把硼酸和磷酸加入到RGO、金属氯化物和DCDA混合物中合成B,NGN和P,N-GN。

图10 0.75V时的质量活性
Zheng[53]以GO为碳源,以尿素为N源,通过水热法合成N-GN用于碱性条件下ORR。N原子以嘧啶N和吡咯N的形式存在。水热法合成的N-GN经过低温热处理后,吡咯类型的N会向石墨型的N转变,石墨型的N对ORR是四电子机理。
3 结 语
石墨烯由于各种特殊的物理化学性质,在燃料电池应用领域有着广泛的应用前景。随着各种制备新技术 (如电化学法、微波法、超声剥离)的不断涌现,石墨烯的合成逐步趋向低能耗、环境友好、合成简单、快速方向发展。因此,绿色、清洁、快速的制备技术将是石墨烯合成研究的热点。近年来,电化学制备的石墨烯在燃料电池的应用潜能已经得到初步证实。石墨烯由于其超大的比表面以及良好的电化学稳定性,有可能成为燃料电池催化剂的最佳载体。改性石墨烯直接应用于燃料电池催化剂对ORR的出色表现,在将来,石墨烯将会替代Pt催化剂,大大降低燃料电池的成本,推动燃料电池的商业化进程。
尽管石墨烯在燃料电池的应用有着巨大的前景,但是,绿色、高质快速的石墨烯制备技术、功能化的方法以及应用研究仍有待发展。在燃料电池应用中,石墨烯性作为功能材料的仍不如传统的材料。作为载体负载金属时,仍然存在团聚严重降低催化活性的问题,而其结构与催化活性的机理也有待进一步研究。为推动材料在实际中的应用,复合石墨烯功能材料的催化剂性能还需要进一步提升。合成 “清洁”以及多元协同催化性复合催化剂是石墨烯基电催化材料发展的重要方向。同时,发展绿色、高质快速、可批量制备尺寸、层数和性能可控的石墨烯是下一步制备技术研究的重点和热点。
[1]Novoselov K S,Geim A K,Morozov S V,et al.Electric field effect in atomically thin carbon films[J].Science,2004,5696(306):666-669.
[2]Geim A K,Novoselov K S.The rise of graphene[J].Nature materials,2007,3(6):183-191.
[3]Lee C,Wei X,Kysar J W,et al.Measurement of the elastic properties and intrinsic strength of monolayer graphene[J].Science,2008,5887(321):385-388.
[4]Balandin A A,Ghosh S,Bao W,et al.Superior thermal conductivity of single-layer graphene[J].Nano Letters,2008,3(8):902-907.
[5]Bolotin K I,Sikes K,Jiang Z,et al.Ultrahigh electron mobility in suspended graphene[J].Solid State Communications,2008,9-10(146):351-355.
[6]Zhang Y,Tan Y W,Stormer H L,et al.Experimental observation of the quantum hall effect and Berry’s phase in graphene[J].Nature,2005,7065(438):201-204.
[7]Abanin D,Morozov S,Ponomarenko L,et al.Giant nonlocality near the dirac point in graphene[J].Science,2011,6027(332):328.
[8]Sahoo N G,Pan Y,Li L,et al.Graphene-based materials for energy conversion[J].Advanced Materials,2012,24(30):4203-4210.
[9]Li Z,Yao Y,Lin Z,et al.Ultrafast,dry microwave synthesis of graphene sheets[J].Journal of Materials Chemistry,2010,23(20):4781-4783.
[10]Park S-H,Bak S-M,Kim K-H,et al.Solid-state microwave irradiation synthesis of high quality graphene nanosheets under hydrogen containing atmosphere[J].Journal of Materials Chemistry,2011,3(21):680-686.
[11]Shen J,Li T,Long Y,et al.One-step solid state preparation of reduced graphene oxide[J].Carbon,2012,6(50):2134-2140.
[12]Wang C,Wang Y L,Zhan L,et al.Synthesis of graphene with microwave irradiation in liquid phase[J].Journal of Inorganic Materials,2012,7(27):769-774.
[13]Janowska I,Begin D,Ersen O,et al.High yield graphene and few-layer graphene synthesis assisted by microwaves[J].Physica E-Low-Dimensional Systems &Nanostructures,2012,6(44):1009-1011.
[14]Sridhar V,Jeon J-H,Oh I-K.Synthesis of graphene nanosheets using eco-friendly chemicals and microwave radiation[J].Carbon,2010,10(48):2953-2957.
[15]Chiu P L,Mastrogiovanni D D T,Wei D,et al.Microwaveand nitronium ion-enabled rapid and direct production of highly conductive low-oxygen graphene[J].Journal of the American Chemical Society,2012,13(134):5850-5856.
[16]Murugan A V,Muraliganth T,Manthiram A.Rapid,Facile microwave-solvothermal synthesis of graphene nanosheets and their polyaniline nanocomposites for energy strorage[J].Chemistry of Materials,2009,21(21):5004-5006.
[17]Hassan H M A,Abdelsayed V,Khder A E R S,et al.Microwave synthesis of graphene sheets supporting metal nanocrystals in aqueous and organic media[J].Journal of Materials Chemistry,2009,23(19):3832-3837.
[18]Liu N,Luo F,Wu H X,et al.One-step ionic-liquid-assisted electrochemical synthesis of ionic-liquid-functionalized graphene sheets directly from graphite[J].Advanced Functional Materials,2008,10(18):1518-1525.
[19]Guo H L,Wang X F,Qian Q Y,et al.A green approach to the synthesis of graphene nanosheets[J].ACS Nano,2009,9(3):2653-2659.
[20]Shao Y,Wang J,Engelhard M,et al.Facile and controllable electrochemical reduction of graphene oxide and its applications[J].Journal of Materials Chemistry,2010,4(20):743-748.
[21]Chen L,Tang Y,Wang K,et al.Direct electrodeposition of reduced graphene oxide on glassy carbon electrode and its electrochemical application[J].Electrochemistry Communications,2011,2(13):133-137.
[22]Wang G,Wang B,Park J,et al.Highly efficient and largescale synthesis of graphene by electrolytic exfoliation[J].Carbon,2009,14(47):3242-3246.
[23]Su C Y,Lu A Y,Xu Y,et al.High-quality thin graphene films from fast electrochemical exfoliation[J].ACS Nano,2011,3(5):2332-2339.
[24]Wang J,Manga K K,Bao Q,et al.High-yield synthesis of few-layer graphene flakes through electrochemical expansion of graphite in propylene carbonate electrolyte[J].Journal of the American Chemical Society,2011,133(23):8888-8891.
[25]AlanyalIoglu M,Segura J J,Or-Sol J,et al.The synthesis of graphene sheets with controlled thickness and order using surfactant-assisted electrochemical processes[J].Carbon,2012,50(1):142-152.
[26]Shinde D B,Debgupta J,Kushwaha A,et al.Electrochemical unzipping of multi-walled carbon nanotubes for facile synthesis of high-quality graphene nanoribbons[J].Journal of the American Chemical Society,2011,12(133):4168-4171.
[27]Shi J J,Yang G H,Zhu J J.Sonoelectrochemical fabrication of PDDA-RGO-PdPt nanocomposites as electrocatalyst for DAFCs[J].Journal of Materials Chemistry,2011,20(21):7343-7349.
[28]Zhou M,Wang Y,Zhai Y,et al.Controlled synthesis of large-area and patterned electrochemically reduced graphene oxide films[J].Chemistry-A European Journal,2009,25(15):6116-6120.
[29]Malesevic A,et al.Synthesis of few-layer graphene via microwave plasma-enhanced chemical vapour deposition[J].Nanotechnology,2008,30(19):305604.
[30]Liu Y,Li Y,Zhong M,et al.A green and ultrafast approach to the synthesis of scalable graphene nanosheets with Zn powder for electrochemical energy storage[J].Journal of Materials Chemistry,2011,39(21):15449-15455.
[31]Fan X,Peng W,Li Y,et al.Deoxygenation of exfoliated graphite oxide under alkaline conditions:a green route to graphene preparation[J].Advanced Materials,2008,23(20):4490-4493.
[32]Yang S,Xu B,Zhang J,et al.Controllable adsorption of reduced graphene oxide onto self-assembled alkanethiol monolayers on gold electrodes:tunable electrode dimension and potential electrochemical applications[J].The Journal of Physical Chemistry C,2010,10(114):4389-4393.
[33]Zhang F J,Zhang K H,Xie F Z,et al.Surface plasmon resonance induced reduction of high quality Ag/graphene composite at water/toluene phase for reduction of H2O2[J].Applied Surface Science,2013(265):578-584.
[34]Wei D P,Mitchell J I,Tansarawiput C,et al.Laser direct synthesis of graphene on quartz[J].Carbon,2013(53):374-379.
[35]Wang Z,Li N,Shi Z,et al.Low-cost and large-scale synthesis of graphene nanosheets by arc discharge in air[J].Nanotechnology,2010,17(21):175602.
[36] 马紫峰,张慧娟,原鲜霞,等.低温燃料电池用非贵金属氧还原催化剂研究进展[J].化工进展,2011,30(1):150-154.
[37]Si Y,Samulski E T.Exfoliated graphene separated by platinum nanoparticles[J].Chemistry of Materials,2008,21(20):6792-6797.
[38]Kou R,Shao Y Y,Wang D H,et al.Enhanced activity and stability of Pt catalysts on functionalized graphene sheets for electrocatalytic oxygen reduction[J].Electrochemistry Communications,2009,5(11):954-957.
[39]Huang J,Zhang L,Chen B,et al.Nanocomposites of sizecontrolled gold nanoparticles and graphene oxide:Formation and applications in SERS and catalysis[J].Nanoscale,2010,12(2):2733-2738.
[40]Guo S J,Dong S J,Wang E W.Three-dimensional pt-on-pd bimetallic nanodendrites supported on graphene nanosheet:Facile synthesis and used as an advanced nanoelectrocatalyst for methanol oxidation[J].ACS Nano.,2010,1(4):547-555.
[41]Arbizzani C,Righi S,Soavi F,et al.Graphene and carbon nanotube structures supported on mesoporous xerogel carbon as catalysts for oxygen reduction reaction in proton-exchangemembrane fuel cells[J].International Journal of Hydrogen Energy,2011,8(36):5038-5046.
[42]Kundu P,Nethravathi C,Deshpande P A,et al.Ultrafast microwave-assisted route to surfactant-free ultrafine Pt nanoparticles on graphene:Synergistic co-reduction mechanism and high catalytic activity[J].Chemistry of Materials,2011,11(23):2772-2780.
[43]Li Y M,Tang L H,Li J H.Preparation and electrochemical performance for methanol oxidation of Pt/graphene nanocomposites[J].Electrochemistry Communications,2009,4(11):846-849.
[44]Xin Y,Liu J-g,Zhou Y,et al.Preparation and characterization of Pt supported on graphene with enhanced electrocatalytic activity in fuel cell[J].Journal of Power Sources,2011,3(196):1012-1018.
[45]Yuyan S,Sheng Z,Chongmin W,et al.Highly durable graphene nanoplatelets supported Pt nanocatalysts for oxygen reduction[J].Journal of Power Sources,2010,195(15):4600-4605.
[46]Liang J,Jiao Y,Jaroniec M,et al.Sulfur and Nitrogen Dual-Doped Mesoporous Graphene Electrocatalyst for Oxygen Reduction with Synergistically EnhancedPerformance[J].Angewandte Communications,2012(51):11496-11500.
[47]Lee K R,Lee K U,Lee J W,et al.Electrochemical oxygen reduction on nitrogen doped graphene sheets in acid media[J].Electrochemistry Communications,2010,8(12):1052-1055.
[48]Zhou Y,Zhang G,Chen J,et al.A facile two-step electroreductive synthesis of anthraquinonegraphene nanocomposites as efficient electrocatalyst for O2reduction in neutral medium[J].Electrochemistry Communications,2012(22):69-72.
[49]YanWen M,LingRong Z,JuanJuan L,et al.Carbon-nitrogen/graphene composite as metal-free electrocatalyst for the oxygen reduction reaction[J].Chinese Sci.Bull,2011,33(56):3583-3589.
[50]Sheng Z-H,Shao L,Chen J-J,et al.Catalyst-free synthesis of nitrogen-doped graphene via thermal annealing graphite oxide with melamine and its excellent electrocatalysis[J].ACS Nano.,2011,6(5):4350-4358.
[51]Ahmed M S,Jeon S.New functionalized graphene sheets for enhanced oxygen reduction as metal-free cathode electrocatalysts[J].Journal of Power Sources,2012,218:168-173.
[52]Choi C H,Chung M W,Kwon H C,et al.B,N-and P,N-doped graphene as highly active catalysts for oxygen reduction reactions in acidic media[J].Journal of Materials Chemistry A,2013,11(1):3694-3699.
[53]Zheng B,Wang J,Wang F B,et al.Synthesis of nitrogen doped graphene with high electrocatalytic activity toward oxygen reduction reaction[J].Electrochemistry Communications,2013(28):24-26.

