用化学学科思想引领高三化学第一轮复习
卢海燕,杨华文
(安宜高级中学,江苏 宝应 225801)
用化学学科思想引领高三化学第一轮复习
卢海燕,杨华文
(安宜高级中学,江苏 宝应 225801)
本文以一次教学效果检测试题分析为例,通过梳理化学学科的教学思想,表明以化学学科思想来引领是第一轮高三化学复习的应有要义。
化学学科思想;结构;转化;强弱;守恒;平衡;理论联系实际
高三化学第一轮复习教什么,怎么教,教到什么程度,对每位高三化学教师来说,都必须有一个清醒的认识。我们认为,以知识的逐点扫描和梳理为主夯实基础是必要的,以《考试说明》所要求的知识内涵和外延的强化训练也是必须的,但我们认为,第一轮高三化学复习让学生形成一定的化学学科思想更为重要。
近期,我校在期中考试后安排了高三学生半学期学习情况问卷,问卷要求学生归纳出学科思想,结果71.2%的理化学生说不出或说不清化学学科有哪些学科思想,究其原因,一方面学生整天忙于作业的应付,“只埋头拉车,不抬头看路”,一方面教师只注重知识的传授,不重视方法的归纳和提炼。下面以我校参加的最近的一次教学效果检测的试题为例,通过梳理化学学科的教学思想,揭示化学学科思想引领第一轮高三化学复习的应有要义。
一、结构观
结构观是基本的化学学科观念,是对物质本质和化学反应本因的深层次认识。这一科学方法源自“内因在事物中发挥决定作用”的哲学论断。有什么样结构就该有什么样的性质,有什么样的性质就“衍射”什么样的结构!有机化学是这一科学观念充分体现。
例1.β——紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,其结构如图1所示(未表示出其空间构型)。下列关于β——紫罗兰酮的性质描述正确的是

A.能与FeCl3溶液发生显色反应
B.能使酸性KMnO4溶液褪色
C.能发生加成、取代、消去反应
D.1mol该物质最多可与3mol H2反应
分析:该题β——紫罗兰酮为载体,考查学生对有机化合物的分子结构、官能团的性质等基础有机化学知识的理解和掌握程度。A.分子无苯环,不能与FeCl3溶液发生显色反应。B、C.分子中的官能团决定了能使酸性KMnO4溶液褪色、能发生加成、取代反应,不能发生消去反应。D.1mol该物质最多可与3mol H2反应。
二、转化观
“同一种元素的不同类物质之间的转化关系”,是高三一轮复习阶段认识元素化合物知识的重要方法。利用图式的方法,引导学生运用分类方法对具体的化学物质及其转化关系进行学习,不仅有利于做好第一轮复习,更为学生今后的学习提供学习思路。
以教材中的习题为例,用化学脉络图可表示下列转化关系:Ca→CaO→Ca(OH)2→CaCO3;C→CO2→H2CO3→Na2CO3→NaHCO3。化学脉络图是一种表征、检查、修正和完善化学知识的认知工具,它通常是将有关某一化学主题不同级别的概念或命题置于方框或圆圈中,再以各种连线将相关的概念或命题连接,形成关于该主题的化学概念或知识网络,借此形象化的方式表征学习者的知识结构,以及对某一化学主题的理解。
三、强弱观
(1)在化学反应中往往表现为:①活泼(非)金属置换不活泼(非)金属,②强酸(碱)制备弱酸(碱),③溶解性强的制备溶解性弱的,④强氧化(还原)剂制备弱氧化(还原)剂。
(2)当同一个体系中,一个反应物与另外多个反应物反应时须遵循一定的顺序,即优先规则。a.有序氧化(还原)。例:少量的Cl2通入FeBr2溶液中,Cl2先氧化Fe2+。b.有序放电。阳离子在阴极放电顺序为:Ag+>(Fe3+)>Cu2+>(H+酸)>Fe2+>Zn2+>(H2O 中的 H+)。阴离子在阳极放电顺序为:金属阳极(Cu、Ag 等)>S2->Cl->OH->含氧酸根离子。c.有序中和。若某一溶液中同时含有几种酸性物质(或碱性物质)当加入一种碱(或酸)时,酸性(或碱性)强的物质先被中和。d.有序沉淀。若某一溶液中同时存在几种能与所加试剂形成沉淀的离子,则溶解度小的物质先沉淀。向KCl、NaBr混合溶液中逐渐加入AgNO3溶液时,先析出AgBr,其次为AgCl。
例2.下列说法正确的是
A.在大量存在 NH+4、Al3+、、CH3COOH 的溶液中,滴加NaOH溶液立即有气体产生。
B.常温下,反应 4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)能自发进行,则该反应的△H<0
C.NaHR(H2R为二元弱酸)溶液的酸碱性取决于HR-的电离程度和水解程度的相对大小
D.向 0.01mol·L-1NH4HSO4溶液中滴加 NaOH 溶液至中性:c(Na+)>c()>c()
分析:本题考查学生对元素化合物知识应用与原理之间的关系的认识。A中与NaOH反应的顺序是:CH3COOH、Al3+、Al(OH)3。B.化学反应自发向生成稳定体系的方向转化,即放出热量(焓变小于零)并且混乱度增加(熵变大于零)的方向转化。C中HR-具有双重性,酸碱性取决于HR-的电离程度和水解程度的相对大小。D中OH-先与H+中和,再与反应一部分。
四、守恒观
在溶液中存在离子的电荷守恒和物料守恒。在氧化还原反应中存在得失电子守恒。在某些复杂多步的化学反应中存在元素守恒。
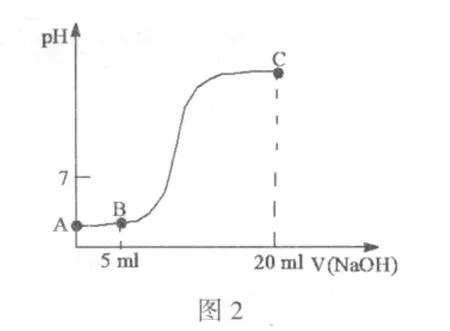
例 3.常温下,向 10mL 0.1mol·L-1的 CH3COOH溶液中逐滴加入0.1mol·L-1NaOH溶液,所得滴定曲线如图2所示。下列说法一定正确的是
A.A点的pH为1
B.B 点时:2c(H+)+c(CH3COOH)=2c(OH-)+c(CH3COO-)
C.在 A→B 之间:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.C 点时:c(H+)+c(Na+)=c(OH-)+c(CH3COO-)
分析:本题以NaOH溶液滴定CH3COOH溶液的滴定曲线为载体,考查溶液中盐的水解、弱电解质的电离、电荷守恒、物料守恒等基本原理的应用。该题的思维容量较大。(1)由于CH3COOH是弱酸,只能部分电离,所以 C(H+)小于 0.1mol·L-1,A 点的 pH 大于1。(2)B点 对 应 的 溶 液 组 成 是 CH3COOH和CH3COONa。根据电荷守恒和物料守恒两式合可得。(3)C中根据图像可以确定在A→B之间 c(H+)>c(OH-),而 c(Na+)与 c(H+)的大小无法确定。在 A→B之间溶液的组成是CH3COOH和CH3COONa。极限法在 A 点 c(H+)>c(Na+)=0,在 B 点 c(Na+)>c(H+)。所以在 A→B 之间也可能存在 c(H+)>c(Na+)。(4)C 点溶液的组成是NaOH和CH3COONa,D考查了电荷守恒。
五、平衡观
动态平衡思想是化学学科思想的重要组成部分,是科学思想的集中体现。勒夏特列原理是自然辩证法在自然科学领域的具体化。中学化学四大平衡包括化学平衡、电离平衡、水解平衡、沉淀溶解平衡。K、Kw、Ksp本质上都是平衡常数,只是温度的函数,其大小只受温度影响。四大平衡受外界条件影响移动时,都遵循勒夏特列原理。
例4.一定温度下,在4个容积均为1L的恒容容器中分别进行反应(各容器中 A 都足量)A(s)+B(g)⇌C(g)+D(g) ΔH=+100kJ·mol-1,某时刻测得部分数据如下表:容器编号n(B)/moln(C)/moln(D)/mol反应时间/min反应速率
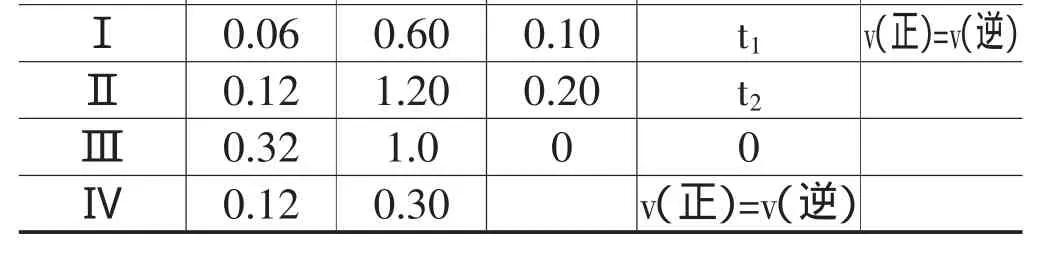
Ⅰ 0.06 0.60 0.10 t1 v(正)=v(逆)Ⅱ 0.12 1.20 0.20 t2Ⅲ 0.32 1.0 0 0Ⅳ 0.12 0.30 v(正)=v(逆)
下列说法正确的是
A.容器Ⅰ中平均反应速率v(B)=0.04/t1mol·L-1·min-1
B.t2时容器Ⅱ中 v(正)>v(逆)
C.容器Ⅲ中反应至平衡时吸热20kJ
D.容器Ⅳ中 c(D)=0.4mol·L-1
分析:本题考查学生对化学反应平均速率的定量计算、平衡常数、化学平衡状态等一般规律的理解程度和运用化学平衡常数进行计算的能力。容器Ⅰ中学生会误以为B的起始浓度为1mol·L-1,而实际上题目并没说明。容器Ⅱ中通过计算得出Q(浓度商)=2>K=1,所以此时平衡逆向移动。容器Ⅲ中可以利用三步法进行计算,算出转化的B的量,来算出平衡时吸收的热量,也可以逆向思维将C中的吸热20kJ当作已知条件,则得出转化的B应为0.2mol,发现此时上述反应未处于平衡状态。容器Ⅳ中v(正)=v(逆)说明此时K=1,利用平衡常数 K=1可以算出 c(D)=0.4mol·L-1。
六、数形结合观
在解决化学问题时常常会用到数学,如果能将数学思想方法加以应用,会使问题简单明了。华罗庚就说过:“数缺形,少直观;形缺数,难入微”。具体地说,就是在解决问题时,根据问题的背景、数量关系、图形特征或使“数”的问题借助于“形”去观察,或将“形”的问题借助于“数”去思考。在化学上,有很多问题也可以用这种数形结合的思想去解决。
例5.化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是( )
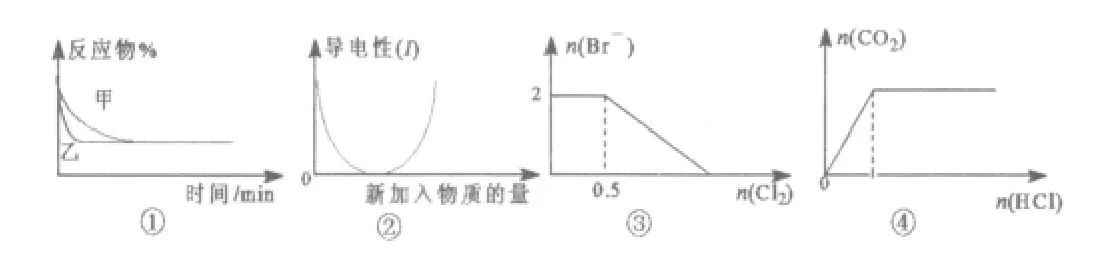
A.图①表示压强对可逆反应 2A(g)+2B(g)⇌3C(g)+D(s)的影响,乙的压强大
B.图②表示乙酸溶液中通入氨气至过量的过程中溶液导电性的变化
C.图③表示在 1L 1mol·L-1FeBr2溶液中通入 Cl2时 Br-的量的变化
D.图④表示一定浓度Na2CO3溶液中滴加盐酸,生成CO2与滴加盐酸物质的量的关系
分析:可逆反应 2A(g)+2B(g)⇌3C(g)+D(s)的气体系数和不为零,所以压强改变对平衡是影响的,而由图像得出的结论为没有影响,这里学生的忽略D(s),得出错误的数字关系。又图②得出的结论是导电性减弱,而乙酸溶液中通入氨气会生成乙酸铵是强电解质,导电性应该增强。一定浓度Na2CO3溶液中滴加盐酸,开始应该没有气体,生成的是碳酸氢钠,而图像是开始就有气体。可以变式为向盐酸溶液中滴加碳酸钠溶液,则图像怎么样。
七、分类观
将大量的物质按照一定的“标准”进行分类,是一种简单易行的、行之有效的科学方法,这种方法是化学学科常用的一种研究方法和学习方法。观察事物的角度不同,就能形成了带有学科特点的分类角度和分类方法。对于数以千万计化学物质,利用分类观,能把繁多的物质通过分类构成一个有序的逻辑体系,有利于把握物质之间的本质区别和联系,进而探讨各类物质之间的转化关系,为从整体上认识化学物质及其变化提供内在线索,这也将有利于学生的认知过程。实践证明,光有许多零碎的知识而没有形成整体的知识结构,就犹如没有组装成整机的一堆零部件而难以发挥其各自功能。
“交叉分类”和“树状分类”是两种常用的、具体的分类方法。“树状分类”可以对多达千万种的化学物质和为数更多的化学反应进行分门别类地研究,使有关的知识系统化;“交叉分类”可以从不同的角度对同一个物质进行多方位的研究,使有关的认识全面化,这便是两者的区别与联系。
化学学科思想是化学家们在长期的实践活动中形成的,既是他们对化学研究领域和研究对象的看法和观点,又是他们研究解决化学问题的思路和方法。在高三化学一轮复习的过程中让学生掌握化学思想,能有效地探求物质变化的规律,有助于从化学的视角去认识和解决日常生活中的化学问题,从而提高学生的科学素养。
张华伟)
