米非司酮治疗子宫肌瘤有效性的Meta分析
王玉晶,单永强,陈大方
子宫肌瘤是女性最为常见的盆腔肿瘤,一般认为35 岁以上女性中 20% 患有子宫肌瘤,而尸检报告中,发生率更高,达到 50%[1-2]。子宫肌瘤虽然为良性肿瘤,很少恶变,但却是造成女性子宫切除的最为常见的单一指征。同时由于手术的风险、损伤和并发症,探索子宫肌瘤的非手术疗法日益受到重视。自1993年Murphy等[3]首次报道应用米非司酮治疗子宫肌瘤后,米非司酮疗法在子宫肌瘤的非手术疗法中日益突出和热门,有关米非司酮治疗子宫肌瘤的研究报道层出不穷,但结论却不尽相同[4-6]。由于至今尚未有任何国家批准子宫肌瘤作为米非司酮治疗的适应证,因此,米非司酮治疗子宫肌瘤的临床应用尚处于经验处方阶段,缺乏规范的指导。本研究拟通过 Meta 分析方法对米非司酮治疗子宫肌瘤的相关研究进行综合评价,以期对米非司酮治疗子宫肌瘤的应用获得一个综合性的结论,为子宫肌瘤的药物治疗提供参考。
1 资料与方法
1.1 资料来源
研究范围限定为1990–2010年发表的应用米非司酮治疗子宫肌瘤效果评价的文章。文献检索对象为中英文文摘索引型数据库和中英文全文型数据库:《中国期刊全文专题数据库》(CNKI)、《万方数据期刊系统》、《中国电子期刊数据库》(维普全文电子期刊)、Medline、Embase、《Elsevier 电子期刊全文数据库》、《保健、医学与药学电子期刊全文数据库》、EBSCO 全文型数据库、OVID 电子期刊全文数据及PubMed Central 全文型数据库等。分别以“子宫肌瘤,uterine leiomyomata”和“米非司酮,mifepristone”作为检索词进行检索。
1.2 资料纳入标准
⑴原始资料为已公开发表的文献;
⑵纳入患者的诊断符合子宫肌瘤治疗的诊断标准,治疗前未使用性激素类药物治疗,并排除心、脑、肝、肾等重要器官疾病;
⑶原始文献必须是自身前后对照试验;
⑷各文献研究方法类似,有评价指标,即用药前后子宫大小、用药前后肌瘤大小、用药前后血红蛋白变化。
1.3 资料排除标准
⑴原始文献数据不完整,如:治疗前后的子宫肌瘤体积均数和标准差不完全,疗效评判标准不是以肌瘤体积变化情况为指标;
⑵原始文献混杂其他治疗方法,如中药、针灸等。
1.4 分析方法
由于本研究针对的为无对照临床试验,因此采用定性质量评估的方法,阅读文献,根据以下几方面内容书写评语:①受试对象的纳入标准是什么,是否具有代表性,诊断有无金标准;②采用何种防止偏倚的措施;③结局(疗效、不良反应、平稳性和经济学评价)选取的指标是什么,可靠程度如何,疗效、不良反应的评定标准是什么;④样本数量估计是否合适,样本数量是否足够;⑤统计学处理是否正确;⑥有无混杂因素、沾染与干扰存在,如治疗过程中其他治疗措施的影响或不一致。
1.5 统计方法
使用 Cochrane 协作网软件 RevMan 4.2 进行 Meta分析,连续变量计算加权均数差及其 95% 置信区间,漏斗图检测潜在的发表偏倚。统计时,同时进行异质性和敏感性分析。
2 结果
2.1 纳入文献情况
2.1.1 中文文献 根据文献的纳入和排除标准,共有20 篇研究报告纳入分析,均为自身前后对照。其中,18 篇应用米非司酮 12.5 mg/d;1 篇应用米非司酮 6.25 mg/d;1 篇应用米非司酮 25 mg/d,观察时间为3~6个月。其中 1 篇为与空白对照组进行对照。
2.1.2 英文文献 根据文献的纳入和排除标准,共有7 篇研究报告纳入分析。7 篇文献中,3 篇为安慰剂对照,4 篇为不同剂量组对照。与安慰剂对照的研究应用米非司酮5 mg/d,采用不同剂量对照的研究应用米非司酮 5 mg/d 与10 mg/d 进行对照。
2.2 临床疗效评估
2.2.1 米非司酮治疗子宫肌瘤的有效性
2.2.1.1 子宫肌瘤缩小水平 由于1 篇中文文献使用米非司酮剂量过大,予以剔除,共纳入文献 20 篇,总病例数为1174 例。经异质性检验,两组非同质,因此采用随机效检验,非同质,因此采用随机效应模型进行分析。分析结果显示,应用米非司酮治疗后,患者血红蛋白水平明显升高,与用药前相比有显著性差异(P<0.00001)(表 3)。

表1 米非司酮治疗后子宫肌瘤缩小水平

表2 米非司酮治疗后子宫体积缩小水平
2.2.2 不同剂量米非司酮治疗子宫肌瘤的有效性
2.2.2.1 对子宫肌瘤大小的影响 仅有 3 篇文献对不同剂量米非司酮的治疗进行了比较,其中 1 篇未提供具体原始数据,予以剔除,共纳入 2 篇文献。纳入分析病例共70 例,经对异质性检验,属同质,因此采用固定效应模型进行分析。分析结果显示,给予 5 mg/d 与10 mg/d 米非司酮治疗后,两组子宫肌瘤大小无显著差异(表 4)。
2.2.2.2 对盆腔疼痛及盆腔压迫症状的改善 纳入 2 篇文献,共 70 例病例。经异质性检验,属同质,因此采用固应模型进行分析。分析结果显示,应用米非司酮治疗后,患者子宫肌瘤体积明显缩小,与用药前相比有显著性差异(P<0.00001)(表1)。
2.2.1.2 子宫体积缩小水平 由于英文文献均未提供米非司酮用药前后子宫体积变化情况,且 1 篇文献用药剂量过大,均予以剔除。最终有 20 篇中文文献纳入分析,总病例数为1072 例。经异质性检验,两组非同质,因此采用随机效应模型进行分析。分析结果显示,应用米非司酮治疗后,患者子宫体积明显缩小,与用药前相比有显著性差异(P<0.00001)(表 2)。
2.2.1.3 血红蛋白升高水平 共 10 篇文献提供了用药前后血红蛋白变化情况,共纳入分析病例484 例。经异质性
定效应模型对比值比(OR 值)进行分析。发现给予 5 mg/d与10 mg/d 米非司酮治疗后,两组对盆腔疼痛及盆腔压迫症状的改善程度无显著性差异(表 5和表 6)。
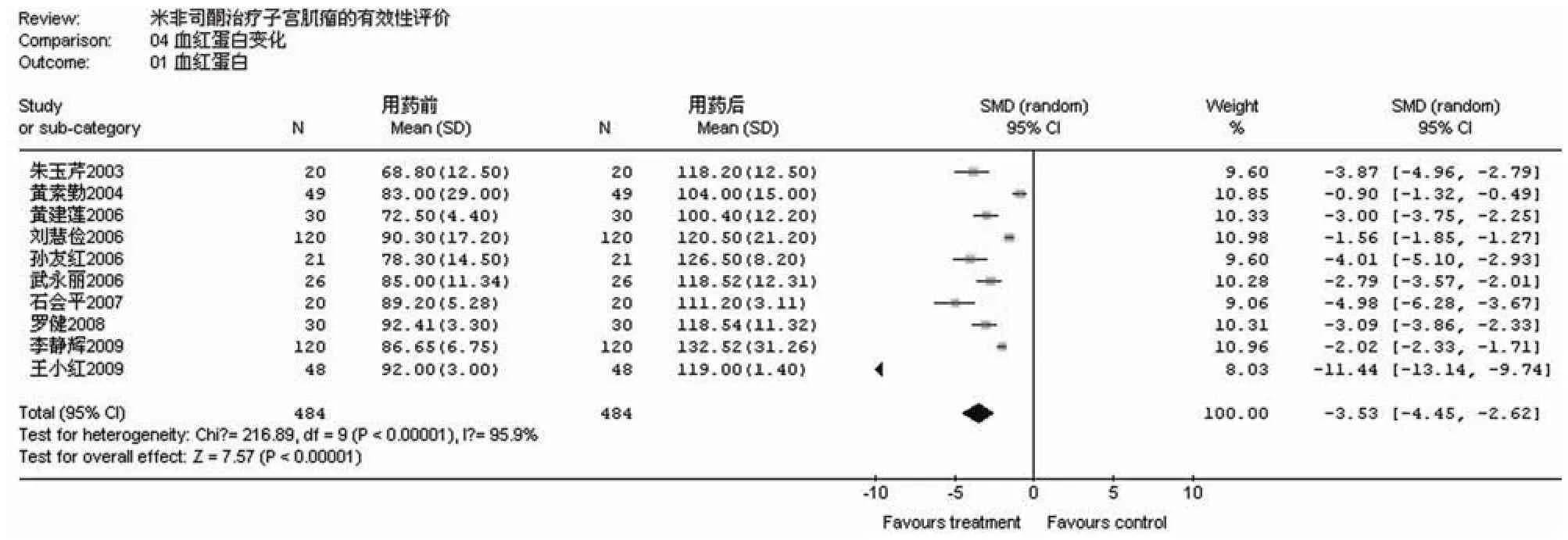
表3 米非司酮治疗后血红蛋白升高水平

表4 5 mg/d 与10 mg/d 米非司酮治疗后子宫肌瘤缩小水平
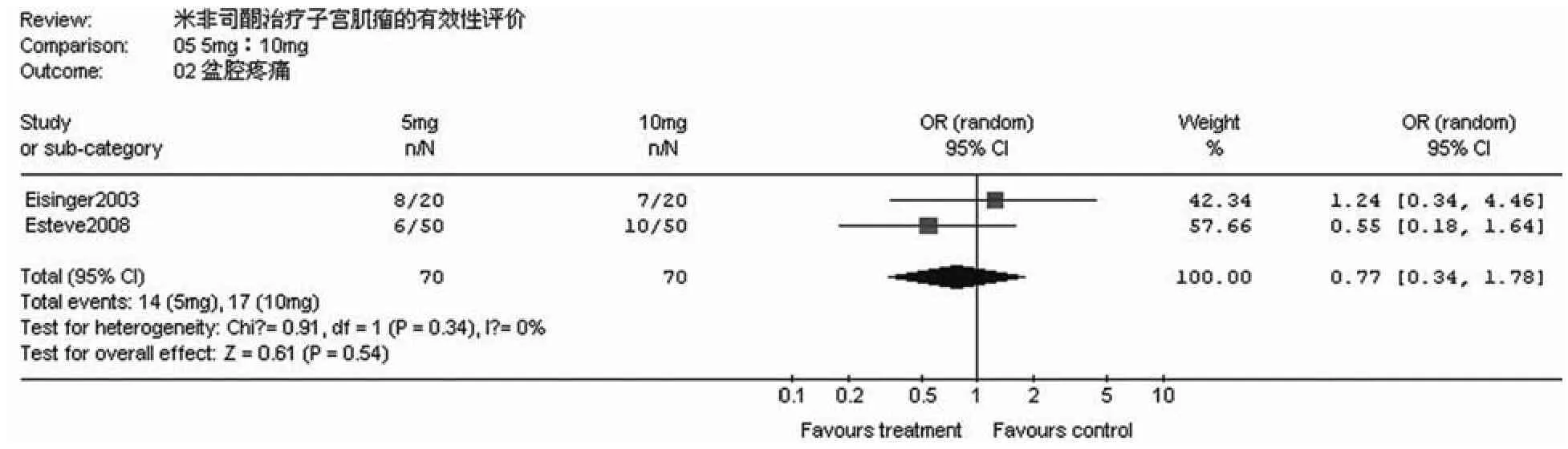
表5 5 mg/d 与10 mg/d 米非司酮治疗后对盆腔疼痛的影响
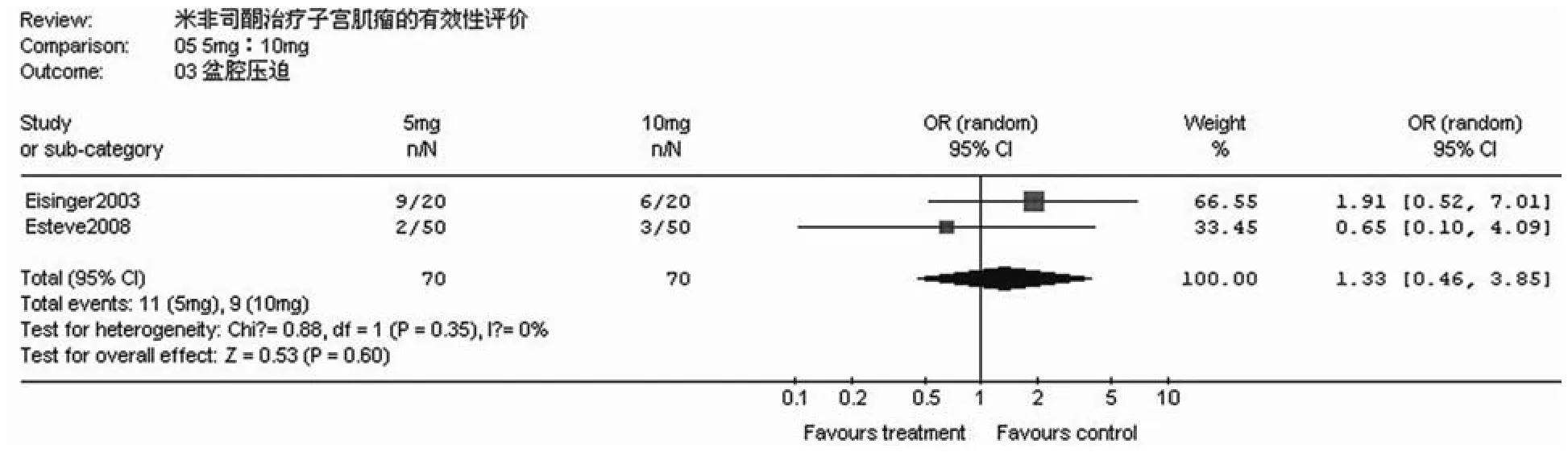
表6 5 mg/d 与10 mg/d 米非司酮治疗后对盆腔压迫的影响
3 讨论
3.1 米非司酮治疗子宫肌瘤的机制
近年来的研究显示孕激素在子宫肌瘤的发生及成长中起着重要作用,孕激素及孕激素受体调节着子宫肌瘤细胞的分裂活动,促进子宫肌瘤的增殖。很多研究均表明子宫肌瘤是具有雌激素受体和孕激素受体的甾体激素依赖性肿瘤。米非司酮具有很强的与孕激素受体相结合的能力,能拮抗体内孕激素刺激肌瘤组织中表皮生长因子的表达,使肌瘤中孕激素受体明显减少,同时雌激素受体也随之减少,血清中雌、孕激素维持在卵泡期较低水平,从而使肌瘤组织中雌、孕激素效应明显降低,导致肌瘤体积缩小[7-9];米非司酮作为孕激素拮抗剂还可影响下丘脑-垂体-卵巢轴,使体内激素水平下降,内膜变薄、萎缩,导致闭经,明显减少子宫动脉血流,所以对于子宫肌瘤导致贫血的患者,米非司酮还可起到止血、减少月经量、纠正贫血的作用[10-11]。
3.2 米非司酮治疗子宫肌瘤的有效性评价
通过回顾分析文献,米非司酮作为保守治疗方法,对子宫肌瘤的控制有明显作用。应用米非司酮 3~6个月后,患者子宫体积和肌瘤体积均明显缩小,同时,血红蛋白水平也有明显提高。
子宫体积和肌瘤体积的缩小,能够使部分围绝经期患者可以仅接受保守治疗而避免手术[12-14]。而对于肌瘤直径大于8cm的患者,通过服用米非司酮进行术前准备,可以有效地缩小肌瘤体积,达到微创手术的要求,降低手术风险和创伤[15-17]。
米非司酮对血红蛋白水平的改善作用,可以有效地纠正贫血,为患者接受手术治疗提供了前提。同时,也能降低患者输血的几率,在降低输血风险的同时,也对节约血源做出了一定的贡献。
3.3 不同剂量米非司酮治疗子宫肌瘤的评价
自1993年首次报道应用米非司酮治疗子宫肌瘤后,国内外临床应用逐渐普遍。但是,由于至今尚未有任何国家批准子宫肌瘤作为米非司酮治疗的适应证,因此,对于米非司酮治疗子宫肌瘤的应用,缺乏规范的指导。我国多数文献报道米非司酮治疗子宫肌瘤的用量为12.5 mg/d[18-20],国外的报道多集中于5 mg/d和10 mg/d 两个剂量[21-23]。通过对文献的回顾,我们发现 5 mg/d 与10 mg/d 在对子宫体积、肌瘤体积、盆腔症状的改善等方面未见明显差异。同时,也有研究显示,米非司酮的浓度达到一定的阈值后,再增加浓度并不能相应增加其抑制作用[24],提示米非司酮的大剂量应用方案可能并不合适。但是,由于缺少大规模的随机对照试验为在中国人群中进行的随机对照试验进行参考,尚无法确定其最佳给药剂量。
通过对国内外文献的回顾,虽然米非司酮目前尚未获得药监部门对子宫肌瘤适应证的批准,但是其治疗子宫肌瘤的作用已经得到肯定。同时也有文献支持米非司酮与茯苓胶囊、雷公藤等中药合用[25],或者与内美通合用[26]可以达到对子宫肌瘤治疗目的。由于目前临床用于治疗子宫肌瘤的促性腺激素释放激素(GnRH)类药物,价格非常昂贵,且复发率高,所以临床需要寻求更为经济有效的治疗途径。米非司酮或将成为治疗子宫肌瘤更经济、更有前途的药物。虽然不能完全代替手术治疗,但是为围绝经期、需要术前准备及有生育要求的育龄患者提供了治疗途径。但是,由于缺乏临床研究的指导,目前米非司酮的临床应用尚处于经验处方阶段,其用药剂量和用药注意事项缺乏规范性和统一性。因此,需要国内外继续进行大规模的临床试验,为米非司酮的合理应用提供指导。
[1]Huang JL, Chen SY, Chen SF.Preoperative application of mifepristone for uterine leiomyomata.Acta Med Sinica, 2006, 19(1):96-97.(in Chinese)黄建莲, 陈树扬, 陈淑芳.米非司酮在子宫肌瘤患者术前的应用.华夏医学, 2006, 19(1):96-97.
[2]Dai X, Liu J, Li AQ, et al.Clinical study of mifepristone in the treatment of leiomyoma.Prac Clin Med, 2004, 5(6):82-84.(in Chinese)戴星, 刘洁, 李爱青,等.米非司酮治疗子宫肌瘤的效果观察.实用临床医学, 2004, 5(6):82-84.
[3]Murphy AA, Morales AJ, Kettel LM, et al.Regression of uterine leiomyomata to the antiprogesterone RU486: dose-response effect.Fertil Steril, 1995, 64(1):187-190.
[4]Murphy AA, Kettel LM, Morales AJ, et al.Regression of uterine leiomyomata in response to the antiprogesterone RU 486.J Clin Endocrinol Metab, 1993, 76(2):513-517.
[5]Li JH.Application of mifepristone for expectant treatment of uterine leiomyomata.China Prac Med, 2009, 4(2):131-132.(in Chinese)李静辉.米非司酮在子宫肌瘤保守治疗中的应用价值.中国实用医药, 2009, 4(2):131-132.
[6]Wang XP, Yang SL, Wu T.Clinical analysis of 56 patients with low dose of mifepristone treating leiomyoma.J Dalian Med Univ, 2005,27(5):374-376.(in Chinese)王雪萍, 杨淑丽, 吴彤.小剂量米非司酮治疗子宫肌瘤 56例临床分析.大连医科大学学报, 2005, 27(5):374-376.
[7]Engman M, Granberg S, Williams AR, et al.Mifepristone for treatment of uterine leiomyoma.A prospective randomized placebo controlled trial.Hum Reprod, 2009, 24(8):1870-1879.
[8]Bagaria M, Suneja A, Vaid NB, et al.Low-dose mifepristone in treatment of uterine leiomyoma: a randomised double-blind placebo-controlled clinical trial.Aust N Z J Obstet Gynaecol, 2009,49(1):77-83.
[9]Fiscella K, Eisinger SH, Meldrum S, et al.Effect of mifepristone for symptomatic leiomyomata on quality of life and uterine size: a randomized controlled trial.Obstet Gynecol, 2006, 108(6):1381-1387.
[10]Reinsch RC, Murphy AA, Morales AJ, et al.The effects of RU 486 and leuprolide acetate on uterine artery blood flow in the fibroid uterus: a prospective, randomized study.Am J Obstet Gynecol, 1994,170(6):1623-1627.
[11]Kettel LM, Murphy AA, Morales AJ, et al.Clinical efficacy of the antiprogesterone RU486 in the treatment of endometriosis and uterine fibroids.Hum Reprod, 1994, 9 Suppl 1:116-120.
[12]Gao XQ, Li X.The clinical observation on mifepristone in treating 40 cases uterus myoma in perimenopausal.Hebei Med, 2009, 15(2):214-216.(in Chinese)高小琴, 李雪.米非司酮治疗围绝经期子宫肌瘤 40例临床观察.河北医学, 2009, 15(2):214-216.
[13]Yu Y, Huang CJ.Clinical analysis of mifepristone for the treatment of perimenopausal uterine leiomyomata.Acta Acad Med Neimongol,2007, 29(4):282-283.(in Chinese)于艳, 黄长江.米非司酮治疗围绝经期子宫肌瘤的临床分析.内蒙古医学院学报, 2007, 29(4):282-283.
[14]Yang HW.Study of therapeutic effects of low-dose mifepristone for the treatment of perimenopausal uterine leiomyomata.China Clin Gynecol Obstet J, 2004, 12(3):952-954.(in Chinese)杨红文.小剂量米非司酮治疗围绝经期子宫肌瘤的疗效研究.中华临床妇科与产科杂志, 2004, 12(3):952-954.
[15]Sun YH, You L, Xu GF.Preoperative application of mifepristone for myomectomy of nonparous women.J Clin Med Prac, 2006, 10(5):92-93.(in Chinese)孙友红, 游丽, 徐国风.米非司酮在未育妇女子宫肌瘤剔除术前的应用.实用临床医药杂志, 2006, 10(5):92-93.
[16]Luo J.Clinical observation of preoperative application of mifepristone for the treatment of uterine leiomyomata.World Health Dig, 2008,5(4):195-196.(in Chinese)罗健.米非司酮子宫肌瘤术前用药的临床观察.中外健康文摘,2008, 5(4):195-196.
[17]Zhu YQ, Zhang Y.Clinical analysis of 36 cases of preoperative application of mifepristone for treatment of uterine leiomyomata.J North China Coal Med Coll, 2003, 5(1):41.(in Chinese)朱玉芹, 张艳.子宫肌瘤手术前应用米非司酮 36例疗效观察.华北煤炭医学院学报, 2003, 5(1):41.
[18]Zhao YL.Clinical analysis of 66 cases of application of mifepristone for treatment of uterine leiomyomata.China Med Herald, 2009, 6(18):37, 39.(in Chinese)赵艳丽.米非司酮治疗子宫肌瘤 66例临床疗效观察.中国医药导报, 2009, 6(18):37, 39.
[19]Hu YL.Clinical analysis of 102 cases of application of mifepristone for treatment of uterine leiomyomata.J Clin Exp Med, 2008, 7(11):129.(in Chinese)胡雁兰.米非司酮治疗子宫肌瘤102例临床疗效分析.临床和实验医学杂志, 2008, 7(11):129.
[20]Liu HJ.Clinical analysis of 120 cases of application of mifepristone for the treatment of uterine leiomyomata.Matern Child Health Care China, 2006, 21(12):1739-1740.(in Chinese)刘慧俭.米非司酮治疗子宫肌瘤120例临床效果观察.中国妇幼保健, 2006, 21(12):1739-1740.
[21]Carbonell Esteve JL, Acosta R, Heredia B, et al.Mifepristone for the treatment of uterine leiomyomas: a randomized controlled trial.Obstet Gynecol, 2008, 112(5):1029-1036.
[22]Eisinger SH, Bonfiglio T, Fiscella K, et al.Twelve-month safety and efficacy of low-dose mifepristone for uterine myomas.J Minim Invasive Gynecol, 2005, 12(3):227-233.
[23]Eisinger SH, Meldrum S, Fiscella K, et al.Low-dose mifepristone for uterine leiomyomata.Obstet Gynecol, 2003, 101(2):243-250.
[24]Eisinger SH, Fiscella J, Bonfiglio T, et al.Open-label study of ultra low-dose mifepristone for the treatment of uterine leiomyomata.Eur J Obstet Gynecol Reprod Biol, 2009, 146(2):215-218.
[25]Xie P, Qiao FN, Feng J, et al.Systematic review of traditional Chinese medicine for the treatment of uterus myoma.Chin J Fam Plann Gynecotokology, 2010, 2(1):56-60.(in Chinese)谢萍, 乔峰妮, 冯俭,等.中医药治疗子宫肌瘤的系统评价.中国计划生育和妇产科, 2010, 2(1):56-60.
[26]Hou XL.Clinical exploration of mifepristone with or without gestrinone in the treatment of uterine leiomyoma.Medical Journal of Casc, 2004, 6(4):36-38.(in Chinese)侯晓兰.米非司酮配伍与不配伍内美通治疗子宫肌瘤临床探讨.中国现代医药杂志, 2004, 6(4):36-38.

