急性感染后肾小球肾炎
梁丹丹 曾彩虹 刘志红
病例摘要
病史 11岁男性患者,因“发作双下肢皮疹1次,尿检异常5d”先后于2011-01-26和2012-01-17两次入院。
患者2011-01-21无明显诱因出现双足背红色皮疹,无瘙痒,亦无关节痛、腹痛、黑便等症状,当日查尿蛋白2+,隐血1+,血压正常,未查肾功能,予地塞米松5mg静脉滴注,口服西咪替丁(0.2g),2d后皮疹消退。我院查尿蛋白定量6.22 g/24h,尿沉渣红细胞计数44万/ml,多形型,血清白蛋白36.7 g/L,血清肌酐(SCr)68 μmol/L,尿素氮(BUN)19 mmol/L,尿酸(UA)543 μmol/L,2011-01-26 首次收入院。病程中无水肿、肉眼血尿、少尿、夜尿增多、高血压,无不规则发热、咳嗽、咳痰、腹痛、腹泻、尿频、尿急、尿痛、脱发、口腔溃疡等。体重无明显变化。精神、饮食、睡眠正常。
既往史、个人史、家族史无特殊。
体格检查 体温36.5℃,血压110/70 mmHg,全身皮肤未见皮疹,扁桃体无肿大,心、肺、腹部查体无明显异常,双下肢无水肿。
实验室检查
血常规 血红蛋白118 g/L,白细胞8.5×109/L,血小板218×109/L。
血生化 白蛋白28 g/L,球蛋白24 g/L,BUN 28 mmol/L,SCr 96 μmol/L,UA 562 μmol/L,胱抑素C 1.78mg/L,谷丙转氨酶16 U/L,谷草转氨酶21 U/L,总胆固醇 3.27 mmol/L,三酰甘油 1.47 mmol/L,钠 136.4 mmol/L,钾 6.12 mmol/L,氯103.1 mmol/L,总二氧化碳24.1 mmol/L,钙 1.93 mmol/L,磷1.85 mmol/L,空腹血糖 5.16 mmol/L。
尿液 尿蛋白定量6.11~6.22 g/24h,尿沉渣红细胞计数44~520万/ml(多形型);C3 2.89mg/L(正常值≤2.76mg/L),α2巨球蛋白(α2-MG)3.0mg/L(正常值≤2.87mg/L),N-乙酰-β-D-氨基葡萄糖苷酶(NAG酶)25.5 U/(g·Cr)[正常值≤16.5 U/(g·Cr)],视黄醇结合蛋白(RBP)0.43mg/L(正常值≤0.5mg/L),溶菌酶(Lyso)0.95mg/L(正常值 <1.0mg/L)。
免疫学 ANA、A-dsDNA、血ENA多肽抗体谱、ANCA 阴性,IgG 16.2 g/L,IgA 2.7 g/L,IgM 1.01 g/L,IgE 222 IU/ml,抗链球菌溶血素“O”(ASO)966 IU/ml,类风湿因子(RF)<20 IU/ml,补体 C3 0.42 g/L,C4 0.08 g/L,抗心磷脂抗体谱 IgM、IgG(-)、IgA阳性179.6APL-U/ml,狼疮样抗凝因子和抗C1q抗体阴性。传染病八项均阴性。红细胞碎片>10枚/全片。外周血淋巴细胞亚群CD4+284个/μl,CD8+712 个/μl,CD3+1 167 个/μl,CD20+274 个/μl。血清 E选择素 140.55 ng/ml(正常值 35~65 ng/ml),血管性血友病因子 197.7%(正常值 <200%),循环内皮细胞 26个/ml(正常值 <20个/ml),人血管内皮细胞黏附分子(VCAM)921.10 ng/ml(正常值300~1 000 ng/ml),血栓调节蛋白(thrombomodulin)3.62 ng/ml(正常值 3.15~5.8 ng/ml)。冷球蛋白411mg/L(正常值≤192mg/L)。
患者住院期间尿量偏少(500~660 ml/d),并出现高钾血症,SCr进行性升至119μmol/L,予以水化、降钾处理后行肾活检术。
第一次肾活检(2011-01-29)
光镜 皮-髓-皮肾组织1条,15个正切体积增大的肾小球。肾小球毛细血管袢内弥漫细胞增生,包括单个核细胞及中性粒细胞>10个/球(图1A);袢腔狭窄,见微血栓,囊壁节段增厚。PASMMasson:肾小球基膜内皮下少量嗜复红物沉积,上皮侧见“驼峰”形成(图1B)。肾小管间质急性病变轻度,多灶性肾小管上皮细胞肿胀、细颗粒变性,散在小管上皮细胞小空泡和粗颗粒变性,皮髓交界区小灶性单个核细胞浸润。小动脉节段透明变性。

图1 A:肾小球弥漫内皮细胞增生、单个核及中性粒细胞浸润(HE,×400);B:肾小球基膜上皮侧“驼峰”,内皮下少量嗜复红物沉积(Masson三色,×400);C:重复肾活检肾小球轻度系膜增生性病变(PAS,×400)
免疫荧光 荧光染色IgA++(图2A),节段分布,呈颗粒状沉积于系膜区和血管袢。C3++弥漫分布,呈现环状沉积于系膜区和血管袢。IgM+、C1q++(图2C),弥漫分布,呈颗粒状沉积于系膜区和血管袢。IgG阴性。肾小管基膜、球门区血管、管间毛细血管、间质血管未见免疫复合物、补体沉积。
免疫组化 CD4细胞:球内平均0个/球,间质平均228个/mm2,CD8细胞:球内平均0个/球,间质平均184个/mm2,CD20细胞:球内平均0个/球,间质平均60个/mm2,CD68细胞:球内平均48.2个/球,间质平均64个/mm2,PCNA细胞:球内平均15 个/球,间质0 个/mm2。
电镜 观察2个肾小球,毛细血管袢内见较多增生的内皮细胞,亦见单核细胞、中性粒细胞浸润,致使袢腔狭小,有的甚至闭塞(图3A);多处基膜上皮侧见“驼峰”(图3B),有的上皮侧电子致密物呈扁平状,内皮下亦见团块状高密度的电子致密物沉积(图3C)。多处系膜区亦见电子致密物沉积。肾小球足细胞胞质较多微绒毛化,足突节段性融合增宽约50%~60%。
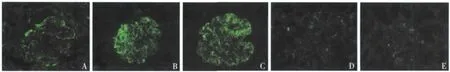
图2 IgA++(A),呈颗粒状节段分布于系膜区和血管袢,C3++(B)、C1q++(C)呈颗粒状,弥漫分布于系膜区和血管袢(IF,×400);重复肾活检:IgA+(D)、C3+(E)呈细颗粒状,弥漫分布于系膜区及血管袢(IF,×400)

图3 A:肾小球毛细血管袢内较多内皮细胞增生,伴单核细胞、中性粒细胞浸润(EM);B:肾小球基膜上皮侧“驼峰”(EM);C:肾小球内皮下电子致密物沉积(EM);D:重复肾活检见肾小球基膜内皮下电子致密物吸收,密度减低(EM)
治疗经过及随访 患者经肾活检诊断为毛细血管内增生性肾小球肾炎,急性肾损伤1期。2011-01-30起予以甲泼尼龙冲击治疗(500mg×2d),复查SCr降至99μmol/L,尿量恢复至1 700 ml/d左右,出院后续以霉酚酸酯0.5 g/d(浓度23.16~26.83mg·h/L)、他克莫司2~3mg/d(浓度3.06~3.78 ng/ml)、泼尼松30mg/d免疫抑制治疗,其中泼尼松服7月后停药,霉酚酸酯、他克莫司维持1年。出院随访半个月时补体升至正常,C3 0.8 g/L,C4 0.1 g/L,ASO降至152 IU/ml,随访4个月时尿检完全缓解,随访7月时抗心磷脂抗体阴性,随访1年时复查冷球蛋白降至正常(101.55mg/L)。于2012-01-17第二次入院行重复肾活检。
重复肾活检(2012-01-18)
光镜 皮质肾组织3条、皮-髓肾组织1条。51个肾小球,系膜区轻度增宽,节段中度增宽,系膜细胞及基质增多(图1C),毛细血管袢开放好,偶见内皮细胞成对,偶见囊壁节段增厚。PASM-Masson:阴性。肾小管间质病变轻,散在小管萎缩、基膜增厚,小灶性小管上皮细胞细颗粒变性。动脉未见明确病变。
免疫荧光 荧光染色IgA+(图2D)、C3+(图2E),弥漫分布,呈细颗粒状沉积于系膜区及血管袢。IgG、IgM、C1q阴性。肾小管基膜、球门区血管、管间毛细血管、间质血管未见免疫复合物、补体沉积。
电镜 观察1个肾小球,肾小球系膜区增宽,系膜细胞及系膜基质增生,系膜区偶见高密度电子致密物沉积。肾小球毛细血管袢开放好,节段内皮下疏松,内皮下偶见高密度电子致密物,见电子致密物吸收,密度减低(图3D),基膜厚约260~510 nm,肾小球上皮侧未见电子致密物沉积。肾小球足细胞胞质少量微绒毛化,足突节段性融合约20%~30%。
小结:结合临床病理诊断为急性感染后肾小球肾炎。
讨 论
患者为青少年男性,病程短,以双下肢发作性皮疹急性起病,临床表现为急性肾炎综合征,SCr最高升至119μmol/L,伴大量蛋白尿、镜下血尿,无水肿、肉眼血尿及高血压,ASO明显升高,补体 C3下降。
患者第一次肾活检病理组织学病变为肾小球毛细血管袢内内皮细胞明显增生,伴较多中性粒细胞、单核细胞浸润致袢腔堵塞;免疫荧光示补体C3呈花环状强阳性沉积于血管袢及系膜区,此外伴IgA、IgM、C1q等免疫球蛋白及补体成分沉积;电镜下观察肾小球基膜上皮侧典型“驼峰”样电子致密物沉积,同时伴有肾小球系膜区、基膜内皮下较多电子致密物沉积。因此结合临床及第一次肾活检诊断为“急性感染后肾小球肾炎”。
目前认为急性感染后肾小球肾炎组织学表现主要有四种:(1)肾小球毛细血管内增生性病变;(2)新月体肾炎;(3)肾小球系膜增生性病变;(4)肾小球膜增生性病变。其中肾小球毛细血管内增生性病变最常见,早期光镜下肾小球病变均匀一致,表现弥漫内皮、系膜细胞增生,同时毛细血管袢内大量中性粒细胞及单核细胞浸润,因此又称为渗出期。该患者第一次肾活检属于肾小球毛细血管内增生性病变,伴大量浸润细胞,为渗出期病变。此外该患者的免疫荧光也具有一定的特殊性,免疫荧光C3沉积表现为“花环型”,同时伴少量IgA、IgM、C1q沉积。而经典的感染后肾小球肾炎,免疫荧光主要表现C3沉积于肾小球,以“星空型”最多见,也有部分病例呈系膜型、花环型,经典的感染后肾小球肾炎除C3沉积外,最常伴IgG沉积,少数病例尚见IgM、IgA、C1q沉积。该患者肾小球C3沉积,但IgG阴性,尚伴少量IgA、IgM、C1q沉积,即使在重复活检毛细血管内增生性病变明显减轻时,肾小球仍有少量C3和IgA沉积。电镜下见肾小球上皮侧“驼峰”,亦可见肾小球系膜区、内皮下、基膜内,甚至球囊壁内电子致密物沉积[1]。Nasr等[2]对86 例年龄≥16 岁的感染后肾小球肾炎患者肾脏病理进行分析,电镜下94%的患者伴肾小球基膜上皮侧电子致密物沉积,且大多数表现为“驼峰”,90.4%伴肾小球系膜区电子致密物沉积,74.7%伴肾小球基膜内皮下电子致密物沉积,但通常小且稀少。免疫荧光C3呈“花环型”沉积,电镜下除上皮侧“驼峰”外,常伴肾小球基膜内皮下和系膜区电子致密物沉积,该患者的免疫荧光C3沉积和电镜下的电子致密物沉积符合以上特点。此时需与膜增生性肾小球肾炎鉴别,后者常伴IgG沉积,光镜下肾小球外周袢分层,电镜下系膜基质插入较明显,临床无ASO的升高。
随着病程的进展,感染后肾小球肾炎的渗出性病变会逐渐吸收,由于重复肾活检的病例很少,对病变吸收的程度和时间了解并不是很多。文献报道感染后肾小球肾炎典型病变在4~10周后逐渐消散,消散期渗出性病变可完全吸收,仅表现肾小球系膜增生性病变,电镜下“驼峰”一般于病后6~8周消失,而系膜增生恢复缓慢,可达数月或数年之久。因此对感染后肾小球肾炎处于恢复期或既往临床隐匿感染、症状不典型的患者行肾活检,其组织学可表现为肾小球系膜增生性病变,病理医生往往会忽视感染后肾小球肾炎的存在[3],因此,感染后肾小球肾炎的发病率远高于现有的发病率数据[4]。
该患者首次肾活检明确诊断后,予甲泼尼龙冲击,后续霉酚酸酯、他克莫司、泼尼松三联免疫抑制治疗,随访半个月时补体和ASO恢复正常,随访4个月时尿检完全缓解,随访7月时抗心磷脂抗体阴性,随访1年时复查冷球蛋白降至正常。为进一步观察患者的肾脏病变的形态学改变,在首次肾活检一年时行重复肾活检发现,肾小球毛细血管内增生性病变明显吸收,袢开放良好,上皮侧“驼峰”消失,仅见轻度系膜增生性病变。从而分别从临床预后和肾脏病理改变上再次证实了急性感染后肾小球肾炎的诊断,说明感染后肾小球肾炎的肾小球毛细血管内增生性病变可完全吸收,而系膜增生性病变的消散则需要较长时间。
此外,该患者临床表现也具有特殊之处,临床存在补体C3、C4均下降,血冷球蛋白升高,抗心磷脂抗体阳性,因此需要从临床和病理上与免疫性疾病如系统性红斑狼疮、抗心磷脂抗体综合征、冷球蛋白血症引起的肾损害进行鉴别:(1)患者虽然补体C3、C4均下降,但自身抗体均阴性,光镜虽表现为增生性病变,但免疫荧光无IgG沉积,不支持狼疮性肾炎的诊断。(2)患者在病初曾出现“皮疹”,但皮疹仅持续两天即消失,未遗留任何痕迹,不似过敏性紫癜的皮疹。且组织学表现为弥漫肾小球毛细血管内增生,免疫荧光以C3沉积为主,虽有IgA的沉积,但分布较节段,且基膜上皮侧见“驼峰”,此外临床存在补体C3的下降,综合以上特点不符合过敏性紫癜性肾炎。(3)冷球蛋白血症肾损害形态学常表现肾小球膜增生性病变伴袢内PAS强阳性的微栓塞,而本例除肾小球内皮细胞增生外,未见PAS强阳性栓塞,电镜下未观察到微管状的电子致密物,而是上皮侧大量“驼峰”,也不支持冷球蛋白血症肾损害的诊断。(4)本例患者抗心磷脂抗体IgA阳性,而抗心磷脂抗体综合征导致的肾损害,多表现为肾小球毛细血管袢内和(或)间质小动脉微血栓,少见如此明显的肾小球毛细血管内增生,因此不支持抗心磷脂抗体综合征肾损害。随着临床及病理改变的好转,抗心磷脂抗体及血冷球蛋白水平均恢复正常,因此可能是感染导致体内的免疫系统过度活化所致。Coppo等[5]检测了91例肾脏病患者的血清冷球蛋白,其中12.5%的原发性肾小球肾炎和22.2%的系统性疾病患者冷球蛋白水平升高。原发性肾小球肾炎中冷球蛋白升高与肾小球细胞增生和渗出性病变有明显关联,如急进性肾小球肾炎、急性感染后肾小球肾炎、膜增生性肾小球肾炎等。Ardiles等[6]发现,48%急性链球菌感染后肾小球肾炎及41.7%的链球菌感染的脓疱病患者的血清抗心磷脂抗体阳性,因此认为抗心磷脂抗体与链球菌感染相关,与肾脏损害无关。
经典的感染后肾小球肾炎是一种多发于儿童,由免疫介导的肾小球肾炎,与A族链球菌感染相关,通常发生在呼吸道或皮肤感染之后1~3周[7]。目前认为,除了A族链球菌外,C组和G组链球菌、葡萄球菌、革兰阴性菌、分支杆菌、寄生虫、真菌以及病毒也可导致感染后肾小球肾炎[8]。本例为青少年患者,属于好发人群,虽经反复追问无明确前驱感染病史,仍不排除存在隐匿感染可能。急性感染后肾小球肾炎的临床表现主要有三类:急性肾炎综合征、急进性肾炎综合征和临床症状不明显的肾小球肾炎,该患者临床表现为急性肾炎综合征。目前关于其发病机制认为主要与两种链球菌致肾炎物质有关,即甘油醛-3-磷酸脱氢酶(GAPDH)和链球菌致热外毒素 B/及其酶原前体(SpeB/zSpeB)[9],两者通过与血清纤溶酶原作用,进而激活胶原酶原或潜在的金属蛋白酶,使基膜降解,致肾炎抗原和其抗原抗体免疫复合物穿过受损的基膜,在其上皮侧形成“驼峰”,对基膜造成的损伤亦可导致足细胞足突融合,使得临床出现蛋白尿[10]。但对这一观点目前仍存在质疑,其发病机制尚未完全明确,亦使得病理表现多样。
本例临床表现为急性肾炎综合征,伴大量蛋白尿,ASO升高,补体C3、C4下降,抗心磷脂抗体阳性和血冷球蛋白升高。首次肾活检组织学表现为肾小球弥漫毛细血管内增生性病变,伴上皮侧嗜复红物沉积,免疫荧光以C3沉积为主,电镜下除肾小球基膜上皮侧“驼峰”外,尚见基膜内皮下及系膜区电子致密物沉积。经过免疫抑制剂治疗1年后,临床完全缓解,重复肾活检仅见轻度系膜增生性病变。两次肾活检很好地体现了急性感染后肾小球肾炎不同阶段的病理形态学特点,并最终证实这一诊断。
1 Sotsiou F.Postinfectious glomerulonephritis.Nephrol Dial Transplant,2001,16(Suppl 6):68 -70.
2 Nasr SH,Markowitz GS,Stokes MB,et al.Acute postinfectious glomerulonephritis in the modern era:experience with 86 adults and review of the literature.Medicine(Baltimore),2008,87:21 -32.
3 Haas M.Incidental healed postinfectious glomerulonephritis:a study of 1012 renal biopsy specimens examined by electron microscopy.Hum Pathol,2003,34(1):3 -10.
4 Ruiz P,Soares MF.Acute postinfectious glomerulonephritis:an immune response gone bad?Hum Pathol,2003,34(1):1 - 2.
5 Coppo R,Boero R,Cirone U,et al.Quantitative and qualitative determinations and clinical and histological correlations of cryoglobulins in glomerulonephritis.Arch Sci Med,1982,139(4):399-405.
6 Ardiles L,Ramirez P,Moya P,et al.Anticardiolipin antibodies in acute poststreptococcal glomerulonephritis and streptococcal impetigo.Nephron,1999,83(1):47 -52.
7 D'Agati VD,Jennette JC,Silva FG.Atlas of Nontumor Pathology:Non-Neoplastic Kidney Diseases.Washington,American Registry of Pathology-Armed Forces Institute of Pathology,2005:269 -321.
8 Montseny JJ,Meyrier A,Kleinknecht D,et al.The current spectrum of infectious glomerulonephritis.Experience with 76 patients and review of the literature.Medicine(Baltimore),1995,74(2):63 -73.
9 Rodriguez-Iturbe B,Batsford S.Pathogenesis of poststreptococcal glomerulonephritis a century after Clemens von Pirquet.Kidney Int,2007,71(11):1094 -1104.
10 Kanjanabuch T,Kittikowit W,Eiam-Ong S.An update on acute postinfectious glomerulonephritis worldwide.Nat Rev Nephrol,2009,5(5):259-269.

