六堡茶遗传毒性试验研究
覃良 李茂 黄宇声 刘冠萍
广西中医药研究院,广西南宁530022
六堡茶遗传毒性试验研究
覃良 李茂 黄宇声 刘冠萍
广西中医药研究院,广西南宁530022
目的:了解六堡茶遗传毒性,为六堡茶的食用、药用安全性提供实验依据。方法:通过A m e s试验、小鼠骨髓嗜多染红细胞微核试验及小鼠精子畸形试验对其遗传毒性进行评价。结果:苦丁茶提取物3项遗传毒性试验结果均为阴性,对所试菌株、小鼠体细胞与雄性生殖细胞无诱变性。结论:在本实验条件下,六堡茶提取物未见遗传毒性作用。
六堡茶提取物;A m e s试验;微核试验;精子畸形试验
广西梧州制药(集团)股份有限公司生产的六堡茶,用法用量为开水冲服,一次3g,一日3次。因其优良的口感深受消费者欢迎。本文报导其遗传毒性试验研究结果。
1 实验材料
1.1 受试药物六堡茶提取物,由广西梧州制药(集团)股份有限公司提供,批号20100408,性状为棕褐色浸膏(每毫升相当于药材1.87g)。用蒸馏水配成1.24g/ml供试验用。
1.2 实验动物KM小鼠90只,体重19~22g,雌雄各半,由广西医科大学实验动物中心提供,生产许可证SCXK2009-0003,动物质量合格证0009925。
2 实验方法与结果
2.1A mes试验采用标准试菌株TA97、TA98、TA100、TA102,在加和不加S-9混合液的条件下,用样品五个剂量组即5000、2500、1000、500及100μg进行平板掺入法试验。同时设自发回变对照组及阳性对照组。样品、阳性对照物敌克松(Dexon 50μg/皿)、甲基磺酸甲酯(MMS 1μL/皿)、2-氨基芴(2-AF 10μg/皿)、1,8-二羟基蒽醌(1,8-Dan 50μg/皿)均用二甲基亚砜(DMSO)溶解。每剂量平行做3皿,试验重复一次。结果样品各剂量组平均回变菌落数均未超过自发回变菌落数的2倍,见表1。
2.2 小骨髓微核试验将60只小鼠随机分为阳性对照组、阴性对照组(环磷酰胺40mg/kg体质量ip)、样品三个剂量组(49.6、24.8、12.4g药材/kg体质量),每组雌雄各5只。各组均用30 h 2次灌胃法,每次0.2mL/10g体质量。第二次灌胃后6h处死动物,取股骨骨髓悬于小牛血清中直接涂片,固定,染色,镜检。每鼠计数1000个嗜多染红细胞的微核细胞数,计算微核发生率,结果用SPSS10.0统计软件中泊松分布u检验进行统计学分析。结果样品各剂量组的细胞微核发生率与阴性对照比较均无统计意义(P>0.05),阳性对照组微核发生率明显高于对照组,有统计意义(P<0.001),见表2。
表1 六堡茶提取物对各菌株回变菌落数的影响(±SD)
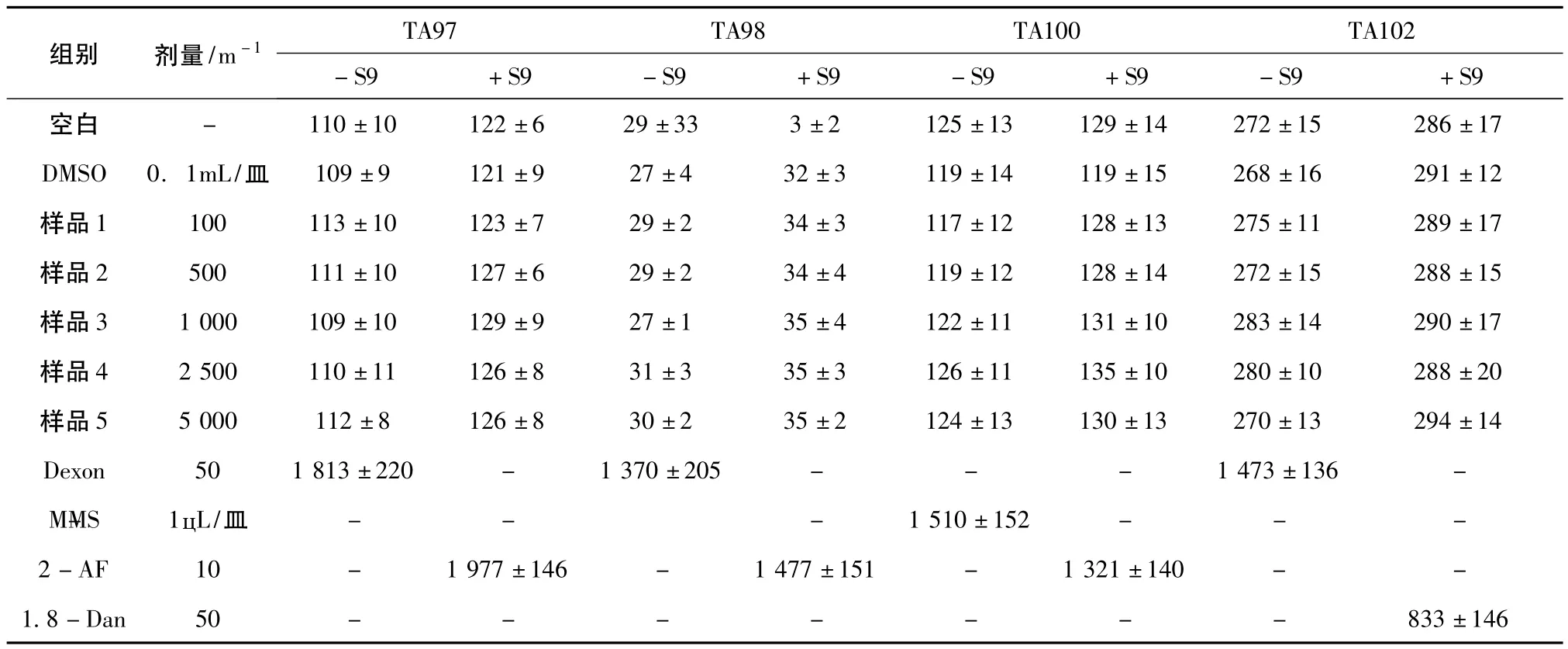
表1 六堡茶提取物对各菌株回变菌落数的影响(±SD)
组别剂量/m-1TA97TA98TA100TA102 86±17 DMSO0.1mL/皿109±9121±927±432±3119±14119±15268±16291±12样品1100113±10123±729±234±3117±12128±13275±11289±17样品2500111±10127±629±234±4119±12128±14272±15288±15样品31 000109±10129±927±135±4122±11131±10283±14290±17样品42 500110±11126±831±335±3126±11135±10280±10288±20样品55 000112±8126±830±235±2124±13130±13270±13294±14 Dexon501 813±220-1 370±205---1 473±136-MMS1цL/皿---1 510±152----S9+S9-S9+S9-S9+S9-S9+S9空白-110±10122±629±333±2125±13129±14272±152-2-AF10-1 977±146-1 477±151-1 321±140--1.8-Dan50-------833±146
2.3 小鼠精子畸形试验将30只小鼠随机分为样品3个计量组(49.6、24.8、12.4g药材/kg体质量)、阴性对照组、阳性对昭组(环磷酰胺40mg/kg体质量,ip),每组5只,各组动物每天灌胃一次,每次0.2mL/10g体质量,连续5d。首次给受试物后的第35 d处死动物,取双侧附睾放入生理盐水中纵向切1~2刀,过滤,吸滤液涂片、固定、2%伊红染色制片。每鼠镜检1 000个精子,计数精子畸形数及畸形类型,计算畸形率。结果用SPSS10.0统计软件中秩和检验统计分析。
结果样品各剂量组与阳性对照组的精子畸形率比较均无统计意义(P>0.05)。阳性对照组精子畸形数明显高于阴性阴对照组,有统计意义(P<0.01),见表3。
表2 六堡茶提取物对小鼠骨髓嗜多染红细胞微核发生率的影响(±SD)
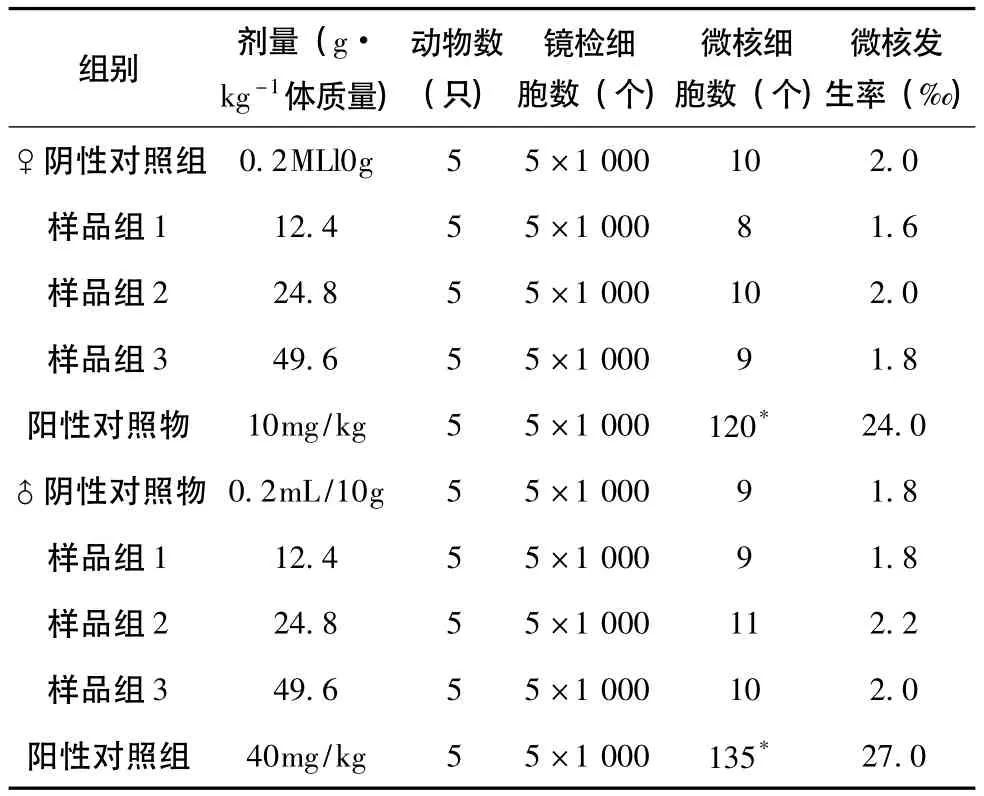
表2 六堡茶提取物对小鼠骨髓嗜多染红细胞微核发生率的影响(±SD)
注:*与阴性对照组比较,P<0.01。
组别剂量(g·kg-1体质量)动物数(只)镜检细胞数(个)微核细胞数(个)微核发生率(‰)0.2MLl0g55×1 000102.0样品组112.455×1 00081.6样品组224.855×1 000102.0样品组349.655×1 00091.8阳性对照物10mg/kg55×1 000120*24.0♂阴性对照物0.2mL/10g55×1 00091.8样品组112.455×1 00091.8样品组224.855×1 000112.2样品组349.655×1 000102.0阳性对照组40mg/kg55×1 000135*♀阴性对照组27.0
3 结论
六堡茶提取物经Ames试验、小鼠微核试验和精子畸形试验结果均为阴性,对所试菌株、小鼠体细胞与雄性生殖细胞无诱变性[1,2]。
研究表明六堡茶安全性好,无遗传毒性。
表3 六堡茶提取物小鼠精子畸形试验结果(±SD)
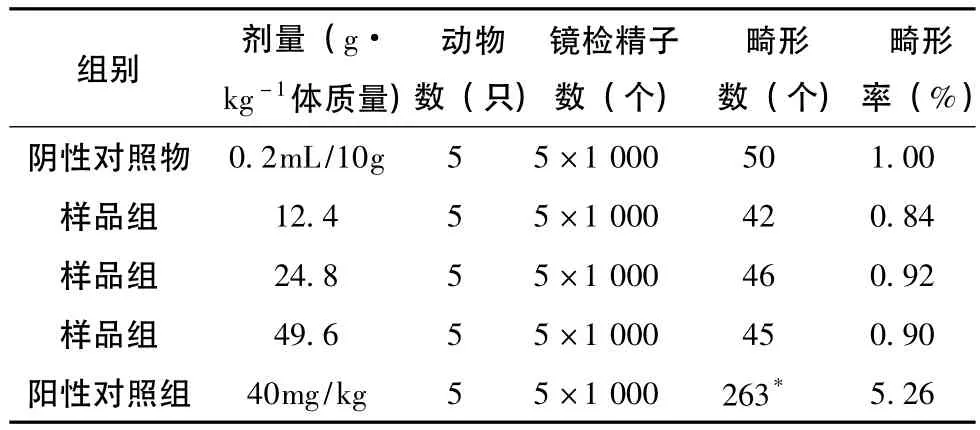
表3 六堡茶提取物小鼠精子畸形试验结果(±SD)
注:*与阴性对照组比较,P<0.01。
组别剂量(g·kg-1体质量)动物数(只)镜检精子数(个)畸形数(个)畸形率(%)0.2mL/10g55×1 000501.00样品组12.455×1 000420.84样品组24.855×1 000460.92样品组49.655×1 000450.90阳性对照组40mg/kg55×1 000263*阴性对照物5.26
[1]中华人民共和国卫生部,食品安全性毒学评价程序和方法[S].北京:卫生部,1994:14-47.
[2]李寿祺.卫生毒理基本原理和方法[M].成都:四川科学出版社,1987:174-175.
[3]庞广昌.生物活性肽的研究进展理论基础与展望[J].食品科学,2001,22(22):80-84.
R965.3
A
1007-8517(2012)21-0055-02
2012.09.27)

