电解质六氟磷酸锂制备进展及难点分析*
张建刚,王 瑶
(贵州省化工研究院,贵州贵阳 550002)
电池材料
电解质六氟磷酸锂制备进展及难点分析*
张建刚,王 瑶
(贵州省化工研究院,贵州贵阳 550002)
六氟磷酸锂(LiPF6)是目前锂离子二次电池中使用最广泛的电解质,纯度要求高,制备难度大。综述了六氟磷酸锂的制备方法,包括气-固法、溶剂法和离子交换法。认为以醚类或酯类作为合成溶剂的方法具有腐蚀小、毒性小、分离提纯简便等优点,可能是今后最有发展前景的生产工艺;同时对制备过程中的难点进行了简要分析。
六氟磷酸锂;制备;纯度;合成效率
近十几年,随着手机、DV、数码相机、笔记本、平板电脑等数码产品的日渐普及,锂离子二次电池的需求量每年都在快速增长,锂离子电池所需的电解质材料消耗量也在快速增加。未来几年,随着电动汽车产业的发展,市场对锂离子电池电解质材料的需求更将成倍提高。由于六氟磷酸锂有机溶液具有良好的导电性和电化学稳定性、能在电极上形成适当的SEI膜以及有较宽广的电化学稳定窗口等优点而成为使用最普遍的电解质锂盐,目前锂离子二次电池基本上都是使用六氟磷酸锂作为电解质。然而,目前六氟磷酸锂产品主要由日本SUTERAKEMIFA、关东电化学工业和森田化学等公司生产,中国自主生产的产品规模和品质都有待提高。笔者就目前六氟磷酸锂的合成方法以及制备难点进行简要综述,以期对六氟磷酸锂的生产有所帮助。
六氟磷酸锂的制备按反应机理可以分为氟化物合成和离子交换两大类。六氟磷酸锂的生成焓为-2 296 kJ/mol±3 kJ/mol(298.15 K)[1],以五氟化磷气体和氟化锂为原料合成六氟磷酸锂反应易于发生,按氟化锂的使用状态可分为气-固法和溶剂法。
1 气-固反应法
五氟化磷气体能与固体氟化锂直接反应生成六氟磷酸锂:
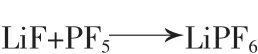
1950年美国氟科学家J.H.Simmons[2]用PF5气体与LiF在镍制容器中在高温高压条件下直接反应制得六氟磷酸锂。该反应为气-固反应,生成的六氟磷酸锂将LiF固体颗粒完全包覆,从而阻止了反应的进一步进行。因而该法所得六氟磷酸锂产品纯度低、产率较低,难以实现大规模生产。为了提高产品纯度和产率,胡启明等[3]将五氟化磷与高纯纳米LiF在气体保护(无氧)、温度为100~150℃、压力为1.0~2.0 MPa条件下反应4~15 h制得纯度大于99.9%的六氟磷酸锂。王德贵等[4]通过制备多孔LiF来提高其与PF5等气体反应的产率,首先将无水氟化氢与LiF反应生成LiHF2,然后升温至160~250℃并抽真空使LiHF2脱掉HF得到多孔状LiF,之后降温至80~100℃后通入PF5制得六氟磷酸锂,使其纯度得以提高。
2 溶剂法
2.1 无机溶剂法
2.1.1 HF溶剂法
HF是一种优良的溶剂,对LiF的溶解性较好。将氟化锂溶于无水HF后通入PF5反应制备六氟磷酸锂的工艺是目前较为成熟的工艺。1960年,R.D. W.Kmmitt等[5]使用不锈钢容器,将LiF溶于无水HF中,于25℃条件下通入PF5,反应维持12 h后挥发除去HF,获得六氟磷酸锂晶体。由于PF5气体较为昂贵,研究者采用PCl5为原料制备六氟磷酸锂。这种方法也是将LiF溶于无水HF中,温度控制在-80~19℃,然后缓慢加入PCl5,反应制得六氟磷酸锂与HCl。但是该法制备的六氟磷酸锂产品容易夹杂氯化物而影响产品品质,并且反应较为剧烈,优选在干冰熔点-78.5℃下进行[6]。
2.1.2 SO2溶剂法
Joubert等[7]采用配备4个阀门的316 L不锈钢容器作为反应器,在含水量低于1×10-5(体积分数)的干燥手套箱中将经过氮气干燥的LiF放入反应器中,之后将反应器取出,先后注入液体SO2和PF5气体,在-10~10℃条件下反应数小时后逐渐升温至30℃,让SO2与PF5充分挥发后得到六氟磷酸锂产品。合成时PF5和LiF物质的量比≥1.05。这种方法虽然避免了HF的使用,且产品中HF含量很低,但是六氟磷酸锂产品中SO2含量较高,需要进一步提纯才能使用。
2.2 有机溶剂法
2.2.1 醚类与酯类溶剂
低链烷基醚或低烷基酯可以作为合成六氟磷酸锂的溶剂使用。低链烷基醚分子式为ROR′,R和R′分别为含有1~4个碳原子的烷基;低烷基酯分子式为RCOOR′,R为H原子或含1~4个碳原子的烷基,R′为含1~4个碳原子的烷基。低烷基醚类包括甲醚、乙醚、甲乙醚等;低烷基酯包括EC(碳酸乙烯酯)、DEC(碳酸二乙酯)和DMC(碳酸二甲酯)等。由于六氟磷酸锂可溶解于低链烷基醚或低烷基酯中,并且对设备和电池材料腐蚀小,因而可能是较有开发价值的工艺方法。由于LiF不溶于醚类和酯类溶剂中,一般先将LiF粉碎至粒度小于150 μm,再加入到溶剂中形成悬浊液。Smith等[8]将PF5以气体形式通入,与悬浮在溶剂中的LiF反应并在其表面生成六氟磷酸锂,在保证溶剂不被PF5饱和的情况下,生成的六氟磷酸锂就能溶解在溶剂中,使LiF与PF5进一步反应。
醚类作溶剂制备工艺的难点在于,六氟磷酸锂在醚溶剂中结晶分离析出难度大,六氟磷酸锂与醚溶剂形成配合物溶解于溶剂中。单用乙醚作溶剂时六氟磷酸锂冷却结晶分离比较困难,而用多醚作溶剂又是以配合物的形式结晶分离出来,将结晶配合物中的多醚配体除去是一个难点[9]。
EC、DEC和DMC等低烷基酯类是锂离子电池常用的电解质溶剂,对六氟磷酸锂有很好的溶解性能。与使用醚类作溶剂相似,将LiF悬浮于酯类溶剂中,然后通入PF5反应也可制备六氟磷酸锂。而且反应生成的六氟磷酸锂溶于溶剂中即得到用于锂电池的电解液,反应中过量PF5可用惰性气体驱除。这种方法制备六氟磷酸锂具有反应易于控制、产率高的优点。但在制备过程中PF5易与有机溶剂发生反应导致溶剂颜色加深、杂质增加。同时该法主要用于制备电解液,目前还难以分离得到六氟磷酸锂晶体[9]。
2.2.2 乙腈溶剂
将LiF悬浮于乙腈中,通入PF5反应制得的六氟磷酸锂也能溶于乙腈中形成Li(CH3CN)4PF6络合物。通过减压蒸馏除去乙腈,可制得纯度高、比表面积大的六氟磷酸锂产品。滕祥国等[10]将LiF加入到无水CH3CN中,以甘油作液封剂使反应体系隔绝空气,在0℃的冰水浴下通入PF5气体,反应1~24 h,反应完全后加热至60℃后过滤,滤液在0~5℃下真空抽滤,滤饼经24 h干燥得到白色粉末状六氟磷酸锂。乙腈对设备腐蚀非常小,因此其作为溶剂制备六氟磷酸锂也是很有发展前景的方法。但是乙腈也存在毒性,对操作者和环境都可能存在不利影响。
3 离子交换法
由于六氟磷酸根的钠、钾、铵以及有机胺盐性质较为稳定,易于制得高纯度物质,因而可以采用这些高纯物质为原料使它们的阳离子与稳定锂盐中的锂离子发生离子交换而制备六氟磷酸锂。Salmon等[11]在NH3存在下,将锂盐(氯化锂、溴化锂、高氯酸锂、硝酸锂或者醋酸锂等)与 NaPF6、KPF6、NH4PF6或R4NPF6(R为含有1~4个碳原子的烷基)等在溶剂中发生交换反应制得六氟磷酸锂。使用的溶剂为乙腈、DEC和DMC等低沸点溶剂,便于在反应结束后加入较高沸点的溶剂将其除去。但是该法反应效率低,反应时间长,难以满足工业化生产的需要。Willmann等[12]采用六氟磷酸(HPF6)作为反应物制备六氟磷酸锂。该法将商品HPF6溶于吡啶中得到配合物C6H5NHPF6,然后将氢氧化锂(LiOH)加入到溶液中反应生成Li(C6H5N)PF6,之后真空分解得到六氟磷酸锂产品。该工艺对原料和反应环境的水分要求不高,但HPF6和LiOH价格昂贵。此外吡啶的沸点为115℃,真空分解Li(C6H5N)PF6时也易使六氟磷酸锂发生分解,从而使产品杂质含量偏高[9]。
4 六氟磷酸锂制备难点分析
4.1 纯度控制
作为锂离子二次电池用六氟磷酸锂产品纯度应大于99.9%,残余HF质量分数≤0.015 0%,水分质量分数≤0.002 0%[13]。要制备如此高纯度的产品,首先需要对原料进行提纯和干燥。通常采用氟气干燥HF,去除其中微量水[14]。反应式为:
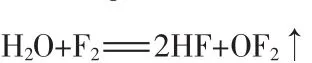
也可以采用电解法去除液体HF中的水分,即以不锈钢板作为阴极,镍板作为阳极,在电压低于7 V的条件下电解水成为H2和OF2气体除去[15]。
其次,设备的材质需要耐腐蚀或者经过耐腐蚀处理。对于以HF作为溶剂的生产设备,需要使用聚四氟乙烯、蒙乃尔合金等耐HF腐蚀的材料,或者在金属上衬四氟或涂覆四氟涂料获得耐蚀效果。闫春生等[16]在不锈钢反应器内壁涂覆厚度为10~20 μm的聚四氟乙烯涂层,使用1个月后六氟磷酸锂产品中的金属离子质量分数仍小于2×10-6,而未涂覆四氟涂层的设备使用同样时间后产品中金属离子质量分数达到(5~10)×10-6。
再次,生产管线需要全封闭,充入惰性气体保护,避免空气和水分进入。
最后,获得的产品通常需要经过真空干燥去除其中的溶剂。对于残存在六氟磷酸锂产品中的LiF,可在六氟磷酸锂干燥过程中加入PF5与之反应去除。宁延生等[17]在干燥六氟磷酸锂过程中,通入PF5和HCl混合气体,使PF5与六氟磷酸锂中夹带的LiF及氟氧磷锂LiPOxFy反应,使之转化为六氟磷酸锂。通过这些方法控制方能得到纯度较高的六氟磷酸锂产品。
4.2 合成效率
由于气-固法效率低,制得的六氟磷酸锂纯度低,而离子交换法成本过高,难以实现工业化,因而溶剂法是最易于实现工业化的生产方法。溶剂法使用PF5气体与溶于HF中的LiF或者悬浮于溶剂中的LiF反应,气液两相混合的效率对反应速率、原料利用率及转化率的影响较为显著。由于PF5制备困难因而价格较高,PF5的利用率决定着生产六氟磷酸锂的成本高低。
P·邦尼特等[18]提出将五氟化磷气体或五氟化磷与HCl的气态混合物与氟化锂的氟化氢溶液在吸收塔中进行接触反应。该法气液接触充分,反应效率高,但是存在所需设备体积较大、投资较大的问题。韩保国等[19]将五氟化磷气体与氟化锂的HF溶液通过管式反应器实现气液混合反应。为了提高混合反应效果,将管式反应器设计为较长的弯曲管道,通过延长气液混合时间和路径来提高原料利用率。袁祥云[20]采用微孔曝气的方法提高气液混合效率。将气态五氟化磷通入超微气泡发生装置中,产生直径为0.1~2 000 μm的微气泡,与事先溶于无水氟化氢的氟化锂反应。这种通过微孔曝气的方法减小了PF5气泡的直径,增大了气液接触表面积,能够显著提高气液混合效率。为提高未反应的五氟化磷的利用率,皇甫根利等[21]将反应后未反应的五氟化磷气体通入到另一盛有氟化锂的无水氟化氢溶液中,继续反应得到六氟磷酸锂成品。这样通过增加反应设备来提高原料五氟化磷的利用率也是较为有效和简便的办法。
5 结论
综述了六氟磷酸锂的制备方法,包括气-固法、溶剂法和离子交换法。指出以无水HF作为溶剂的制备方法具有腐蚀性和毒性,对设备材质要求较高,对操作人员危害大,且产品中残存的HF对电池性能有影响;离子交换法成本较高,难以实现工业化;有机溶剂对设备腐蚀小,反应温和,应是未来发展的方向,由于乙腈有毒性,因而以醚类或酯类作为溶剂的方法将是最具发展前景的方法。纯度控制和提高合成效率是制备六氟磷酸锂技术的关键和难点。
[1]Gavritchey K S,Shamatava G A,Smagin A A.Calorimetric study of thermal decomposition of lithium hexafluorophosphate[J].J.Therm. Anal.Calorim.,,2003,73(1):71-83.
[2]Simmons J H.Practice of fluorine science in lithium hexafluorophosphate[J].Fluorine Chemistry,1950,22(1):164-166.
[3]中南大学.高纯六氟磷酸锂的制备方法:中国,101195481[P]. 2008-06-11.
[4]西北核技术研究所.一种含氟锂盐的气流式反应合成法:中国,1171368[P].1998-01-28.
[5]Kemmitt R D W,Russell D R,Sharp D W A.The structural chemistry of complex fluorides of general formula AIBVF6[J].J.Chem.Soc.,1963,8:4408-4413.
[6]Solvay Fluor und Derivate GmbH(Hanover,DE).Method of preparing LiPF6:US,5866093[P].1999-02-02.
[7]Atofina(Paris la Defense Cedex,FR).Method for making lithium hexafluorophosphate:US,6500399[P].2002-12-31.
[8]Foote Mineral Company(Exton,PA).Preparation of lithium hexafluorophosphate:US,3607020[P].1971-09-21.
[9]李凌云,张志业,陈欣.六氟磷酸锂的制备工艺新进展[J].化学工业与工程,2005,22(3):224-228.
[10]滕祥国,戴纪翠,马培华.锂离子二次电池电解质材料LiPF6的制备及表征[J].无机化学学报,2004,20(9):1109-1111.
[11]FMC Corporation(Philadelphia,PA).Preparation of lithium hexafluorophosphate solutions:US,5378445[P].1995-01-03.
[12]Centre National D'Etudes Spatiales(FR).Solvate of lithium hexafluorophosphate and pyridine,its preparation and preparation process for lithium hexafluorophosphate using said solvate:US, 5993767[P].1999-11-30.
[13]HG/T 4066~4067—2008 六氟磷酸锂和六氟磷酸锂电解液[S].
[14]蔚山化学株式会社.六氟磷酸锂的制备方法:中国,1263047[P]. 2000-08-16.
[15]郭爱红,毕成良,丁飞,等.电解法去除氟化氢中微量水[J].南开大学学报:自然科学版,2005,38(5):62-64.
[16]多氟多化工股份有限公司.一种合成六氟磷酸锂的装置:中国,201634427U[P].2010-11-17.
[17]天津化工研究设计院.六氟磷酸锂的纯化方法:中国,1850593[P].2006-10-25.
[18]Elf Atochem S A.Process for manufacture of lithium hexafluorophosphate:US,5935541[P].1999-08-10.
[19]洛阳森蓝化工材料科技有限公司.六氟磷酸锂连续化制备工艺及装置:中国,101544361[P].2009-09-30.
[20]袁翔云.六氟磷酸锂非水溶剂法的合成工艺:中国,101423207[P].2009-05-06.
[21]多氟多化工股份有限公司.一种制备六氟磷酸锂的方法:中国,101570328[P].2009-11-04.
Progress in preparation of lithium hexafluorophosphate electrolyte and analysis on difficulties thereof
Zhang Jiangang,Wang Yao
(Guizhou Research Institute of Chemical Industry,Guiyang 550002,China)
Lithium hexafluorophosphate(LiPF6)is a kind of electrolyte that is widely used in secondary lithium ion battery. But the preparation is very difficult because of the requirement of high purity.Present preparation methods,such as gas-solid method,solvent method,and ion exchange method,of lithium hexafluorophosphate were summarized.It was believed that the method using ether or ester as synthesis solvent will be the most promising technology in the future due to its advantages of little corrosion,low toxicity,and easy separation and purification operation etc..Meanwhile,the difficulties of preparation were also analyzed.
lithium hexafluorophosphate;preparation;purity;synthetic efficiency
TQ131.11
A
1006-4990(2012)06-0057-04
贵州省优秀科技教育人才省长专项资金项目[黔省专合字(2010)60号];贵州省科学技术基金项目(黔科合J字[2011]2021号)。
2012-02-09
张建刚(1977— ),男,工学博士,高级工程师,主要研究方向为磷氟精细化工产品研发,已发表论文6篇。
联系方式:zhangjg009@126.com

