南瓜皮提取物的体外抑菌活性
张 忠,郑小义,毕 阳,王 义,徐 建
(甘肃农业大学食品科学与工程学院,甘肃兰州730070)
南瓜皮提取物的体外抑菌活性
张 忠,郑小义,毕 阳*,王 义,徐 建
(甘肃农业大学食品科学与工程学院,甘肃兰州730070)
为了揭示南瓜较长贮存期与其皮部活性物质功能之间的关系,通过使用石油醚、乙酸乙酯、丙酮、甲醇、水5种不同极性强度的溶剂对南瓜皮进行连续梯度提取,采用孢子萌发抑制法、琼脂孔扩散法和对倍稀释法测定了不同提取物对5种真菌:扩展青霉(Penicillium expansum)、尖孢镰刀菌(Fusarium oxysporum)、黑根霉(Rhizopus stolonifer)、互格交链孢(Alternaria alternate)和粉红单端孢(Trichothecium roseum)和5种细菌:枯草芽孢杆菌(Bacillus subtilis)、大肠杆菌(Escherichia coli)、金黄葡萄球菌(Staphylicoccus aureus)、荧光假单孢杆菌(Pseudomonas fluorescence)和乳酸菌(Lactobacillus plantarum)的抑菌活性和最低抑菌浓度;并用扫描电镜观察了水提取物对菌体形态的影响。结果表明:除石油醚提取物外,四种提取物对供试菌有不同程度的抑制活性,其中水提取物的抑菌活性最强,水提取物处理使菌体外表形态发生明显的伤害性变化。初步说明南瓜皮中的预存抗菌物质是有助于南瓜较长贮存期的一个因素。
南瓜,外果皮提取物,抑菌活性,琼脂孔扩散法,最低抑菌浓度
南瓜是我国主要的经济作物之一,种植面积大、品种多、总产量约占世界总产量的1/3左右[1]。南瓜果实保藏期较长,表面完好的可保存半年以上,但表皮受损后保藏期则大大缩短[2]。尽管南瓜的诸多营养保健功能早己为人们所熟知,但有关南瓜中天然抗菌活性成分的报道不多。南瓜的长贮存性长期以来被认为与其外表皮的高度木质化和其内的天然抗菌物质有关,并分离出一个与木质素代谢密切关联的抗菌物质反式香豆醛[3]。Wang等发现南瓜籽中存在一种富含精氨酸,谷氨酰胺和甘氨酸的抗菌肽[4]。Alice等的研究对南瓜籽中抗菌蛋白质进行了纯化[5],江英等对南瓜果肉的抗菌性进行了研究[6]。Park等从黄皮南瓜皮中分离到一种分子量为14ku的抗菌蛋白,该蛋白对Botrytis cinerea,Colletotrichum coccodes等5种真菌病原菌在体外具有抑制活性[7]。但是对我国主产的绿皮南瓜大磨盘的各种皮提取物和对一些果蔬腐败菌的抗性的研究未见报道。本研究采用4种有机溶剂和水对南瓜皮活性物质进行提取和分离,测定各种提取物对5种采后真菌以及5种腐败细菌在体外条件下的抑制效果,并通过扫描电镜观察有效提取物处理对部分供试菌形态结构方面的影响,为南瓜的长贮存期和皮部活性物质的抗菌作用提供部分科学依据。
1 材料与方法
1.1 实验材料
供试南瓜 品种:大磨盘,采自甘肃省民勤县收成乡露天大田,网袋包装后运抵本校实验室,于室温(20±5)℃下贮藏待用;扩展青霉菌(Penicillium expansum)、尖孢镰刀菌(Fusarium oxysporum)、黑根霉(Rhizopus stolonifer)、枯草芽孢杆菌(Bacillus subtilis)、大肠杆菌(Escherichia coli)CICC10032、金黄葡萄球菌(Staphylicoccus aureus)CMCC26003、荧光假单孢杆菌(Pseudomonas fluorescence)AS10235、乳酸菌(Lactobacillus plantarum) 由广东微生物研究所购得并在本院采后生物学实验室保藏;互格交链孢(Alternaria alternate)和粉红单端孢(Trichothecium roseum) 由本院采后生物学实验室从发病果实分离保藏。
1.2 实验方法
1.2.1 样品处理 参照董周永[8]方法并修改。先将南瓜用自来水冲洗干净,自然晾干后取1~5mm厚的果皮及皮下组织,在-70℃,0.08MPa条件下(Clean V2C8真空冻干机)冻干48h后用粉碎机粉碎,过40目筛,用PE袋(17cm×12cm)包装,于0℃冰箱中贮藏待用。
1.2.2 提取物制备 参照冯俊涛[9]的方法并修改。取低温储存的南瓜皮粉100g放入到500mL的具塞三角瓶中,采用石油醚、乙酸乙酯、丙酮、甲醇、纯水5种提取液3倍量体积从低极性到高极性的逐级提取的方法。用锡箔纸封住瓶口,置于30℃,120r/min的摇床上振荡浸提,每3h过滤,滤渣用相同溶剂重复提取4次,合并相同溶剂提取液。减压浓缩后用原溶剂定容至100mL,得到5种质量浓度为1g/mL的提取液,并分别根据提取溶剂标记为PE,EE,AE,ME和WE。
1.2.3 菌体细胞悬浮液的配制 参照Bi[10]的方法。取25℃下培养10d的带菌PDA平皿一个,加入含0.5%(v/v)Tween20的无菌水约10mL,用玻璃棒刮下平板上的病原菌孢子,然后转入50mL三角瓶中,在WYX-A微型旋涡混合器上振荡15s,再用双层纱布过滤,滤液用血球计数板计数算出孢子悬浮液的浓度,最后稀释至所需浓度1×106CFU/mL。细菌菌悬液的制备采用平板菌落计数法[11],菌体浓度为5× 106CFU/mL。
1.2.4 真菌孢子萌发率测定 参照潘金菊[12]的方法并修改。将4个直径1cm的琼脂块放在同一灭菌载玻片上。在每个琼脂块表面加入10μL的供试孢子悬浮液,其中两个再添加10μL含2%(v/v)二甲亚砜的南瓜皮提取液,另外两个分别添加10μL含2% (v/v)二甲亚砜的相应提取溶剂作对照,将载玻片置于饱和湿度的平皿中,在28℃下培养1h后开始进行显微观察并用计数器记数,每隔1h计数1次,实验重复三次,计算萌发率。
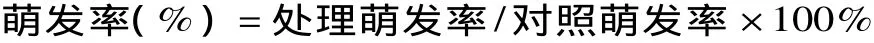
1.2.5 琼脂孔扩散法抑菌活性测定 参照 Cakir[13]的方法并修改。在无菌条件下,将高压灭菌的琼脂培养基(细菌用牛肉膏蛋白胨培养基,真菌用PDA培养基)趁液态倒入干燥灭菌的直径9cm培养皿内,厚度约为4mm,待培养基冷凝后,加入0.1mL菌悬液并均匀涂布平板,然后用无菌金属打孔器(d=6mm)在培养基中心打小孔1个,用无菌牙签除去孔内琼脂,并用移液枪吸取一滴液体琼脂封底。分别吸取不同的南瓜皮提取物0.2mL加入孔内,并用各自的提取溶剂作空白对照。然后将培养皿置于恒温培养箱中培养(细菌于37℃培养18~24h,真菌于28℃培养48~96h)。后用十字交叉法测量有效抑菌圈直径(简称抑菌圈直径),实验重复三次。

1.2.6 最低抑菌浓度(MIC)的测定 参照杨华明[14]的方法。取8支无菌小试管,于第1~8管中各加入培养基(细菌用牛肉膏蛋白胨液体培养基,霉菌用PDA液体培养基)1mL。取南瓜皮不同提取液1mL加入第1管中,混匀后取1mL加入第2管,依次倍比稀释,自第7管吸去1mL弃去,第8管作为空白对照。然后在各管中加入事先制备好的菌悬液20μL,混匀后置于恒温培养箱中培养(细菌置于37℃恒温培养箱中培养18~24h,霉菌置于28℃的恒温培养箱中培养48~96h)。观察试管澄清度,若液体培养基混浊,表示菌体生长,若液体培养基完全清亮,表示无菌体生长。无菌体生长的最小浓度即为最小抑菌浓度。实验重复三次。
1.2.7 水提取物对A.alternata和P.fluorescence菌体形态的研究 为了研究南瓜皮抑菌活性物质作用于供试菌后其菌体表面形态的变化情况,选择抑菌效果最好的提取物,扫描电镜观察在相应最低抑菌浓度处理后其对最为敏感的真菌 A.alternata和细菌P.fluorescence的菌体形态的影响。
参照高向阳[15]的方法。取处理的菌丝及对照菌丝若干,在4℃冰箱中用2%(v/v)戊二醛固定2h,磷酸缓冲溶液洗3次,每次10min;再浸泡于1%(v/v)的锇酸溶液中,4℃下放置2h左右;用50%、70%、95%、100%(v/v)的系列乙醇各脱水10min。醋酸异戊酯置换20min。以上各步骤均在4℃下进行,临界点干燥,真空镀金。扫描电镜观察并采集照片。
1.2.8 数据处理 用Origin8.0处理数据计算标准偏差并作图。
2 结果与分析
2.1 不同提取物对真菌孢子萌发率的影响
处理后第6h各真菌孢子的萌发率(图1)表现出了明显的差异。南瓜皮水提取物处理使真菌孢子萌发率整体上降低最明显,其中 F.oxysporum 和A.alternate仅萌发1/3左右。石油醚提取物对孢子萌发影响最小。A.alternata对水提取物最为敏感,而在丙酮提取物和石油醚提取物的处理下孢子萌发率最高。R.stolonifer对各种提取物的敏感程度最低,仅水提取物处理下萌发率为56%,其余各处理下萌发率均高于89.7%。说明水提取物整体上对抑制孢子萌发最有效,而A.alternate和F.oxysporum对各提取物整体上最敏感。
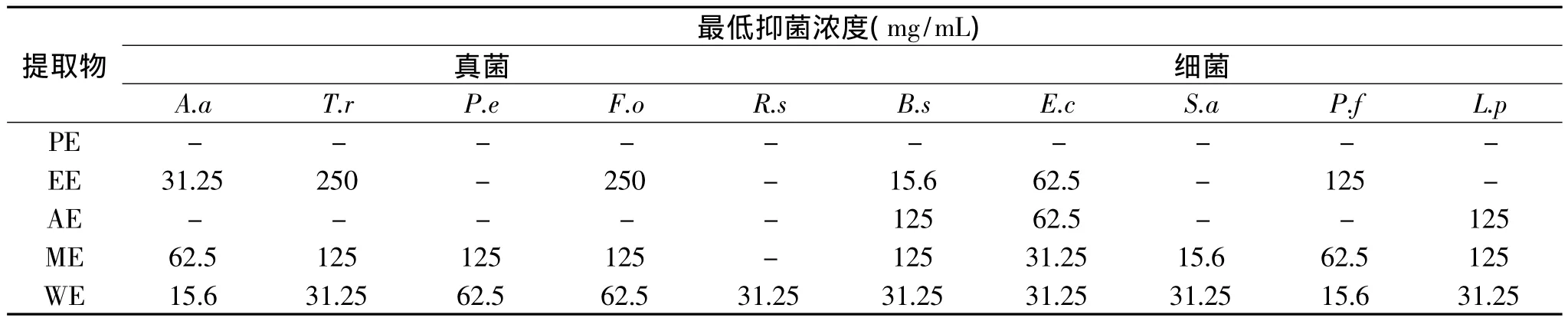
表1 不同提取物对供试菌的最低抑菌浓度Table 1 Minimum inhibitory concentrations of various extracts to bioassay microbes
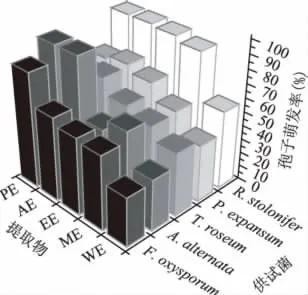
图1 不同提取物对真菌孢子萌发率的影响Fig.1 Effect of various extracts on the germination ratio of bioassay fungi
2.2 不同提取物对供试真菌的抑菌效果
从处理后培养96h时各提取物对不同真菌的抑菌圈看(图2),南瓜皮水提取物在抑制真菌菌落生长方面最有效,其次是甲醇提取物和乙酸乙酯提取物,但甲醇提取物能抑制四种菌的生长而乙酸乙酯提取物仅抑制三种菌的生长。水提取物对A.alternata的抑菌圈直径达4.27cm,对F.oxysporum的抑菌圈直径也达3.85cm。另外水提取物对其它三种真菌的抑菌圈也达到或超过3.35cm。甲醇提取物和乙酸乙酯提取物对有效菌的抑菌圈直径都超过1.3cm。石油醚提取物和丙酮提取物对供试真菌的菌落生长无抑制效果。
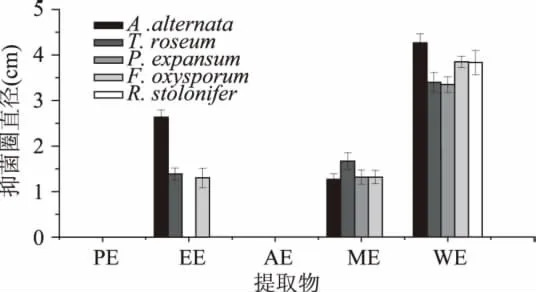
图2 各提取物对不同真菌的抑菌圈直径Fig.2 Inhibition zone diameter of various extracts to bioassay fungi
2.3 不同提取物对供试细菌的抑菌效果
不同提取物处理供试细菌后培养48h的抑菌圈直径的大小(图3)表明,除石油醚提取物外,其余每种南瓜皮提取物至少对两种以上的细菌菌落生长有抑制效果。其中水提取物的抑制效果整体上最为明显且能抑制五种供试菌,该提取物对S.aureus的抑菌圈达3.33cm;对其它四种细菌的抑菌圈直径也都在2.52cm以上。甲醇提取物对细菌的抑制活性次之,它对S.aureus的抑菌圈直径达2.87cm,对其余三种菌的抑菌圈直径也在1.33cm以上。乙酸乙酯提取物和丙酮提取物抑制细菌生长的活性也较强,对有效菌的抑菌圈直径都在1.22cm以上。
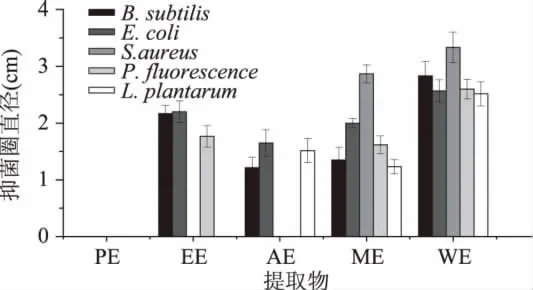
图3 各提取物对不同细菌的抑菌圈直径Fig.3 Inhibition zone diameter of various extracts to bioassay bacteria
2.4 不同提取物对供试菌的最低抑菌浓度
最低抑菌浓度(MIC)定量地表示了抑菌物质抑菌活性的强弱。南瓜皮各种提取物对供试菌的MIC值(表1)中水提取物对各种菌的MIC普遍较低,对A.alternata和P.fluorescence的MIC为15.6mg/mL。除对P.expansum和F.oxysporum的MIC为62.5mg/mL外,对其余菌的MIC均为31.25mg/mL。甲醇提取物对S.aureus的MIC和乙酸乙酯提取物对B.subtilis的MIC都为15.6mg/mL。从MIC值可知水提取物整体上对各种菌的抑制活性最强。
2.5 水提取物对A.alternata和P.fluorescence形态结构的影响
2.5.1 水提取物对A.alternata形态结构的影响 南瓜皮水提取物最低抑菌浓度处理A.alternata后菌丝的表面形态发生了明显的伤害性变化(图4)。扫描电镜观察到对照(C1和C2)的菌丝呈规则的线形结构;分生头部发育良好,光滑壁厚,基部较健壮;菌丝串规则,局部形态呈线形。而且菌丝直径稳定,基本为单列,均一,表面光滑的健壮菌丝。相比较处理(T1和T2)后的菌丝分生头部发生明显的变形,表面粗糙畸形、出现凸状小点。另外分生头部也观察到一些明显的破裂和完整性的缺失。大部分菌丝的线形形态被破坏,外形皱曲萎缩,粗细不均,菌丝串混乱无序,集结消退。菌丝萌发较少,发生了明显的畸形,局部不规则膨胀。出现了较多的扁平空菌丝和崩溃菌丝。处理后菌丝形态的微观特征变化与整体菌落边缘近药物端的宏观形态的特征是一致的。
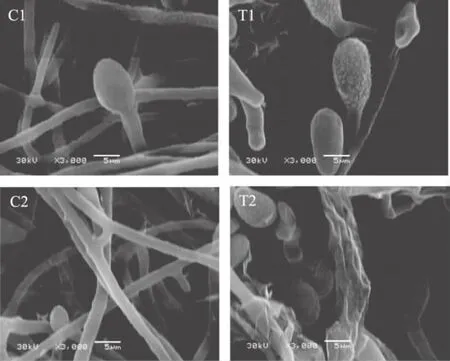
图4 扫描电镜观察南瓜皮水提取物最低抑菌浓度处理后的A.alternata菌丝形态(T1和T2)与对照(C1和C2)Fig.4 Morphological comparison under scan electron microscope of A.alternate hyphae treated with WE at MIC (T1 and T2)and counterpart control(C1 and C2)
2.5.2 水提取液对P.fluorescence形态结构的影响南瓜皮水提取物处理后P.fluorescence菌体形态发生的伤害性变化(图5)。从扫描电镜观察到对照(C1和C2)的菌体细胞完整,表面光滑,菌体细长,呈均匀的节状。菌体之间有序束状排列,健壮茂密。而水提取物处理(T1和T2)后的菌体外在形态发生明显的伤害性变化,菌体的细胞完整性遭到很大破坏,出现较多的细胞碎片。细胞外壁粗糙,出现明显的变形和崩溃。菌体萎缩退化,排列混乱。处理后菌体的微观形态变化和处理后出现较大的抑菌圈的宏观生物学现象相一致。
3 讨论与结论
不同溶剂提取物对供试菌的生长抑制能力和抑菌谱不同。根据相似相容原理,可以初步判定各类提取物的极性特征。从较低极性的石油醚提取物到较高极性的水提取物,不同极性提取物表现出了不同的抑菌活性。低极性的石油醚提取物对各种供试菌都无抑制活性,而水提取物的抑菌活性最高,但是在本实验中,丙酮提取物的抑菌活性整体上也较低。从活性的极性分布范围来说,在本研究体系中,表现活性的并非单一的某种物质,这一点可从丙酮提取物对供试真菌没有抑制活性得到验证。在高极性的甲醇和水提取物中存在着一些黄酮类、固醇类、多酚和单宁[16]。而大多数被研究植物中,酚类和单宁类是主要的抗菌物质[17]。在水提取物中,酚类与大分子的蛋白质结合成复合体,作用于微生物表面的氧化还原酶系,抑制了微生物细胞表面的一些受体,进而抑制了微生物的生长[18]。南瓜皮部分提取物的抑菌圈大小与其相应的最低抑菌浓度未完全成对应关系,左国营[19]的研究也得到了类似的结论,这可能与提取物在不同介质中的分散性有关。
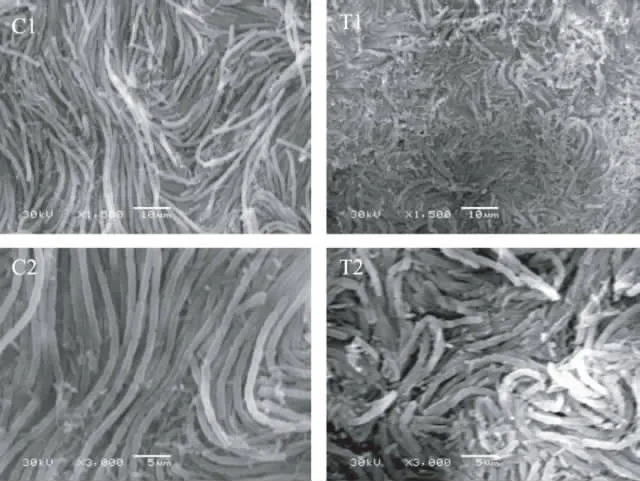
图5 扫描电镜观察南瓜皮水提取物最低抑菌浓度处理后的P.fluorescence菌体形态(T1和T2)与对照(C1和C2)Fig.5 Morphological comparison under scan electron microscope of P.fluorescence cells treated with WE at MIC(T1 and T2)and counterpart control(C1and C2)
真菌和细菌对各种提取物的敏感程度也表现出了相似性。两类菌都对石油醚提取物不敏感,其次是对丙酮提取物敏感性整体上也较差。供试细菌中,格兰氏阳性菌和阴性菌对提取物的敏感性没有表现出规律性,这也说明有效提取物可能是作用于菌的非细胞壁部位[20]。扫描电镜观察显示南瓜皮水提取物处理造成菌体形态特征发生许多伤害性的变化,这可能是菌体膜表面某些酶蛋白受到提取物活性分子的攻击而造成了连锁性的代谢紊乱有关[21]。
本研究表明南瓜皮乙酸乙酯,丙酮,甲醇和水提取物对P.expansum,F.oxysporum,R.stolonifer,T,roseum和 A.alternate 5 种 真 菌 与 E.coli,S.aureus,P.fluorescence,L.plantarum和B.subtilis 5种细菌的生长都有不同程度的抑制作用。其中水提取物对10种供试菌的抑制效果最好;甲醇提取物的抑制效果次之,对9种供试菌有抑制作用;依次是乙酸乙酯提取物,对6种菌有抑制作用;丙酮提取物,仅对3种供试细菌有抑制作用;石油醚提取物则对10种供试菌均无抑制作用。这些提取物中存在的活性抑菌分子可能与南瓜的长贮存期和抗病性有关。
[1]王洪伟.南瓜功能成分研究进展[J].食品与机械,2004 (4):55-57.
[2]江璐,何计国,范慧红.南瓜多糖的研究进展[J].食品与药品,2007(9):51-53.
[3]Richard R,Sims J J,Midland S L,et al.Isolation of a phytoalexin,trans-p-coumaryl aldehyde,from Cucurbita maxima,Cucurbitaceae[J].Phytochemistry,1999(1):41-43.
[4]Wang H X,Ng T B.Isolation of cucurmoschin,a novel antifungal peptide abundant in arginine,glutamate and glycine residues from black pumpkin seeds[J].Peptides,2003(7): 969-972.
[5]Alice G V,Gregory M N,Rosemary C,et al.Purification and mass spectrometry-assisted sequencing of basic antifungal proteins from seeds of pumpkin(Cucurbita maxima)[J].Plant Science,1998(2):141-162.
[6]江英,邓辉,杨艳彬.南瓜抑菌作用的研究[J].食品科技,2005(10):37-39.
[7]Park S C,Kim J Y,Lee J K,et al.Antifungal mechanism of a novel antifungal protein from pumpkin rinds against various fungal pathogens[J].Journal of Agricural and Food Chemistry,2009 (19):9299-9304.
[8]董周永,胡青霞,刘兴华.石榴果皮中抑菌活性物质提取工艺优化[J].农业工程学报,2008(3):274-277.
[9]冯俊涛,石勇强,张兴.56种植物抑菌活性筛选实验[J].西北农林科技大学学报:自然科学版,2001(2):65-68.
[10]Bi Y,Tian S P,Guo Y R,et al.Sodium silicate reduces postharvest decay on Hamimelons:Induced resistanceand fungistatic effects[J].Plant Disease,2006(3):279-283.
[11]沈萍,范秀容,李光武.微生物学实验[M].第三版.北京:高等教育出版社,1999.
[12]潘金菊,刘峰,慕卫.黄瓜炭疽病菌对杀菌剂敏感性的优化测定方法研究[J].农药科学与管理,2005(6):19-22.
[13]Cakir A,Kordali S,Zengin H,et al.Composition and antifungal activity of essential oils isolated from Hypericum hyssopifolium and hypericum heterophyllum[J].Flavour and Fragrance Journal,2004(9):62-68.
[14]杨华明,易滨.现代医院消毒学[M].北京:人民军医出版社,2002:316-317.
[15]高向阳,林碧润,姚汝华.新抗生素万隆霉素对黄瓜疫病菌抑菌形态学研究[J].华南农业大学学报,2004(4):27-29.
[16]Dougnari J H,Obidah J S.Antibacterial potentials of stem bark extracts of Leptadenia lancifolia against some pathogenic bacteria[J].Pharmacology Online,2008(3):172-180.
[17]Choi N H,Choi G J,Jang K S,et al.Antifungal activity of the methanol extract of Myristica malabarica fruit rinds and the active ingredients malabaricones against phytopathogenic fungi[J].Plant Pathology,2008(3):317-321.
[18]Cowan M M.Plant products as antimicrobial agents[J]. Clinical Microbiology Review,1999(4):564-572.
[19]左国营,韩峻,余巍.47种中草药提取物的体外抗菌活性筛选研究[J].中国药房,2005(10):798-799.
[20]Baidez A G,Gomez P,Delrio J A.Antifungal capacity of major phenolic compounds of Olea europaea L.against Phytophthora megasperma Drechsler and Cylindrocarpon destructans(Zinssm.)Scholten[J].Physiological and Molecular Plant Pathology,2006(4-6):224-229.
[21]Paulo L,Ferreira S,Gallardo E,et al.Antimicrobial activity and effects of resveratrol on human pathogenic bacteria[J].World Journal of Microbiology and Biotechnology,2010(8):1533-1538.
In vitro antimicrobial activity of extracts from autumn squash rind
ZHANG Zhong,ZHENG Xiao-yi,BI Yang*,WANG Yi,XU Jian
(College of Food Science and Engineering,Gansu Agricultural University,Lanzhou 730070,China)
To explore the possible relevance between the long safe storage period of autumn squash and the contribution of its rind bioactive substances,petroleum ether,ethyl acetate,acetone,methanol and water were used to conduct a subsequent polarity gradient extraction on autumn squash rind.The activity of various extracts and their minimum inhibitory concentrations(MIC)against five fungi(Penicillium expansum,Fusarium oxysporum,Rhizopus stolonifer,Alternaria alternate and Trichothecium roseum)and five bacteria(Bacillus subtilis,Escherichia coli,Staphylicoccus aureus,Pseudomonas fluorescence and Lactobacillus plantarum)were evaluated based on the methods of spore germination counting,agar well diffusion and double dilution.The modification on strain morphology ensuing the aqueous extract treatment at MIC was also investigated through electron scanning microscope.Results showed that all extracts but the one of petroleum ether displayed some inhibition capabilities on the growth of bioassay microbes and among them the strongest was the aqueous extract.Obvious detrimental alteration was observed on the cells or mycelium surface after aqueous extract treatment.Preliminary suggestion was that phytoalexin in the extracts from the rind was contributed to the long storage period of autumn squash.
autumn squash;rind extract;antimicrobial activity;agar well diffusion method;minimum inhibitory concentration(MIC)
TS255.1
A
1002-0306(2012)08-0128-05
2011-08-15 *通讯联系人
张忠(1977-),男,讲师,硕士,主要从事天然抗菌活性物质的研究。
国家自然科学基金面上项目(30671465)。

