改性壳聚糖脱除马氏珠母贝糖胺聚糖中镉的初步研究
衣美艳,范秀萍,吴红棉,胡雪琼
(广东海洋大学食品科技学院,广东湛江524025)
改性壳聚糖脱除马氏珠母贝糖胺聚糖中镉的初步研究
衣美艳,范秀萍*,吴红棉,胡雪琼
(广东海洋大学食品科技学院,广东湛江524025)
采用L-半胱氨酸改性壳聚糖对马氏珠母贝糖胺聚糖中的重金属镉离子进行脱除研究,通过单因素实验和正交实验探讨了pH、反应时间和改性壳聚糖的添加量对糖胺聚糖中镉离子的脱除率和糖胺聚糖(GAG)含量的影响,并且利用SPSS对正交实验的数据进行处理分析,结果表明:在马氏珠母贝酶解液中添加L-半胱氨酸改性壳聚糖吸附镉离子的最佳pH为6.0,时间为5h,添加量为0.6g/50mL,然后将酶解液经离心、醇沉得到的糖胺聚糖中镉离子的脱除率达到56.7%,GAG含量为42.8%。
L-半胱氨酸改性壳聚糖,SPSS,糖胺聚糖,镉脱除率
1 材料与方法
1.1 实验材料
马氏珠母贝全脏器 购自湛江东风市场,经去壳放冰箱冷冻备用;壳聚糖、L-半胱氨酸(BR)、阿利新蓝 均购自上海蓝季科技发展有限公司;其余试剂 均为分析纯。
1.2 实验方法
1.2.1 L-半胱氨酸改性壳聚糖的制备[15]壳聚糖与戊二醛反应,制得Schiff碱壳聚糖[16],再与环氧氯丙烷反应制得含Schiff碱的环氧醚类壳聚糖中间体[17];然后与L-半胱氨酸反应得到L-半胱氨酸Schiff碱壳聚糖;最后脱去戊二醛,制得带有羧基的多官能团不溶性的L-半胱氨酸改性壳聚糖[18]。
1.2.2 马氏珠母贝糖胺聚糖的制备[19]原料→解冻、匀浆→酶解(双酶水解)→灭酶→单层纱布粗滤→(滤液)脱色→双层纱布精滤→离心→上清液醇沉→离心、去上清液→洗涤→干燥→GAG粗品
1.2.3 糖胺聚糖粗品中镉的检测 参照GB/T 5009.15—1996《食品中镉的测定方法》[20],样品经湿法消化后,用火焰法原子吸收光谱法测定镉的含量。
1.2.4 糖胺聚糖粗品中GAG含量的测定 采用阿利新蓝比色法测定马氏珠母贝糖胺聚糖粗品中GAG的含量[2]。
1.2.5 镉脱除率与GAG含量的计算 计算公式如下:
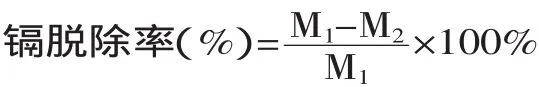
式中:M1:脱镉前GAG粗品中镉含量(mg/kg);M2:脱镉后GAG粗品中镉含量(mg/kg)。
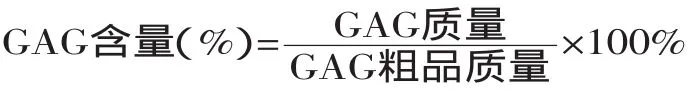
1.2.6 单因素实验
1.2.6.1 酶解液pH实验 量取50mL珠母贝酶解液,置于100mL锥形瓶中,分别调节酶解液的pH为5.0、6.0、7.0、8.0、9.0,加入改性壳聚糖0.5g,常温下搅拌5h,离心,上清液醇沉制得糖胺聚糖粗品,测定其中镉含量。3次重复。
1.2.6.2 脱除时间实验 量取50mL珠母贝酶解液,置于100mL锥形瓶中,调pH7.0,加入改性壳聚糖0.5g,常温下分别搅拌3、4、5、6、7h,离心,上清液醇沉制得糖胺聚糖粗品,测定其中镉含量。3次重复。
1.2.6.3 改性壳聚糖添加量实验 量取50mL珠母贝酶解液,置于100mL锥形瓶中,调pH7.0,分别加入L-半胱氨酸改性壳聚糖0.3、0.4、0.5、0.6、0.7g/50mL,常温下搅拌5h,离心,上清液醇沉制得糖胺聚糖粗品,测定其中镉含量。3次重复。
1.2.7 正交实验 根据单因素实验的结果,选择pH(A)、反应时间(B)和改性壳聚糖添加量(C)三因素,外加一空白项(D),进行有空白列的L9(34)的正交实验[21](见表1),并用SPSS对实验数据进行处理分析[22-24],考察改性壳聚糖对GAG粗品中镉的最佳脱除条件。

表1 正交实验因素水平表Table 1 Factors and levels of L9(34)experiment for synthesis of sodium cyclamate
2 结果与分析
2.1 GAG粗品中镉脱除条件的单因素实验结果
2.1.1 反应pH对GAG粗品中镉脱除率和GAG含量的影响 由图1可看出,L-半胱氨酸改性壳聚糖对糖胺聚糖的脱镉率在pH=5.0时最高,随着pH的增大,脱镉率呈显著降低趋势。这是因为,在酸性条件下改性壳聚糖分子结构中的羧基呈酸性,结构中活性基团活性增强[15],所以在酸性条件下脱镉率最大;而在碱性条件下,Cd2+会与-OH-形成Cd(OH)2沉淀而不利于吸附,故脱镉率降低。在pH为5.0和9.0之间GAG含量先增大后减小,在pH=7.0时达到最大值。说明过酸和过碱的条件都会明显影响GAG的含量。因此,综合考虑L-半胱氨酸改性壳聚糖最佳的吸附条件是pH6.0~8.0之间。
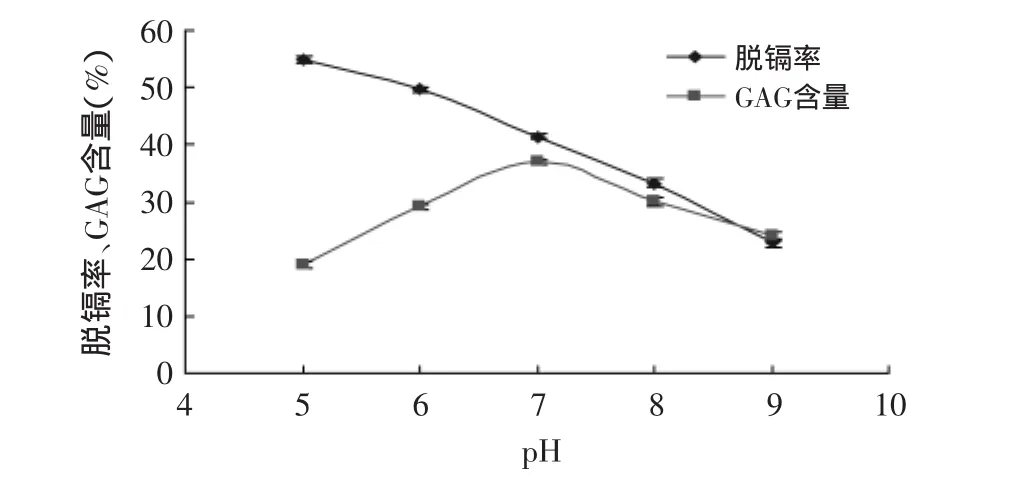
图1 pH对脱镉率和GAG含量的影响Fig.1 Influence of pH on cadmium removal rate and GAG yield
2.1.2 反应时间对GAG粗品中镉脱除率和GAG含量的影响 由图2可看出,随着反应时间的增加,脱镉率也在不断增加,从3h到5h阶段,脱镉率增加迅速,在5h时脱镉率达到最大,之后基本趋于稳定。原因可能是在5h时L-半胱氨酸改性壳聚糖对镉离子的吸附达到饱和,再延长时间也不会增大脱镉效果。而GAG含量在6h之前随时间的增加几乎无变化,但6h之后GAG含量开始降低,可能是因为L-半胱氨酸改性壳聚糖对镉离子的吸附达到饱和之后,会吸附部分的糖胺聚糖导致GAG含量下降。

图2 反应时间对脱镉率和GAG含量影响Fig.2 Influence of adsorption time on cadmium removal rate and GAG yield
2.1.3 改性壳聚糖添加量对GAG粗品中镉脱除率和GAG含量的影响 由图3可知,随L-半胱氨酸改性壳聚糖添加量的增大,脱镉率明显增大,在0.5g/50mL时达到最大值,之后则基本趋于稳定。这是因为在0.5g/50mL时,L-半胱氨酸改性壳聚糖对镉离子的吸附几乎达到饱和,再增加用量时,镉的去除率趋于稳定,增加不明显。而GAG含量在0.6g/50mL之前基本不变,当再增加用量时,GAG含量开始下降,可能是由于过量的L-半胱氨酸改性壳聚糖吸附掉了部分的糖胺聚糖。
2.2 GAG粗品中镉脱除条件的正交实验结果
通过SPSS软件对脱镉率和GAG含量的正交实验见表2,分析结果如表3、表4所示。

图3 L-半胱氨酸改性壳聚糖添加量对脱镉率和GAG含量的影响Fig.3 Influence of L-cysteine modified chitosan dosage on Cadmium removal rate and GAG yield
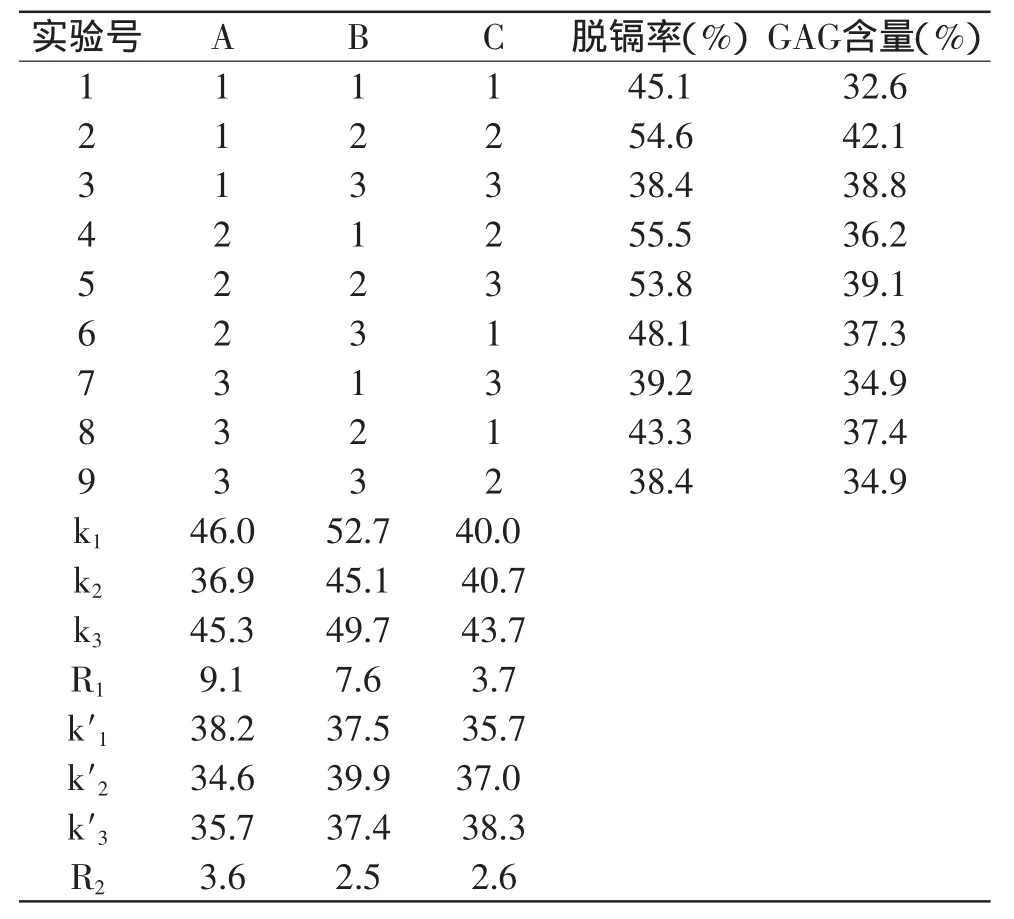
表2 正交实验结果表Table 2 Experimental results of the orthogonal design

表3 方差分析(脱镉率)Table 3 Variance analysis(cadmium removal rate)
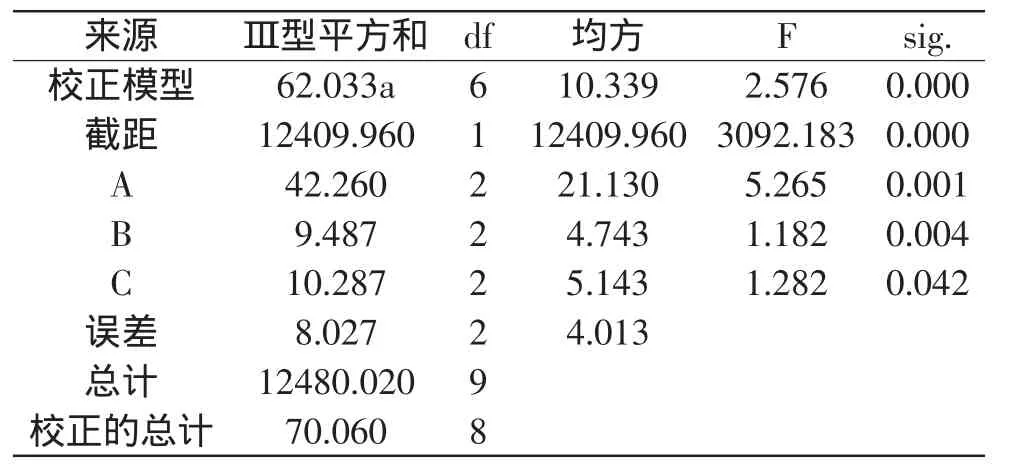
表4 方差分析(GAG含量)Table 4 Variance analysis(GAG yield)
极差R越大,表明该因素对脱镉率和GAG含量的影响越大。由表2分析结果可以看出,各因素对脱镉率影响的大小顺序依次为:反应pH>反应时间>添加量。根据值比较分析,最优组合为A1B1C3,即吸附的最佳条件为:pH为6.0,反应时间为4h,添加量为0.6g/50mL。各因素对GAG含量影响的大小顺序依次为:反应pH>添加量>反应时间。根据值比较分析,最优组合为A1C3B2,即吸附的最佳条件为:pH为6.0,添加量为0.6g/50mL,反应时间为5h。
因为本实验研究的是糖胺聚糖中镉的脱除率,所以在保证具有良好的镉脱除效果的同时,糖胺聚糖的结构与含量是需要考虑的重要因素,根据SPSS软件对正交实验数据的分析结果(表3、表4)可看出,B对脱镉率的显著值(sig.)为0.041(p<0.05),对GAG含量的显著值(sig.)为0.004(p<0.01),说明反应时间对GAG含量的影响较脱镉率更显著[25]。所以对以上分析结果进行综合考虑,得出L-半胱氨酸改性壳聚糖吸附脱除糖胺聚糖中镉离子的最优条件组合为:A1B2C3,即pH为6.0,反应时间为5h,添加量为0.6g/50mL。根据得到的最佳脱除条件,进行验证性实验,实际得到的脱镉率为56.7%,GAG含量为42.8%,验证实验结果与正交实验结果相符,说明L-半胱氨酸改性壳聚糖在该条件下稳定可行。
3 结论
本实验利用L-半胱氨酸改性壳聚糖进行马氏珠母贝糖胺聚糖中镉脱除研究,通过正交实验优化法和SPSS软件数据分析法得到的最佳吸附条件为:pH为6.0、吸附时间5h、添加量为0.6g/50mL。在此条件下,糖胺聚糖中镉的脱除率为56.7%,GAG含量为42.8%。本方法在保证活性物质糖胺聚糖含量的前提下,有效降低了其中重金属镉的含量,可为贝类尤其是马氏珠母贝中镉的脱除提供有益参考。
[1]Hemorth B.Factors in fluencing bactericidal activity of bluemussel (Mytilus edulis) haemocytes against Salmonellatyphimurium[J].Fish Shellifsh Immuno,2003,14(2):93-104.
[2]张惟杰.糖复合物生化研究技术[M].杭州:浙江大学出版社,1999:79,397-400.
[3]XU B,PER H,HENRIK S,et al.Endo-beta-1,4-Mannanases from bluemussel,mytilus edulis.Purification,characterization andmode of action[J].J Biotechno,2001(2):267-277.
[4]张豁中,温玉麟.动物活性成分化学[M].天津:天津科学技术出版社,1995:996-998.
[5]王长云,管华诗,李八方.氨基多糖研究概况与展望[J].生物工程进展,1995,15(6):2-9.
[6]沈鸣,陈建伟.氨基多糖的药理研究进展[J].上海医药,2001,22(6):268-270.
[7]廖艳,吴晓萍.湛江常见食用贝类体内痕量Pb、Cd的含量分析[J].微量元素与健康研究,2007,24(5):31-32.
[8]食品中铅限量卫生标准.GB14935-94[S].
[9]梁鹏,吴晓萍,徐慧,等.壳聚糖脱除牡蛎匀浆液中重金属镉的初步研究[J].食品工业科技,2010,31(7):107-109.
[10]CriniG.Recent developments in polysaccharide-basedmaterials used as adsorbents in wastewater treatment[J].Prog Polym Sci,2005,30(1):38-70.
[11]Rinaudo M.Chitin and chitosan:Properties and applications[J].Progress Polym Sci,2006,31(7):603-632.
[12]程红霞,林强.壳聚糖对中药水提液中重金属残留的吸附特性研究[J].北京联合大学学报:自然科学版,2006,20(1):69-72.
[13]孙继鹏,汪东风,李国云,等.壳寡糖钙、镁配合物对栉孔扇贝体内镉的脱除[J].中国海洋大学学报,2010,40(2):33-37.
[14]刘炳杰,汪东风,孙继鹏,等.交联壳聚糖树脂对扇贝裙边酶解液中镉的脱除研究[J].安徽农业大学学报,2010,37(1):11-14.
[15]吴晓萍,梁鹏,章超桦,等.L-半胱氨酸改性壳聚糖的合成与表征[J].功能材料,2010,S1:172-174.
[16]Kim J H,Lee Y M.Polymer[J].Membr Sci,1993,34(9):1952.
[17]庄莉,杨智宽.含硫壳聚糖研究——氨基硫脲接枝壳聚糖的合成[J].化学试剂,2002,24(5):283.
[18]杨智宽,袁扬,汪玉庭.氮杂冠醚壳聚糖研究(Ⅲ)──双羟基中环二胺交联壳聚糖的制备[J].化学试剂,2002,22(2):69.
[19]吴红棉,雷晓凌,洪鹏志,等.珠母贝糖胺聚糖的纯化及其化学性质[J].水产学报,2000,24(6):570-574.
[20]食品中镉的测定方法.GB/T 5009.15—1996[S].
[21]何秋月.SPSS在L9(34)正交实验数据处理中的应用[J].应用技术,2005,12(3):27-29.
[22]邓振伟,于萍,陈玲.SPSS软件在正交实验设计、结果分析中的应用[J].电脑学习,2009(5):15-17.
[23]张福生,郭顺星.SPSS正交设计在福建金线莲组织培养中的应用[J].中国中药杂志,2009,34(20):2581-2585.
[24]张凌云,孙其富,孙庆磊,等.SPSS软件在绿茶鲜汁浸提工艺研究中的应用[J].粮油加工与食品机械,2003(3):58-60.
[25]孙影.SPSS13.0软件在化学正交设计实验中的应用[J].化学教育,2006(8):48-49.
Study on removing cadmium in glycosaminoglycan from Pinctada martensii by adding modified chitosan
YI Mei-yan,FAN Xiu-ping*,WU Hong-mian,HU Xue-qiong
(College of Food Science and Technology,Guangdong Ocean University,Zhanjiang 524025,China)
The cadmium ion in glycosaminoglycan(GAG)from Pinctada martensii was removed by L-cysteine modified chitosan.The effects of pH,adsorption time and L-cysteine modified chitosan dosage on cadmium removal rate and GAG yield were discussed through single factor and orthogonal experiment.And the data in orthogonal experiment were processed and analyzed by using SPSS.The experiment results indicated that removal conditions were pH=6.0,the adsorption time 5h and L-cysteine modified chitosan dosage 0.6g/50mL. Under the optimized conditions,cadmium removal rate reached 56.7%,GAG yield reached 42.8%.
L-cysteine modified chitosan;SPSS;glycosaminoglycan;cadmium removal rate
TS201.2+3
A
1002-0306(2012)07-0105-04
糖胺聚糖(GAG)是贝类生物中含量丰富的生物活性物质[1-3],是作为新型创新药物和功能性保健食品的重要资源,日益受到人们的重视[4-5],现已发现其在抗癌、提高免疫、降血脂、抗氧化、抗血栓等方面有较强的活性[6]。然而由于环境污染日趋严重,加上贝类对重金属具有较强的蓄积能力,使得一些贝类重金属含量过高。廖艳等对湛江常见的11种食用贝类进行研究[7],参照国家限量卫生标准[8],发现马氏珠母贝镉含量高达3.26mg/kg。重金属作为一种持久性污染物已越来越多地受到关注和重视,重金属污染现已成为全球较普遍的食品安全问题。梁鹏等[9]利用壳聚糖对牡蛎水解液中镉的吸附率达98.0%以上,但壳聚糖溶于酸性溶液,应用范围受到很大限制,也不利于回收再利用。因此,人们通过改变壳聚糖的结构性质制备出多种优质改性壳聚糖,应用于水体、中药、贝类中重金属的吸附,取得了大量的研究和实践成果[10-13]。其中,刘炳杰等[14]利用交联壳聚糖CTS-Zn树脂对扇贝裙边酶解液中镉的脱除率达80.0%以上,但对其他矿质元素和营养成分有一定的吸附作用。目前很少有脱除贝类多糖中重金属的相关报道,因此对于在如何尽可能地保证糖胺聚糖含量的前提下,进行有效地除去或减少多糖中重金属的研究是非常必要的。因此,本文采用L-半胱氨酸改性壳聚糖[15]进行马氏珠母贝糖胺聚糖中镉的脱除研究,对L-半胱氨酸改性壳聚糖吸附酶解液中镉离子的条件进行初步探讨,为贝类多糖中重金属镉的脱除方法提供实验依据。
2011-07-07 *通讯联系人
衣美艳(1984-),女,在读硕士研究生,研究方向:海洋生物活性物质。

