超临界流体色谱纯化柠檬酸
吕惠生,莫绪飞,张敏华,杨 淼
(天津大学石油化工技术中心,绿色合成与转化教育部重点实验室,天津300072)
超临界流体色谱纯化柠檬酸
吕惠生,莫绪飞,张敏华*,杨 淼
(天津大学石油化工技术中心,绿色合成与转化教育部重点实验室,天津300072)
采用超临界流体色谱法(SFC)直接从柠檬酸发酵液中提纯制备柠檬酸。以二氧化碳为流动相,采用ZorBaxSBCN色谱柱(250mm×9.4mm I.D.,5μm)为固定相,在改性剂含量约0~16%,CO2流速10~30g·min-1,压力10~25MPa,温度310~325K,上载量0.02~0.05mL范围内考察了各因素对柠檬酸提纯效果的影响,确定了较适宜的色谱提纯条件为:CO2流速15g·min-1,柱温313.15K,柱压13MPa,上载量0.05mL;此条件下对柠檬酸发酵液进行色谱提纯,得到的产品纯度为99.6%(wt)。
超临界流体色谱,柠檬酸,分离度
柠檬酸(CA)是一种重要的有机酸产品,广泛应用于食品、医药及化妆品等行业[1-2]。目前,柠檬酸生产主要采用微生物发酵法,发酵液中除含有柠檬酸和水以外,还含有菌体、残糖、蛋白质、色素、胶体、有机杂酸及无机盐等多种杂质,因此需要采用各种物理与化学方法来纯化柠檬酸。传统的柠檬酸提纯工艺通常采用钙盐法,但该工艺存在着工序繁杂、辅料消耗高、环境污染严重等问题(如生产1t CA要消耗1t硫酸和1t碳酸钙,同时产生10m3二氧化碳、40t废水和2.5t硫酸钙废渣),严重阻碍了我国柠檬酸行业的进一步发展[3]。近些年来,随着色谱技术的发展,特别是模拟移动床色谱(SMB)、环形色谱等大型连续制备色谱技术的不断进步及工业应用,工业级色谱分离技术由于其具有较高的分离选择性和良好的分离效率,引起了人们的浓厚兴趣,越来越多的学者尝试利用色谱技术从发酵液中直接提取产品。对于柠檬酸生产过程,人们做了许多利用离子交换色谱技术从发酵液中提纯柠檬酸的研究。彭奇均[4]等采用模拟移动床离子交换色谱技术从柠檬酸发酵液中直接分离提纯柠檬酸,该工艺具有流程简单、收率较高等特点。张洪勋[5]等提出了先使用阴离子交换树脂从发酵液中直接吸附柠檬酸,用氨水洗脱为柠檬酸铵,再通过阳离子交换树脂吸附转型成柠檬酸的生产工艺,柠檬酸回收率可达93%以上。但是离子交换树脂具有一定的寿命,需要经常的更换,会产生大量的固体废弃物与废液,并且整个分离过程稳定性较差,由此限制了离子交换色谱的进一步应用。超临界流体色谱技术(Supercritical fluid chromatography,SFC)[6]作为一种新型环保色谱分离技术,具有分离高效、工艺简单等特点,在生物化工、医药领域得到了越来越多的应用。在SFC提纯过程中,溶质随流动相进入色谱柱内,根据溶质中各组分在固定相中的保留行为不同,实现混合物的分离。本文拟采用超临界色谱技术(SFC)从柠檬酸发酵液中提纯柠檬酸,考察流动相、压力和温度对色谱分离效果的影响,对SFC提纯过程中的容量因子规律进行研究,为超临界流体模拟移动床色谱的放大研究与应用提供基础数据与理论指导。
1 材料与方法
1.1 材料与仪器
实验样品 参照相关厂家的实测数据,配制的柠檬酸模拟发酵液,其中柠檬酸的浓度为120.7g·L-1,乌头酸的浓度为3g·L-1,为避免发酵液中的固体物质阻塞管路和污染色谱柱,进样前用0.45μm的微孔滤膜过滤[7];柠檬酸 天津市江天化工技术有限公司,分析纯;CO2天津市六方气体厂,SFC级;乙醇、甲醇、甲酸 天津市江天化工技术有限公司,分析纯;乌头酸 上海化学试剂厂,≥98.5%(wt.%);乙腈 美国Fisher公司,色谱纯。
Thar SFC 200型超临界制备色谱装置 美国Thar公司,实验装置如图1所示。钢瓶中的二氧化碳经过降温、液化,再通过高压计量泵加压,之后经过恒温水浴加热升温成为超临界流体(Supercritical fluid)。改性剂通过改性剂泵进入系统中与二氧化碳混合,而后进入色谱柱。超临界流体通过进样器溶解样品,通过色谱柱进行分离。出柱之后,流体直接通过高压紫外检测器进行检测,并将紫外信号传输给色谱工作站,然后流体经过背压阀降压,分离的物质可以通过收集釜(500mL)收集起来,二氧化碳尾气可以排空。
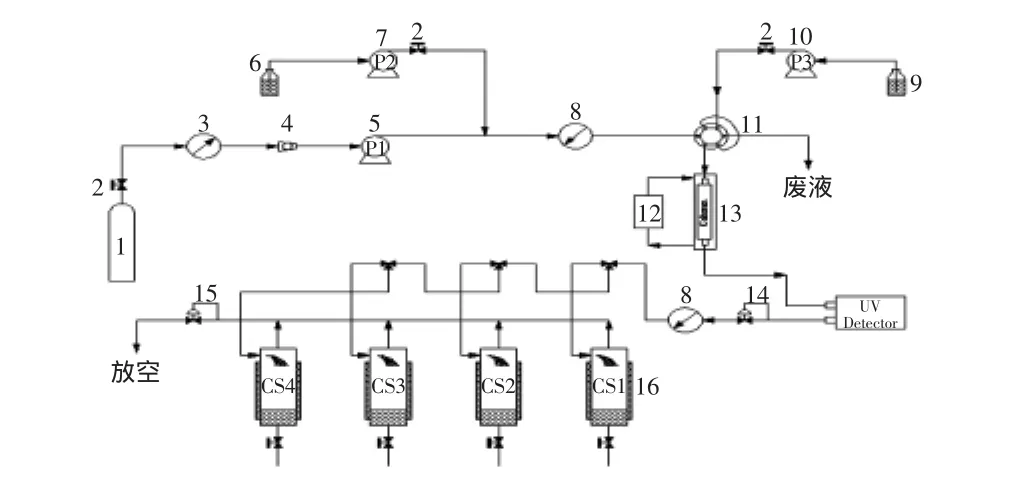
图1 柠檬酸SFC纯化实验流程图Fig.1 Experimental schematic gram of citric acid purification by SFC
1.2 实验方法
实验采用Agilent 1100高效液相色谱仪(HPLC)分析柠檬酸含量,色谱柱为ZorBaxSB-C18(250mm×4.6 mm I.D.,5μm),流动相为0.1%(wt.%)甲酸水溶液∶甲醇=80∶20(V/V),外标法定量分析,该方法线性范围较宽,重现性、稳定性、精密度和加样回收率均较好。
为了判断相邻组分在色谱柱中的分离情况,可用分离度R作为色谱柱整个系统的分离效能指标。分离度R的定义为相邻两组分色谱峰保留值之差与两组分色谱峰峰底宽度之和的一半的比值。
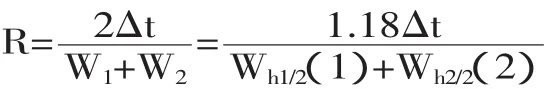
式中:△t是两组分保留时间的差值;W1、W2是色谱峰峰底宽度;Wh1/2(1)、Wh2/2(2)是两组分的半高峰宽。
容量因子k′是描述溶质在固定相和流动相中分布特性的重要参数,是反映色谱柱对组分保留能力的重要参数,k′值越大,说明色谱系统对该组分的保留时间就越长。用公式表示为:
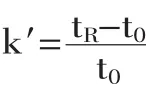
式中:tR是从进样开始到柱后被测组分出现浓度最大值所需的时间(min);t0表示不被固定相滞留的组分从进样开始到柱后出现浓度最大值所需的时间(min)。
1.3 实验条件
色谱条件:采用ZorBaxSB-CN色谱柱(250mm× 9.4mm I.D.,5μm),在改性剂(甲醇、乙醇)含量约0~16%,CO2流速10~30g·min-1,压力10~25MPa,温度310~325K,上载量0.02~0.05mL的范围内考察超临界流体色谱分离柠檬酸的规律;紫外检测器的检测波长为215nm。
2 结果与讨论
2.1 改性剂对分离的影响
因为柠檬酸发酵液中分离组分柠檬酸极性较强,实验选用极性色谱柱ZorBaxSB-CN(250mm×9.4mm I.D.,5μm填料)为固定相[8-9],并考虑加入一定量的改性剂以改善流动相的极性,以提高柠檬酸在流动相中的溶解性[10-11],从而提高色谱分离的效率。
SFC分离过程中常用的改性剂有甲醇和乙醇等,加入量一般为0~20%[9]。实验以柠檬酸峰与相邻乌头酸色谱峰的分离度为目标函数(见图2与图3)。在CO2流速15g·min-1,柱压14MPa,柱温313.15K,进样量0.01mL,紫外检测器波长215nm条件下,考察了不同含量(改性剂在CO2中的质量百分含量)改性剂对分离度的影响,结果如表1所示。
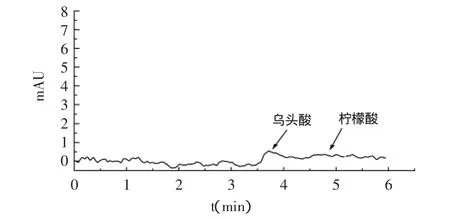
图2 未加改性剂时柠檬酸发酵液样品SFC分离色谱图Fig.2 Chromatography of citric acid sample by SFC separation without modifier
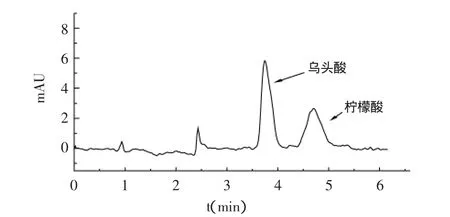
图3 加入甲醇改性剂时柠檬酸发酵液样品SFC分离色谱图Fig.3 Chromatography of citric acid sample by SFC separation with modifier methanol
从图2与图3对比可知,未加改性剂时,乌头酸与柠檬酸出峰不明显,没有得到较好的分离;在加入改性剂后,出峰较明显,峰形更加对称。由表1可知,乙醇作为改性剂时,柠檬酸与相邻的乌头酸的分离度比甲醇作改性剂时高,并且当乙醇加入量为8%时,两者分离度已达到2.02,乙醇的浓度进一步增加,当乙醇的加入量为9.7%(wt)时,分离度增加较小,两者的分离度达到最大,为2.023。分析其中原因,可能是由于在改性剂浓度较低时,随着改性剂浓度的增加,流动相的极性增加,样品在流动相中的溶解能力增大,样品中各组分在流动相和固定相间的吸附与脱附行为更强,以致超临界流体色谱分离过程的效率较高。随着改性剂浓度的增加,样品在流动相中的溶解能力增加得越来越慢,所以当改性剂浓度达到一定值时,分离度增加得较小。但是当改性剂浓度过高时,改性剂与二氧化碳可能不会以均相的形式通过整个色谱柱,这样就降低了整个色谱过程的效率。
由于柠檬酸大多用于食品、医药行业,因此对柠檬酸的安全要求比较严格。甲醇具有一定毒性,若残留在柠檬酸中会危害人体健康。故选择SC-CO2/乙醇二元体系作为SFC提纯柠檬酸操作的流动相是比较合适的,乙醇加入量为9.7%(wt)。
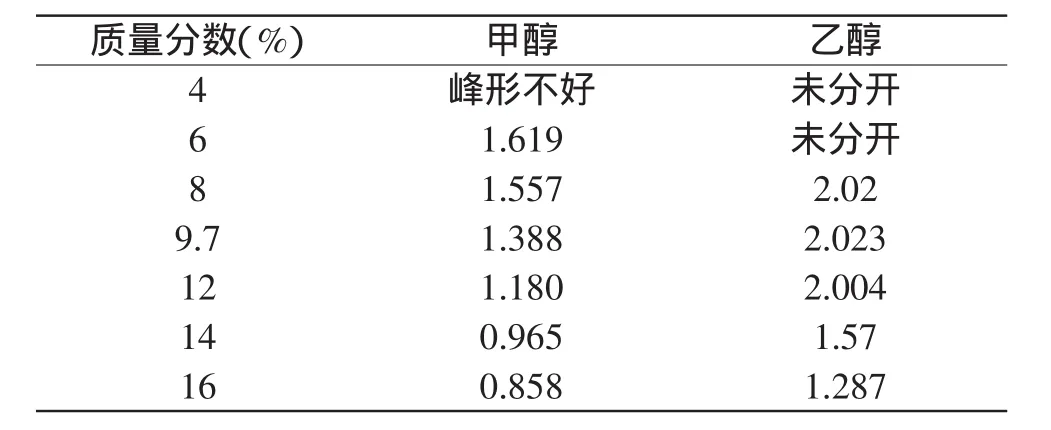
表1 不同改性剂不同百分含量对分离度的影响Table 1 RCA-Aco at different modifier contents
2.2 CO2流速对分离的影响
考察了CO2流速对整个色谱分离过程的影响,以SC-CO2/乙醇二元体系为流动相,在柱压14MPa,改性剂乙醇含量9.7%(wt),柱温313.15K,进样量0.01mL,紫外检测器波长215nm条件下,CO2流速对分离度的影响如表2所示。

表2 不同CO2流速下的分离度Table 2 RCA-Aco at different velocities of CO2
流动相流速决定了色谱柱内填料与流动相内溶质的接触时间,影响样品中各组分在填料表面的扩散程度,从而影响各组分在固定相和流动相之间的分配平衡。随着CO2流速的增加,单位时间通过色谱柱内单位截面的CO2量增多,使得CO2对样品组分的溶解能力增强。由于对柠檬酸发酵液中不同组分洗脱能力增强程度的不同,在流速较小时,对柠檬酸的洗脱能力的增强程度要高于乌头酸组分,使得分离度逐渐增大。当CO2流速为15g·min-1时,分离度达到最大,为2.02。当CO2流量过大时,即溶质分子在尚未扩散到固定相的表面时就已经被流动相带出,从而使分离度下降。在色谱过程中,根据Van Deemter方程,随着流动相线速度的增加,色谱柱的塔板高度呈先减小后增大的趋势,即只有当流动相在色谱柱中的线速度达到一定数值时,色谱柱能达到最佳柱效。故此实验条件下,CO2的最佳流速是15g·min-1。
2.3 压力对分离的影响
色谱操作压力是影响SFC分离过程的重要因素之一。以SC-CO2/乙醇二元体系为流动相,CO2流速为15g·min-1,进样量0.01mL,样品中柠檬酸浓度为120.7g·L-1,紫外检测器波长215nm条件下,不同温度下,柠檬酸的容量因子以及分离度随压力的变化趋势分别如图4和图5所示。
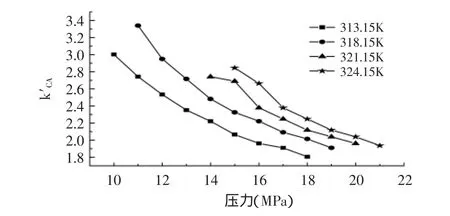
图4 压力对柠檬酸容量因子的影响Fig.4 Effect of pressure on k′CA
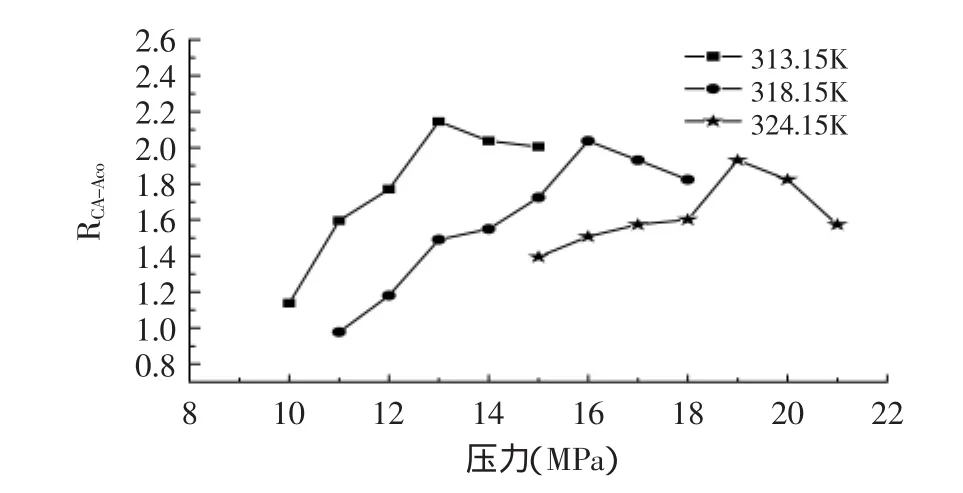
图5 压力对分离度的影响Fig.5 Effect of pressure on RCA-Aco
如图4所示,一定温度下,随着压力的增加,柠檬酸的容量因子呈下降的趋势。这可能是由于压力的增大,SC-CO2的密度会随之增大,样品溶液中各组分在流动相中溶解度亦增大,以致流动相对柠檬酸的洗脱能力增强,同时SC-CO2的黏度也会增大,扩散能力减弱,使得溶质在固定相表面和流动相中的扩散系数减小,传质阻力增大,传质效率降低。但是因为压力的增加,流动相溶解能力的变化程度大于流动相扩散性能的变化程度,故总体上而言,随着压力增加,流动相溶解柠檬酸的能力增加,在固定相上的保留时间减少,使得柠檬酸的容量因子减小。
从图5中可知,不同温度下,随着压力的增加,分离度呈先增大后减小的趋势。在分离度达到最大值之前,随着压力的增加,流动相对柠檬酸和乌头酸的溶解能力逐渐增强,但流动相对柠檬酸溶解能力的增强程度比乌头酸小,因而分离度呈上升趋势。但当压力过大时,流动相对柠檬酸和乌头酸的溶解能力又趋于接近,以致分离度降低。可以观察到,在温度为313.15K、压力为13MPa时分离度达到最大,为2.14。随着温度的升高,分离度达到最大值时的操作压力增大。故选择13MPa作为SFC提纯制备柠檬酸操作最佳压力。
2.4 温度对分离的影响
色谱分离温度是影响SFC分离过程的又一重要因素。以SF-CO2/乙醇二元体系为流动相,改性剂乙醇含量9.7%(wt),流速为15g·min-1,进样量0.01mL,紫外检测器波长215nm条件下,不同压力下,容量因子及分离度随温度的变化趋势见图6和图7。
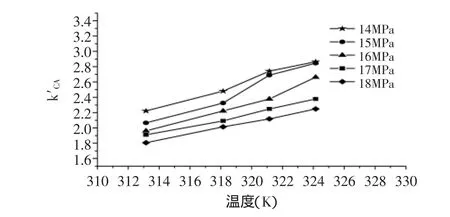
图6 温度对柠檬酸容量因子的影响Fig.6 Effect of temperature on k′CA
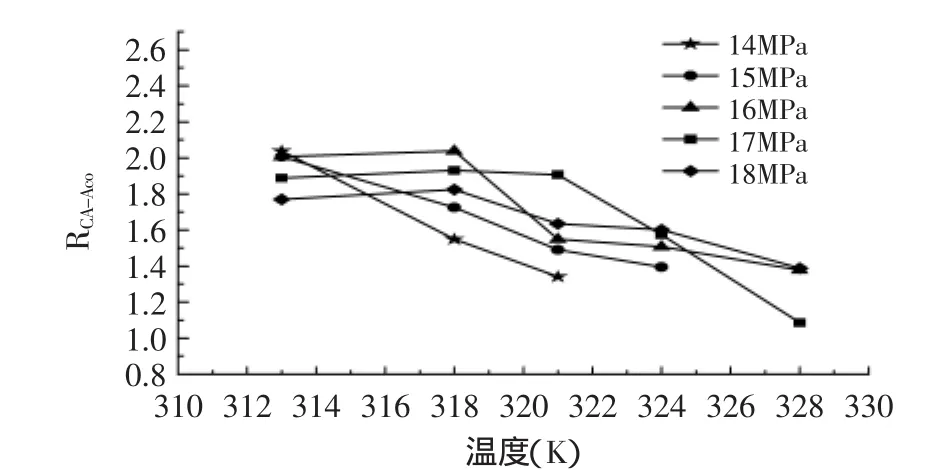
图7 温度对柠檬酸分离度的影响Fig.7 Effect of temperature on RCA-Aco
如图6所示,一定压力条件下,随着温度的升高,柠檬酸的容量因子呈增大的趋势,这可能是因为温度的升高,导致SC-CO2的密度减小,流动相对柠檬酸的溶解能力减弱;但同时SC-CO2的黏度会下降,其扩散能力也会增强,溶质在固定相表面和流动相中的扩散系数增大,传质阻力减小,传质效率增加,溶质在固定相与流动相之间的吸附与脱附能力更大。总体上而言,流动相对柠檬酸溶解能力减小的程度较大,柠檬酸在流动相中的扩散系数增加的程度较小。因此随着温度的升高,流动相对柠檬酸的溶解能力减小,流动相对柠檬酸的洗脱能力减弱,导致柠檬酸的容量因子增大。
从图7中可知,不同压力下,随着温度的升高,两组分之间的分离度呈下降的趋势,究其原因,可能是由于温度的升高,流动相的密度减小对柠檬酸的影响小于对乌头酸的影响,总之,导致流动相对柠檬酸的洗脱能力减低,因而分离度呈下降趋势。在压力为13MPa、温度为313.15K时分离度最大,为2.14。故选择313.15K作为SFC提纯制备柠檬酸操作最佳温度。
2.5 SFC制备柠檬酸产品
对于制备色谱,在保证一定纯度要求基础上,应尽可能提高产品产量,减少CO2的消耗,因此在以上实验基础上,又对上载量进行了考察。具体实验条件如下:色谱柱ZorBaxSB-CN(250mm×9.4mm I.D.,5μm)为固定相,以SC-CO2/乙醇二元体系为流动相,改性剂乙醇含量9.7%(wt),CO2流速:15g·min-1,柱温:313.15K,柱压:13MPa,进样样品中柠檬酸浓度120.7g·L-1,紫外检测器波长215nm。
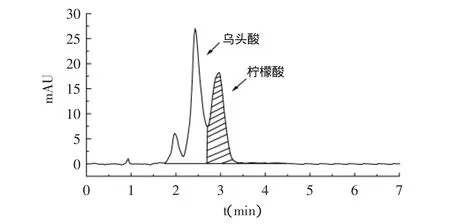
图8 进样量为0.05mL时柠檬酸样品SFC分离的色谱图Fig.8 Chromatogram of sample by SFC separation at injection volume=0.05mL
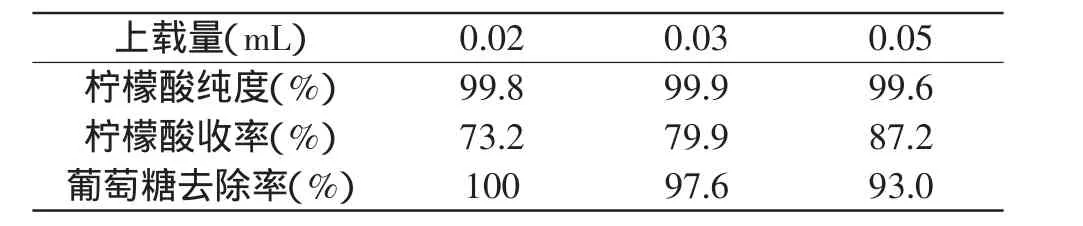
表3 不同上载量时SFC制备得到柠檬酸分析结果Table 3 Analytic results of citric for different injected volume by SFC
通过实验观察,柠檬酸上载量增加时,柠檬酸峰色谱谱带变宽,样品的岀峰时间相应延长,在上载量为0.05mL时,柠檬酸峰与相邻的乌头酸峰未达到基线分离(见图8)。但是由表3可知,增大进样量后柠檬酸的纯度仍然在99.5%以上,产品提取率在70%以上。为提高产品产量,减少CO2的消耗,选择0.05mL为适宜的进样量。
3 结论
3.1 通过考察改性剂、流动相流速、压力和温度对分离的影响,确定了SFC提纯制备柠檬酸操作较适宜的工艺条件为:CO2流速15g·min-1,压力13MPa,温度313.15K,上载量0.05mL。并且在此工艺条件下,从发酵液中提纯柠檬酸,得到了质量百分含量为99.6%的柠檬酸产品。
3.2 超临界流体色谱提纯技术作为一种绿色清洁生产技术,具有高效、低碳等特点。但目前SFC制备柠檬酸还处在实验室阶段,有必要对超临界色谱制备技术的工业放大作进一步的研究。
[1]王博彦,金其荣.发酵有机酸生产与应用手册[M].北京:中国轻工业出版社,2000:147-221.
[2]尤新.2006年我国食品添加剂发展趋势[J].食品工业科技,2007(2):11-15.
[3]伍时华,路敏,童张法.从发酵液中提取柠檬酸的研究进展[J].广西工学院学报,2005,16(3):9-14.
[4]彭奇均,徐玲.柠檬酸生产中色谱提纯分离技术的应用[J].中国食品添加剂,2001(2):45-48.
[5]张洪勋,刘德明,薛茂杰,等.柠檬酸提取新工艺[P].中国专利,1153821A,1997-07-09.
[6]韩布兴.超临界流体科学与技术[M].北京:中国石化出版社,2005.
[7]庞斐.超临界流体色谱纯化青蒿素的研究[J].高校化学工程学报,2010,24(4):569-573.
[8]丁明玉.现代分离方法与技术[M].北京:化学工业出版社,2006:144.
[9]Lesellier E,West C.Effects of modifiers in subcritical fluid chromatography on retention with porous graphitic carbon[J]. Journal of Chromatography A,2005,1087(1):64-76.
[10]Berger T A.Separation of polar solutes by packed column supercritical fluid chromatography[J].Journal of Chromatography A,1997,785:3-33.
[11]何岩,张敏华,董秀芹.常用夹带剂在超临界CO2中无限稀释扩散系数的MD计算[J].高校化学工程学报,2008,22(1):152-156.
Study on purification of citric acid by supercritical fluid chromatography
LV Hui-sheng,MO Xu-fei,ZHANG Min-hua*,YANG Miao
(Key Laboratory for Green Chemical Technology of State Education Ministry Tianjin,R&D Center for Petrochemical Technology,Tianjin 300072,China)
Supercritical fluid chromatography(SFC)was employed for the purification of citric acid from the citric acid fermentation broth.Citric acid was purified by SFC on a ZorBaxSB-CN column(250mm×9.4mm I.D.,5μm)under following conditions:concentration of the modifier was 0~16%,velocity of CO210~30g·min-1,column pressure 10~25MPa and temperature 310~325K,injected volume 0.02~0.05mL.The optimal conditions for chromatographic purification were determined:velocity of CO215g·min-1,temperature of column 313.15K,pressure of column 13MPa,injected volume 0.05mL.The citric acid fermentation broth was purified under these conditions,and citric acid with the content of 99.6%(wt)was obtained.
supercritical fluid chromatography;citric acid;retention
TS201.1
B
1002-0306(2012)07-0271-05
2011-06-20 *通讯联系人
吕惠生(1963-),男,副教授,研究方向:绿色化学,新能源等。

