离子液体萃取-荧光猝灭法测定富硒保健品和食盐中的硒(Ⅳ)
武玉杰,孙汉文*,夏祥华
(河北大学化学与环境科学学院,河北省分析科学重点实验室,河北 保定 071002)
离子液体萃取-荧光猝灭法测定富硒保健品和食盐中的硒(Ⅳ)
武玉杰,孙汉文*,夏祥华
(河北大学化学与环境科学学院,河北省分析科学重点实验室,河北 保定 071002)
建立保健品和食盐中硒(Ⅳ)的离子液体萃取-荧光猝灭法。样品经微波消解,在0.2mol/L盐酸介质条件下,硒(Ⅳ)氧化碘化钾,其反应产物I3-与罗丹明B形成离子缔合物。10g/100mL碘化钾1mL,0.005g/100mL罗丹明B 3mL,以0.5mL 1-丁基-3-甲基咪唑六氟磷酸盐将离子缔合物萃取进入离子液体相。结果表明,荧光淬灭值与硒(Ⅳ)的质量浓度呈正比,线性范围2~60μg/L,方法的定量限(RSN=10)为20μg/kg,平均回收率为87.9%~105%。该方法具有操作简易、无污染、灵敏度高等优点,可用于富硒保健品和食盐中微量硒的测定。
微波消解;室温离子液体;荧光猝灭;硒;食品
硒是一种人体的必须微量元素,但摄入量过多或过少都会对人体产生伤害[1],因此,富硒产品的质量控制与评价越来越重要。关于硒的测定方法已有综述报道[2-4]。湿法消解-原子光谱法已用于食品中硒的检测[5-8]。分子荧光法已作为国家标准方法用于食品中硒的测定[9],该方法的弱点在于试样以混合酸消化过夜耗时过长,且所用环己烷试剂有一定毒性,部分操作尚需在暗室中进行,方法的灵敏度低,其检出限仅为5μg/L。分子荧光法已用于食用菌[10]、富硒油菜籽[11]、银杏叶[12]、蒜[13]、硒盐[14]和茶叶[15]中微量硒的测定,其检出限为0.17~4.5μg/L。这些分析方法中的样品处理采用酸消解,耗时过长,且对实验室环境和人体健康造成不利影响。微波消解在样品前处理方面有很大的优势,其试剂消耗量少、消解速度快,从而解决了样品处理时间长和元素挥发损失的问题[16]。为提高方法的灵敏度,离子液体因其萃取能力高而被用于液液萃取[17-18]。本实验优化前处理方法,旨在建立用于检测保健品和食盐中微量硒的荧光猝灭新方法。
1 材料与方法
1.1 材料与试剂
锌硒宝 深圳市绿世纪生物科技有限公司;硒强化营养盐 中盐河北盐业专营有限公司。
硒标准溶液(GSB G62029-90(3401)) 国家钢铁测试材料中心;离子液体1-丁基-3-甲基咪唑六氟磷酸盐(C4MIM)PF6(分析纯)) 上海成捷化学有限公司;盐酸(优级纯)、硝酸(分析纯)、双氧水(分析纯)、盐酸羟胺和氢氧化钠(分析纯);所用玻璃器皿在使用前均用10%的硝酸浸泡过夜,用自来水冲洗干净,再用高纯水冲洗3次,烘干后使用。
硒标准工作溶液:用体积分数为20% HCl溶液将1000 μg/mL的硒标准溶液逐级稀释成250μg/L标准使用液;碘化钾溶液(10g/100mL);抗坏血酸(3.2×10-6mol/L)。
1.2 仪器与设备
F-7000 荧光光度计 日本日立公司;MAESXpress微波消解/萃取系统 美国培安公司;BHW-09C恒温消解仪赶酸仪 上海博通化学科技有限公司;TGL-16M高速台式冷冻离心机 湘仪离心机仪器有限公司;HE-9202S型水浴恒温振荡器 太仓市科教器材厂;pHS-2型酸度计 上海雷磁仪器厂。
1.3 方法
1.3.1 样品处理
锌硒宝:准确称取0.5000g样品,置于消解罐中,为防止消解时反应太剧烈加入2mL浓硝酸、2mL H2O2浸泡30min后放入微波消解仪中消解。消解完成后,将消解罐放入恒温赶酸仪赶酸至溶液剩余1.0mL左右。待溶液冷至室温后转入25mL比色管,测定荧光强度。
硒强化营养盐:称取5.000g硒强化营养盐溶于100mL容量瓶中,为去除碘酸钾的干扰加入1mL 质量浓度为10g/100mL的盐酸羟胺溶液,待反应30min后,用高纯水定容。取1mL于25mL的比色管中,待荧光分析。
1.3.2 仪器条件
微波消解采用爬坡模式,参数见表1。

表1 微波消解参数Table 1 Parameters for microwave-assisted digestion
1.3.3 测定方法
分别移取0.2、0.5、1.0、2.0、4.0、6.0mL 250μg/L硒(Ⅳ)于25mL比色管中,加入lmol/L盐酸2.0mL,用水稀释至10mL左右,加人3.0mL 0.005g/100mL罗丹明B(RhB)溶液摇匀,再加入3.2×10-6mol/L抗坏血酸溶液2.0mL,10g/100mL碘化钾溶液1mL,用水稀释至刻度并摇匀放置20~25min。加入0.5mL的1-丁基-3-甲基咪唑六氟磷酸盐((C4MIM)PF6)后振荡20min,以5000r/min离心7min,取出上层水相。离子液体相用无水乙醇溶解并加入0.2mL lmol/L的硝酸定容至5mL。同时做空白实验。用荧光光度计于Ex350nm/Em583.0nm处测定试剂空白荧光强度(F0)和标准系列溶液的荧光强度(F),计算ΔF=F0-F。基于ΔF值与硒(Ⅳ)质量浓度之间的线性关系,以标准曲线法测定硒含量。
2 结果与分析
2.1 荧光光谱

图1 罗丹明B体系的荧光光谱Fig.1 Emission fluorescence spectra of the Rhodamine B (RhB)
4种罗丹明B反应体系的荧光特性,如图1所示。罗丹明B在稀盐酸介质中,其荧光波长为588nm。硒(Ⅳ)的加入,罗丹明B的荧光波长和荧光强度没有发生变化,说明硒(Ⅳ)和罗丹明B在稀盐酸介质中未发生化学反应。在盐酸介质中,碘化钾能使罗丹明B荧光猝灭。当在碘化钾-罗丹明B体系中加入硒(Ⅳ)时,I-被硒(Ⅳ)氧化生成I3-,I3-与RhB形成离子缔合物,从而使荧光型罗丹明B转化成无荧光型罗丹明B,荧光猝灭程度进一步增强。
2.2 离子缔合条件对荧光猝灭的影响
2.2.1 酸介质的影响
比较盐酸、磷酸、硫酸和硝酸介质对荧光猝灭的影响。结果显示以盐酸作为介质,反应时间快且荧光猝灭ΔF值大。取0.5~4mL 1mol/L盐酸加入10mL反应体系,即体系的盐酸介质强度为0.05~0.4mol/L。考察盐酸介质强度对荧光猝灭程度的影响。结果表明,当盐酸介质为0.05mol/L时,荧光猝灭较弱,ΔF为34。当盐酸介质强度为0.1~0.2mol/L(pH1.48~1.25),荧光猝灭程度最大,ΔF为60。本实验选用0.2mol/L盐酸介质。
2.2.2 罗丹明B用量对荧光猝灭的影响

图2 罗丹明B用量对ΔF值的影响Fig.2 Effect of amount of Rhodamine B solution on ΔF
由图2可知,罗丹明B用量在0.5~3.0mL时,ΔF值随着罗丹明B用量的增加而增大。当罗丹明B的用量为3.0mL时,ΔF达67。当其用量超过3.0mL时,ΔF值逐渐减小,原因可能是罗丹明B浓度大时形成二聚体或多聚体,还可能是由于罗丹明B本身存在的自熄灭作用增强致使F0变小[19],故ΔF随着罗丹明B的增大反而减小。实验选用加入3.0mL罗丹明B。
2.2.3 碘化钾用量对荧光淬灭的影响
碘化钾用量在1.0~2.0mL范围内ΔF值最大且比较稳定。当碘化钾用量超过2.0mL时,由于过量的碘化钾会使空白猝灭明显,致使ΔF值降低。故实验时选用加入1.0mL碘化钾溶液。
2.2.4 抗坏血酸用量对荧光淬灭的影响
加入抗坏血酸可以保护碘化钾不被其他离子氧化。考察0.5~4.0mL抗坏血酸用量对荧光猝灭的影响。由图3可看出,抗坏血酸用量为2.0mL时,荧光猝灭最明显,ΔF值达64。由此,选用加入2.0mL抗坏血酸。

图3 抗坏血酸用量对ΔF值的影响Fig.3 Effect of amount of ascorbic acid solution on ΔF
2.2.5 反应时间和温度的影响
随着反应时间的延长荧光猝灭越来越明显,反应时间20~25min,ΔF值最大且稳定。在室温条件下反应,荧光淬灭值较大,但随着温度的升高,其荧光猝灭ΔF值反而降低,原因在于所生成的离子缔合物稳定性降低所致,故选室温条件。
2.3 离子液体萃取条件的优化
2.3.1 罗丹明B用量和pH值对萃取回收率的影响
罗丹明B用量小时,线性范围窄;当罗丹明B用量过大时,荧光猝灭ΔF变小。综合离子缔合物形成条件和离子液体萃取条件选用3.0mL罗丹明B。在pH 1.0~3.0范围内,酸介质对硒的回收率影响较小。结合pH值对离子缔合物的形成的影响,选用0.2mol/L盐酸介质(pH 1.25),回收率达95%。

图4 离子液体(C4MIM)PF6用量对回收率的影响Fig.4 Effect of amounts of ionic liquid (C4MIM)PF6 on recovery
2.3.2 离子液体用量对回收率的影响由图4可知,离子液体的加入量小于0.5mL时,回收率低。当加入量大于0.5mL时,回收率稳定。选用加入0.5mL离子液体,回收率达到99.6%。
2.3.3 振荡时间和振荡后放置时间对荧光猝灭的影响加入离子液体后,振荡萃取20min,萃取率可达到
99%以上。离子液体相用无水乙醇溶解,并加入0.2mL l mol/L的硝酸定容至5mL。溶液配制之后需放置一段时间再上机测定。由图5可知,振荡后放置5~25min基本稳定,配制好后可在此时间段内测定。

图5 放置时间对ΔF的影响Fig.5 Effect of time onΔF
2.4 共存离子干扰
在选定的实验条件下,对于25μg/L硒(Ⅳ)的测定,相对误差小于5%时,以下干扰离子(允许倍数)为:Zn2+、Cl-、NO3-(2000);Ca2+、Mg2+、Ba2+(1000);Cr6+(500);Ni2+(400);Co2+(200);As3+(100);Cu2+(10);Fe3+、Cd2+(5)。这说明方法有较好的选择性。由于食盐样品中含有大量IO-3,加入1mL 25g/L盐酸羟胺可消除0.5mg IO-3干扰。
2.5 线性范围与检出限
在最优条件下,在2~60μg/L范围内硒(Ⅳ)含量与ΔF呈良好的线性关系,线性回归方程ΔF=7.996+4.575C,相关系数r=0.9986。空白溶液经连续11次测量,得到仪器检出限(RSN=3)为0.12μg/L。根据取样量和稀释因子,本方法的检出限(RSN=3)为6μg/kg,定量限(RSN=10)为20μg/kg。本方法的检出限优于文献报道的荧光法[9-15]。
2.6 样品分析
按照前述的样品处理方法平行处理5份样品,以标准曲线法测定锌硒宝和硒强化营养盐中硒含量,并进行加标回收实验,结果见表2。
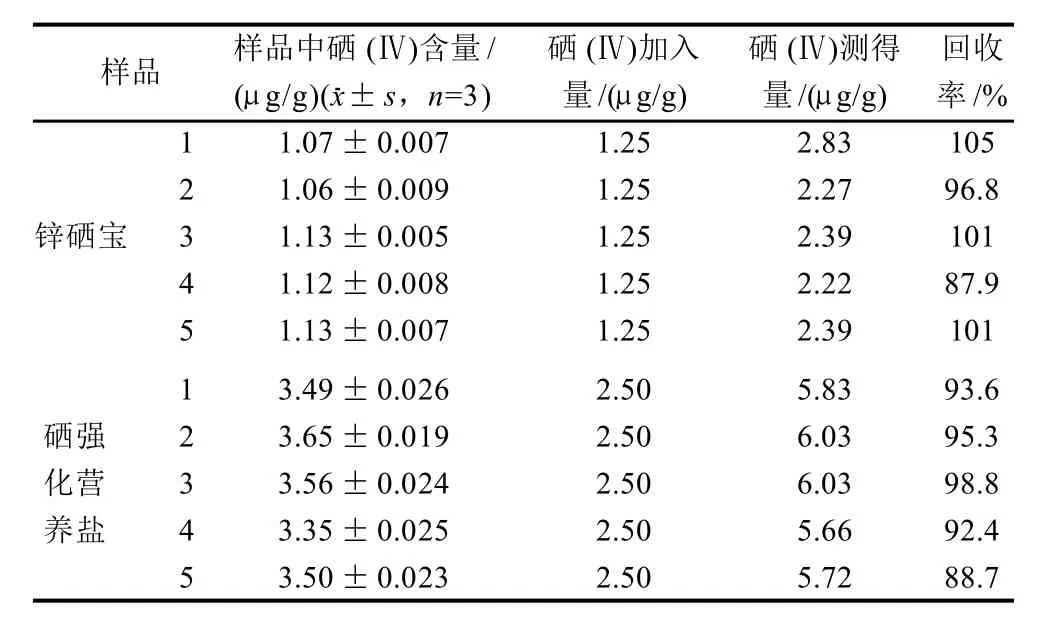
表2 锌硒宝和硒强化营养盐中硒含量的测定Table 2 Selenium determination in zinc-selenium enriched health food and nutrient salt fortified with selenium
对5份样品的分析结果表明:锌硒宝中的硒含量为1.10μg/g,相对标准偏差(relative standrad deviation,RSD)为5.9%,平均回收率为98.3%;强化营养盐中的硒含量为3.51μg/g,RSD为6.2%。平均回收率为93.7%。硒强化营养盐的硒含量符合食品质量要求(3~5μg/g)[20],而锌硒宝的硒含量远低于其标示值(18.2μg/g),应引起有关方面的关注。
3 结 论
微波消解样品的速度快、效果好。离子液体(C4MIM)PF6具有高的疏水性和低的挥发性,具有高的萃取率和富集倍数,可以作为绿色反应介质代替传统的挥发有机溶剂。该方法具有操作简易、无污染、灵敏度高等优点,可用于保健品和硒强化营养盐中硒的常规检测和食品质量控制。
[1] STRANGES S, NAVAS A A, RAYMAN M P, et al. Selenium status and cardiometabolic health∶ State of the evidence[J]. Nutrition, Metabolism and Cardiovascular Diseases, 2010, 20(10)∶ 754-760.
[2] 史丽英. 微量元素硒的测定方法综述[J]. 微量元素与健康研究, 2007,24(4)∶ 63-65.
[3] PEDRERO Z, MADRID Y. Novel approaches for selenium speciation in foodstuffs and biological specimens∶ a review[J]. Analytica Chimica Acta, 2009, 634(2)∶ 135-152.
[4] AGRAWAL K, PATEL K S, SHRIVAS K. Development of surfactant assisted spectrophotometric method for determination of selenium in waste water samples[J]. Journal of Hazardous Materials, 2009, 161(2)∶1245-1249.
[5] SUN Hanwen, FENG Bo. Speciation of organic and inorganic selenium in selenium enriched eggs by hydride generation atomic fluorescence spectrometry[J]. Food Analytical Methods, 2011, 4(2)∶ 240-244.
[6] ALEXIU V, VLADESCN L Optimization of a chemical modifier in the determination of selenium by graphite furnace atomic absorption spectrometry and its application to wheat and wheat flour analysis[J]. Analytical Scincies, 2005, 21(2)∶ 137-141.
[7] 张涛, 高愈希, 李柏, 等. 高效液相色谱-等离子体质谱联用方法研究富硒大米中硒的形态[J]. 分析化学, 2008, 36(2)∶ 206-210.
[8] 孙汉文, 冯波. 悬浮进样-氢化物发生原子荧光法用于面粉和富硒盐中微量硒形态分析[J]. 食品科学, 2010, 31(16)∶ 225-228.
[9] GB 5009.93—2010食品中硒的测定[S].
[10] 黄高凌, 王秋铭, 邱恩. 荧光法测定食用菌中痕量硒的研究[J]. 集美大学学报∶ 自然科学版, 2006,11(4)∶ 310-314.
[11] 张寒俊, 刘大川. 分子荧光法测定富硒油菜籽中的硒含量[J]. 中国油脂, 2006, 31(3)∶ 31-33.
[12] 郭华, 侯冬岩, 回瑞华, 等. 4-甲基-邻苯二胺荧光光度法测定痕量硒[J]. 光谱实验室, 2006, 23(1)∶ 88-90.
[13] 成永强, 鲍所言, 石生勋. 荧光猝灭法测定痕量硒(Ⅳ)[J]. 理化检验∶化学分册, 2005, 41(4)∶ 259-260; 263.
[14] 蔡瑜娜, 黄凌, 贾文平. 苯并咪唑衍生物荧光猝灭法测定硒盐中的微量硒[J]. 浙江化工, 2006, 37(12)∶ 26-28.
[15] 李建国, 王耀, 魏永前, 等. 硒(Ⅳ)-碘化物-罗丹明6G 体系荧光猝灭反应测定茶叶中痕量硒[J]. 分析试验室, 1997, 16(5)∶ 52-54.
[16] 曹璨, 吴志刚. 微波消解-原子荧光光谱法测定鸡蛋中痕量硒[J]. 光谱实验室, 2008, 25(5)∶ 796-800.
[17] LIU Rui, LIU Jingfu, YIN Yongguang, et al. Ionic liquids in sample preparation[J]. Analytical and Bioanalytical Chemistry, 2009, 393(3)∶871-883.
[18] 孙汉文, 冯波, 吴远远, 等. 室温离子液体在原子光谱分析中的应用研究进展[J]. 河北大学学报∶ 自然科学版, 2010, 30(2)∶ 216-224.
[19] 黄保军, 李建军, 屈凌波. 罗丹明B荧光光谱机理的研究[J]. 天津师范大学学报∶ 自然科学版, 2005, 25(3)∶ 8-10.
[20] QB 2238.3—2005 强化营养盐∶ 硒强化营养盐[S].
Determination of Se (Ⅳ) in Se-Enriched Health Food and Salt Samples Using Ionic Liquid Extraction Combined with Fluorescence Quenching Method
WU Yu-jie,SUN Han-wen*,XIA Xiang-hua
(Key Laboratory of Analytical Science of Hebei Province, College of Chemistry and Environmental Science,Hebei University, Baoding 071002, China)
Sample was digested by microwave. Potassium iodide is oxidized by Se (Ⅳ) in medium of 0.2 mol/L hydrochloric acid,the product I3-reacts with rhodamine B to form ion complex. Potassium iodide of 1 mL at 10 g/100mL and rhodamine B of 3 mL at 0.005 g/100mL were used. The formed ion complex was extracted into the 0.5 mL ionic liquid phase (C4MIM)PF6.The quenched fluorescence was observed for rhodamine B in the presence of Se (Ⅳ). The linear determination range of Se (Ⅳ)was between 2 and 60μg/L. The limit of quantification of method (RSN=10) for selenium was 20μg/kg, and the average recoveries were from 87.9% to 105%. The proposed method has the characteristics of easy operation, no pollution and high sensitivity, and it can be used for the analysis of trace selenium in zinc-selenium health food and fortified nutrient salt.
microwave digestion;room temperature ionic liquid;fluorescence quenching;selenium;food
O657.39
A
1002-6630(2012)10-0264-04
2011-07-06
河北省自然科学基金项目(B2008000583)
武玉杰(1986—),女,硕士研究生,研究方向为光谱和痕量分析。E-mail:wuyujie1016@126.com
*通信作者:孙汉文(1945—),男,教授,硕士,研究方向为光谱学与痕量分析。E-mail:hanwen@hbu.edu.cn

