脑心通治疗血管性痴呆效果的Meta分析
李敏,胡波,熊光润,谭晓敏
血管性痴呆(vascular dementia,VaD)是一种由于各种脑血管病(包括缺血性或出血性脑血管病)或低血氧-低灌流而引起智力及认知功能障碍的综合征,是导致痴呆的第2位原因,仅次于阿尔茨海默病(Alzheimer's disease)[1]。研究表明,脑血管病患者中痴呆发生率是26%,约为无脑血管病者的5.8倍[2-3];中国老年人痴呆发病率约为3.9%,其中VaD占68.5%而高居首位[4-5]。随着我国进入老龄化社会,VaD的患病率明显上升,给社会和家庭带来沉重负担。
VaD的致病因素明确,包括卒中复发、高血压、糖尿病、高血脂、肥胖、吸烟、高钠饮食等[1-7];VaD 也是目前惟一可预防的痴呆类型[1-2,6]。目前,西医尚无肯定的治疗方法和药物可以改善VaD的整个病程,临床主要针对其病理过程中的某个环节进行治疗,用于干预的西药主要包括胆碱酯酶抑制剂、改善脑组织细胞代谢药物、改善脑部循环及血供的药物、神经保护药物、兴奋性氨基酸受体拮抗剂以及自由基清除剂等[1-2,4,6],但均未能取得较满意的疗效。近年来关于中药治疗VaD的研究较多:三个[8-10]关于银杏叶制剂治疗痴呆的系统评价或Meta分析表明与安慰剂相比银杏叶有较好的临床疗效,与其他治疗痴呆的药物相似但具有更好的安全性;另有多个关于其他中药治疗VaD的系统评价或Meta分析结果亦显示了中药的优越性,这证明中医药在防治VaD中发挥着重要的作用。目前,有较多研究脑心通治疗VaD的临床研究,但其结果各异甚至是矛盾的[11-18]。为综合评价脑心通治疗VaD的临床疗效,本研究拟采用Cochrane协作网推荐的方法对当前发表的相关研究进行Meta分析,以期为临床用药提供参考。
1 资料与方法
1.1文献纳入和排除标准
1.1.1文献类型所有脑心通与西药对比治疗VaD的随机对照试验(RCT)或半随机对照试验,无论是否采用分配隐藏或盲法。
1.1.2研究对象确诊为VaD的患者,试验组和对照组的基线情况基本一致,具有可比性,种族及性别不限。诊断标准为相应时期较公认的标准(详见表1)。
1.1.3干预措施在其它处理措施相同的基础上,干预组加用脑心通,对照组加用西药。
1.1.4结局指标结局指标选择临床指标:①痴呆疗效:依据《中药新药治疗痴呆的临床研究指导原则》[19-20],以简易智能量表(MMSE)得分为主要参考指标,采用尼莫地平法计算,分为显效、有效和无效三个等级,总有效率=显效+有效;计算公式:[(治疗后积分-治疗前积分)÷治疗前积分]×100%,以百分数表示。显效:症状、体征明显改善,证候积分减少≥70%;好转:症状、体征均有好转,证候积分减少≥30%;无效:症状、体征无明显改善,甚或加重,证候积分减少不足30%。②中医证侯疗效:依据《中药新药治疗痴呆的临床研究指导原则》[19]或中国中医药学会内科延缓衰老专业委员会2002年《血管性痴呆诊断、辨证及疗效评定标准(研究用)》[21]判断,分为显效、有效和无效三个等级,总有效率=显效+有效;③对患者和医生实施盲法;④对结果评价实施盲法;⑤结果数据的完整性;⑥无选择性报告结果;⑦无其他偏倚来源。“Low risk”表示低偏倚风险,“High risk”表示高偏倚风险,“Unclear risk”表示文献对偏倚评估未提供足够的或不确定的信息。完全满足上述质量标准,发生偏倚的可能性最小;部分满足上述质量标准则发生偏倚的可能性为中度;完全不满足上述质量标准,发生偏倚的可能性为高度。采用各种量表行客观评分:MMSE、长谷川痴呆量表(HDS)或改良长谷川量表(HDS-R)、日常生活活动量表(ADL)、躯体性自理能力量表(PSMS)、Blessed行为量表评分(BBS)、自觉症状评分、简明精神病评定量表(BPRS)或社会功能调查表(FAQ);④不良反应:主要为胃部不适、恶心或食欲不振。

表1 纳入研究的一般特征
1.1.5排除标准①不符合纳入标准;②重要资料不全且联系作者无回复者;③重复发表(以中英文发表,以会议论文及期刊论文发表);④无法获取全文且联系作者未得到回复;⑤同一个机构的2个研究报道了相似的随访区间及相同的目标结果时,纳入质量更好或信息更全面的报道,并联系第一作者澄清分歧。
1.2检索策略2名评价员(李敏,谭晓敏)独立检索公开发表的研究,并交叉核对,遇有争议则第3位评价员(熊光润)介入并通过讨论达成一致。计算机检索中国生物医学文献服务系统(Sinomed)、中国期刊全文数据库(CNKI)、中文科技期刊全文数据库(VIP)和万方数据库(WANFANG)。同时手工检索纳入文献的参考文献,以期扩大检索范围。检索时间均为1990年至2011年11月30日。同时,从已查阅文章所附参考文献中手检可能漏查的文献。以Sinomed为例,中文检索策略为:#1血管性痴呆;#2脑心通;#3#1and#2。
1.3资料提取阅读全文后,由两名评价者(李敏,谭晓敏)独立进行资料提取,若遇分歧则第三名评价者(胡波)介入并通过探讨达成一致。内容包括:纳入研究的第一作者姓名、发表年限、研究对象情况(样本量、年龄、性别等)、干预的内容、结局指标。缺乏的资料试通过电话或邮件与作者联系进行补充。1.4质量评价由2名评价员(李敏,熊光润)按照Cochrane系统评价员手册5.1版偏倚风险评估标准[22],独立评估纳入的RCT,不一致的地方通过第3位评价员(胡波)介入并通过讨论达成一致。评价标准包括:①随机分配方案的产生;②分配方案隐藏;
1.5统计分析采用Cochrane协作网提供的Rev-Man 5.1软件对资料进行Meta分析。首先通过χ2和I2检验对同类研究间的异质性进行评价,若P≥0.1,I2≤50%,说明研究间同质性较好,使用固定效应模型进行合并;若P<0.1,I2>50%,说明研究间具有异质性,则首先对异质性来源进行分析,若无临床异质性则采用随机效应模型,若有临床异质性则根据可能出现的异质性因素进行亚组分析,如亚组只有一项研究则仍采用与Meta分析相同的统计量,必要时采用敏感性分析对检验结果的稳定性进行分析,若异质性过大则放弃Meta分析改为描述性分析。计数资料采用相对危险度(RR)作为分析统计量,对连续性资料,如使用测量工具相同,则采用加权均数差(MD)进行分析;若对相同变量使用不同测量工具,则采用标准化均数差(SMD)进行分析。所有分析均计算95%可信区间(CI)。同时,当纳入研究数≥9时,采用漏斗图进行发表偏倚的分析[23]。所有数据输入由李敏执行,谭晓敏负责监督。
2 结果
2.1文献检索结果初检出相关文献158篇,经筛选最终纳入8个研究[11-18],文献筛选流程如图1。

图1 文献检索流程图
2.2纳入研究的一般特征共纳入符合条件的8项研究536例患者。该8项研究均应用脑心通胶囊做为中药治疗组,其中3项研究[11-13]使用喜得镇、2项研究[14,18]采用都可喜、1 项研究[15]采用尼莫同片、1项研究[16]采用茴拉西坦胶囊、1 项研究[17]采用脑复新片做为西药对照(表1)。
2.3纳入研究的质量评价根据Cochrane协作网推荐的偏倚风险评估方法,纳入的8项研究基线具有可比性,但均有不同水平的偏倚(图2)。①在随机分组方面,所有纳入研究均提及“随机”,但均未进行详细描述,结合文中信息亦未能判定随机的真假,故判定为“unclear risk”。②所有研究均未报道是否实行分配隐藏,从文中信息能判定一个研究[11]实施之外,其余均未能进行判断。③在医生和患者盲法方面,1项研究[11]提及患者和医生双盲,并正确采用了双模拟的方法,故判定为“low risk”;其余研究尽管均未报道医生和患者的盲法,结合文中信息可判定此双盲法无法做到,故均判定为“high risk”。在评价者盲法方面,所有研究均未行评价者盲法的报道,从文中信息亦无法判断,故判定为“unclear risk”。④一项研究[15]报道了失访但未行相关的处理,故判定为“high risk”;其余研究均无失访、退出情况,判定为“low risk”。所有研究均完整的提供了研究数据及无选择性报告结果,判定为“low risk”。⑤2项研究[15,17]结合文中信息可以判定为有其他偏倚来源,故判定为“high risk”;其余研究均因信息不足而无法判断是否有选择性报告结果及是否有其它偏倚来源,故判定为“unclear risk”。

图2 偏倚风险图
2.4疗效分析
2.4.1总有效率7项研究[11-14,16-18]报道了痴呆临床疗效,按照诊断标准的不同分成了6个亚组,异质性分析提示各亚组间无异质性(P=0.96,I2=0%);按照对照组药物的不同分成了4个亚组,异质性分析提示各亚组间无异质性(P=0.65,I2=0%);按照治疗周期的不同分为2个月、3个月、6个月三个亚组,异质性分析提示各亚组间无异质性(P=0.82,I2=0%)。根据异质性分析的结果,可以认为各诊断标准、药物种类及治疗周期各个亚组间的差异可以忽略不计,故直接按照脑心通与西药的分组进行合并分析。各研究间同质性较好(P=0.87,I2=0%),故采用固定效应模型合并。Meta分析结果显示:与西药组相比,脑心通能够显著提高痴呆临床疗效总有效率,且差异有统计学意义(RR=1.25,95%CI:1.12~1.40,P <0.01)(图3)。
2项研究[11,15]报道了中医证侯疗效,各研究间同质性较好(P=0.24,I2=28%),故采用固定效应模型合并。Meta分析结果显示:与西药组相比,脑心通能够提高中医证侯疗效总有效率,但差异无统计学意义(RR=1.23,95%CI:0.95 ~1.60,P=0.11)(图4)。
2.4.2评分的变化7项研究[12-18]采用了MMSE评分(按照诊断标准、西药种类和治疗周期的亚组分析均提示亚组间无异质性),各研究间同质性好(P=0.44,I2=0%),故采用固定效应模型合并。Meta分析结果显示:与西药组相比,脑心通能够提高MMSE评分,且差异有统计学意义(MD=1.70,95%CI:1.17~2.23,P <0.01)(图5)。
4 项研究[12,14,16-17]采用了 HDS 评分(按照诊断标准、西药种类和治疗周期的亚组分析均提示亚组间无异质性),各研究间同质性较好(P=0.18,I2=39%),故采用固定效应模型合并。Meta分析结果显示:与西药组相比,脑心通能够提高HDS评分,且差异有统计学意义(SMD=0.61,95%CI:0.41~0.82,P<0.01)(图6)。
3 项研究[14-15,17]采用了 ADL 评分,各研究间具有异质性(P=0.0002,I2=89%),故采用随机效应模型合并。Meta分析结果显示:与西药组相比,脑心通能够降低ADL评分,但差异无统计学意义(MD=-1.87,95%CI:-4.81 ~1.07,P=0.21)(图 7)。采用逐个剔除法行敏感性分析,结果均未发生改变。
周伟[16]使用了FAQ评分发现,经治疗后脑心通组和茴拉西坦胶囊组FAQ评分均有降低,但两组间差异无统计学意义(MD=-0.05,95%CI:-1.09~1.19,P=0.93)。王伟佳[18]使用了 BBS 评分发现,经治疗后脑心通组和都可喜组BBS评分均有降低,但脑心通组降低的幅度更大,两组间差异有统计学意义(MD=-2.67,95%CI:-3.33 ~ -2.01,P <0.01);但其使用自觉症状评分发现,经治疗后两组自觉症状评分均有降低,但两组间差异无统计学意义(MD=-0.26,95%CI:-0.61 ~0.09,P=0.15)。郑德俊[15]使用了PSMS评分发现,经治疗后脑心通组和尼莫同组组PSMS评分均有降低,但两组间差异无统计学意义(MD=-0.59,95%CI:-1.22~0.04,P=0.07)。金爱国[17]使用了 BRPS 评分发现,经治疗后脑心通组和脑复新片组BRPS评分均有降低,但脑心通组降低的幅度更大,两组间差异有统计学意义(MD=-3.01,95%CI:-4.02 ~ -2.00,P <0.01)。
2.4.3不良反应4 项研究[12,14,16-17]报道了不良反应发生情况,各研究间同质性较好(P=1.00,I2=0%),故采用固定效应模型合并。Meta分析结果显示:与西药组相比,脑心通能够降低不良反应发生率,但差异无统计学意义(RR=0.75,95%CI:0.38~1.50,P=0.42)(图 8)。
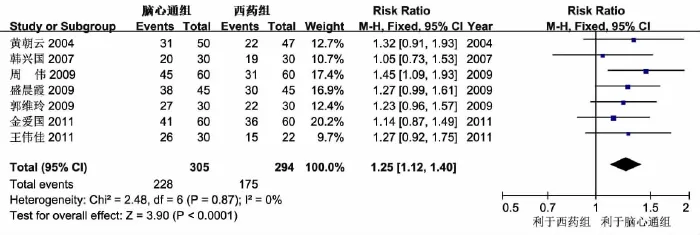
图3 临床疗效总有效率比较

图4 中医证侯疗效总有效率比较

图5 MMSE评分比较

图6 HDS评分比较

图7 ADL评分比较

图8 不良反应的发生情况比较
3 讨论
随着我国进入老龄化社会和脑血管疾病发病率的不断上升,作为最常见的老年性痴呆类型之一的VaD也明显增加,给社会和患者家庭带来了沉重的经济和精神负担,已经引起了医学界的极大关注。目前,临床上采用西药针对VaD病理过程中的某个环节治疗取得了一定的疗效,但西药尚无肯定的治疗方法和药物可以改善VaD的整个病程[1-2,4-6]。在中医理论中,VaD属于“痴呆”、“呆症”、“健忘”等范畴,认为其源在心脑,发病与肝脾肾关系密切。因此,中医治疗VaD一般多从脑、心、肾等不同脏腑及气、血、痰、瘀、火、郁等病机辨证论治。
脑心通胶囊是一种中药制剂,主要成分有黄芪、全蝎、地龙、三七、乳香、红花、赤芍、葛根等组成,具有:①益气活血、扩张血管、增加脑血流量、防止血栓形成、增强蛋白溶解活性、抑制血栓形成及溶栓的作用;②醒脑开窍、宜痹止痛,可达到有效保护神经、稳定血管、活化脑细胞等作用;③降脂抗凝,改善血液凝聚状态的作用;④能有效作用于血管而显著改善血管内皮功能、稳定粥样硬化斑块、抑制内膜增殖、缓解血管痉挛、保护脑梗死缺血再灌注晚期微血管的完整性;⑤对血管与血流有双重作用,能阻断脑血管发生发展的恶性病理链,从而更有效的治疗脑血管病[24-26]。
本Meta分析共纳入8个RCT,包括536例VaD患者,各RCT的试验组均采用口服脑心通胶囊,对照组采用口服西药,各试验组与相应对照组的基线相似。方法学质量评价结果显示均为中等。在改善临床疗效总有效率方面,脑心通能够显著提高痴呆临床疗效总有效率,且差异有统计学意义;尽管结果表明脑心通能够提高中医证侯总有效率,但差异无统计学意义。MMSE量表[27]是1975年Folstein编制的适用于老年认知功能障碍的一种筛查工具,积分越小,表示痴呆程度越重,本Meta分析结果表明脑心通能够提高MMSE评分,且差异有统计学意义;HDS量表[28]是日本学者编制的适用于老年认知功能障碍的一种筛查工具,积分越小,表示痴呆程度越重,Meta分析结果表明脑心通能够提高HDS评分,且差异有统计学意义;ADL量表主要用于评价日常生活活动能力,ADL积分越大,表示痴呆程度越重,Meta分析结果提示脑心通能够降低ADL评分,但差异无统计学意义;其余评分量表因皆有一个研究涉及,所以无法进行Meta合并,但均有脑心通组优于西药组的趋势。在不良反应上,脑心通能够降低发生率,但差异无统计学意义。
与前期的Meta分析[29]相比,本Meta分析其检索文献全面、对照组明确、效应指标妥当、格式更标准。由于纳入Meta分析的文献数目和样本量较少,故未采用漏斗图行发表偏倚分析。另外,本Meta分析尚存在以下不足,有待于进一步研究和完善:①国内临床证据等级偏低,缺乏高质量、标准化的RCT;②虽然对文献进行了广泛的检索,但诸如增刊、会议论文及部分灰色文献无法获取,且纳入研究信息的限制,该研究只能就相关指标予以评价,因而不能排除潜在的发表偏倚;③本研究纳入的RCT研究地点均在国内,可能影响研究结果的外推性;④受原始研究样本量的限制及研究设计的局限,使得对研究结果的真实性降低;⑤纳入RCT的诊断标准、服用剂量、治疗疗程等信息均不一样,尽管针对这些差异进行的亚组分析提示组间无异质性,但合并的综合效应值只能视为一个粗略的探讨,临床医师需审慎选择。
综上,当前证据表明脑心通治疗VaD是一种安全有效、值得推广的中成药物[30],但鉴于本研究的局限性,建议严格按照CONSORTS标准[31]设计高质量、大样本的随机盲法对照试验对其有效性进一步验证,并对其安全性进行评价。
[1]Moretti A,Gorini A,Villa RF.Pharmacotherapy and prevention of vascular dementia[J].CNS Neurol Disord Drug Targets,2011,10(3):370-390.
[2]Black SE.Vascular cognitive impairment:epidemiology,subtypes,diagnosis and management[J].J R Coll Physicians Edinb,2011,41(1):49-56.
[3]Plassman BL,Langa KM,McCammon RJ,et al.Incidence of dementia and cognitive impairment,not dementia in the United States[J].Ann Neurol,2011,70(3):418-426.
[4]Venketasubramanian N,Sahadevan S,Kua EH,et al.Interethnic differences in dementia epidemiology:global and Asia-Pacific perspectives[J].Dement Geriatr Cogn Disord,2010,30(6):492-498.
[5]Huang J,Meyer JS,Zhang Z,et al.Progression of mild cognitive impairment to Alzheimer's or vascular dementia versus normative aging among elderly Chinese[J].Curr Alzheimer Res,2005,2(5):571-578.
[6]Lee AY.Vascular dementia[J].Chonnam Med J,2011,47(2):66-71.
[7]Hobbelen JS,Tan FE,Verhey FR,Koopmans RT,et al.Prevalence,incidence and risk factors of paratonia in patients with dementia:a one-year follow-up study[J].Int Psychogeriatr,2011,23(7):1051-1060.
[8]Weinmann S,Roll S,Schwarzbach C,et al.Effects of Ginkgo biloba in dementia:systematic review and meta-analysis[J].BMC Geriatr,2010,10:14.
[9]Ernst E,Pittler MH.Ginkgo biloba for Dementia:A Systematic Review of Double-Blind,Placebo-Controlled Trials[J].Clinical Drug Invest,1999,17(4):301-308.
[10]Loew D.Value of Ginkgo biloba in treatment of Alzheimer dementia[J].Wien Med Wochenschr,2002,152(15-16):418-422.
[11]黄朝云,章军建,张晓琴.脑心通治疗血管性痴呆50例临床研究[J].中西医结合心脑血管病杂志,2004,2(l0):610-611.
[12]韩兴国,孙开珍,张荣沭,等.脑心通胶囊治疗血管性痴呆30例临床观察[J].健康大视野·医学分册,2007,(4):6-7.
[13]郭维玲,刘盛军,林维进.步长脑心通胶囊治疗血管性痴呆疗效观察[J]. 中国中医急症,2009,18(5):696.
[14]盛晨霞,苏南湘,何明大,等.步长脑心通胶囊治疗血管性痴呆的临床观察.当代医学,2009,15(27):157-158.
[15]郑德俊,徐俊,方穗雄,等.步长脑心通对血管性痴呆患者行为学障碍影响[J]. 中医药信息,2009,26(4):75-76.
[16]周伟,吴永斌,许贤瑞.脑心通胶囊治疗血管性痴呆患者临床观察[J]. 山东医药,2009,49(8):99-100.
[17]金爱国,金钊,张文玲.脑心通胶囊治疗血管性痴呆的疗效观察[J]. 实用心脑肺血管病杂志,2011,19(8):1319-1320.
[18]王伟佳.步长脑心通胶囊治疗脑血管性痴呆临床调查[J].中外医学研究,2011,9(20):119-120.
[19]中华人民共和国卫生部.中药新药临床研究指导原则[S].第1辑.1993:206.
[20]中华人民共和国卫生部.中药新药临床研究指导原则(试行).第2辑[S].北京:中国医药科技出版社,2002:98.
[21]田金州,韩明向.血管性痴呆诊断、辨证及疗效评定标准(研究用)[S]. 中国老年学杂志,2002,22(9):329-331.
[22]Higgins JPT,Green S(editors).Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0[updated March 2011].The Cochrane Collaboration,2011.Available from www.cochranehandbook.org.
[23]Egger M,Smith GD.Bias in location and selection of studies[J].BMJ,1998,316(7124):61-66.
[24]方正农,袁灿兴,颜乾麟,等.步长脑心通胶囊治疗脑卒中的临床研究[J].中西医结合心脑血管病杂志,2003,1(1):32-34.
[25]魏瑞,何明大.步长脑心通对血管性痴呆大鼠血管内皮细胞生长因子作用的影响[J].脑与神经疾病杂志,2006,14(2):108-110.
[26]何明大,刘石梅,苏南湘.脑心通胶囊对拟血管性痴呆大鼠学习记忆及抗氧化作用的影响[J].中西医结合心脑血管病杂志,2006,4(4):315-317.
[27]Dick JP,Guiloff RJ,Stewart A,et al.Mini-mental state examination in neurological patients[J].J Neurol Neurosurg Psychiatry,1984,47(5):496-499.
[28]Tsai N,Gao ZX.Validity of Hasegawa's Dementia Scale for screening dementia among aged Chinese[J].Int Psychogeriatr,1989,1(2):145-152.
[29]刘伟,肖建新,方瑾,李晟.步长脑心通治疗血管性痴呆的Meta分析[J]. 医学信息(中旬刊),2011,24(1):243-244.
[30]亓鲁光,王艳,管子函.步长脑心通步长脑心通胶囊治疗糖尿病合并脑动脉硬化症临床疗效观察[J].中国医药,2010,5(10):900-901.
[31]Bian Z,Liu B,Moher D,et al.Consolidated standards of reporting trials(CONSORT)for traditional Chinese medicine:current situation and future development[J].Front Med,2011,5(2):171-177.

