磁性灭藻剂的制备及性能分析
魏燕芳,刘鸿辉
(华侨大学化工学院,福建厦门361021)
磁性灭藻剂的制备及性能分析
魏燕芳,刘鸿辉
(华侨大学化工学院,福建厦门361021)
以壳聚糖为原料,用反相悬浮聚合法合成磁性壳聚糖微球(MCS),经进一步改性,制备出磁性灭藻剂——载铜磁性壳聚糖微球.采用傅里叶变换红光谱对样品进行表征,并研究MCS的载铜能力和载铜MCS的释铜性能.研究结果表明:硫酸铜初始质量浓度为750 mg·L-1,MCS用量为15 mg,p H值为5,吸附平衡时间为15 min,温度为25℃,是MCS对Cu2+的最佳载铜条件.载铜MCS的释铜量随着时间和用量的增加而增加,且载铜MCS的用量在比较低的情况下,理论上能保证有效而持续地灭藻;当p H值在6~8的范围内变化时,对释铜量影响不大.
磁性灭藻剂;磁性壳聚糖微球;反相悬浮聚合法;硫酸铜;吸附;缓释
目前,湖泊水作为供给水已占全国城市供水量的26%,而水体中藻类的大量繁殖给饮用水生产带来诸多危害,因此,去除水中藻类是给水工程中亟待解决的问题.硫酸铜作为一种广谱而高效的灭藻剂在国内外被广泛使用[1-3],它能与微生物蛋白质的半胱氨酸的巯基反应,使其钝化,并可破坏某些藻类的细胞壁、细胞膜及内含物,使其灭活甚至解体,从而杀死活体藻细胞.此法应用灵活,成本较低,但若直接投放到水体中会导致水中局部铜离子浓度上升,危害水生生物及人体健康.因此有必要研究一种缓释载铜灭藻剂,使其既可持续灭藻,又不会对环境造成危害.壳聚糖作为天然高分子化合物容易生物降解,含有羟基、氨基等功能团,具有较好的吸附性能.将其改性后制备的磁性壳聚糖微球具有磁响应性,可在外加磁场的作用下方便地分离,在细胞分离、固定化微生物、水处理等领域都有着广泛的应用[4-6].因此,磁性壳聚糖微球是载铜灭藻剂的理想载体.本文以壳聚糖为原料,制备磁性壳聚糖微球(MCS),研究其对铜离子的吸附性能;然后,在此基础上合成载铜磁性壳聚糖灭藻剂,研究其缓释铜的能力.
1 实验部分
1.1 试剂和仪器
1)试剂.壳聚糖(CTS,脱乙酰度为91%~92%);体积分数为25%戊二醛(BR级);磁流体(自制);液体石蜡(CP级);石油醚、无水硫酸铜、二乙氨基二硫代甲酸钠、酒石酸钾钠等均为分析纯.
2)仪器.NEXVS-470型傅里叶变换红外光谱仪(美国Nicolet公司),UV-3100型分光光度计(上海美谱达仪器有限公司),JJ-3型控温电动搅拌器(江苏金坛县佳美仪器有限公司),DHG-9031型电热恒温鼓风干燥箱(上海荣丰科学仪器有限公司).
1.2 磁性壳聚糖微球的制备[7]
在烧杯中依次加入20 m L,质量分数2%的壳聚糖醋酸溶液,2.0 m L的磁流体,4.0 m L的Span-80及80 m L的液体石蜡,常温下充分搅拌30 min;然后,加入4.0 m L,体积分数为25%的戊二醛,在40℃下反应60 min,升高温度到60℃反应4 h,产物依次用石油醚、丙酮、无水乙醇洗涤,过滤;最后,将样品于60℃下干燥,通过100目的筛子,备用.
1.3 磁性壳聚糖微球对Cu2+的吸附
称取一定量的MCS于三角锥瓶中,加入一定质量浓度的硫酸铜溶液中,恒温振荡一定时间后,取上层清液.用分光光度计测定溶液中剩余的Cu2+质量浓度,根据下式计算吸附量Q,即
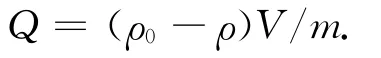
其中:ρ0,ρ分别表示吸附前、后溶液中Cu2+的质量浓度;V为溶液体积;m为吸附剂质量.
1.4 磁性灭藻剂的制备
在最优吸附条件下合成载铜磁性壳聚糖微球,离心过滤后烘干,即为载铜磁性灭藻剂.
1.5 载铜MCS的释铜能力
取一定量的载铜MCS于三角锥形瓶中,加入250 m L去离子水,室温下静置,每隔一段时间取上清液,测定溶液中Cu2+质量浓度,研究载铜MCTS的释铜情况.
2 结果与讨论
2.1 MCS对Cu2+的吸附作用
2.1.1 吸附时间对吸附的影响 准确称取15 mg的MCS,加入质量浓度为750 mg·L-1的硫酸铜溶液,于25℃下振荡吸附,分别在2,5,10,15,18,20 min时取样测定,结果如图1所示.由图1可知:刚开始一段时间内,MCS对Cu2+的吸附很快很快;15 min左右,吸附达到平衡,此后吸附变化不大,基本达到平衡.这表示开始时,Cu2+主要被吸附在MCS的外表面,吸附容易发生,速率极快.随着吸附过程的进行,MCS表面达到饱和,导致吸附速率变慢.吸附后期,吸附反应主要在MCS内表面进行,且质量浓度推力越来越小,吸附基本达到平衡.
2.2.2 硫酸铜初始质量浓度对吸附的影响 准确称取15 mg的MCS于锥瓶中,在25℃下振荡,平衡吸附15 min,分别测量Cu2+质量浓度为100,200,300,400,500,600,750,800 mg·L-1时的平衡吸附量,结果如图2所示.由图2可以看出:当硫酸铜质量浓度达到750 mg·L-1之前,吸附量基本是呈线性增加的;当硫酸铜质量浓度达到750 mg·L-1时,吸附量达到最大值296 mg·g-1,而后趋于平衡且略有下降趋势,这可能是因为少量的Cu2+释出所致.
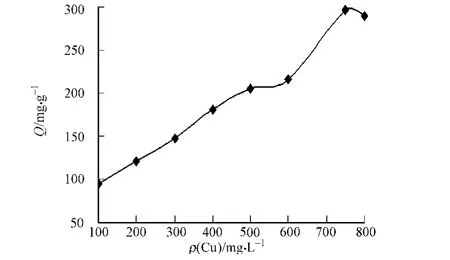
图2 硫酸铜初始质量浓度对吸附的影响Fig.2 Effect of CuSO4initial concentration on adsorption
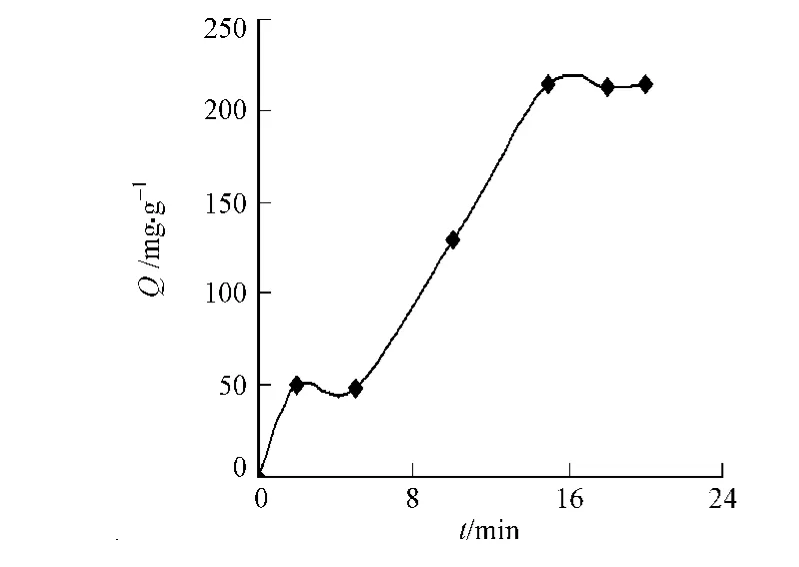
图1 吸附时间对吸附的影响Fig.1 Effect of adsorption time on adsorption
2.2.3 MCS初始用量对吸附的影响 在Cu2+初始质量浓度为750 mg·L-1下,于25℃振荡吸附15 min,分别测定MCS初始用量为5,10,15,20,25,30 mg对Cu2+的吸附量的影响,结果如图3所示.
由图3可知:随着MCS用量的增加,吸附量不断增加;当用量增加到15 mg时,吸附量达到最大值220 mg·g-1;而后MCS用量继续增加,吸附量反而减少.出现这一现象的原因有可能是用量在15 mg之前,随着载体的氨基数目的增加,吸附量随之增大;当用量大于15 mg时,部分螯合基团利用不充分.另外,为了维持吸附解吸的动态平衡,部分Cu2+释放,导致吸附量下降.
2.2.4 p H值对吸附的影响 p H值是影响吸附作用最主要的因素,较多的研究者认为p H值能影响MCS上的活性位点的功能[8].在Cu2+初始质量浓度为750 mg·L-1,MCS用量15 mg时,于25℃振荡吸附15 min,考察p H值为3,3.5,4,4.5,5,5.5对吸附量的影响,如图4所示.由图4可知:随着p H值的增加,吸附量上升,在p H=5附近,吸附量最高;当p H值大于5.5时,Cu2+会形成氢氧化铜沉淀,吸附量下降[9].在较低p H值时,MCS对Cu2+的吸附量较低,是由于载体上-NH2的质子化反应使能够螯合Cu2+的-NH2数目减少;同时吸附剂表面带正电荷与同种电荷的金属离子斥力增强,吸附减弱[10].随着p H值升高,MCS中的游离-NH2增多,有利于增加其对金属离子的吸附.
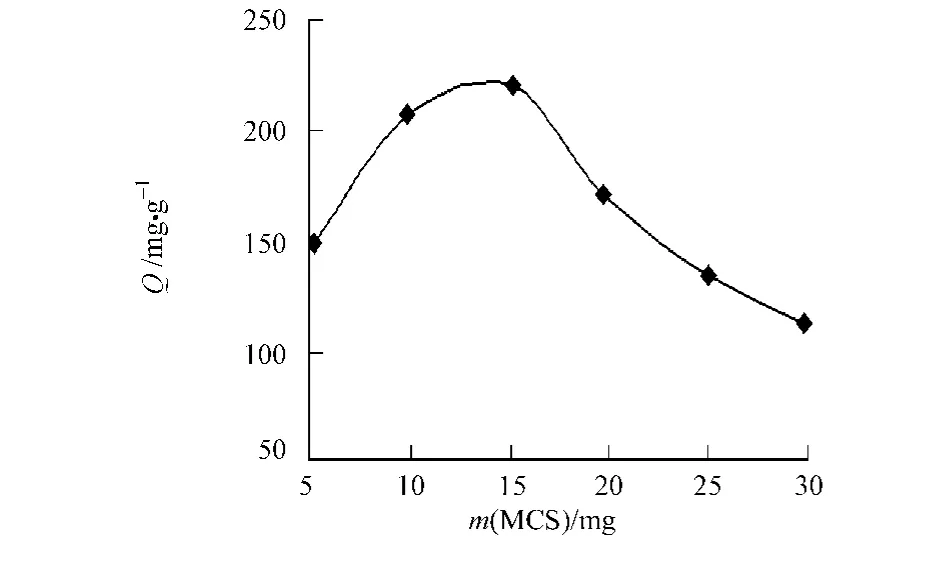
图3 MCS初始用量对吸附的影响Fig.3 Effect of MCS initial dosage on adsorption

图4 p H值对吸附的影响Fig.4 Effect of p H on adsorption
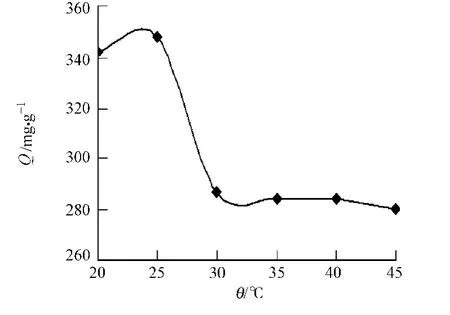
图5 温度对吸附的影响Fig.5 Effect of temperature on adsorption
2.2.5 温度对吸附的影响 其他条件不变,分别在20,25,30,35,40,45℃时测定MCS对Cu2+吸附量的影响,如图5所示.由图5可知:在温度为25℃时,Cu2+的吸附量最大;继续升高温度,吸附量降低.说明MCS对Cu2+的吸附可能为放热过程,温度太高不利于反应进行.
2.3 产物红外光谱表征
采用红外光谱仪,测定CTS,MCS及载铜MCS的红外吸收光谱,如图6所示.从图6(a)可知:在1 710 cm-1处的小峰是悬挂醛基的吸收峰,出现的原因,一方面是由于这个交联过程中,戊二醛过量;另一方面可能是当戊二醛的一个醛基与壳聚糖分子中的-NH2反应后,由于壳聚糖大分子的刚性和缠绕,会造成某些氨基由于空间原因,无法与戊二醛分子的另一个醛基交联,而出现“悬垂”醛基.在1 630 cm-1处,出现新的Shiff键C=N特征吸收峰,表明戊二醛与壳聚糖的交联反应确已发生;在610 cm-1处的强吸收峰为对应为Fe3O4键的特征峰,表明Fe3O4被壳聚糖包覆在内[11].
从图6(b)可以发现,MCS和载铜MCS谱线的3 480 cm-1,3 511 cm-1处是羟基伸缩振动吸收峰,在与Cu2+配合之后,载铜MCS谱线的羟基伸缩振动吸收峰红移,且大大减弱.说明MCS的羟基与Cu2+发生了配位作用[12].
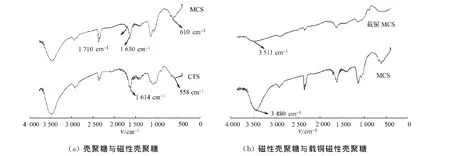
图6 产物的红外吸收光谱图Fig.6 FTIR spectra of MCS and MCS-Cu
2.4 磁性壳聚糖微球对Cu2+的解吸作用
2.4.1 时间对Cu2+释放的影响 称取15 mg的载铜MCS,加入到250 m L的去离子水中,静置观察随着时间的变化其释铜情况,结果如图7所示.由图7可以看出:刚开始时,Cu2+的释放速率较快;约10 h后,释放速率明显减缓且趋于平衡.实验结果显示:载铜MCS能持续释放Cu2+且持续时间长,24 h后释放量可达2.26 mg·L-1.这表明,当将载铜MCS投到富营养化水体中,能够持续缓慢地释放出Cu2+,保持其杀灭能力,达到除藻效果.
2.4.2 载铜MCS用量对Cu2+释放的影响 称取15,30,40,50,60,70 mg的载铜MCS,加入到250 m L的去离子水中,静置观察不同载铜MCS用量对释铜量的影响,结果如图8所示.由图8可知:随着载铜MCS用量的增加,释铜量也逐渐增加,且增长趋势一致,都是先呈线性增长,而后释放速率明显减慢,释铜量也趋于平衡.常用灭藻剂CuSO4有效用量一般为0.3~0.7 mg·L-1,而载铜MCS的用量为15 mg(即60 mg·L-1)时,释放24 h后,释铜量可达0.618 mg·L-1.因此,载铜MCS在较低用量时就能保证有效灭藻,且持续较长的时间.

图7 时间对解吸的影响Fig.7 Effect of time on desorption

图8 载铜MCS用量对释铜量的影响Fig.8 Effect of dosage of MCS-Cu on desorption

图9 p H值对解吸的影响Fig.9 Effect of p H on desorption
2.4.3 p H值对Cu2+释放的影响 称取15 mg的载铜MCS于p H值分别为3,4,5,6,7,8的去离子水中,静置观察不同p H值对载铜MCS释铜量的影响,结果如图9所示.由图9可知:当p H值较低时,体系中的H+与MCS结构上的-NH2形成了-NH3+,结果影响到MCS对Cu2+的螯合,显示出较大的释铜能力;随着p H值的提高,载铜MCS释铜的速率减小;在为p H值为6~8的范围内,对释铜能力影响不大,表现为一条平稳的曲线.富营养化水体一般呈弱碱性,正好处于曲线平稳阶段,说明载铜MCS在富营养化水体中能够缓慢释放Cu2+,又不会导致局部Cu2+质量浓度过高[13].
3 结论
1)采用反相悬浮聚合法制备磁性MCS,进一步合成了载铜磁性MCS,对CTS,MCS和载铜MCS进行红外表征,说明制备反应成功.
2)MCS对铜离子的吸附实验结果表明:MCS对Cu2+的吸附最佳条件为铜离子初始质量浓度为750 mg·L-1,MCS用量为15 mg,p H=5,吸附平衡时间为15 min,温度为25℃.
3)载铜MCS释铜实验结果表明:释铜量随着时间的增加而增加,p H值在6~8范围内波动时,对释铜能力影响不大;释铜量随载铜MCS用量的增加而增加,载铜MCS在较低用量时就能保证有效灭藻,且持续时间长.
[1] WILDE K L,STAUBER J L,MARKICH S J,et al.The effect of p H on the uptake and toxicity of copper and zinc in a tropical freshwater algae(Chlorella sp.)[J].Archives of Environmental Contamination Toxicology,2006,51(2):174-185.
[2] BOSSUYT B T,JANSSEN C R.Copper toxicity to different field-collected cladoceran species:Intra-and inter-species sensitivity[J].Environmental Pollution,2005,136(1):145-154.
[3] 赵小丽,宋立荣,张小明.硫酸铜控藻对浮游植物群落的影响[J].水生生物学报,2009,33(4):596-601.
[4] LIU Xiao-wang,HU Qi-yan,FANG Zhen,et al.Magnetic chitosan nanocomposites:A useful recyclable tool for heavy metal ion removal[J].Langmuir,2009,25(1):3-8.
[5] ELWAKEEL K Z.Removal of reactive black 5 from aqueous solutions using magnetic chitosan resins[J].Journal of Hazardous Materials,2009,167(1/2/3):383-392.
[6] FANG Hua,HUANG Jun,DING Li-yun,et al.Preparation of magnetic chitosan nanoparticles and immobilization of laccase[J].Journal of Wuhan University of Technology-Materials Science Edition,2009,24(1):42-47.
[7] 洪爱真,魏燕芳,陈盛.磁性壳聚糖微球对酸性偶氮染料废水的脱色研究[J].福建轻纺,2003(2):1-5.
[8] 李琼,余燕平,王振东.壳聚糖对废水中Cu2+的吸附研究[J].工业水处理,2003,23(4):30-32.
[9] 魏永锋,张苏敏,杭超伦,等.壳聚糖Cu(Ⅱ)配合物的合成及吸附性能[J].西北大学学报:自然科学版,2005,35(4):413-415.
[10] 刘娟.壳聚糖改性及其吸附性能研究[D].太原:山西大学,2003:28-29.
[11] 余艺华,薛博,孙彦,等.壳聚糖亲和磁性毫微粒的制备及其对蛋白质的吸附性能研究[J].高分子学报,2000(3):340-344.
[12] 毕双玉,张全启,徐甲坤,等.壳聚糖铜抑菌剂的制备及其应用研究[J].中国海洋大学学报:自然科学版,2007,37(增刊1):200-202.
[13] 刘斌,孙向英,徐金瑞.改性壳聚糖絮凝螯合及释放Cu2+的性能研究[J].华侨大学学报:自然科学版,2003,24(4):364~368.
Preparation and Characterization of Magnetic Algicide
WEI Yan-fang,LIU Hong-hui
(College of Chemical Engineering,Huaqiao University,Xiamen 361021,China)
With chitosan as raw material,magnetic chitosan microspheres(MCS)were prepared through inverse suspension cross-linking,then a new magnetic algicide—magnetic chitosan microspheres carrying copper(i.e.MCS-Cu)was prepared by further modification,and its structure was characterized by infrared spectrum.The adsorption ability of MCS toward Cu2+and desorption performance of MCS-Cu toward Cu2+were studied.Results showed that the optium adsorption as follows:initial concentration of Cu2+was 750 mg·L-1,the dosage of MCS was 15 mg,p H was 5,adsorption equilibrium time was 15 min,temperature was 25℃.The quantity of Cu2+released from MCS-Cu increased with time extending and raise of MCS-Cu dosage,and theoretically,it could guarantee removal efficiency of algae efficiently and continually.But the quantity of Cu2+released from MCS-Cu didn′t change obviously when p H varied from 6 to 8.
magnetic algicide;magnetic chitosan microspheres;inverse suspension cross-linking;copper sulfate;adsorption;desorption
O 636.1
A
(责任编辑:陈志贤 英文审校:刘源岗)
1000-5013(2012)05-0547-05
2011-12-29
魏燕芳(1979-),女,讲师,主要从事水环境污染治理的研究.E-mail:weiyanfang@hqu.edu.cn.
中央高校基本科研业务费专项资金资助项目,华侨大学科研基金资助项目(10 HZR11)

