欧洲型和美洲型PRRSV双重PCR 检测方法的建立
张松林,刘 磊,张太翔,马永彪,王文秀,肖 娜,沈志强,*
(1.山东省滨州畜牧兽医研究院,山东滨州256600;2.山东省绿都生物科技有限公司,山东滨州256600;3.潍坊出入境检验检疫局,山东潍坊261041)
猪繁殖与呼吸综合征(Porcine reproductive and respiratory syndrome,PRRS)于1987在美国首次发现,目前该病已在全世界范围内流行,对养猪业造成了重大的经济损失。在美国,每年因为PRRS造成的经济损失达6.6亿美元[1]。该病的主要特征是母猪繁殖障碍,哺乳仔猪死亡率升高,各年龄段猪特别是哺乳和保育阶段仔猪的呼吸道疾病以及生长和育肥猪的流感样症状。在我国,自1996年首次分离到PRRSV以来,尤其2006年春季流行的高致病性PRRS给我国的养猪业带来了巨大的经济损失[2-3]。按照血清型和遗传性差异,PRRSV可划分为欧洲型(基因I型,代表株Lelystad virus,LV)和美洲型(基因Ⅱ型,代表株VR2332)。目前,根据世界各地分离株的基因变异程度,欧洲型和美洲型PRRSV又被划分为几个不同的系统进化树[4]。
PRRSV属于动脉炎病毒科动脉炎病毒属(Arterivirus)成,其基因组为不分节段的单股正链RNA,全长约15.1kb~15.5kb,直径为50nm~65 nm,包括9个开放读码框(ORF1a,ORF1b,ORF2~7)。PRRSV基因组两端为对RNA合成过程起调控作用的非编码区,其中5'端具有甲基化的帽状结构和3′poly(A)尾[5-7]。ORF1a和 ORF1b约占全基因组的75%,通过核糖移码机制,翻译得到2个大的聚合蛋白pp1a和pp1ab。通过4种蛋白酶(位于Nsp1的PCPa、PCPβ,位于 Nsp2的CP,位于 Nsp4的SP),RNA依赖性RNA聚合酶(NSP9),解旋酶(NSP10),核酸内切酶(NSP11)的作用,pp1a和pp1ab被切割产生14个非结构蛋白(non-structural proteins,NSPs)[6-7]。迄今为止,除了复制、切割、聚合酶活性外,关于这些非结构蛋白的其他功能还知之甚少。
欧洲型和美洲型PRRSV之间存在抗原性差异,二者结构蛋白氨基酸同源性为55%~79%。欧、美洲型毒株之间同源性ORF2为65%~67%、ORF3为61%~64%、ORF4为63%~66%、ORF5为61%~63%、ORF6为79%~81%、ORF7为67%。ORF6和ORF7基因序列在美洲型毒株内和欧洲型PRRSV毒株内相对保守,同源性达96%~100%。有学者还比较了10个美洲型毒株ORF2~ORF7序列,发现美洲型毒株间的核苷酸差异在2.5%~7.9%间,但与LV株比较差异则达35%,因为这些核苷酸差异零星分布于结构基因中,因此无法解释导致各PRRSV株明显的遗传性差异的机制[8]。
我国每年从欧洲国家进口生猪,其中以英国和法国为最多,分别占进口生猪总数的21%和18%左右[9]。然而,关于欧洲型PRRSV的报道却很少。为调查我国欧洲型和美洲型PRRSV流行情况,同时减少2个亚型检测的工作量,本文根据GenBank上已发表的美洲型PRRSV、欧洲型PRRSV的基因组全序列,分别设计了2对能特异性扩增欧洲型和美洲型PRRSV的引物,建立并优化了可同时检测欧洲型和美洲型PRRSV的双重PCR方法。本方法的建立对这两种病毒亚型的快速诊断有十分重要的意义。
1 材料与方法
1.1 材料
1.1.1 病毒和细胞 Marc-145细胞,2株PRRSV分离株AME株和DY株均由山东省兽医生物技术重点开放实验室分离、鉴定和保存。
1.1.2 工具酶和主要试剂 LATaqDNA聚合酶和Oligo d(T)18为宝生物工程(大连)有限公司产品;MLV反转录酶,Trizol Reagent为invitrogen公司产品;其余的化学试剂均为进口或者国产分析纯。
1.2 方法
1.2.1 引物的设计与合成 根据GenBank上的PRRSV欧洲型LV株(登录号:M96262)和PRRSV美洲型VR2332株(登录号:AY150564)的全基因序列,分别在各病毒基因组的保守区域用Primer Premier 6软件设计2对特异性扩增引物(其中欧洲型为815bp,美洲型为329bp),并由上海生工生物工程技术服务有限公司合成,引物序列信息见表1。

表1 PCR引物名称,序列及位置Table 1 The name,sequence and position of primers for PCR
1.2.2 病毒核酸的提取和PRRSV基因组cDNA的合成 参照Trizol说明书提取样品(细胞,血清,组织)总RNA,溶解到50μL无RNA ddH2O中,置-70℃保存备用。取PRRSV样品10μL RNA作为模板,进行cDNA的合成。反转录引物用Oligo d(T)18。反应体系为:10μL RNA模板,2μL 10×反转录缓冲液,1μL Oligo d(T)18,1μL M-MLV反转录 酶,2μL dNTP (10mmol/L),4.0μL 无RNA ddH2O。反应条件为42℃60min,99℃5 min,4℃5min。
1.2.3 单项PCR扩增 用各自病毒的特异引物进行单项PCR,在PCR反应管中分别加入:病毒cDNA 5μL,上下游引物(10μmol/L)各1μL,dNTP(2.5mmol/L)4μL,10×LATaqDNA 聚合酶缓冲液2.5μL,LATaqDNA聚合酶(5U/μL)0.5 μL,加ddH2O至25μL。欧洲型PRRSV PCR反应参数:95℃5min;94℃30s,55℃30s,72℃1min,30个循环;72℃10min。美洲型PRRSV PCR反应参数:95℃5min;94℃30s,55℃30s,72℃30s,30个循环;72℃10min。
1.2.4 双重PCR扩增 将欧洲型和美洲型PRRSV的引物和模板进行混合,进行PCR扩增。反应条件为:95℃5min;94℃30s,55℃30s,72℃1min,30个循环;72℃10min。
1.2.5 PCR特异性检测 在PCR反应管中加入猪日本脑炎病毒(JEV)模板、猪瘟病毒(CSFV)模板、猪流行性腹泻病毒(PEDV)模板、猪传染性胃肠炎病毒(TGEV)模板、猪伪狂犬病毒(PRV)模板、猪细小病毒(PPV)模板、猪圆环病毒2型(PCV-2)模板以及欧洲型和美洲型PRRSV模板,进行PCR特异性检测。PCR程序为:95℃5min;94℃30s,55℃30s,72℃1min,30个循环;72℃10min。在此检测试验中,除PRRSV外,其他每种病毒的阴性对照都添加了2对PRRSV引物,病毒扩增采用特异性引物。
1.2.6 PCR反应条件的优化 分别按照下列条件进行多重PCR以确定各自的最佳条件:①退火温度:选择53.9、55.1、56.3、57.5、58.7℃进行梯度PCR。②引物浓度:选择25、12.5、6.25、2、1、0.5 μmol/L进行反应。③扩增增强剂:甜菜碱和甘油分别按30、80、150g/L加入。
2 结果
2.1 单项PCR扩增结果
反应结束后,PCR产物各取5μL,在8g/L琼脂糖凝胶上进行电泳分析。LV株扩增出一条800 bp大小的条带,VR2332株扩增出一条300bp大小的条带,大小与预期设计相符(图1)。
2.2 双重PCR扩增结果
将欧洲型和美洲型PRRSV的引物和模板进行混合,进行双重PCR扩增,2种PRRSV亚型均扩增出相应大小的条带(图2)。

图1 单项PCR扩增结果Fig.1 The amplification results of single PCR products

图2 双重PCR扩增结果Fig.2 The amplification results of duplex PCR products
2.3 PCR特异性试验结果
以欧洲型和美洲型PRRSV引物均扩增不出JEV、CSFV和PEDV等病毒条带,而以各个检测病毒特异引物均能得到特异性目的条带(图3)。说明本文的2对PRRSV特异性好,可以用于临床检测。

图3 PCR特异性检测结果Fig.3 The detection results of PCR specificity
2.4 PCR反应条件的优化结果
本研究对影响PCR扩增效果的退火温度、引物浓度、Taq浓度以及PCR扩增增强剂进行了探索研究。在不同退火温度扩增试验中,53.9℃~58.7℃各个温度均能扩增出2个亚型的特异条带,且各个温度扩增组均无非特异性扩增,因此53.9℃~58.7℃5个退火温度均可用于本研究的PCR反应(图4)。在不同退火温度扩增试验中,1μmol/L~25μmol/L引物浓度均可特异扩增出2个亚型PRRSV产物,伴随着引物浓度的增加,引物二聚体条带逐渐增加。0.5μmol/L扩增组只能扩增出美洲型PRRSV产物,因此,本研究最佳引物浓度为1μmol/L(图5)。在PCR扩增增强剂试验中,加入30、80、150mL/L的甘油均无法扩增出欧洲型产物(图6),加入80g/L 和150g/L 的甜菜碱 均可PRRSV扩增出欧洲型和美洲型PRRSV特异性条带,而加入30g/L甜菜碱试验组,只能扩增出美洲型PRRSV产物(图7)。
3 讨论
尽管全世界众多的科学家和科研机构投入大量的精力研究PRRSV,但PRRS防控仍然不理想。PRRSV就像人类免疫缺陷病毒(HIV)和丙型肝炎病毒(HCV)一样,其防控和研发有效疫苗面临巨大的挑战。对于PRRSV检测来说,由于病毒自身基因高度变异特性,研究人员通常选择不同亚型均高度保守的区域进行引物设计和扩增。由于PRRSV结构蛋白M和N是所有不同亚型较保守基因,因此M和N蛋白基因被认为是理想的PRRSV检测候选基因[10-16]。
与以往文献报道不同,本研究的引物设计选择了PRRSV Nsp9和Nsp10部分区域。Nsp9和Nsp10-11是尼多病毒最保守蛋白[17]。Nsp9编码RNA依赖性RNA聚合酶(RNA-dependent RNA polymerase,RdRp),它由复制功能区及其上游未知功能区域组成。Nsp10具有解旋酶活性,包含有锌指结构(Zinc finger,ZF),同Nsp9一起组成动脉炎病毒RNA合成的关键酶。ZF包含13个十分保守的半胱氨酸和组氨酸残基,对于维持ATPase和解旋酶活性是必须的[18]。Nsp11具有内切核糖核酸酶(endoribonuclease,NendoU)活性和抑制干扰素产生功能,并且在所有尼多病毒共有的 “自杀酶”[19]。

图4 最佳退火温度的测定结果Fig.4 The detecting results of optimal annealing temperature
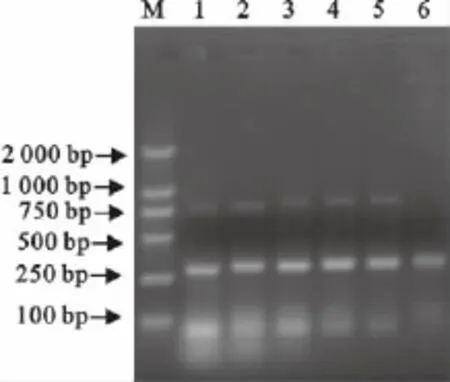
图5 不同引物浓度扩增结果Fig.5 The amplified results with different primer concentrations

图6 不同甜菜碱浓度扩增结果Fig.6 Different betaine concentration amplification results

图7 不同甘油浓度扩增结果Fig.7 Different glycerol concentration amplified results
本研究参考PRRSV欧洲型LV株和美洲型VR2332株的NSP9和NSP10部分区域设计了2对引物,试验结果表明,该引物对LV株和VR2332具有高度特异性。无论单项PCR还是双重PCR扩增结果,除了目的条带外,均无其它非特异性扩增杂带(图1和图2)。因此,本文所建立的方法适用于实验室快速检测欧洲型和美洲型PRRSV。
影响多重PCR效果的因素很多,主要包括退火温度、引物浓度、Taq浓度和 Mg2+浓度等。此外,对于一些二级结构复杂的基因需要使用扩增增强剂。为了使双重PCR具有更稳定的扩增效果,降低一些生物试剂的使用量,本研究对退火温度等因素进行了优化。结果显示本研究在经典PCR反应条件下可以完成扩增,将引物浓度调整至1μmol/L并加入80g/L甜菜碱可提高反应的特异性,并特异性增加扩增产物量。
我国每年从欧洲国家进口大量的生猪,但欧洲型PRRSV的相关检测、功能基因组和蛋白质组学等研究却很少报道。本研究建立的方法具有快速、简便、特异性强等优点,可同时检测欧洲型和美洲型PRRSV毒株。本方法的建立,对于跟踪、监测进口生猪的PRRSV不同亚型的感染情况具有重要意义。
[1] Lalit K B,Phat X D,Fernando A,et al.Cellular Poly(C)binding proteins 1and 2interact with porcine reproductive and respiratory syndrome virus nonstructural protein 1and support viral replication[J].J Virol,2011,85(24):12939-12949.
[2] Li Y F,Wang X L,Bo K,et al.Emergence of a highly pathogenic porcine reproductive and respiratory syndrome virus in the Mid-Eastern region of China[J].Vet J,2007,174(3):577-584.
[3] Dokland T.The structural biology of PRRSV[J].Virus Res,2010,154(1-2):86-97.
[4] Fang Y,Schneider P,Zhang W P,et al.Diversity and evolution of a newly emerged North American Type 1porcine arterivirus:analysis of isolates collected between 1999and 2004[J].Arch Virol,2007,152(5):1009-1017.
[5] Huang Y W,Fang Y,Meng X J.Identification and characterization of a porcine monocytic cell line supporting porcine reproductive and respiratory syndrome virus(PRRSV)replication and progeny virion production by using an improved DNA-launched PRRSV reverse genetics system [J].Virus Res,2009,145(1):1-8.
[6] Fang Y,Snijder E J.The PRRSV replicase replicase:Exploring the multifunctionality of an intriguing set of nonstructural proteins[J].Virus Res,2010,154(1-2):61-76.
[7] Wissink E H J,Kroese M V,Van W,et al.Envelope protein requirements for the assembly of infectious virions or porcine reproductive and respiratory syndrome virus [J].J Virol,2005,79(19):12495-12506.
[8] Murtaugh M P,Faaberg K S,Laber J,et al.Genetic variation in the PRRS virus[J].Adv Exp Med Biol,1998,440:787-794.
[9] 张 宁.2011年中国养猪行业发展总体概况,http://www.chinaswine.org.cn/piaofu/20120316/,2012-03-16.
[10] Dal Y K,Troy J K,Kyle H,et al.Insertion and deletion in a non-essential region of the nonstructural protein 2(nsp2)of porcine reproductive and respiratory syndrome(PRRS)virus:effects on virulence and immunogenicity [J].Virus Genes,2009,38(1):118-128.
[11] Kim S H,Roh I S,Choi E J,et al.A molecular analysis of European porcine reproductive and respiratory syndrome virus isolated in South Korea[J].Vet Microbiol,2010,143(2-4):394-400.
[12] Wieringa R,de Vries A A,Van D M J,et al.Structural protein requirements in equine arteritis virus assembly [J].J Virol,2004,78(23):13019-13027.
[13] Deshpande A,Wang S,Walsh M A,et al.Structure of the equinearteritis virus nucleocapsid protein reveals a dimer-dimer arrangement[J].Acta Crystallogr D Biol Crystallogr,2007,63(5):581-586.
[14] Lee C,Hodgins D,Calvert J G,et al.Mutations within the nuclear localization signal of the porcine reproductive and respiratory syndrome virus nucleocapsid protein attenuate virus replication[J].Virology,2006,346(1):238-250.
[15] Song C,Lu R,Bienzle D,et al.Interaction of the porcine reproductive and respiratory syndrome virus nucleocapsid protein with the inhibitor of MyoD family-a domain-containing protein[J].Biol Chem,2009,390(3):215-223.
[16] Gorbalenya A E,Enjuanes L,Ziebuhr J,et al.Nidovirales:evolvingthe largest RNA virus genome [J].Virus Res,2006,117(1):17-37.
[17] Seybert A,Posthuma C C,Snijder E J,et al.A complex zinc finger controls the enzymatic activities of nidovirus helicases[J].J Virol,2005,79(2):696-704.
[18] Nedialkova D D,Ulferts R,Born E,et al.Biochemical characterization of arterivirus nonstructural protein 11reveals the nidovirus-wide conservation of a replicative endoribonuclease[J].J Virol,2009,83(11):5671-5682.
[19] Nedialkova D D,Ulferts R,Born E,et al.Biochemical characterization of arterivirus nonstructural protein 11reveals the nidovirus-wide conservation of a replicative endoribonuclease[J].J Virol,2009,83(11):5671-5682.

