PS/SiO2复合微球包覆过程的可控研究
杨 侃,叶 莹,张高文
(湖北工业大学化学与环境工程学院,湖北 武汉430068)
近年来具有光、电、磁和化学等特性的有机-无机核壳型复合微球一直是人们研究的热点[1].其中以SiO2为无机层的复合微球因其优良的化学稳定性和价廉等优点而备受关注[2-4].制备SiO2复合微球的方法主要有层层自组装法(LBL)和溶胶凝胶法[5-6].Caruso[7]利用层层自组装法(LBL)在 PS微球上交替吸附聚二甲基二烯丙基氯化铵(PDADMAC)、聚对苯乙烯磺酸钠(PSS)、PDADMAC和SiO2纳米粒子,制备出壳层厚度均匀的PS/SiO2复合微球.为提高 SiO2壳层稳定性,Tissot[8]和邓伟[9]等在表面含硅羟基的PS微球上经TEOS的溶胶凝胶反应制备了核壳结构PS/SiO2复合微球,微球表面的可反应性基团与无机前驱体的化学反应,或直接利用了聚合物胶体粒子表面与无机纳米粒子间的静电引力作为吸附动力,并取得良好的效果;但很少有文献对SiO2包覆过程中微球表面的电位变化进行报道.本文直接采用了经甲基丙烯酰氧乙基三甲基氯化铵(DMC)共聚改性的表面带正电的PS微球为模板,经溶胶凝胶过程制备了PS/SiO2微球,利用微球表面电荷和TEOS的用量实现对壳层厚度的调控,对包覆过程中不同制备条件下微球表面电荷密度的变化进行了系统研究,并对复合微球形貌进行了表征.
1 实验部分
1.1 实验原料
苯乙烯(St),分析纯,通过5%NaOH提纯去除阻聚剂;偶氮二异丁腈(AIBN),分析纯,重结晶提纯;甲基丙烯酰氧乙基三甲基氯化铵(DMC),分析纯;聚乙烯比咯烷酮(PVP),分析纯;无水乙醇,分析纯;正硅酸乙酯(TEOS),分析纯;氨水,分析纯.
1.2 阳离子PS微球的制备
实验中以乙醇和水为混合介质,以偶氮二异丁腈(AIBN)为引发剂,以甲基丙烯酰氧乙基三甲基氯化铵(DMC)为共聚单体,采用分散聚合法制备了单分散阳离子PS微球.取约1g的PVP置入四口烧瓶中,加入水和无水乙醇配成的混合介质(V(水)∶V(无水乙醇)=8∶2)100mL,搅拌速度为160r/min,温度控制在70℃,一次性加入10g St、0.2g AIBN和适量的DMC,氮气保护下反应12h,反应完成后将PS微球用乙醇洗涤多次,最后将PS微球分散在无水乙醇中备用.
1.3 PS/SiO2 核壳微球的制备
取约0.5g自制的PS微球,用90mL的无水乙醇超声分散到三颈瓶中,然后取一定量的正硅酸乙酯(TEOS)加入反应体系中,待分散均匀后,将2 mL氨水缓慢滴加到反应体系,继续搅拌反应9h,再用乙醇离心洗涤多次,即可得到PS/SiO2核壳微球.
1.4 结构表征
采用美国Brookhaven公司Zetaplus型Zeta电位及激光粒度分析仪测定微球粒径及其表面Zeta电位.采用日本电子JMS6390型扫描电镜和日本电子JEM-2100F型透射电镜观察微球的微观形貌.
2 结果与讨论
2.1 氨水用量对微球包覆过程的影响
采用分散聚合法,DMC用量为0.4%时制备得到的PS微球表面的电荷密度可达+45.62mV;以此PS微球为模板,TEOS为前驱体,TEOS用量为2g,氨水用量分别为1mL、2mL、3mL、4mL,经溶胶凝胶法制备了PS/SiO2复合微球.在包覆过程中采用Zeta电位仪对微球表面的Zeta电位的变化进行了研究,结果如图1所示.

图1 包覆过程中微球表面电位随时间的变化
将不同量的氨水加入到PS与TEOS均匀混合体中.从图1可知,当氨水用量为1mL,反应前4h微球表面电位变化不大,反应进行到9h微球表面电位还有+11.33mV;而当氨水用量超过2mL,微球表面的电位均在4h前实现电性反转,且氨水用量越大,实现典型反转的时间越短.微球表面电性发生反转是因为经溶胶凝胶反应生成的SiO2带负电,并通过静电作用包覆到带正电的PS表面.实验结果显示,氨水用量为1mL时,TEOS溶胶凝胶反应速率过小,以致PS微球上包覆的带负电的SiO2的量很少;而随着氨水用量增加,溶胶凝胶反应速率明显增加,特别是当氨水用量达到4mL,反应2h微球表面电位即可达到-30.84mV.
由图2可见,不同氨水用量的PS/SiO2复合微球的表面均比较光滑,氨水用量为1mL时微球粒径为1 480nm,与PS微球粒径(1 468nm)相比增加幅度不大;而当氨水用量超过2mL,微球粒径均在1 520nm左右.表明氨水用量为1mL时,TEOS水解不充分,包覆到PS微球表面上的SiO2量较少;而当氨水用量超过2mL,TEOS能够充分水解和包覆,SiO2壳层厚度也没有很明显的变化.
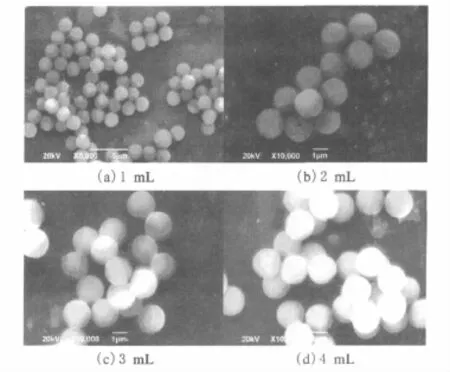
图2 不同氨水用量制备的PS/SiO2复合微球SEM图
2.2 PS微球表面电荷对包覆过程的影响
实验中PS微球表面的电荷密度可以通过共聚过程中DMC的用量加以调节.当DMC用量分别为0.1%、0.2%、0.3%、0.4%时,PS微球表面电荷密度分别为33.51mV、38.36mV、45.62mV、43.08 mV.以上述四种不同表面电位的PS微球为模板,在TEOS用量为2g,氨水用量为2mL的条件下,考察了微球表面电位在包覆过程中的变化,结果如图3所示.

图3 表面电位不同的微球包覆过程电位随时间的变化
图中曲线变化相似,表明四种微球的表面电位变化趋势相似,均在2~6h之间发生急剧变化,并实现电性反转,而后的变化趋于平缓.在出现电性反转的过程中,DMC量为3%和4%制备的PS微球电位下降趋势更加明显.这说明由于DMC用量增加使PS微球表面正电荷密度较大,在包覆过程中对带异向电荷的SiO2的静电吸附能力增强.
2.3 TEOS用量对微球表面电位的影响
DMC用量为0.3%时制备得到的PS微球为模板,当氨水用量为2mL,TEOS用量分别为1g、2 g、3g、4g时包覆过程中微球表面电位的变化如图4所示.
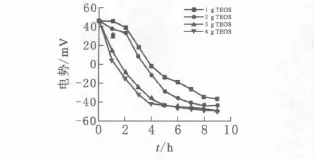
图4 TEOS用量对包覆过程中微球表面电位的影响
由图4可见,TEOS用量不同,SiO2包覆速度有差异,但在包覆过程中达到9h均能吸附完全,并形成较为稳定的表面电位.当TEOS用量为1g、2g时,包覆过程前2h微球表面电位变化并不明显,且实现电性反转所需时间明显比TEOS用量大于2g时要长.随着TEOS用量的增加,电位的下降趋势趋于明显,出现电位反转所需的时间越短,负电性越大.这是由于TEOS用量的增加使水解后反应体系中SiO2的浓度增大,PS微球在体系中与SiO2接触概率增大,使PS表面更容易通过静电吸附一层SiO2.实验结果表明,整个包覆过程均可以在9h完成;随着TEOS用量的提高,微球表面包覆的速度也会随之加快,从而缩短了实验的反应时间.

图5 不同TEOS用量制备的PS/SiO2复合微球TEM图
根据图5,TEOS用量为1g、2g、3g、4g时复合微球的平均粒径分别为1 505nm、1 520nm、1 535nm、1 558nm,随着TEOS用量的增加,复合微球的壳层厚度也随之增加.除了微球直径的增大,当TEOS用量为4g时,微球表面也随之变得粗糙,这是由于SiO2在体系中分散不均匀也会造成浓度过大,形成小的团聚体或是以多层的形式不均匀的包覆在PS球的表面,使包覆后的复合微球表面粗糙.
3 结束语
以阳离子PS微球为模板,通过检测包覆过程中微球表面Zeta电位的变化,实现了PS/SiO2核壳型复合微球包覆过程的可控,且发现随着氨水和PS表面电荷密度的增大,会使SiO2更容易包覆在阳离子PS微球表面,缩短整个反应时间,但对壳层厚度的影响不明显;复合微球的壳层随着TEOS量的增加而增厚,因此通过改变TEOS用量,根据需要可以有效调控包覆的壳层厚度.
[1]Caruso F.Nanoengineering of particle surfaces[J].Adv Mater,2001,13:11-22.
[2]Yu J,Zhao L,Cheng B.Facile preparation of monodispersed SiO2/TiO2composite microspheres with high surface area[J].Mater Chem Phys,2006,96:311-316.
[3]张玉红,陈 浩,邹其超.非离子乳化剂细乳液聚合制备草莓型PS/SiO2纳米复合微球[J].高分子学报,2011,6:661-665.
[4]唐琴琼,文庚男,陈 敏.SiO2/PVAc无机-有机复合微球的合成及其膜性能研究[J].高分子学报.2008,9:843-848.
[5]王吉会,董 青.SiO2空心微球的制备与表征[J].材料开发与应用,2009,24(4):42-46.
[6]吉海宾,祖国胤,姚广春.碳酸镁颗粒表面包覆二氧化硅的研究[J].东北大学学报(自然科学版),2009,30(5):701-703.
[7]Caruso F.Hollow capsule processing through colloidal templating and self-assembly[J].Chem Eur J,2000,6:413-419.
[8]Tissot I,Reymond J P,Lefebvre F,et al.SiOH-functionalized polystyrene latexes:a step toward the synthesis of hollow silica nanoparticles[J].Chem Mater,2002,14(3):1 325-1 331.
[9]邓 伟,陈 国,王满意,等.pH值和前驱体用量对核壳结构PS/SiO2复合微球结构形态的影响[J].高分子学报,2011,3:307-310.
