我国国家药物政策领域现存问题的文献评价Δ
孙慧,傅鸿鹏,徐竞然,杨洪伟(1.首都医科大学卫生管理与教育学院,北京100069;2.北京市疾病预防控制中心,北京 10001;.卫生部卫生发展研究中心,北京 100191;.中国人民大学商学院,北京 100872)
世界卫生组织(WHO)2007年出版的《如何制定和实施国家药物政策》中将国家药物政策的关键组成划分为9个部分,分别为基本药物的遴选、可负担性、药品资金筹措、供应系统、药品监管、药品的合理使用、研究、人力资源开发以及监测和评估。我国现阶段虽然还没有出台系统的国家药物政策,但已有不少针对这9个领域研究的文献发表。基于此,本文系统评价了公开发表在中国期刊全文数据库(CNKI)和万方中文数据库中讨论国家药物政策关键组成部分在我国实施过程中出现的问题的文献,以为我国制定系统的国家药物政策提供参考。
1 资料与方法
1.1 文献纳入/排除标准
由于本研究的主要目的是为了了解国家药物政策关键组成部分在我国实施过程中出现的问题,因此只检索和纳入中文文献。纳入明确定性或定量分析上述9个领域中1个或多个在我国出现的问题的文献,排除仅在前言或讨论部分提及相关问题但未进行深入探讨的文献。
1.2 检索策略
检索数据库为CNKI和万方中文数据库,检索年份未作限定。检索主题词包括:基本药物遴选、药品支付能力、药品筹资、药品供应、药品监管、药品安全、药品不良反应监测、药品合理使用、药品研究、药品研发、药品人力资源开发、药品监测和评估、基本药物遴选的问题、药品支付能力的问题、药品筹资的问题、药品供应的问题、药品监管的问题、药品安全问题、药品不良反应监测的问题、药品合理使用的问题、药品研究的问题、药品研发的问题、药品人力资源开发的问题、药品监测和评估的问题等。
1.3 文献整理与分析
(1)阅读文献题目和摘要,排除不相关的文献;(2)浏览文献全文,排除关联不密切的文献;(3)对符合要求的文献进行重点信息摘录。
2 结果
2.1 纳入文献描述
经过检索,目前国内只针对基本药物遴选、药品供应、药品监管、药品不良反应监测、药品合理使用以及药品研发这6个领域有相关的文献研究,共检索到178篇文献,经过筛选,最终获得133篇符合要求的文献。文献分布情况见表1。

表1 文献分布情况Tab 1 Distribution of literatures
2.2 六大领域存在问题分析
2.2.1 基本药物遴选存在的问题 基本药物遴选作为建立国家基本药物制度的关键环节,在以下6个方面尚存在问题,详见表2。

表2 基本药物遴选存在的问题Tab 2 Problems of the selection of essential drugs
1)遴选过程及更新程序未见公开[1]。《WHO基本药物示范目录》的遴选与调整、更新,要求全过程必须公开、透明,从药物遴选和调整的申请,到目录出台均公布在官方网站上;遴选专家委员会成员及其利益冲突声明、遴选过程和遴选证据等都可供全球用户免费上网查阅和监督。我国虽公布了《关于建立国家基本药物制度的实施意见》、《国家基本药物目录管理办法(暂行)》及《国家基本药物目录·基层医疗卫生机构配备使用部分》(2009版)(以下简称“2009年版《国家基本药物目录》”),但遴选过程透明化和时效性与WHO相比还相差甚远,亟待跟进和完善。
2)基本药物目录中遴选收录中药注射剂的科学性有待提高。2009年版《国家基本药物目录》中102种中成药包含8种中药注射剂,然而中药注射剂组方中所含中药的成分复杂,即便仅含单味药材,成分也极其复杂,容易出现不良反应。因此,在证据有限、而安全性问题突出的情况下,如何科学遴选中成药,既保证基本药物遴选的科学性,又能反映中医药的地位和特点还需进一步研究[2]。
3)基本药物目录缺乏具体配套的基本药物政策[3~5]。基本药物配套政策与制度包括建立药物专业评价机构、开展合理使用基本药物的培训、制定标准治疗指南和处方集、基本药物生产供应保障机制等,与WHO制定的基本药物目录相比,我国基本药物目录的配套政策和制度尚待健全。
4)基本药物“临床首选”科学性不充分。某一种药物作为基本药物进入2009年版《国家基本药物目录》应该具有不可替代性及优越性。但2009年版《国家基本药物目录》遴选出的药品相对于同类未进入目录的品种的不可替代性及优越性表现都不充分。例如,遴选进入2009年版《国家基本药物目录》的抗高血压药共有9种,分别为卡托普利、依那普利、硝普钠、硫酸镁、尼群地平、吲达帕胺、酚妥拉明、复方利血平、复方利血平氨苯蝶啶。抗高血压药种类很多,根据其作用部位可分为四大类[6]:交感神经抑制药、血管扩张药、利尿降压药、肾素-血管紧张素系统抑制药,每一大类药物可细分为多个小类别,而每个小类别又包含多种药物。例如,血管扩张药可分为直接扩张血管药、钙通道阻滞药等,钙通道阻滞药又包括硝苯地平、尼群地平等品种。将尼群地平作为此类药的“临床首选”欠缺有力依据,其不可替代性表现也不充分[6]。因此,在基本药物遴选过程中“临床首选”原则的科学性还有待提高。
5)基本药物遴选“价格合理”没有具体的评价标准,论述不科学。目前,公众对于“价格合理”只是单纯地理解为价格低廉,概念仍然很模糊。公众对于概念理解不准确,原因就是遴选原则中对“价格合理”缺乏具体的评价标准,没有对价格的“合理性”进行明确的论述[6]。
6)缺乏《标准治疗指南》和《药品处方集》。我国至今还没有一本由政府牵头编制的《标准治疗指南》,《中国国家处方集》也是2010年才公布。大多数地区医院中只有各科室零散汇编的针对本科室所处理疾病的治疗指南,实施起来也不规范,医师在治疗过程中则主要依赖经验,给临床治疗工作埋下了安全隐患。
2.2.2 药品供应存在的问题 药品供应在以下两方面存在问题,详见表3。

表3 药品供应存在的问题Tab 3 Problems of drug supply
1)药品集中招标采购政策执行不力[7]。药品集中招标采购在实施过程中取得一些成效的同时,它的缺陷也日益暴露出来。如,在操作上不能按照严格规定,缺乏监督,甚至出现一旦中标的药品马上会从市场上消失的恶劣情况。这在很大程度上影响了药品的及时供应,导致了药品供应不足,甚至短缺。2)药品采购环节缺乏有力监督。药品采购环节供货商众多,但我国却没有相关企业资质考查的法律法规,这就容易出现没有经营资质的隐性主体进行暗箱操作,将假冒伪劣药品流入市场的现象,使得药品的质量难以保障[8]。
2.2.3 药品监管存在的问题 药品监督管理是保证人民群众用药安全的重要举措,然而在我国,药品监管仍然存在以下几方面的问题[9~12],详见表4。
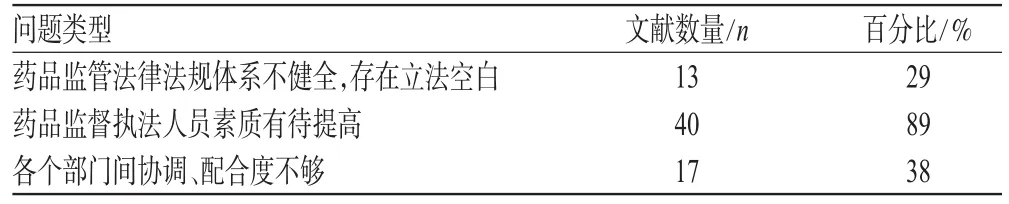
表4 药品监管存在的问题Tab 4 Problems of drug regulations
1)药品监管法律法规体系不健全,存在立法空白。我国虽出台了《药品管理法》,但有关药品管理的法律法规并未真正发挥其作用,仍然存在某些药品制造商无证生产药品,生产假药、劣药的恶劣现象,各项规章制度未落到实处,甚至形同虚设。
2)药品监督执法人员素质有待提高。药品是一种特殊的商品,药品监管部门作为监管药品研究、生产、经营、使用全过程的政府部门,可谓责任重大。为保证做好药品监管工作,对药品监管执法人员的素质必须高标准、严要求。但从目前情况来看,药品监管执法人员的素质尚不尽如人意,执法人员素质不高,工作方法粗糙,滥用权利。尤其是在基层,远远不能适应药品监管这一专业性很强的工作的需要。
3)各个部门间协调、配合度不够。国家药品管理体制改革后,国务院药品监督管理部门负责药品监管,但卫生、工商、物价、经贸等部门仍有相关管理的职责。各部门虽然出台了一些规章,但由于部门与部门间协调不够,有的规章出现了相互不一致的情况,给药品监管工作带来困难。
2.2.4 药品不良反应监测工作存在的问题 药品不良反应监测工作在我国起步较晚,尚处于初级阶段,所以还存在以下几方面的问题,详见表5。

表5 药品不良反应监测工作存在的问题Tab 5 Problems of adverse drug reaction monitoring
1)政府对药品不良反应监测宣传力度不够。政府在药品不良反应宣传工作上的欠缺,一方面没有让人们充分认识到药品不良反应的危害及药品不良反应监测的必要性,医药工作者没有意识到上报药品不良反应病例是自己的职责与义务;另一方面没有使人们正确认识药品不良反应的含义,致使群众将药品不良反应与医疗事故及药品质量问题联系在一起,造成医务人员及药品生产企业不愿意报告药品不良反应病例。
2)药品不良反应监测水平不高,工作多流于形式。开展药品不良反应监测工作最主要的目的之一是要发现具有警戒意义的、新的、严重的药品不良反应,而目前的报告约有98%是已知的不良反应,而医院的药品不良反应报告中多数只注重报告的数量,而忽视报告的质量,由于对相关知识掌握不全面而致诊断欠妥,远远没有达到通过监测体系发现预警信号进而开展风险管理的目的[13]。
3)配套法规不健全。《药品不良反应监测管理办法(试行)》虽已颁布,但某些相关法律法规与之不协调。例如,在1999年5月1日开始实施的《中华人民共和国执业医师法》中,尚无药品不良反应的相关规定。另外,也缺乏具体的“实施办法”、“实施细则”、“ 奖惩办法”、“ 赔偿规定”等与之相配套的法规[14]。
4)中药不良反应监测工作有待加强。中药的应用已有几千年的历史,但长期以来人们对中药不良反应没有引起足够的重视,习惯上认为中药不良反应少,甚至没有。另外,由于中药的特殊性,增加了开展中药不良反应监测的难度。由此种种,造成目前对中药不良反应的认识远远落后于西药。对中药不良反应的不够重视和不诚实,严重影响着中药在人们心目中的形象和地位,这已经成为影响中药现代化的瓶颈[14]。
2.2.5 药品合理使用存在的问题 影响药品合理使用的因素很多,各方联系较复杂,既有医疗卫生机构及监管部门的问题,也有患者本身的原因,所以我国药品的合理使用还存在一定的问题,详见表6。

表6 药品合理使用存在的问题Tab 6 Problems of rational use of drugs
1)政府财政补偿的缺失成为医院追求高价药品的动力,合理用药难以实现。医疗卫生机构的药品基本是通过医师处方销售的,医师受利益驱动处方高价药以获取高额回扣或开单提成的现象普遍存在。究其原因主要由于我国政府在医疗服务中财政补偿的缺失导致了“以药养医”补偿体制,造成医疗卫生机构过度依赖药品收入,使得药品能否被合理使用,很大程度上取决于其是否能够满足医疗卫生机构的回扣期望,而不是药品的安全性、有效性及价格的合理性[15]。
2)合理用药缺乏有效监管[16]。由于医患双方的信息不对称,医师的用药行为决定了患者的购买行为,在缺乏有效监管和约束机制的情况下,医师的处方行为也未得到完善指导和有效监督。这种行为不仅造成了有效的基本药物资源浪费,也是不合理用药的根源之一。
2.2.6 药品研发存在的问题 我国药企新药研究开发技术及手段远远落后于发达国家,长期以来以仿制国外药物为主,很少有自己的创新药物,药品研发面临严重困境,详见表7。

表7 药品研发存在的问题Tab 7 Problems of drug researches
药品研发缺乏指导安排和激励机制。虽然国家《药品注册管理办法》第四条已经明确指出,国家鼓励研究创制新药对创制的新药实行特殊审批,并为此制定了《新药注册特殊审批管理规定》[17],可是我国的药品生产企业数量多,且大部分企业规模小、资金实力薄弱,专利药品开发耗时耗资又非常大,而我国除上述规定外并没有出台相应的指导安排和激励机制,导致绝大多数药品生产企业重市场轻研发,只重视眼前利益,缺乏远见,严重阻碍了我国创新药品的研发进程[18,19]。
3 结语
药物政策在每个国家卫生战略中都是至关重要的组成部分。国家药物政策为确定国家目标及承诺提供了一个宝贵的战略框架。我国现阶段还没有制定出系统的国家药物政策,因此更应该规范上述存在问题的领域,为制定完善、合理的国家药物政策打下良好的基础。
[1]李幼平,王 莉,杨晓妍,等.我国基本药物目录制定及实施的循证思考[J].中国循证医学杂志,2009,9(11):1 131.
[2]王 莉,袁 强,成 岚,等.我国基本药物目录遴选与评价方法的问题与反思[J].中国药房,2010,21(16):1 453.
[3]张 川,王 莉,袁 强,等.我国基本药物目录、基本医疗保险药物目录和WHO基本药物目录比较[J].中国循证医学杂志,2009,9(7):765.
[4]王 莉,喻佳洁,周帮日文,等.17国国家药物政策的系统评价[J].中国循证医学杂志,2009,9(7):715.
[5]王 莉,周帮日文,宋佳佳,等.25国基本药物目录循证评价[J].中国循证医学杂志,2009,9(7):754.
[6]孟 锐,蓝培元,任晓宇.我国基本药物目录遴选相关问题探析[J].中国药房,2010,21(24):63.
[7]刘兰茹,孙志丹,金 瑞.医疗机构药品供应问题及对策[J].中国医院管理,2009,29(1):63.
[8]姚红卫,解庆东.药品招标采购对医院药品供应的影响[J].中国药业,2009,18(22):1.
[9]楚亚林.浅谈我国药品安全监督管理面临的问题及对策[J].科技创新导报,2008,(9):142.
[10]侯茂虎.基层药品监管工作几个问题的思考[J].中国药事,2004,18(6):334.
[11]杨永岐,杨志强,傅小英.药品监管中应重视的问题及对策[J].东南国防医药,2003,5(2):97.
[12]闫锦严.药品监管中亟待解决的一些问题探析[J].中国药业,2003,12(11):14.
[13]傅孟兰.药品不良反应监测工作存在的问题及其对策[J].中国现代医生,2010,48(26):90.
[14]廖广仁,赖伟华.药品不良反应监测工作的现状及存在的问题[J].中国药房,2004,15(3):137.
[15]王 芳,孙利华.我国在合理用药中的问题与对策[J].中国医药技术经济与管理,2008,2(1):72.
[16]吴红雁.基本药物合理使用存在的问题及建议[J].临床合理用药,2010,3(11):133.
[17]国家食品药品监督管理局.新药注册特殊审批管理规定[Z].2009.
[18]唐 玲,邱家学.谈我国制药企业的药品研发问题[J].国际医药卫生导报,2005,13:71.
[19]王水强.创新药物研发中的立题问题与临床研究原则[J].中国新药杂志,2010,19(11):930.

