健康体检人群中乙型肝炎病毒感染者的自然转归
李福玮 王桂茹 牛俊奇 刘 群 (吉林大学第一医院体检中心,吉林 长春 130021)
乙型肝炎病毒(HBV)感染呈世界性流行,但不同地区HBV感染的流行强度差异很大。根据世界卫生组织报道,全球大约20亿人曾感染过HBV,其中3.5亿人为慢性HBV感染者,每年约有100万人死于HBV感染所致的肝衰竭、肝硬化及原发性肝细胞癌 (HCC)〔1,2〕。2006年全国乙型肝炎流行病学调查显示,我国1~59岁一般人群HBsAg携带率为7.18%,5岁以下儿童的乙型肝炎表面抗原(HBsAg)为0.96%〔3,4〕国际多中心随机对照临床试验显示,乙肝e抗原(HBeAg)阳性的慢性乙型肝炎患者,聚乙二醇化干扰素α-2a(PegIFN-α2a)治疗(87%为亚洲人)48 w,停药随访24 w时HBeAg血清学转换率为 32%〔5,6〕;停药随访48 w 时 HBeAg 血清学转换率达43%〔7〕。但部分患者在非药物治疗的情况下也会发生HBeAg血清学转换,研究表明自发性HBeAg血清学转换主要出现在免疫清除期,年发生率约为2% ~15%,其中年龄小于40岁、丙氨酸转氨酶(ALT)升高以及感染HBV基因A型和B型者发生率较高〔8,9〕。HBeAg血清学转换后每年大约有 0.5% ~1.0%发生HBsAg 清除〔10〕。
1 材料与方法
1.1 研究对象 对1993~2010年在吉林大学第一医院健康体检的HBV感染人群的HBV血清学标志物(包括HBsAg,抗-HBs,HBeAg,抗-HBe,抗-HBc等)进行相应的流行病学分析。HBsAg阳性4103人次;年龄11~90岁;其中<18岁15人次;18~50岁2895人次;>50岁1191人次(以上年龄均为受检时年龄,并非目前实际年龄)。男性2860人次;女性1243人次。其中做2次体检680人,3次591人,4次328人,5次192人,6次79人,7次47人,8次1人。
1.2 研究方法 采用酶联免疫吸附试验(ELISA)检测HBV血清学标志物,试剂盒为科华乙肝两对半试剂盒,分析仪为tecan全自动酶联免疫分析仪。
1.3 统计学分析 采用SAS8.0统计学分析软件。
2 结果
HBsAg阳性率及分布趋势见表1。HBsAg阳性人群年龄构成比及性别分布,见表2。HBeAg自发血清转化率1.91%/年;HBeAg自发转阴率2.79%/年。1年、2年、3年、4年HBeAg转阴及血清转化情况见表3~表7。2003~2009年HBeAg转阴1例(12.05%),HBeAg血清转化0例;2004~2010年HBeAg转阴2例(5.13%),HBeAg血清转化0例。而2003~2010年HBeAg转阴1例(100%),HBeAg血清转化0例。
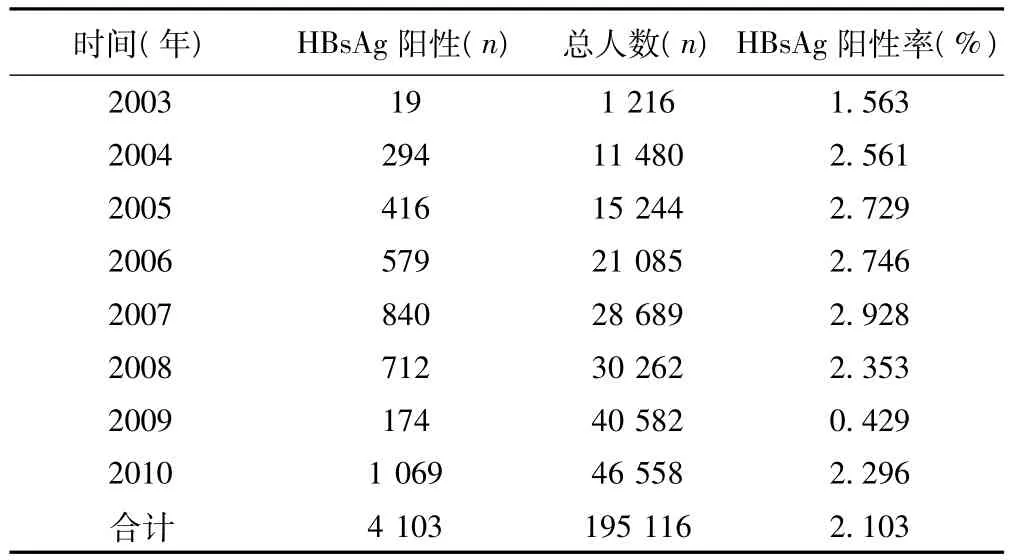
表1 2003~2010年HBsAg阳性率分布〔n(%)〕
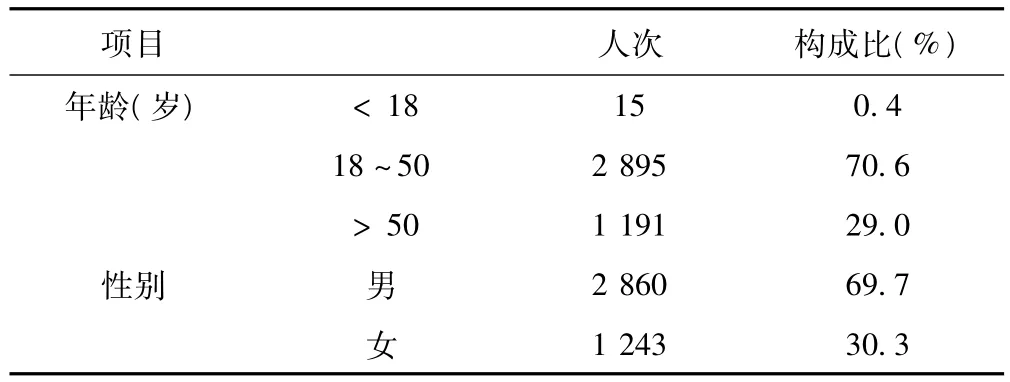
表2 4103人次HBsAg阳性人群年龄及性别分布
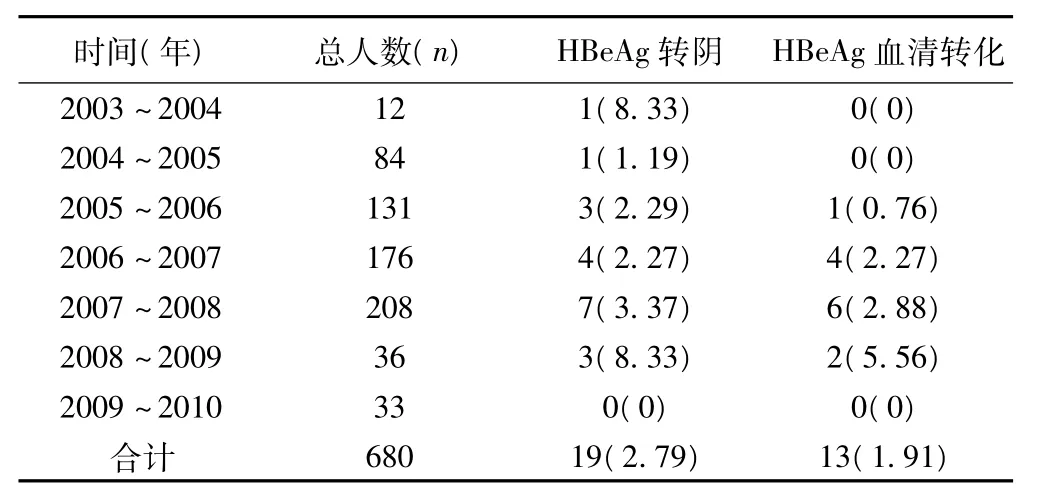
表3 1年HBeAg转阴及HBeAg血清转化分布〔n(%)〕

表4 2年HBeAg转阴及HBeAg血清转化分布〔n(%)〕
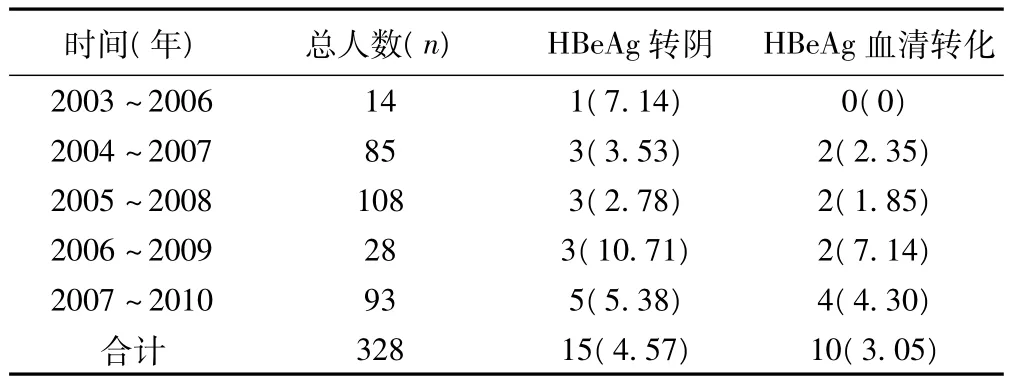
表5 5年HBeAg转阴及HBeAg血清转化分布〔n(%)〕

表6 4年HBeAg转阴及HBeAg血清转化分布〔n(%)〕

表7 5年HBeAg转阴及HBeAg血清转化分布〔n(%)〕
3 讨论
HBsAg阳性率低于2006年我国乙型肝炎流行病学调查1~59岁一般人群HBsAg携带率为7.18%的结果;2003年的研究例数较少,可能存在一定程度的偏倚。从总体来看,2004~2007年HBsAg阳性率相对稳定的处在较高水平,2008~2010年HBsAg阳性率有较明显的降低,可能与国家实行乙肝疫苗政策、当地卫生条件改善,卫生政策完善与个人预防保健意识增强有关。
HBsAg阳性者主要集中于青壮年人群。<18岁人群构成比低与我国1992年开始将乙肝疫苗纳入免疫规划管理、2002年开始将乙肝疫苗纳入儿童免疫规划有关。由于体检人群多为成年人群,18岁以下人群数据明显不足,可能会导致此年龄段构成比低于实际值。>50岁人群构成比较青壮年人群降低,可能与老年人体质下降肝炎恶化导致死亡有关。HBsAg阳性者男性明显高于女性,可能与男女体质差异及生活方式不同有关,确切的相关因素还有待于深入研究。
HBeAg自发血清转化率低于中华医学会《慢性乙型肝炎防治指南2010年更新版》中所述年发生率2% ~15%的范围。不同人种、地域的差异较大,此结论具有人群、地域的独特性。
总之,需要政府与卫生部门继续加强对疾病的预防与控制,需要提高人群对乙肝疫苗接种的认识,特别是成年人群。需要更多的专业人才投入到预防和疾病治疗的研究中,同时对疾病人群加强随访;需要公共卫生人员加大宣传力度,不断提高人群的自我保护意识,定期进行健康体检,积极进行预防接种,指导患病人群主动接受疾病治疗。
1 Ganem D,Prince AM.Hepatitis B virus infection-natural history and clinical consequences〔J〕.N Engl J Med,2004;350(11):1118-29.
2 Organization WH,Hepatitis B.World Health Organization Fact Sheet 204 dex.(Revised October 2000)〔EB/OL〕.WHO Web site.http://www.who.int/mediacentre/factsheets/fs204/en/in html.
3 Liang X,Bi S,Yang W,et al.Epidemiological serosurvey of hepatitis B in China-declining HBV prevalence due to hepatitis B vaccination〔J〕.Vaccine,2009;27(47):6550-7.
4 Liang X,Bi S,Yang W,et al.Evaluation of the impact of hepatitis B vaccination among children born during 1992-2005 in China〔J〕.J Infect Dis,2009;200(1):39-47.
5 Tai DI,Chen CH,Chang TT,et al.Eight-year nationwide survival analysis in relatives of patients with hepatocellular carcinoma:role of viral infection〔J〕.J Gastroenterol Hepatol,2002;17(6):682-9.
6 中国疾病预防控制中心.乙型肝炎疫苗儿童计划免疫技术管理规程(试行)〔C〕.中华人民共和国卫生部、财政部.2002.
7 Piratvisuth T,Lau G,Chao YC,et al.Sustained response to peginterferon alfa-2a(40 kD)with or without lamivudine in Asian patients with HBeAg-positive and HBeAg-negative chronic hepatitis B〔J〕.Hepatol Int,2008;2(1):102-10.
8 Liaw YF.Natural history of chronic hepatitis B virus infection and longterm outcome under treatment〔J〕.Liver Int,2009;29(1):100-7.
9 Liaw YF.Hepatitis flares and hepatitis B e antigen seroconversion:implication in anti-hepatitis B virus therapy〔J〕.J Gastroenterol Hepatol,2003;18(3):246-52.
10 Chu CM,Hung SJ,Lin J,et al.Natural history of hepatitis B e antigen to antibody seroconversion in patients with normal serum aminotransferase levels〔J〕.Am J Med,2004;116(12):829-34.

