海南广藿香药材中百秋李醇和广藿香酮的含量测定*
张宏武,程雪宁,魏建和,杨兴全,喻长远,邹忠梅
(1.中国医学科学院北京协和医学院药用植物研究所,北京 100193; 2.北京化工大学生命科学与技术学院,北京 100029; 3.中国医学科学院北京协和医学院药用植物研究所海南分所,海南 万宁 571533)
广藿香为唇形科植物广藿香 Pogostemon cablin(Blanco)Benth.的干燥地上部分,是临床上常用的芳香化湿药,味辛、性微温,归脾、胃、肺经,具有芳香化浊、开胃止呕、发表解暑的功效[1],是著名中成药藿香正气丸(水)的主要组方药材。广藿香主要成分为挥发油类成分,主要为百秋李醇 (patchouli alcohol)[2],因此我国药典是以百秋李醇的含量作为广藿香药材质量的评价指标[1]。但研究表明,具有抗菌活性的主要成分为广藿香酮(pogostone)[3]。广藿香商品分为石牌藿香、高要藿香、海南藿香,以石牌藿香为道地药材,但目前市场上流通的主流商品为海南广藿香。笔者对广藿香药材提取方法进行了改进,首次建立了同时测定广藿香药材中百秋李醇和广藿香酮含量的方法,并对市场上流通的主流商品海南广藿香药材的质量进行了考察。
1 仪器与试药
Agilent 6890GC型气相色谱仪,Agilent FID检测器,N2为载气;AT201型十万分之一电子天平(梅特勒-托利多仪器<上海>有限公司)。百秋李醇对照品购于中国药品生物制品检定所;广藿香酮对照品为自制,经光谱分析和GC-FID面积归一化法测定含量为98%;试剂均为分析醇。11批海南广藿香药材均于2008年6月采于中国海南省,由中国医科院药用植物研究所海南分所杨兴全助理研究员鉴定为唇形科植物广藿香 Pogostemon cablin(Blanco)Benth的干燥地上部分。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:Agilent DB-5弹性毛细管石英柱(30 m×0.25 mm×0.25 μm);程序升温:初始温度160℃,保持1 min,以每分钟5℃速率升温至220℃,保持1 min,再以每分钟10℃速率升温至300℃,保持10 min;检测器温度为300℃,进样口温度为250℃;分流比为5∶1。在该色谱条件下,百秋李醇和广藿香酮均能达到基线分离,见图1。

图1 气相色谱图
2.2 溶液制备
精密称取百秋李醇和广藿香酮对照品,加正己烷制成每1 mL各含3.0 mg的溶液,作为对照品溶液。称取广藿香药材约10 g,用粉碎机粉碎,过60目筛,精密称取广藿香药材粉末2.0 g,置50 mL具塞三角瓶中,加30 mL甲醇,称重。超声30 min,放冷,补重,过滤,取中滤液作为供试品溶液,0.45 μm滤膜过滤备用。
2.3 方法学考察
线性关系考察:精密量取对照品溶液 25,100,200,400 μL,分别置2 mL容量瓶中,用正己烷定容,分别取稀释后溶液及对照品溶液各1 μL注入气相色谱仪,以百秋李醇和广藿香酮的峰面积对质量浓度进行线性回归,得回归方程,百秋李醇为 Y=928.62 X -6.6192(r=0.9999),广藿香 酮为 Y=509.27 X -16.788(r=0.9995)。结果表明,百秋李醇质量浓度在 0.0775 ~6.200 g/L 内,广藿香酮质量浓度在 0.0725~5.800 g/L 范围内与峰面积呈良好的线性关系。
精密度试验:取同一份对照品溶液,按2.1项下色谱条件日内重复进样5次,并连续测定5 d,记录峰面积。结果百秋李醇和广藿香酮日内峰面积的 RSD分别1.39%和1.52%(n=5),日间峰面积的 RSD分别为2.04%和2.27%(n=5),表明仪器精密度良好。
重复性试验:精密称取同一批药材粉末5份,依法制备供试品溶液,按上述色谱条件重复进样5次,记录峰面积。结果百秋李醇和广藿香酮峰面积的 RSD分别为1.07%和2.20%,表明方法重复性良好。
稳定性试验:精密吸取同一供试品溶液1 μL分别在0,2,4,8,12,24 h时进样。结果百秋李醇峰面积的 RSD为2.57%,广藿香酮峰面积的 RSD为2.72%,表明溶液在24 h内稳定性良好。
加样回收试验:精密称取同一已知含量的广藿香药材粉末0.8,1.0,1.2 g,置 50 mL 具塞三角瓶中,分别加入百秋李醇对照品 3.6,4.5,5.4 mg,广藿香酮对照品 1.0,1.3,1.6 mg。依法制备供试品溶液,取续滤液,按上述色谱条件测定,记录峰面积,由测得量与加入量计算回收率。结果见表1。
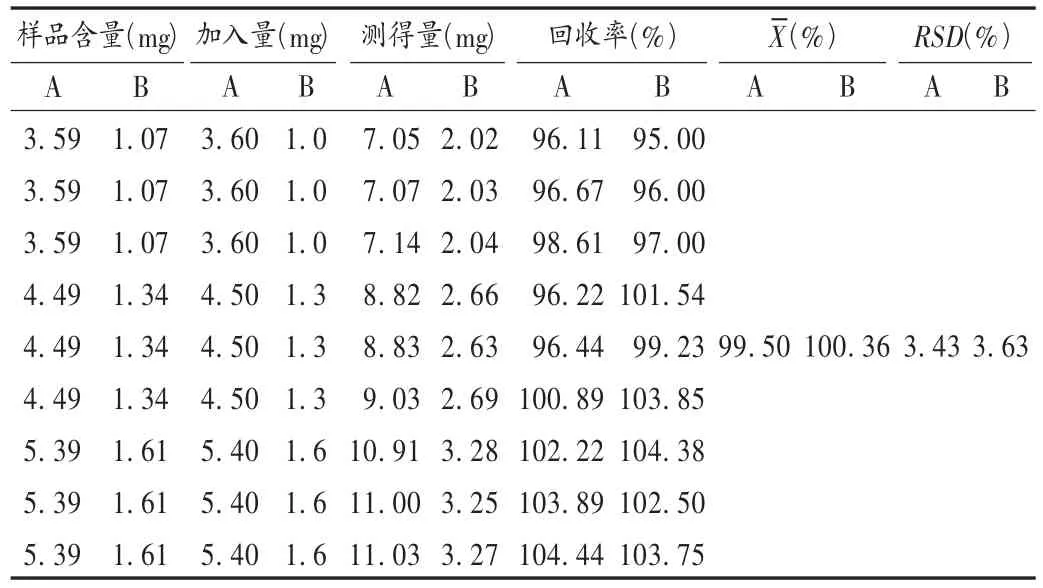
表1 加样回收试验结果(n=3)
2.4 样品含量测定
取11批海南产广藿香药材,依法制备供试品溶液,按上述色谱条件进样1 μL,记录峰面积,分别计算广藿香药材中百秋李醇、广藿香酮含量。结果见表2。
3 讨论
3.1 广藿香药材提取方法的选择
2005年版《中国药典(一部)》中供试品溶液的制备方法为:加三氯甲烷50 mL,超声处理3次,每次20 min,滤过,合并滤液,回收溶剂至干,残渣加正己烷溶解,转移至5 mL量瓶中。笔者比较了甲醇和三氯甲烷作为提取溶剂的效果,发现同一份药材使用甲醇超声提取其百秋李醇、广藿香酮的含量分别为0.261%和0.134%,而药典提取方法其百秋李醇、广藿香酮的含量分别为0.156%和0.079%。进一步对提取次数进行了考察,发现超声1次基本可以将百秋李醇和广藿香酮完全提取,大大简化了操作。由于百秋李醇和广藿香酮均为易挥发性化合物,因此在回收溶剂过程中会有较大的损失,无法客观、准确测定百秋李醇和广藿香酮的含量,所建立的方法避免了溶剂回收问题,可比药典方法更准确地反映广藿香药材中两种成分的含量。
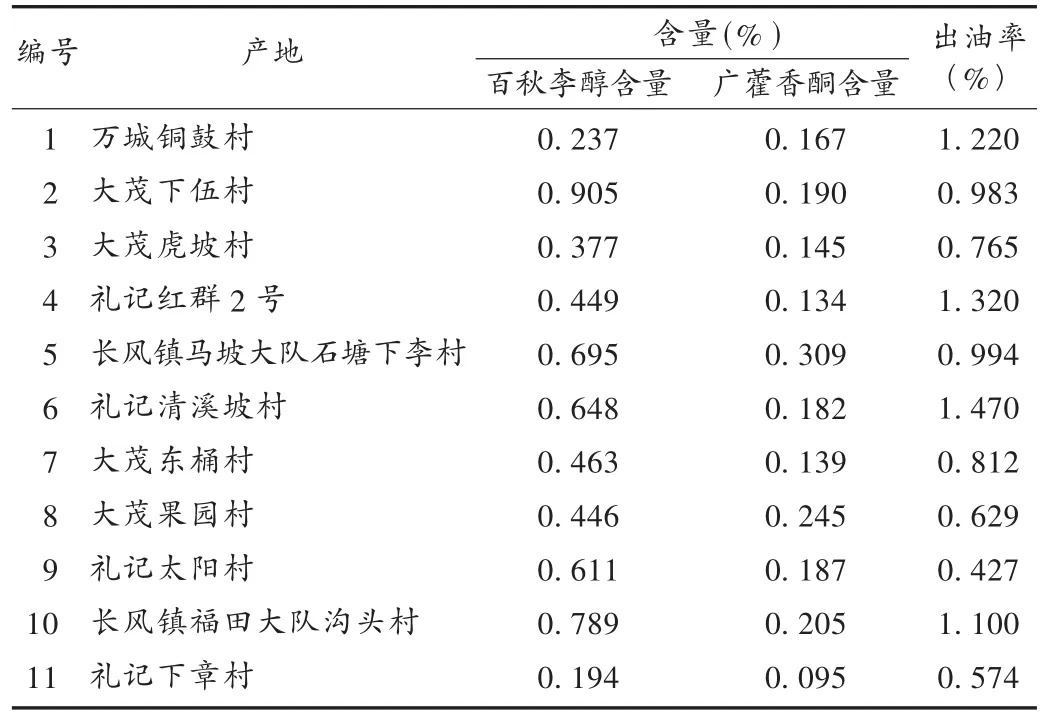
表2 样品含量测定结果(n=3)
3.2 出油率与广藿香药材质量的关系
笔者用水蒸气蒸馏法对11批海南广藿香药材的出油率进行了考察,发现出油率与广藿香中百秋李醇和广藿香酮的含量并无直接关系。如编号为6的广藿香药材,其出油率最高(1.47%),但其百秋李醇和广藿香酮的含量均不是最高。但若出油率过低(<0.6%),百秋李醇和广藿香酮的含量则均较低。
3.3 广藿香药材样品测定结果
从11批海南产广藿香药材中百秋李醇和广藿香酮含量测定结果来看,海南产广藿香药材中百秋李醇含量均达到药典要求,但来自不同栽培地药材中百秋李醇和广藿香酮含量有一定差异,如5号、10号样品来自长风镇地区,其广藿香醇和百秋李醇含量均较高,而来自万城铜鼓村的1号样品和礼记下章村11号样品中百秋李醇和广藿香酮含量均较低。导致含量差异的原因是种质不同,还是环境和种植条件不同,有必要进一步考察。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:化学工业出版社,2005:30-31.
[2]Wu JF,Xin L,Tang WY,et al.Application of comprehensive twodimensional gas chromatography-time-of-flight mass spectrometry in the analysis of volatile oil of traditional Chinese medicines[J].J Chromatography A,2004,1034(1 -2):199 -205.
[3]张广文,蓝文键,苏镜娱,等.广藿香精油化学成分分析及其抗菌活性(Ⅱ)[J].中草药,2002,33(3):210 -212.

