高效液相色谱法测定红霉素肠溶胶囊的含量
伍 蓉,刘融融,万 莉
红霉素肠溶胶囊为大环内酯类抗生素,作为治疗对青霉素过敏感染患者的替代用药。该制剂原质量标准[1]为抗生素微生物检定法,此方法烦琐费时、影响因素多。笔者采用高效液相色谱(HPLC)法测定红霉素肠溶胶囊中红霉素的含量,简便快速,准确可靠,为该制剂的质量控制提供了新的测定方法,现报道如下。
1 仪器与试药
岛津公司LC-20A型高效液相色谱仪(LC-20AT泵,SIL-20A自动进样器,CTO-20A柱温箱,SPD-20A紫外检测器);赛多利斯公司 CP224S型电子天平(最大值210 g;d=0.1 mg),ME235S型电子天平(最大值210 g;d=0.01 mg)。红霉素对照品(中国药品生物制品检定所,批号为130307-200716,含量为93.5%);红霉素肠溶胶囊(天圣制药集团股份有限公司,批号分别为 101104,101223,110101,110305,110517,规格为 0.25 g);甲醇、乙腈为色谱纯;水为重蒸馏水;其他试剂为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱:Diamonsil C18柱 (250 mm ×4.6 mm,5 μm);流动相:0.067 mol/L磷酸二氢铵溶液(用三乙胺调pH值至6.5)-乙腈(58 ∶42);流速:1.0 mL/min;检测波长:210 nm;柱温:30 ℃;进样量:20μL。按外标法以峰面积计算。
2.2 溶液制备
精密称取红霉素对照品40 mg,至10 mL量瓶中,加甲醇1 mL使溶解,用流动相稀释至刻度,摇匀,作为对照品溶液。取本品20粒的内容物,研细,混匀,精密称取适量(约相当于红霉素100 mg),置25 mL量瓶中,加甲醇2.5 mL使溶解,用流动相稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液。按处方比例,取除红霉素外的其他组分制得阴性样品,按供试品溶液方法制成阴性对照品溶液。取甲醇1 mL至10 mL量瓶中,加流动相至刻度,摇匀,作为空白溶液。
2.3 方法学考察
专属性试验:分别取对照品溶液、供试品溶液、空白溶液和阴性对照品溶液各20μL,注入液相色谱仪,按拟订的色谱条件测定,记录色谱图,结果见图1。可见,溶剂及其他成分对红霉素的测定无干扰,红霉素峰的保留时间约为6 min,能达到基线分离,分离度符合要求,理论板数大于2 000。
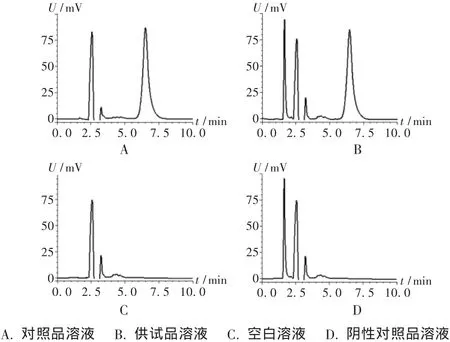
图1 高效液相色谱图
线性关系考察:精密吸取2.2项下的对照品溶液5,10,15,20,25,30,35μL,注入液相色谱仪,按拟订的色谱条件测定红霉素峰面积,以红霉素进样量(X)为纵坐标、峰面积(Y)为横坐标进行线性回归,得回归方程 Y=2.93×104+1.33×105X,r=0.999 9(n=7)。结果表明,红霉素质量浓度在20~140 g/L范围内与峰面积线性关系良好。
精密度试验:精密量取对照品溶液20μL,重复进样6次,按拟订的色谱条件测定。结果峰面积的 RSD=0.35%(n=6),表明方法精密度良好。
重复性试验:取同一批样品(批号为110101)6份,依法制备供试品溶液,并按拟订的色谱条件测定。结果红霉素的平均含量(标示百分含量)为 101.37% ,结果的 RSD 为 0.68%(n=6),表明方法重复性良好。
稳定性试验:取同一供试品溶液 20 μL,分别于 0,2,4,6,8,10,24 h时进样测定。结果的 RSD=0.87%(n=7),表明供试品溶液在24 h内基本稳定。
加样回收试验:精密称取已知含量的供试品6份(每份约相当于红霉素50 mg)至25 mL量瓶中,加甲醇2.5 mL使溶解,分别精密加入质量浓度为 4 g/L 的对照品溶液 10.0,10.0,12.5,12.5,15.0,15.0 mL,用流动相稀释至刻度,摇匀,滤过,取续滤液按拟订的色谱条件测定,计算回收率。结果见表1。
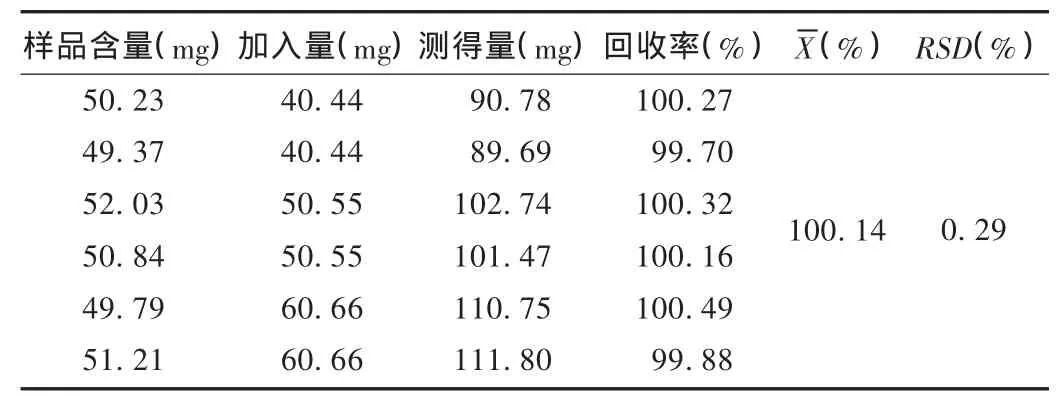
表1 加样回收试验结果(n=6)
2.4 样品含量测定
取5批样品,按2.2项下的方法制备供试品溶液,精密量取20μL,按拟订的色谱条件测定。结果见表2。

表2 微生物检定法和HPLC法检测结果比较(n=5)
2.5 微生物检定法和HPLC法的比较
比较了5个批号样品的微生物检定法和HPLC法检测结果,见表2。两者测得标示量比较,差异无统计学意义(P>0.05),表明本法可替代微生物检定法对红霉素肠溶胶囊的含量进行控制。
3 讨论
在检测波长选择上,取对照品溶液和供试品溶液分别按拟订的色谱条件在安捷伦1260液相色谱仪(二极管阵列检测器)上测定,记录0~10 min,200~400 nm波长范围内的等吸收图和3D图,发现对照品溶液和供试品溶液的光谱图基本一致,红霉素虽在280 nm波长处有最大吸收峰,但吸光强度较弱;而210 nm波长虽不是最大吸收波长,但该处吸光强度较高,辅料杂质干扰较小。试用210 nm测定,取得了满意的线性关系,且有较好的重现性和精密度。故选用该波长作为检测波长。
首先选择乙腈-水为流动相。因样品的极性较大,选磷酸盐作为流动相成分之一,在进行多次试验后,最终选用0.067 mol/L磷酸二氢铵溶液(用三乙胺调pH至6.5)-乙腈(58∶42)作为流动相,可取得较好的峰形和分离度。
红霉素的高效液相色谱法比微生物检定法简便、准确、灵敏度高、重现性好,为红霉素肠溶胶囊的质量控制提供了依据。
[1]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:302.

