漂白粉中固体总钙量的测定*
韩立坤
(潍坊学院,山东 潍坊 261061)
钙在生物体中是一种重要的元素。动物体内的钙不仅参加骨骼和牙齿的组成,而且参与新陈代谢[1]。钙元素是骨骼﹑牙齿﹑蛋壳和细胞壁形成时的重要结构组分,它能降低毛细血管及细胞膜的通透性,从而减少人体的过敏性反应,它是神经传导过程的信使,对于释放激素﹑传递神经脉冲﹑心肌的正常收缩与舒张及血液的凝结等生理过程,均起着极为重要的作用[2]。
钙含量的测定方法有很多种,其中常量钙的测定方法有EDTA配位滴定法、氧化还原法等。微量钙的测定方法有火焰原子吸收光谱法、紫外可见分光光度法、EDTA光度滴定法、微波等离子体—发射光谱法(MPT-AES)等。漂白粉中固体总钙量的测定属于常量钙的测定,与氧化还原滴定法相比,EDTA配位滴定法具有简便、快速等优点,是钙测定方法中应用的较多的领域之一。EDTA络合滴定法是指在pH≥12的条件下,以钙指示剂为指示剂,用EDTA标准溶液滴定。钙指示剂与钙离子生成酒红色络合物,当用EDTA滴定至化学计量点时,游离出指示剂,使溶液呈现纯蓝色[3]。通过实验改变EDTA与钙离子生成络合物的实验条件(如指示剂加入量、NaOH的加入量、NaNO2的加入量及静置时间)的选择,来探究对实验结果最有利的实验条件,从而达到优化实验的目的。
1 实验部分
1.1 主要仪器和试剂
YP502N电子天平(上海精密科学技术有限公司);FA2004N电子分析天平(上海精密科学技术有限公司);A1B气流烘干器(中外合资深圳天南海北有限公司)。
乙二胺四乙酸二钠(天津市科密欧化学试剂开发中心);95%乙醇(青岛海滨化学试剂厂);氢氧化钠(莱阳化工实验厂);碳酸钙(国药集团化学试剂有限公司);钙指示剂(天津市化学试剂研究所)
以上所用试剂均为分析纯试剂,均用蒸馏水配制。
1.2 试剂的配制
CaCO3溶液的配制:置CaCO3基准物质于称量瓶中,在110℃烘箱中干燥2h,冷却后置于干燥器中再冷却至室温后,用差减法准确称取0.26g~0.32g CaCO3基准试剂于250mL烧杯中,加少量蒸馏水润湿,盖上表面皿,慢慢滴加1∶1HCl溶液约3mL使其溶解,加少量蒸馏水稀释,加热微沸几分钟以除去CO2。冷却后用少量蒸馏水冲洗烧杯内壁和表面皿,定量转移到250mL容量瓶中,摇匀[4]。
EDTA溶液的配制:在电子台秤上取量7.4g乙二胺四乙酸二钠,置于500mL干净的烧杯中,加300mL蒸馏水,温热溶解。若浑浊,应过滤。转移到2000mL干净的试剂瓶中,稀释至2000mL,摇匀[5]。
钙指示剂的配制:称取0.5g钙指示剂于100mL乙醇溶液中,充分搅拌使其溶解[6]。
其它试剂:6mol/LNaOH 溶液;1∶1HCl溶液;10%NaNO2溶液。
1.3 实验方法
1.3.1 CaCO3标准溶液的配制和标定
准确称取0.26g~0.32gCaCO3基准试剂于250mL烧杯中,加少量蒸馏水润湿,盖上表面皿,慢慢滴加1∶1HCl溶液约3mL使其溶解,加少量蒸馏水稀释,定量转移到250mL容量瓶中,摇匀。用25mL移液管准确移取Ca2+基准试液于锥形瓶中,加入4滴6mol/LNaOH溶液及NN指示剂4~5滴,用待标定EDTA标准溶液滴定至溶液由酒红色变为纯蓝色即为终点。平行3次,计算EDTA溶液的平均浓度。
1.3.2 漂白粉中固体总钙量的测定
准确称取0.80g~1.00g漂白粉于1000mL烧杯中,加蒸馏水溶解,定量转移到1000mL容量瓶中,摇匀。
用25mL移液管准确移取漂白粉试液于锥形瓶中,加入10mL 10%NaNO2溶液,静置8min。再加入4滴6mol/LNaOH溶液,调节pH≥12加入NN指示剂4~5滴,用EDTA标准溶液滴定至溶液由酒红色变为纯蓝色既为终点。平行3次,计算漂白粉中固体总钙的平均含量。
2 结果与讨论
2.1 标定条件的选择
2.1.1 NN指示剂加入量的影响
控制NaOH的加入量为3mL,改变NN指示剂的加入量,所测数值见表1。
2.1.2 NaOH溶液加入量的影响
以上加入3mL NaOH的实验现象中,均有沉淀,说明NaOH过量,保持NN指示剂的加入量为4滴,改变NaOH的加入量,所测定的数值见表2。

表1 NN指示剂的加入量对滴定终点颜色变化灵敏度的影响
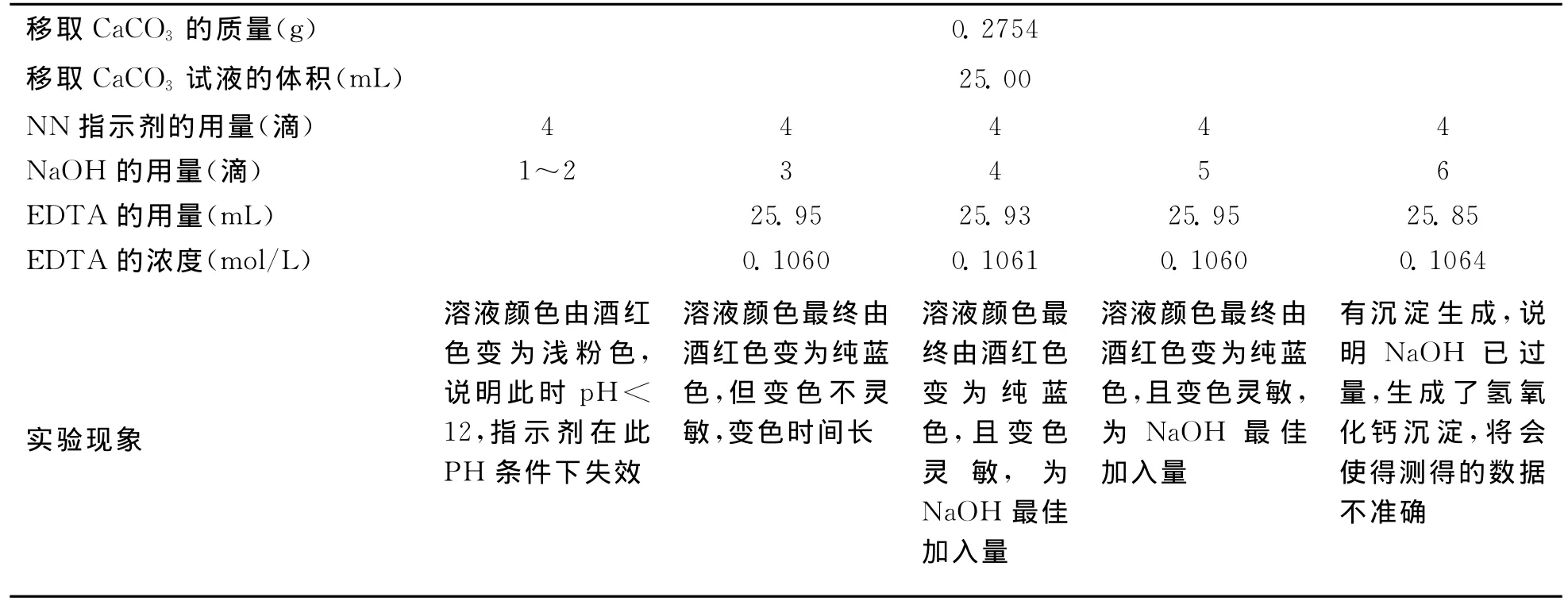
表2 NaOH加入量对测定结果的影响
通过表1、表2可以看出,控制NN指示剂的加入量为4滴,NaOH的加入量为4滴时,变色过程明显,灵敏度高。
2.2 测定条件的选择
2.2.1 静置时间对实验结果的影响
在最佳实验条件下,加入10mL10%NaNO2溶液,改变静置时间,所测定的数值见表3。

表3 静置时间对测定结果的影响
从表3可以看出,加入10%的NaNO2溶液后,静置8min时,为最佳静置时间,此时Ca(ClO)2与NaNO2恰好反应完全,不会对后来加入的指示剂造成影响。
2.2.2 NaNO2加入量对实验结果的影响(见表4)

表4 NaNO2的加入量对实验结果的影响
从表4可以看出,NaNO2的加入量不会对实验结果造成任何影响,但是,不加NaNO2会使得终点无法到达,以致实验无法进行。
3 结束语
本实验以EDTA络合滴定法对漂白粉中的钙含量进行了测定,该方法与氧化还原法[7]相比,不仅操作简便迅速,操作技术易于控制,成本也较低,适于普遍推广,也是钙含量方法中应用最广泛的一种方法。随着工业生产和环境科学的迅速发展,以及人类生活水平的提高,要求分析化学提供更加灵敏快速简便的方法来进行高纯材料和人体微量元素的痕量检测,这需要我们不断寻求新的分析方法。
[1]洪昭毅,薛敏波.人体的钙营养[J].中国儿童保健杂志,2001,(2):105-108.
[2]同济大学普通化学及无机化学教研室.普通化学[M].1版.北京:高等教育出版社,2004:313.
[3]华中师范大学.分析化学[M].3版.北京:高等教育出版社,2001.
[4]余振宝,姜桂兰.分析化学实验[M].1版.北京:化学工业出版社,2005:44.
[5]余振宝,姜桂兰.分析化学实验[M].1版.北京:化学工业出版社,2005:43.
[6]武汉大学.分析化学实验[M].4版.北京:高等教育出版社,2001:285.
[7]陈妙兰.高锰酸钾滴定法测定钙片中钙的含量[J].辽宁化工杂志,2009,38(4):272-275.

