铬黑T光度法测定粮食中的微量铜
斯琴高娃,刘英红,陈文宾,姚 瑶
铬黑T光度法测定粮食中的微量铜
斯琴高娃1,2,刘英红1,陈文宾1,姚 瑶3
(1.江苏省海洋资源开发研究院,江苏 连云港 222005;2.淮海工学院化学工程学院,江苏 连云港 222005;3.南京理工大学化学化工学院,江苏 南京 210094)
建立光度法测定粮食中微量铜(Ⅱ)的新方法。研究表明,pH 10.0硼酸-氯化钾-氢氧化钠缓冲介质中,铜(Ⅱ)与铬黑T发生灵敏的显色反应,生成桃红色的配合物,当显色时间20min,显色剂用量达2.5mL时为最佳条件。配合物最大吸收波长为540nm,表观摩尔吸光系数(ε)为2.99×104L/(mol·cm),铜(Ⅱ) 在0~1.2μg/mL范围内遵循比尔定律。样品测定结果与原子吸收分光光度法的测定结果一致。
铬黑T;光度法;铜;粮食
铜是人体必须的微量元素之一,它具有促进造血机能,维护心血管与骨骼的健康,促进生长发育,保证内分泌正常等多种生理功能[1-2]。缺铜可引起冠心病发病率的提高、皮肤脆弱、思维迟钝等后果,但如果铜在人体内积累过多会引起中毒[3-4]。我国国家标准中规定粮食中铜含量不得高于10mg/kg。因此,粮食及食品中铜元素含量测定非常重要。目前测定微量铜的方法不断涌现[5-11],其中常用的二乙基二硫代氨基甲酸钠法测定食品中的铜,操作繁锁、费时[12];用国家标准方法原子吸收分光光度法测定,仪器昂贵,难以推广应用[13]。分光光度法因具有仪器简单,操作简便,测定快,准确度高等优点而被广泛采用[14-15]。本实验采用分光光度法测定粮食中铜的含量,并与原子吸收分光光度法(atomic absorption spectroscopy,AAS)的测定结果进行比较。
1 材料与方法
1.1 材料、试剂与仪器
玉米、大米、糯米样品 市售。
铬黑T(EBT)、乙醇、CuCl2·2H2O、硼酸-氯化钾-氢氧化钠均为分析纯,实验用水为超纯水。
722N可见分光光度计、pHS-25数显pH计 上海精密科学仪器有限公司。
1.2 溶液的配制
1×10-3mol/L EBT溶液:称取0.2307g的EBT,用无水乙醇溶解,移入500mL容量瓶,用无水乙醇稀释至刻度定容摇匀,浓度为1×10-3mol/L。
铜(Ⅱ)标准储备液(1.0g/L):称取0.6659g CuCl2· 2H2O,加入蒸馏水使其溶解,移入250mL容量瓶中,以水稀释至刻度,摇匀。
铜(Ⅱ)标准工作溶液(10μg/mL):移取2.5mL铜(Ⅱ)标准储备液(1.0g/L)于250mL容量瓶中,以水稀释至刻度,摇匀。
硼酸-氯化钾-氢氧化钠缓冲溶液:取25mL 0.1mol/L NaOH溶液,43.9mL 0.2mol/L硼酸-氯化钾溶液定容至100mL,得pH10.0的缓冲溶液。
1.3 方法
1.3.1 标准曲线的绘制
准确移取适量铜(Ⅱ)标准工作液于25mL容量瓶中,依次加入2.5mL 10-3mol/L EBT溶液,2.5mL pH10.0硼酸-氯化钾-氢氧化钠缓冲溶液,定容于25mL容量瓶,摇匀。20min后,用1cm比色皿,于540nm波长处,以试剂空白为参比,测定溶液的吸光度。
1.3.2 样品测定方法
取干净的玉米、大米、糯米样品2g(准确称量)于250mL的锥形瓶中,加入20mL浓硝酸放置过夜,加5mL浓高氯酸,于沸水浴加热1h,取出后在电炉上暗火加热至冒白烟,当白烟基本消退时,冷却至室温,加5mL HNO3-HClO4(4∶1,V/V)混合液,在电炉上暗火加热至冒白烟,当白烟消退时,冷却至室温,加水,用NaOH调节至近中性,定量转移至250mL容量瓶,摇匀、用超纯水定容,待测。
2 结果与分析
2.1 吸收光谱
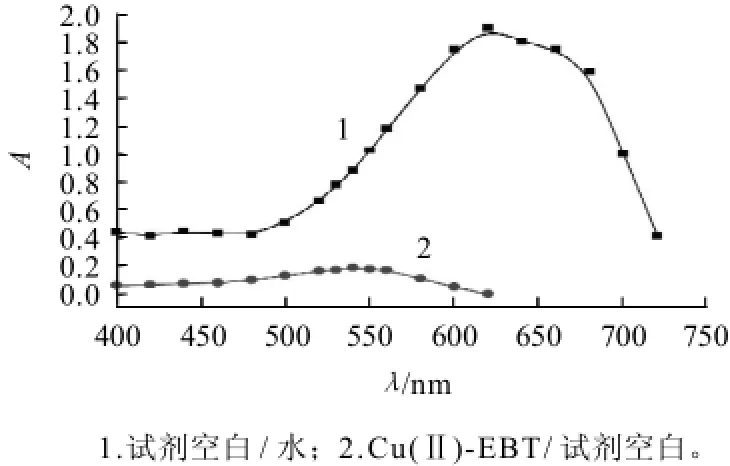
图1 吸收光谱Fig.1 Absorption spectra of Cu(Ⅱ)-EBT complex and blank sample
分别向25mL容量瓶中加入1.0 mL 10μg/mL铜(Ⅱ)标准工作液、2.5mL 10-3mol/L EBT溶液和2.5mL pH10.0硼酸-氯化钾-氢氧化钠缓冲溶液,用水稀释至刻度,并配制相应的不含铜(Ⅱ)的试剂空白溶液。反应20min后,以水为参比,分别对待测溶液和试剂空白溶液进行波长扫描并绘制吸收曲线,结果如图1所示。从图1可以看出,在碱性条件下(pH10.0),试剂EBT最大吸收峰在620nm处,该试剂与Cu2+形成桃红色配合物,配合物最大吸收峰在540nm处,对比度Δλ=80nm,故选540nm为配合物测定波长。
2.2 酸度及缓冲溶液用量
在选定波长(540nm)下,考察不同酸度的硼酸-氯化钾-氢氧化钠缓冲体系对EBT与铜(Ⅱ)显色反应的影响。结果表明,在pH9.4~10.6的缓冲溶液中,加入的缓冲溶液的体积在2.0~5.0mL时,体系的吸光度最大且稳定,如图2、3所示。选用pH10.0的H2B4O7-KCl-NaOH缓冲溶液,用量为2.5mL。

图2 酸度对显色反应的影响Fig.2 Effect of pH on color development reaction
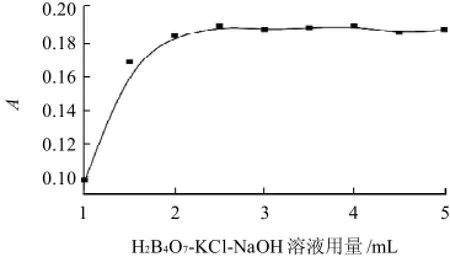
图3 缓冲溶液用量对显色反应的影响Fig.3 Effect of buffer dosage on color development reaction
2.3 显色剂用量
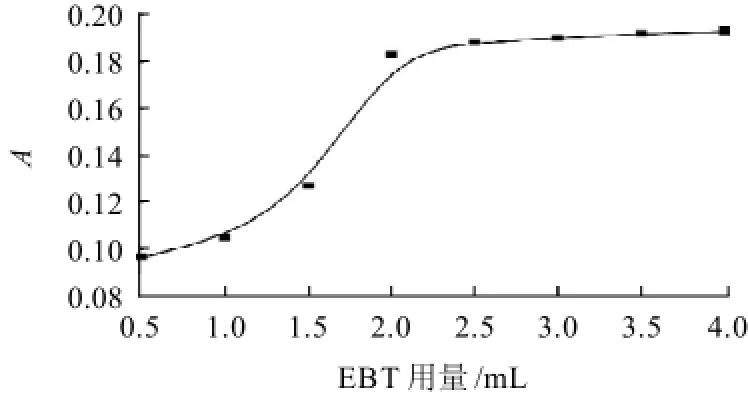
图4 EBT用量对显色反应的影响Fig.4 Effect of EBT dosage on color development reaction
选用pH10.0的H2B4O7-KCl-NaOH缓冲溶液用量为2.5mL条件下,改变EBT溶液的加入体积,考察EBT用量对吸光度的影响,结果如图4所示。实验表明,EBT溶液的用量小于2mL时,吸光度随着EBT体积的增加而增加,说明反应不完全。EBT用量在2.0~3.5mL范围内,配合物的吸光度达到最大且稳定,所以本实验选用2.5mL显色剂。
2.4 显色时间及配合物的稳定性
在以上优化条件下,考察反应时间对体系吸光度的影响,结果如图5所示。实验证明按实验顺序加入试剂:Cu2+→EBT→H2B4O7-KCl-NaOH→稀释至刻度,在室温条件下该体系20min可显色稳定,有色配合物至少可稳定1.5h以上。本实验选择反应20min后进行测定。
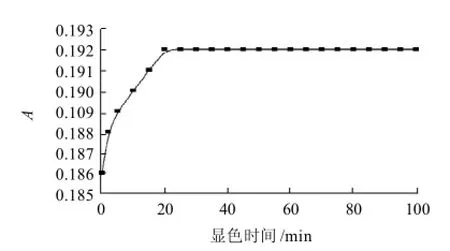
图5 显色时间对显色反应的影响Fig.5 Effect of reaction time on color development reaction
2.5 工作曲线及灵敏度
准确吸取一定量的铜(Ⅱ)标准工作液于25mL容量瓶中,按实验方法操作,以相应试剂空白作参比,测定溶液的吸光度,以吸光度(A)为纵坐标、铜(Ⅱ)质量浓度(C)/(μg/25mL)为横坐标,绘制工作曲线。其线性回归方程为:A=0.0120C+0.0676,线性相关系数r=0.9999;表观摩尔吸光系数ε=2.99×104L/(mol· cm)。Cu(Ⅱ)在0~1.2μg/mL范围内遵循比尔定律。
2.6 干扰离子的影响
在选定条件下,测定25mL显色液中10μg Cu(Ⅱ),相对误差不大于±5%时可允许下列离子共存(以μg计):K+、Na+、As3+、Cl-、、等对测定无干扰。实验结果表明,以下干扰离子对EBT溶液与铜(Ⅱ)的显色反应的影响程度不同,Ca2+、Mg2+、Sr2+、Zn2+、Ni2+、Hg2+、Pb2+、Fe3+、Al3+、Sn4+、Mn2+、Co2+、Ag+等属于此情况。除Mn2+、Co2+能被草酸掩蔽,Fe3+、Al3+能用三乙醇胺掩蔽,其他阳离子能被柠檬酸溶液掩蔽,允许较多量存在。
2.7 样品分析
样品按照1.3.2节方法处理,按标准曲线绘制方法测定样品溶液的吸光度,然后按照标准曲线的回归方程计算样品中铜的含量,将测定结果与原子吸收分光光度法进行比较,同时进行加标回收实验,结果如表1所示,加标回收率在98.0%~104.0%,效果较好。
3 结 论
本实验确定了铬黑T光度法测定食品中铜的最佳条件,并在最佳条件下对粮食中的微量铜含量进行了测定,该方法的加标回收率在98.0%~104.0%,说明方法具有较好的准确度。干扰实验结果表明方法具有较好的选择性。同时采用了简单操作的分光光度计和常用的分析试剂,使得该方法易于普及,具有较好的应用前景。
[1]王丽涛. 微量元素锌铜与人体健康[J]. 微量元素与健康研究, 2007, 24(4)∶ 66.
[2]李青仁, 王月梅. 微量元素铜与人体健康[J]. 微量元素与健康研究, 2007, 24(3)∶ 61-63.
[3]张奶玲, 刘景华, 孙凤春. 铜与人体健康的关系[J]. 世界元素医学, 2007, 14(1)∶ 15-17.
[4]孙健慧. 谈谈铜与人体健康[J]. 心血管病防治知识, 2008(8)∶ 56-58.
[5]严小平. 催化动力学褪色分光光度法测定痕量铜(Ⅱ)及其在食品中的应用[J]. 光谱实验室, 2010, 27(6)∶ 2167-2169.
[6]刘永和, 刘南辉, 黄海燕. 胶束增敏催化分光光度法测定水中痕量铜[J]. 理化检验∶ 化学分册, 2010(9)∶ 1075-1077.
[7]张文德. 微分电位溶出同时测定食盐中铅、铜[J]. 中国调味品, 1999 (11)∶ 26-27.
[8]黄荣斌, 刘连庆, 刘文涵, 等. 催化光度法测定食品中的痕量铜[J].食品科学, 2005, 26(7)∶ 189-191.
[9]YEBRA M D, MORENO-CID A, CANCELA S. Flow injection determination of copper and iron in seafoods by a continuous ultrasoundassisted extraction system coupled to FAAS[J]. International Journal of Environmental Analytical Chemistry, 2005, 85(4/5)∶ 315-323.
[10]BAYTAK S, TURKER A R. Application of ram horn powder (RHP) for the preconcentration and determination of copper in various samples by flame atomic absorption spectrometry[J]. Journal of Analytical Chemistry, 2006, 61(5)∶ 483-489.
[11]TAKAHASHI J, KAWASAKI K. Three-dimensional atom probe analysis of chromium and copper-added nitriding steel[J]. Surface and Interface Analysis, 2007, 39(2/3)∶ 232-236.
[12]魏新军, 汪选兵, 张永生. 二乙基二硫代氨基甲酸钠示差光度法测定微量铜[J]. 食品科学, 2007, 28(10)∶ 458-460.
[13]王晖, 郝莉花, 王龙霞. 火焰原子吸收分光光度法快速测定饮料中的铜[J]. 食品科学, 2007, 28(1)∶ 308-310.
[14]赵丽杰, 赵丽萍, 常勇, 等. 邻菲啰啉活化催化褪色光度法测定食品中痕Cu2+[J]. 食品科学, 2009, 30(10)∶ 169-172.
[15]高向阳, 冉慧慧, 王坤, 等. 南阳彩色小麦面粉中微量铜的快速测定方法研究[J]. 食品科学, 2007, 28(6)∶ 274-276.
Spectrophotometric Determination of Trace Copper in Food Grains with Eriochrome Black T
Siqingaowa1,2,LIU Ying-hong1,CHEN Wen-bin1,YAO Yao3
(1. Jiangsu Marine Resources Develepment and Research Institute, Lianyungang 222005, China;2. School of Chemical Engineering, Huaihai Institute of Technology, Lianyungang 222005, China;3. School of Chemical Engineering, Nanjing University of Science and Technology, Nanjing 210094, China)
A new spectrophotometric method was developed for the determination of trace Cu (Ⅱ) in food grains based on the fact that eriochrome black T (EBT) can form a pink color complex with Cu (Ⅱ) in the presence of H2B4O7-KCl-NaOH medium at pH 10.0. The best color development results were obtained by allowing the reaction to proceed for 20 min in the presence of 2.5 mL of the color developer. The formed complex showed maximum absorption at 540 nm and an apparent molar absorption coefficient of 2.99 × 104L/(mol·cm). Over the range of 0-1.2μg/mL Cu (Ⅱ) solution obeyed Beer,s law. The results obtained for Cu (II) content by this method were in agreement with those obtained by atomic absorption spectrophotometry. Key words:eriochrome black T (EBT);spectrophotometry;copper;food grains
TS211.7
A
1002-6630(2012)18-0223-03
2011-07-17
国家自然科学基金青年科学基金项目(21101069);江苏省海洋资源开发研究院科技开放基金项目(JSIMR10E07);淮海工学院自然科学科研基金项目(2010150018)
斯琴高娃(1978—),女,实验师,硕士,研究方向为分析化学。E-mail:siqingowa@yahoo.cn

