黄铁矿催化类Fenton反应处理阳离子红X-GRL废水
冯 勇,吴德礼,马鲁铭 (同济大学环境科学与工程学院,污染控制与资源化研究国家重点实验室,上海 200092)
染料废水由于具有浓度高、色度深、成分复杂、毒性大、生物可降解性差等特点,已成为工业废水处理的难点之一[1].染料抗光解、抗生物氧化的发展趋势,使得染料废水处理日,仅靠常规处理工艺难以达到理想处理效果[2].阳离子红X-GRL,作为一种偶氮染料中,在印染行业中被广泛使用,且不易被传统的生物处理如活性污泥工艺等降解[3].对其转化降解规律进行研究,对于开发新型有效的印染废水处理工艺具有很强的现实指导意义.传统Fenton反应应用于染料废水的处理已有诸多报道[4-5].但传统Fenton反应pH值适应范围广、催化剂不能重复利用、大量铁泥产生的缺点制约了其大规模应用.研究表明,相对于均相催化反应,多相催化具有催化剂重复利用性好、不易受 pH值影响等优点[6-7].在众多类Fenton催化剂当中,天然含铁矿物由于廉价易得、催化效果好、适用pH值范围广、重复利用性强等优点而受到重视[8-9].本课题组初步研究表明,黄铁矿具有良好的催化活性,能与 H2O2发生高效类Fenton反应,具有作为类Fenton反应新型催化剂的巨大潜力.本研究以阳离子红X-GRL为目标污染物,以黄铁矿为类 Fenton催化剂,在多影响因素正交实验基础上,考察了催化剂跟双氧水用量、溶液初始pH值、目标污染物初始浓度对催化反应的影响;对黄铁矿自身的表面酸性氧化特性进行了考察,包括离子溶出规律及溶液 pH值变化情况等;并对催化机理进行了探讨.
1 实验部分
1.1 试剂与仪器
实验所用双氧水(H2O2质量浓度30%,AR)、浓盐酸(AR)、氢氧化钠(AR)、七水合硫酸亚铁(AR)均购自上海国药集团有限公司;叔丁醇(AR)购自上海润捷化学试剂有限公司;离子色谱用标液(Cl-、SO42-)购自北京上立方联合化工技术研究院;色谱级甲醇购于Fisher Scientific;实验用水为超纯水,黄铁矿过200目筛后使用.所用染料为阳离子红X-GRL,在530nm有最大吸收峰,其化学结构见图1,是一种难以生物降解的偶氮染料.
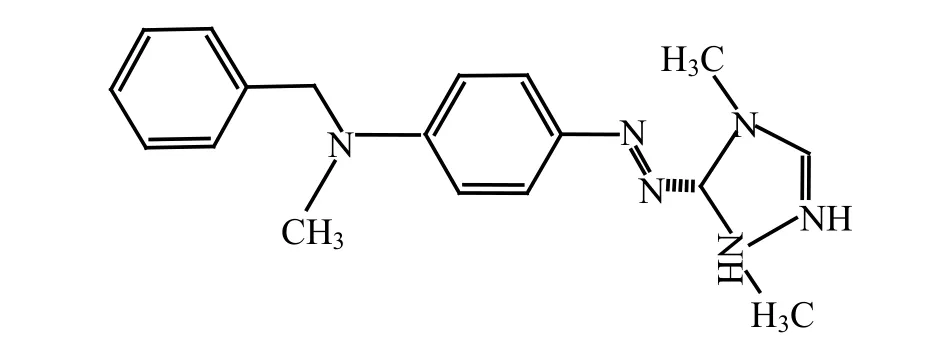
图1 阳离子红X-GRL结构式Fig.1 Structure of Cationic Red X-GRL
XL30扫描电子显微镜,Link300EDS探测器,荷兰Philips公司;TU-1810紫外可见分光光度计,北京普析通用仪器;AG285精密天平,瑞士Mettler Toledo;ICS 900离子色谱,AS23分析柱,戴安;Optima 2100DV电感耦合等离子体发射光谱仪(ICP-AES),PerkinElmer;JJ-4A多头磁力搅拌器,常州国华电器有限公司;Anke TGL-16C高速离心机,上海安亭科学仪器厂;PHS-2F型pH计,上海精科仪器有限公司.
1.2 实验方法
1.2.1 实验步骤 使用实验室配制模拟废水进行研究.取 100mL一定浓度的阳离子红 X-GRL溶液到 200mL烧杯中,加入一定量催化剂和H2O2后,置于磁力搅拌器上慢速搅拌.按设定好的时间定时取样 4.8~5mL离心管中,加入 10μL叔丁醇终止反应后再15000r/min下离心5min后,再进行染料浓度的测定.在无特别说明情况下,本研究中阳离子红 X-GRL溶液初始浓度均为50mg/L,pH值为溶液初始值.
1.2.2 分析测定方法 配置 1,5,10,20,40,50mg/L阳离子红X-GRL溶液,在其最大吸收波长530nm处测定吸光度,得到浓度与吸光值关系.运用紫外分光光度计测定催化氧化降解过程中阳离子红X-GRL的浓度,反应后pH值采用pH计测定.亚铁离子采用 1,10-邻菲啰啉分光光度法测定,总铁采用 ICP-AES测得.反应后溶液中的氯离子、硫酸根离子由离子色谱测定.
1.2.3 正交实验
黄铁矿催化H2O2氧化降解污染物的反应受催化剂和双氧水用量、溶液初始pH值、污染物初始浓度等多种因素的影响.为了综合研究各因素的影响和内在关系,本研究设计了以 H2O2浓度、催化剂用量、反应初始pH值和反应时间为变量的4因素5水平正交实验,见表1.
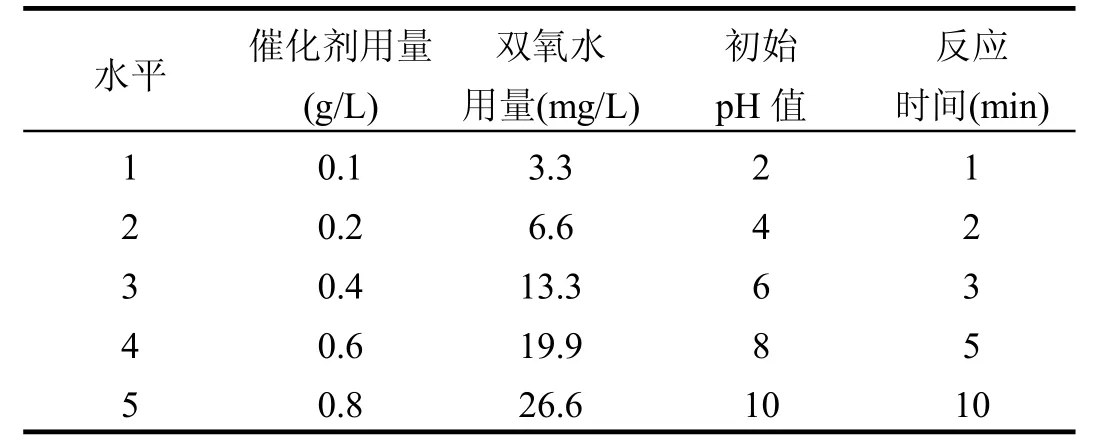
表1 正交实验因素水平Table 1 Factor levels of orthogonal experiment
2 结果与讨论
2.1 黄铁矿表征分析
实验所用黄铁矿为天然矿物磨碎后的微米级颗粒状黄铁矿.由图 2可见,黄铁矿的微观结构较为复杂,有块状、柱状及板块状形态共同存在.其中,在柱状构型上,还可明显观察到有许多孔隙.

图2 黄铁矿的SEM图像(×20000)Fig.2 SEM image of pyrite(×20000)
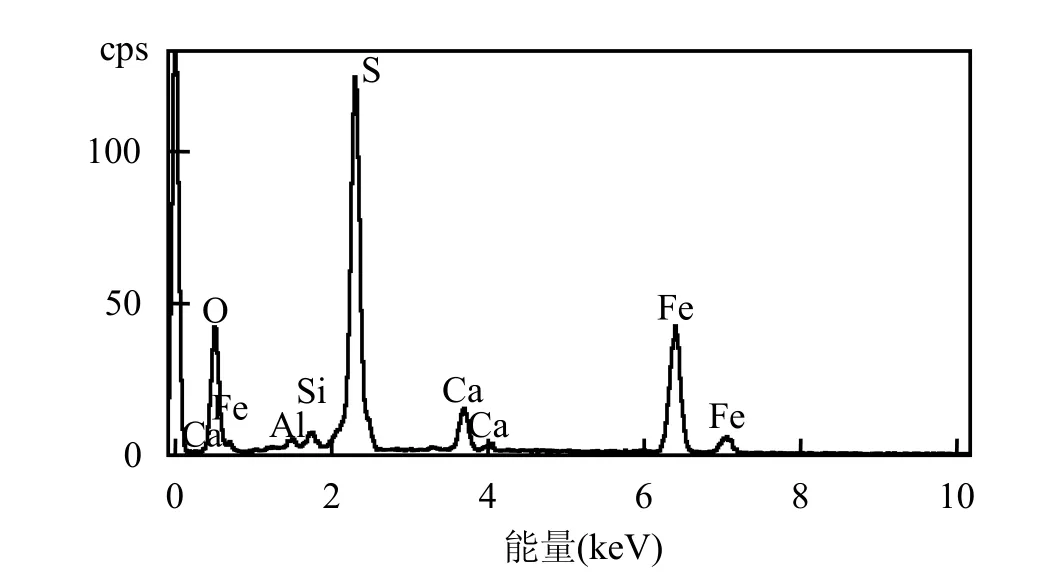
图3 黄铁矿EDS图谱Fig.3 EDS image of pyrite
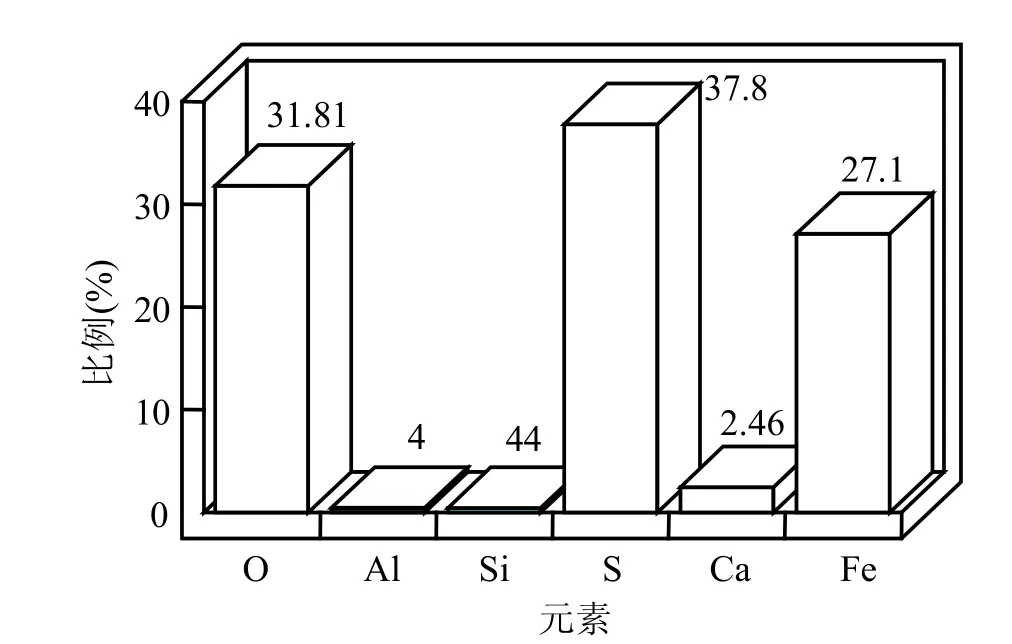
图4 黄铁矿中各元素所占比例Fig.4 Proportion of each element in pyrite
黄铁矿 EDS能谱图显示(图 3),该矿物主要由S、Fe、O元素构成.此外,还可观察到如Si、Al、Ca等少量其他元素存在.图4分析表明,O、S、Fe各元素所占比例分别为31.81%、37.8%、27.1%.黄铁矿主要成分以FeS2晶体形式存在.
2.2 多影响因素正交实验结果
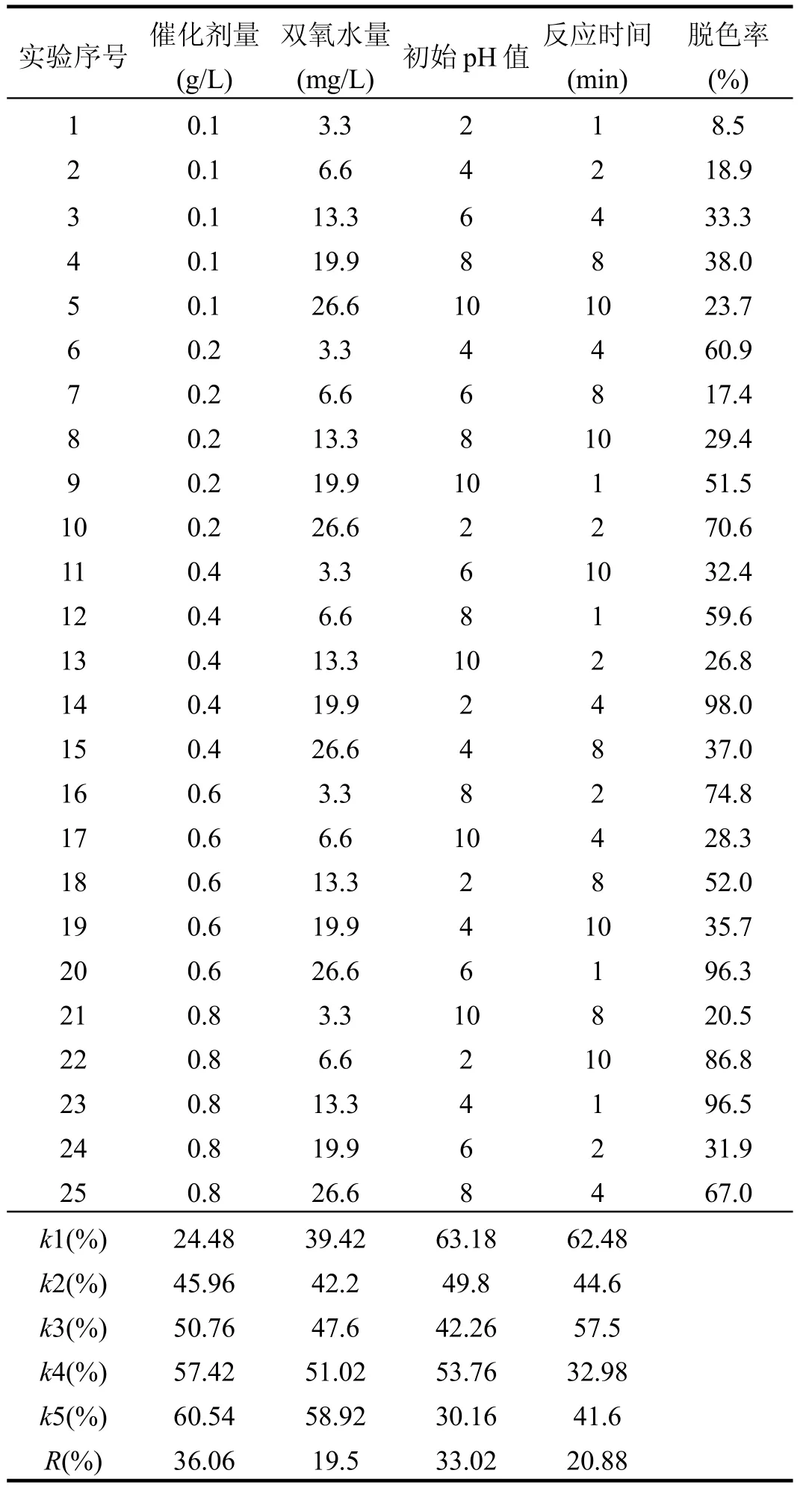
表2 正交实验结果Table2 Result of orthogonal experiment
由正交实验的直接分析法可知,根据极差值大小,在选定的矿跟 H2O2所用剂量范围内,矿的用量对阳离子红 X-GRL的脱色具有很大影响,为最主要影响因素.由于黄铁矿催化 H2O2的反应属于自由基反应,产生的氧化中间产物羟自由基等能快速地破坏染料的显色基团,使阳离子红X-GRL脱色.由表2可看出,反应时间由2min增加至10min对染料的脱色率影响不大.这一现象有别于文献[10]中报道的其他矿物催化下非均相类Fenton反应受反应时间影响较大的特点,因此,推测本研究中染料的快速脱色反应可能不是一个非均相反应控制过程.根据表2结果,确定催化剂和H2O2浓度分别为0.8g/L、13.3mg/L.
2.3 单因素对阳离子红X-GRL脱色效果的影响
2.3.1 溶液pH值对阳离子红X-GRL显色效果的影响 在本实验中,染料的脱色率是通过测定废水的色度来计算的,而很多染料的显色会受到pH的很大影响.所以,首先进行了阳离子红X-GRL在不同pH值条件下的显色实验研究,结果如图5所示.
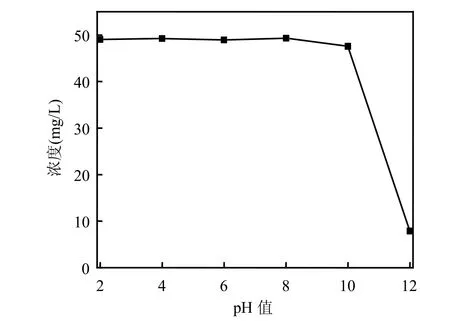
图5 溶液pH值对阳离子红X-GRL显色效果的影响Fig.5 Effect of pH on the color of Cationic Red X-GRL
当pH处于2~10之间时,对阳离子红X-GRL显色影响很小.而当pH值上升至12左右时,测得阳离子红X-GRL浓度小于10mg/L,表明强碱性环境对该染料显色影响很大.在本研究中,除特殊说明外,实验都是在中性条件下进行.
2.3.2 H2O2浓度对阳离子红 X-GRL脱色效果的影响 在1g/L矿用量下,阳离子红X-GRL脱色效果随 H2O2浓度的增加而呈上升趋势.当H2O2浓度为 13.3mg/L时,反应10min后,染料脱色率高达80%以上.此外,从图6还可明显看出反应时间对染料脱色效果的影响不显著.这说明在该氧化反应体系中,阳离子红 X-GRL的脱色过程非常迅速.
2.3.3 黄铁矿用量对阳离子红 X-GRL脱色效果的影响 如图7所示,在H2O2浓度26.6mg/L,没有黄铁矿存在的情况下,溶液的脱色率仅为5%左右,且不随反应时间发生变化.当黄铁矿用量为0.5g/L时,阳离子红X-GRL的脱色率在反应前5min内随反应时间的延长而提高.当矿用量达1g/L以上时,溶液脱色效果随时间的变化关系不明显.
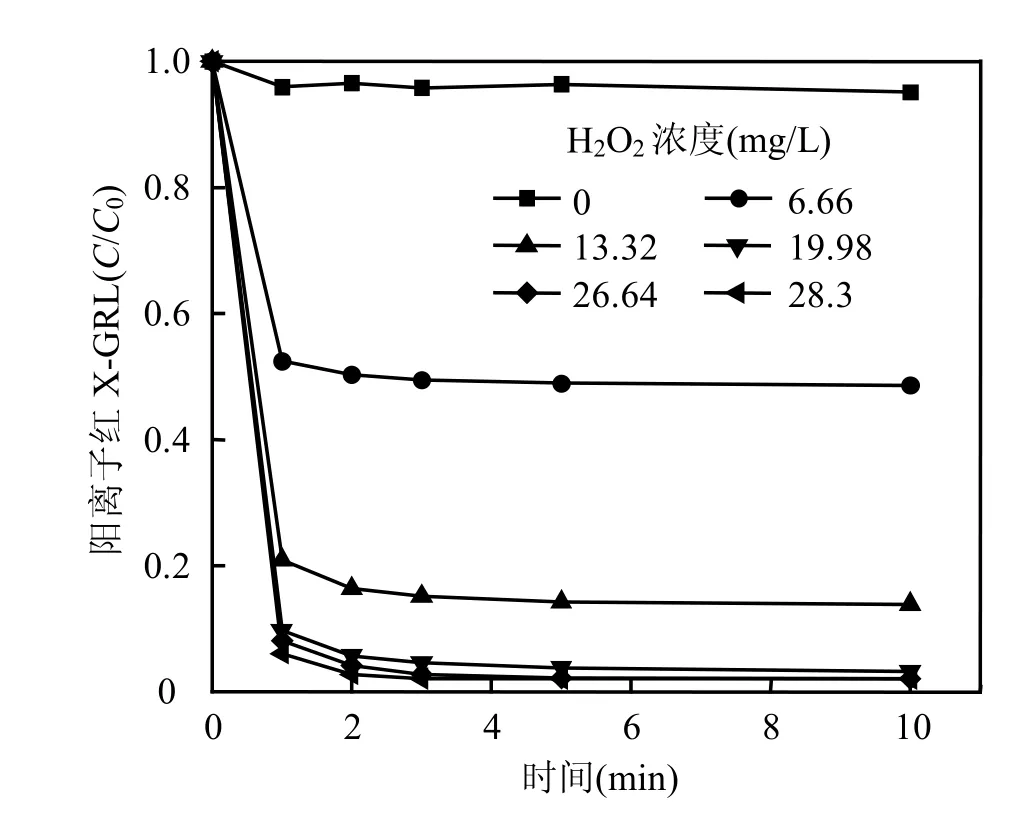
图6 H2O2浓度对阳离子红X-GRL脱色效果的影响Fig.6 Effect of H2O2concentration on the color removal efficiency
黄铁矿催化H2O2的反应属于固液界面反应,目前对于该反应过程的合理解释之一是反应物质首先扩散到催化剂表面,再与催化剂形成络合物,紧接着发生系列的电子转移,最终产生的氧化产物发生脱附及活性位点的再生.因此,反应的快慢会受到催化剂用量多少的影响.
2.3.4 阳离子红 X-GRL初始浓度对脱色效果的影响 图8显示了不同阳离子红X-GRL初始浓度对脱色效果的影响.在H2O2浓度19.98mg/L,矿用量 1g/L条件下,反应10min后,初始浓度为50mg/L的阳离子红 X-GRL溶液脱色率高达95%以上.在同样 H2O2跟黄铁矿用量条件下,提高阳离子红 X-GRL初始浓度后,脱色率呈明显下降趋势.当染料初始浓度为 300mg/L,反应10min后,去除率仅为45%左右.这一过程主要受制于反应体系中H2O2的浓度,如果增加H2O2的投加量,染料则可以继续氧化脱色.值得注意的是,目标污染物初始浓度的提高并没有影响反应速率,说明黄铁矿催化 H2O2氧化是非常快速的反应.
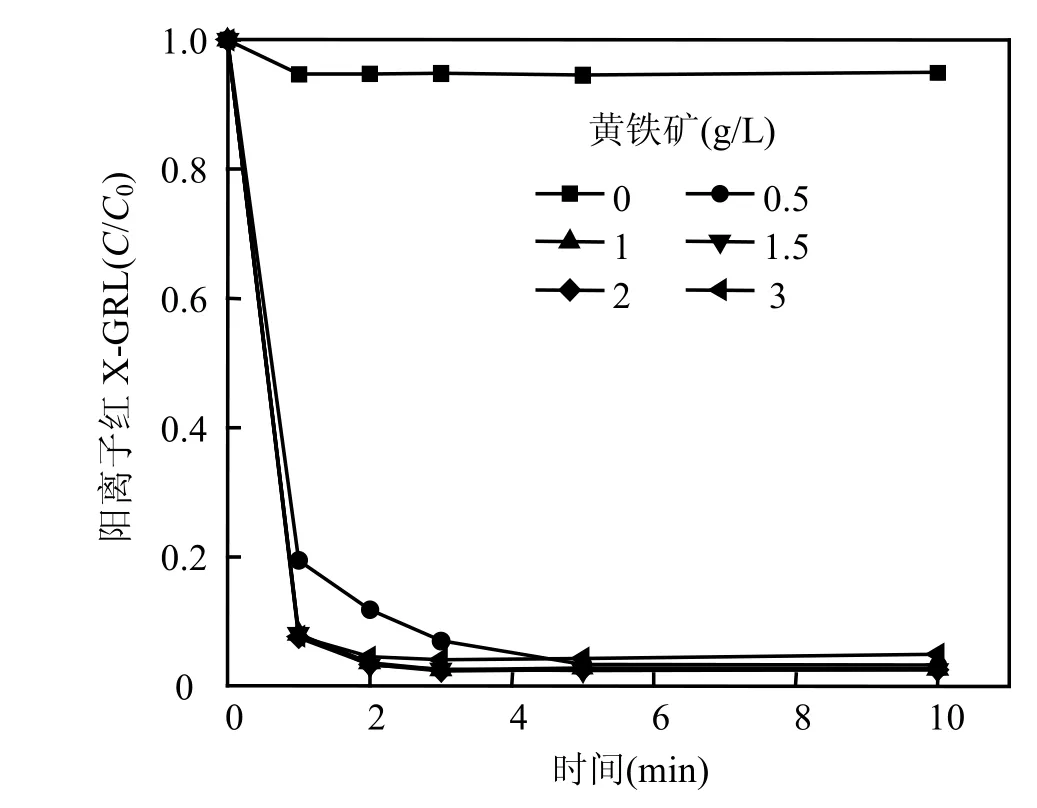
图7 黄铁矿用量对阳离子红X-GRL脱色效果的影响Fig.7 Effect of pyrite dosage on the color removal efficiency
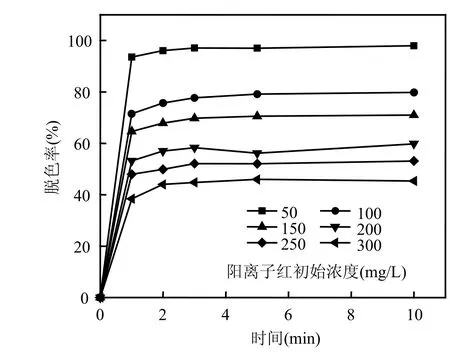
图8 阳离子红X-GRL初始浓度(mg/L)对脱色效果的影响Fig.8 Effect of initial substrate concentration on the color removal efficiency
2.3.5 溶液初始 pH值对脱色效果的影响pH值是 Fenton反应最重要的影响因素之一,传统Fenton反应受 pH值影响很大,非均相类 Fenton虽然能在较广 pH值范围内保持较高反应活性,但仍受溶液pH值影响.
吴大清等[10-11]使用磁黄铁矿催化H2O2降解苯酚的研究中表明,反应速率受 pH值的影响很大,溶液 pH值较低时反应速率较快.pH 3. 81时,20min内苯酚被分解99 %以上.随pH值升高,反应速率下降,pH5. 54时,需反应1h苯酚分解率才达99%.而pH5. 88时,达到同样效果需反应7h左右.在使用针铁矿、纤铁矿、赤铁矿和磁铁矿4种矿物分别催化 H2O2对苯酚的处理研究中,当pH>5时,苯酚在4种反应体系中均没有发生明显的转化和矿化现象.本研究中,初始 pH值对溶液脱色效果的影响见图9.由图9可知,无论是在强酸还是强碱条件下,脱色效果都受到了很大程度的抑制.当溶液初始pH值为2时,反应10min后,溶液脱色率仅 50%左右.这可能是强酸性条件下H2O2分解受到抑制,致使产生的氧化中间产物量减少的缘故.当pH为12时,溶液的脱色率达75%左右.值得注意的是,pH值对阳离子红X-GRL显色效果影响的结果(图4)表明,碱性环境对阳离子红X-GRL显色有较大的副作用.如果仅考虑pH值对显色的影响,脱色率应该远高于 75%(图 5).值得注意的是,本研究所用黄铁矿自身有很强的酸性氧化特性.在与水及 O2的作用下,表面能够迅速发生一系列化学反应,同时释放出大量 Fe2+和H+,降低溶液的pH值(图11).因此,黄铁矿加入初始pH值为12的溶液后,溶液pH值迅速降低,从而对染料显色的副作用减弱.图 9观察到的75%左右的脱色率是氧化与溶液pH值共同作用的结果.
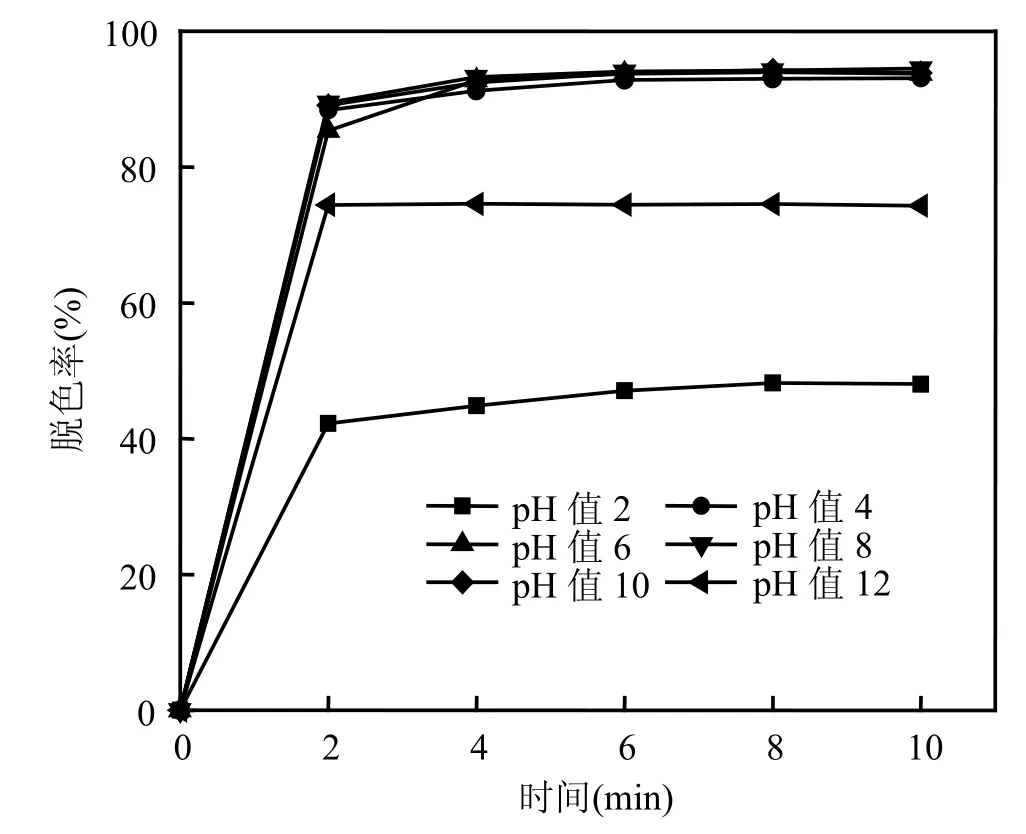
图9 溶液初始pH值对脱色效果的影响Fig.9 Effect of initial pH on the color removal efficiency
2.3.6 反应前后紫外扫描图谱 图10显示了阳离子红X-GRL溶液反应前和催化反应后的紫外扫描图谱.矿与H2O2浓度分别为1g/L、13.32mg/L.反应之前,在 530nm 处可明显观察到阳离子红X-GRL有最强吸收峰,且在近紫外波长190~400nm 范围内吸光值普遍较低.当加入黄铁矿跟H2O2,反应1min后,530nm处染料的特征吸收峰明显减弱,近紫外区吸收显著增强.说明大部分阳离子红 X-GRL的显色基团已经被破坏,且可能有大量新物质的产生.由图 10还可看出,反应时间对染料溶液脱色的影响不显著.
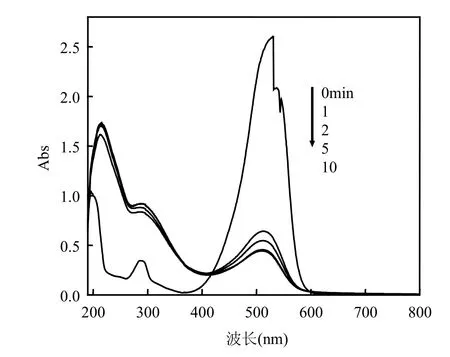
图10 反应前后光谱扫描Fig.10 Spectral scan image of dye water solution
2.3.7 反应机理探讨 Fenton试剂的反应机理,一般认为是 Fe2+、Fe3+、H2O2、•OH、HO2•、O2-•等无机物之间的反应,实质是H2O2在Fe2+的催化作用下产生高反应活性的羟自由基.关于 Fe2+和H2O2之间的链式反应机理[12]可表示为:

Fe2+与H2O2的反应速率很快,在pH 5时反应速率高达5.7×102.产生的羟自由基具有强氧化能力和加成反应特性,其氧化能力仅次于氟,高达2.80V,可以氧化降解水中各种污染物,使其彻底矿化为CO2、H2O及无机盐类等小分子物质.
将天然黄铁矿用于催化H2O2的类Fenton反应还未见报道.但将含铁矿物如磁铁矿、赤铁矿、针铁矿等用于催化剂研究已受到广泛重视.目前,对于矿物催化类Fenton反应机理的解释,仍未获得一致的结论.Lin等[13]在研究针铁矿催化分解H2O2时指出,非均相类Fenton反应是一自由基反应过程.反应开始是 H2O2在铁矿物表面形成一种内层配合物.该内层配合物可视为一基态物质,在配合物与金属元素之间的可逆性电子转移起中介作用.具体反应过程可表示如下[13]:
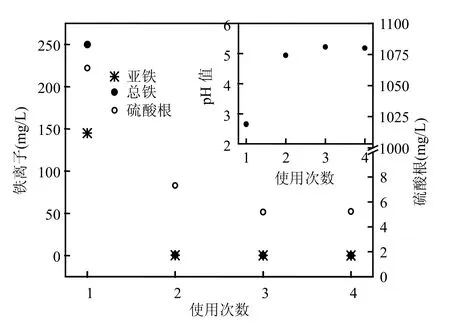
图11 铁离子、硫酸根及溶液pH值随矿使用次数的关系Fig.11 Effect of reutilization times on the leaching of iron and sulfate. Inset, solution pH over reutilization times.
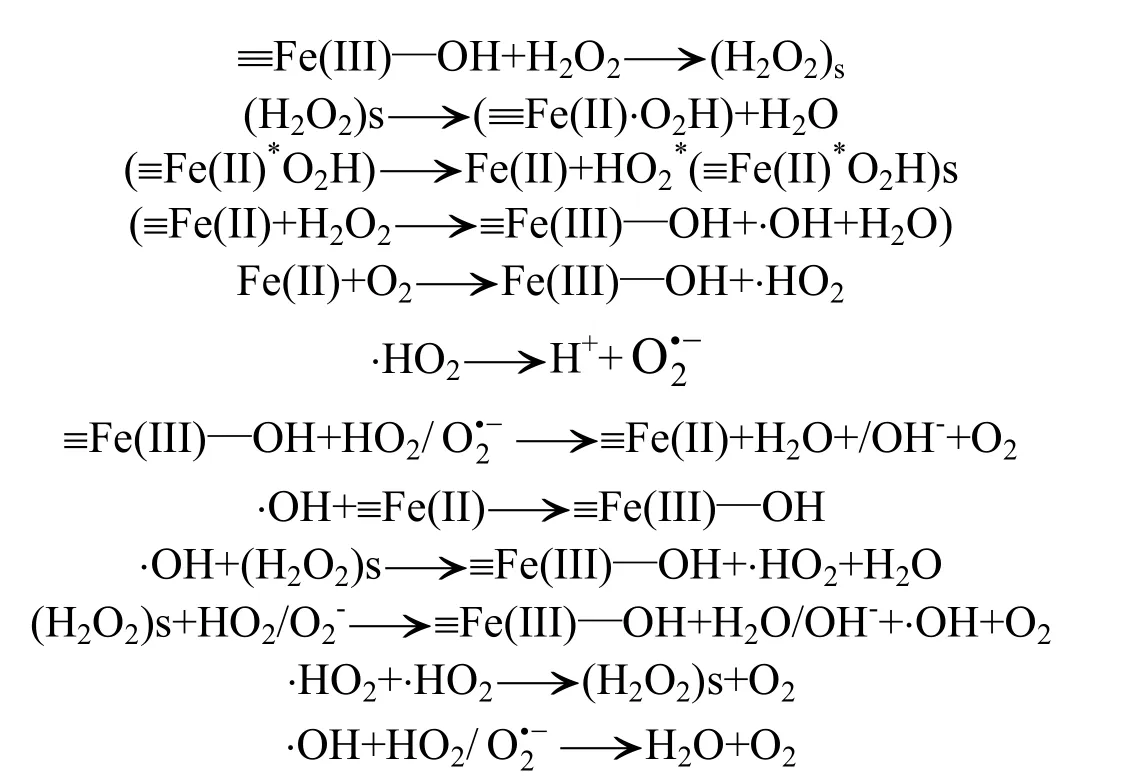
在本研究中,阳离子红 X-GRL溶液脱色迅速,反应时间对脱色效果的影响不显著.因而,黄铁矿/H2O2反应体系有别于其他矿物催化下的类Fenton反应[13-14].通过测定溶液中铁离子、硫酸根离子浓度及反应前后pH值的变化,对黄铁矿单一体系在水溶液中的酸性氧化行为进行了研究.同时,为了考察黄铁矿的重复利用性能,进行了多次重复利用实验,黄铁矿用量均为 5g/L,反应时间均为 10min,其结果如图 11所示.由实验结果得知,黄铁矿在初次使用时能够产生大量的溶解态Fe2+和SO42-,且能够使水溶液pH值由初始6.2降低至2.7左右.然而,在进行2次及以上重复利用实验时,溶出的 Fe2+和 SO42-大大减少,且对水溶液pH值的影响也明显下降.但目前大多认为黄铁矿的酸性氧化过程可通过式(1)来表示[15]:
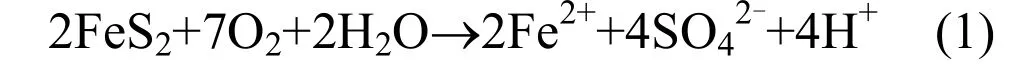
结合实验现象,表明阳离子红 X-GRL溶液的快速脱色是由黄铁矿酸性氧化过程产生的Fe2+与H2O2以Haber-Weiss机理发生均相Fenton反应产生的氧化性物种造成的.当黄铁矿第 2次使用时,由于酸性氧化溶出的Fe2+大为降低,因此反应速率应大为下降,氧化性物种主要通过发生在黄铁矿表面的非均相反应产生.
3 结论
3.1 黄铁矿作为一种新型类Fenton反应催化剂,具有非常高的催化活性,在 H2O2浓度为26.6mg/L、黄铁矿用量1g/L、溶液初始pH值为6.4的条件下,反应2min后, 初始浓度50mg/L的染料溶液脱色率高达95%左右.
3.2 初次使用时,黄铁矿自身具有很强的酸性氧化特性.在与H2O及O2作用下,该过程有大量的 Fe2+、SO42-及 H+溶出.重复使用时,该酸性氧化效果不显著.
3.3 染料溶液的快速脱色主要归因于酸性氧化过程溶出的Fe2+与加入的H2O2发生均相Fenton反应产生的氧化性物种.
[1]Wang Z H, Ma W H, Chen C C, et al. Light-assisted decomposition of dyes over iron-bearing soil clays in the presence of H2O2[J]. Journal of Hazardous Materials, 2009,168(2/3):1246-1252.
[2]Yang Y W, Zhou T L, Qiao Q C, et al. Experimental study of wastewater treatment of reactive dye by phys-chemistry method[J]. Journal of China University of Mining and Technology,2007,17(1):96-100.
[3]Zhao W R, Xu X H, Shi H X. Degradation mechanism of cationic red X-GRL by ozonation [J]. Chinese Chemical Letters,2003,14(12):1309-1312.
[4]Bianco B B, Michelis I D, Veglio F. Fenton treatment of complex industrial wastewater: Optimization of process conditions by surface response method [J]. Journal of Hazardous Materials,2011,186(2/3):1733-1738.
[5]Kim T H, Park C, Yang J M. Comparison of disperse and reactive dye removals by chemical coagulation and Fenton oxidation [J].Journal of Hazardous Materials, 2004,112(1/2):95-103.
[6]Barreiro J C, Capelato M D, Martin N L. Oxidative decomposition of atrazine by a Fenton-like reaction in a H2O2/ferrihydrite system [J]. Water Research, 2007,43(1):55-62.
[7]张亚平,韦朝海,吴超飞,等.光Fenton反应的Ce-Fe/Al2O3催化剂制备及特性表征 [J]. 中国环境科学, 2006,26(3):320-323.
[8]Xue X, Hanna K, Abdelmoula M, et al. Adsorption and oxidation of PCP on the surface of magnetite: Kinetic experiments and spectroscopic investigations [J]. Applied Catalysis B:Environmental, 2009,89(3/4):432-440.
[9]吴德礼,段 冬,马鲁铭.黄铁矿烧渣催化 H2O2氧化废水中难降解污染物 [J]. 化工学报, 2010,61(4):1001-1008.
[10]吴大清,刁桂仪,袁 鹏.氧化铁矿物催化分解苯酚的动力学速率及其产物特征 [J]. 矿物岩石地球化学通报, 2006,25(4):293-298.
[11]吴大清,刁桂仪,袁 鹏.磁黄铁矿催化分解苯酚反应动力学及其产物特征 [J]. 矿物岩石地球化学通报, 2007,26(2):132-135.
[12]Bossmann S H, Oliveros E, Setal G B. New evidence against hydroxyl radicals as reactive intermediate in the themal and photochemically enhanced Fenton reaction [J]. Phys. Chem. A,1998,102(28):5542-5550.
[13]Lin S S, Gurol M. Catalytic decomposition of hydrogen peroxide on iron oxide: kinetics, mechanism, and implications [J].Environmental Science and Technology, 1998,32(10):1417-1423.
[14]Kwan W P, Voelker B M. Rates of hydroxyl radical generation and organic compound oxidation in mineral-catalyzed Fentonlike systems [J]. Environmental Science and Technology,2003,37(6):1150-1158.
[15]Pascale B G, Alnot M, Ehrhardt J J, et al. Surface oxidation of pyrite as as function of pH [J]. Environmental Science and Technology, 1998,32(19):2839-2845.

