重组人生长激素治疗特发性矮小12个月疗效评估
武华红 李 辉 孙淑英
自20世纪80年代基因重组人生长激素(rhGH)问世以来,已成为治疗身材矮小的主要手段。特发性矮小(ISS)作为身材矮小患者中所占比例最大的一组人群,是否需要给予rhGH治疗也成为争议的焦点[1]。2003年,美国FDA批准ISS为rhGH治疗的适应证。但ISS患儿病因未明,其本身可能包含了很多种未知的疾病,而且自身GH并不缺乏,故rhGH治疗效果不如GH缺乏患儿明显,且个体疗效差异较大。近年来,应用rhGH治疗的ISS患儿逐渐增多,国内外相关研究对ISS患儿的治疗进行了影响因素分析,并建立了疗效的预测模型[2,3],以此作为指导临床用药和优化治疗效价比的方法,但其临床应用并不多见,对于不同人群的适用性和有效性还需进一步论证。本研究回顾性分析了ISS患儿治疗过程中生长指标的变化,探讨ISS患儿疗效及影响因素,为寻求优化治疗方案提供参考依据。
1 方法
1.1 病例纳入标准 本研究数据资料来源于首都儿科研究所(我院)专家门诊部病例库的现存病历,满足以下条件的病例被纳入:①2003年2月至2011年7月在我院生长发育门诊确诊为ISS的患儿;② 遵循医嘱规律用药、用药时间在1年以上且在治疗后定期随访的患儿。
1.2 ISS诊断标准 ①身高在同性别、同年龄、同种族正常人群的2个标准差分值(SDS)以下;②出生时身长和体重正常,而且身材匀称;③生长速率稍慢或正常,一般每年生长速率<5 cm,骨龄正常或延迟;④两种药物的GH兴奋试验(可乐宁,左旋多巴,精氨酸或胰岛素低血糖试验)中至少有一项GH峰值≥10 μg·L-1;⑤染色体检查正常,排除其他内分泌疾病和慢性疾病[4]。
1.3 设组 ISS患儿就诊时依据家长意愿给予或不给予rhGH治疗,将入组病例分为rhGH组(予rhGH治疗)和对照组(未予rhGH治疗)。同时依据年龄分为青春期前(男≤10岁,女≤9岁)、青春早中期(男~13岁、女~12岁)和青春后期(男>13岁、女>12岁)。
1.4 随访 rhGH组患儿在治疗后1、3、6、9和12个月随访。纳入本文分析的随访项目包括:rhGH用量、身高、体重、骨龄(BA)、身高年龄(HA)和胰岛素样生长因子(IGF-1)等。
1.5 分析指标 身高采用2009年颁布的中国儿童体格发育新标准进行标化[5],以HtSDS表示,计算采用国际公认的LMS方法[6],公式:

其中X为实测值,M为中位数,S为变异系数,L为将资料转换成对称分布所需的度量偏度的Box-Cox转换幂。
本研究分析的指标有以下几项:①治疗后不同时点HtSDS;②治疗后不同时点生长速度(GV);③治疗后不同时点与基线时点HtSDS的变化(ΔHtSDS)、身高的变化(ΔHt)、BA的变化(ΔBA)和HA的变化(ΔHA)。
2 结果
2.1 一般情况 符合纳入标准的ISS患儿68例进入分析,男38例,女30例。rhGH组35例,平均rhGH用量为(0.15±0.03)U·kg-1·d-1,青春期前14例、青春早中期15例、青春后期6例;对照组33例。一般情况如表1所示。
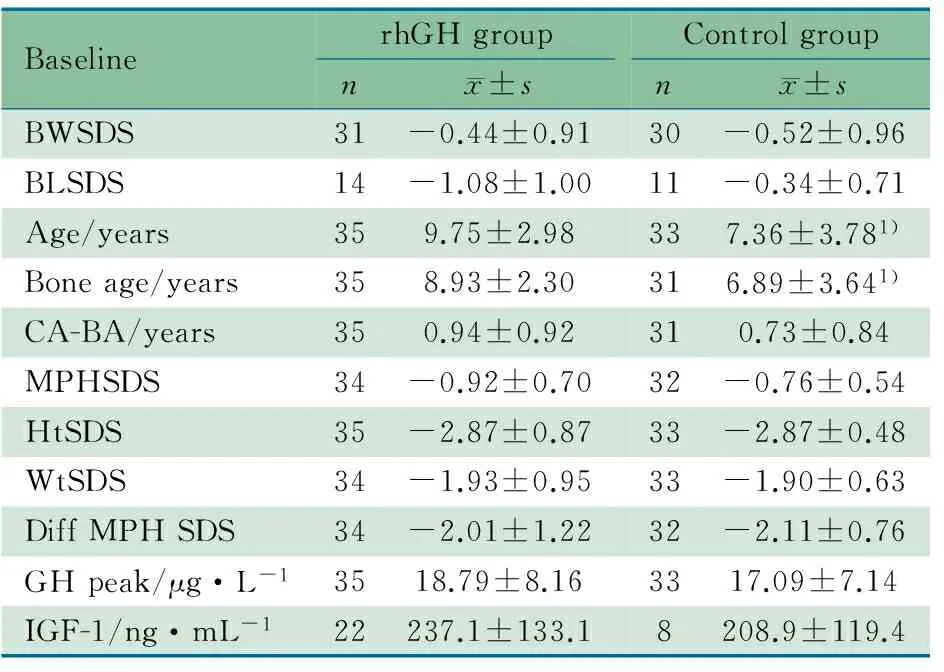
表1 rhGH组和对照组的基线资料
Notes 1)P<0.05; BW:birth weight; BL:birth length; CA-BA: chronological age-bone age; MPH:midparent height; Ht: height; Wt: weight; SDS: standard deviation score; GH peak was the peak value in the GH stimulation test; IGF-1: insulin-like growth factor; MPH: (father height+mother height+/-13 cm)/2; Diff MPH SDS: HtSDS-MPHSDS
rhGH组平均年龄为9.8岁,平均BA为8.9岁,与对照组差异均有统计学意义(P<0.05),余基线资料(出生体重、遗传身高、父母身高中值、身高和体重的SDS、GH峰值和IGF-1水平)两组差异均无统计学意义(P>0.05)。
2.2 身高水平的变化 rhGH组治疗后12个月随访到33/35例,对照组随访到26/33例。rhGH组治疗前、治疗后12个月HtSDS分别为(-2.87±0.87)和(-2.19±0.97),呈增长趋势(P<0.05);对照组分别为(-2.87±0.48)和(-2.80±0.45),未见升高趋势(P>0.05)。
进一步分析rhGH组治疗后不同时段的疗效(表2),结果显示,治疗后0~3个月的ΔHtSDS水平均高于~6、~9和~12个月,但差异无统计学意义。按每6个月进行分析,治疗后0~6个月ΔHt和ΔHtSDS水平均显著高于~12个月。
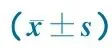


Ther-apyinter-valΔHt/cmΔHtSDSGV/cm·year-1Every3months(n=32)0-32.61±0.760.22±0.1310.78±2.70-62.60±0.620.20±0.1010.52±2.44-92.10±0.660.12±0.148.31±2.78-122.14±0.620.14±0.158.50±2.29P>0.05>0.05>0.05Every6months(n=32)0-65.24±1.230.43±0.2010.48±2.17-124.24±1.090.27±0.248.48±2.39P<0.01<0.01<0.01
2.3 影响疗效的因素 分析rhGH组治疗12个月的疗效,结果显示疗效的个体差异较大,身高水平增长最大为1.51 SDS,最小为-0.23 SDS,平均为0.68 SDS;GV最大为14.55 cm·year-1,最小为6.46 cm·year-1,平均为9.54 cm·year-1。
相关性分析仅发现治疗后12个月ΔHtSDS与治疗开始时的年龄呈负相关(r=-0.428,P=0.01),与治疗后0~3个月的ΔHtSDS呈正相关(r=0.715,P=0.00)。治疗后12个月GV水平与患儿治疗前的GH峰值(r=-0.367,P=0.04)和治疗后3个月的GV(r=-0.692,P=0.00)呈负相关。
进一步按不同年龄进行分析,结果显示,治疗后12个月青春期前、青春早中期和青春后期ΔHtSDS分别为(0.89±0.35)、(0.58±0.30)和(0.46±0.44),差异总体上有统计学意义(P=0.016),其中青春期前显著高于青春早中期和青春后期(P<0.05),青春早中期与青春后期差异无统计学意义。青春期前、青春早中期和青春后期GV分别为(9.65±1.76)、(9.92±1.98)和(8.24±1.26)cm·year-1,差异无统计学意义(P=0.240)。
2.4 BA和HA的变化 rhGH组治疗后12个月ΔBA为(1.22±0.60)岁,对照组为(1.17±0.89)岁,两组差异无统计学意义(P=0.88)。rhGH组ΔHA为(1.55±0.37)岁,对照组为(0.87±0.18)岁,两组差异有统计学意义(P=0.00)。
2.5 治疗过程中IGF-1的变化 rhGH组治疗期间IGF-1变化如图1所示,IGF-1治疗后1个月升高较明显,之后升高趋势减缓。未发现治疗后不同时点IGF-1水平与身高增长有显著相关性。
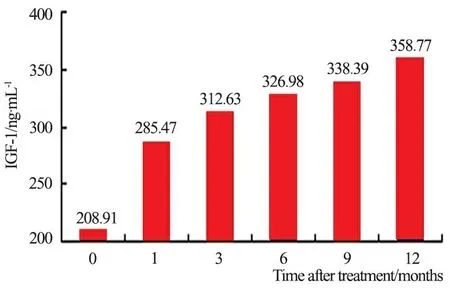
图1 rhGH组治疗12个月IGF-1变化趋势
Fig 1 The first year changes of IGF-1 in rhGH group
3 讨论
本研究rhGH组平均年龄和BA分别为9.75岁和8.93岁,均显著高于对照组,余基线资料差异无统计学意义,可能提示患儿年龄和BA是影响是否选择GH治疗的因素。
本研究结果显示,rhGH组身高水平处于升高趋势,治疗不同时点的疗效不同。从每3个月的疗效来看,0~3个月的ΔHtSDS和GV高于~6、~9和~12个月,但差异无统计学意义,考虑可能与本研究样本量较少有关;治疗0~6个月疗效优于~12个月,考虑可能因为治疗初期经历了一个快速追赶生长期后,进入了一个相对稳定的生长阶段[7],但也有学者认为与治疗过程中出现了GH抵抗有关[8]。另有多项研究也证实了GH用于ISS患儿可提升其身高水平[9~11],但考虑到ISS病因不明确,有可能包含了很多未知的疾病,因此疗效的个体差异较大,疗效也不如GH缺乏患儿明显。有研究报道,ISS患儿治疗1年后身高增长3.65~12.0 cm,ΔHtSDS为0~0.7;随访至最终身高者,患儿身高平均增长1.3 SDS,实际增长值约8.0 cm[3,12,13]。本研究rhGH组治疗12个月身高平均增长9.54 cm和0.68 SDS,与国内外同类研究相符。与我院生长发育门诊确诊为GH缺乏患儿疗效[14]的比较显示,rhGH治疗第1年身高增长10.56 cm和0.93 SDS,身高增长较ISS患儿明显。
考虑到ISS不同个体疗效差异较大,治疗开始时的年龄是影响疗效的关键因素之一,前期的治疗反应可作为长期治疗效果的一个预测因素。本研究中疗效与治疗开始时的年龄及患儿体内的基础GH分泌峰值有关。治疗开始时间越早效果越好,但rhGH在小年龄患儿的耐受性较差,推荐rhGH治疗的最佳年龄为5岁至青春期[15]。Moore等[16]对ISS患儿的研究也发现,唯一具有临床显著性的预测因素是治疗开始时的年龄,但GH峰值无法预测治疗反应,这可能与GH刺激试验的重复性较差有关。Ranke等[2]和Albertsson-Wikland等[13]对ISS患儿应用rhGH治疗的效果分析显示,除疗效与治疗开始时的年龄以及GH分泌峰值有关外,还与GH用量存在剂量依赖性。本研究因样本量不足,未能建立预测模型,也未发现疗效与GH剂量间的相关性,可能与患儿用药剂量相对固定有关。另有研究发现24 h GH分泌高峰与瘦素对治疗反应有预测作用;ISS患儿的GH受体多态性对治疗反应也有影响[17~19],但这些指标在临床实践由于测量方法较复杂,应用还较少。同时,本研究发现治疗前3个月的疗效与治疗12个月的效果显著相关,提示在今后的治疗中可用短期的治疗来预判患儿对rhGH的反应,为进一步治疗方案的制定或调整提供参考。
本研究显示,rhGH治疗不会使ISS患儿BA出现明显加速。以HA作为患儿身高水平的指标,可见rhGH治疗1年后,ΔHA大于ΔBA;rhGH组与对照组相比,HA明显提高,但BA增长并无显著差异;与相关文献报道结果较为一致[20,21],提示rhGH治疗不会引起ISS患儿BA的过快进展,损害生长潜力。
治疗过程中,定期监测IGF-1水平对保障治疗的安全性和有效性均有一定意义。本研究中IGF-1在予rhGH治疗后呈升高趋势,治疗的第1个月升高最为明显,未发现IGF-1变化与身高增长水平之间的关系,考虑与样本量较小有关。Cutfield等[22]评估了IGF-1在rhGH疗效中的价值,显示治疗第1年的IGF-1水平变化与rhGH疗效的相关性更为明显,提示在rhGH治疗过程中监测IGF-1水平,不仅可判断对治疗的依从性,还可确保在长期的rhGH治疗中将IGF-1水平保持在正常范围内,有助于临床在患儿进入青春期后调整rhGH剂量,使其血清IGF-1水平达到正常,以使患儿保持正常生长或加快生长。另外,与GH缺乏患儿相比,ISS患儿对GH的敏感性较低,故在治疗过程中应动态监测IGF-1水平并基于IGF-1的水平调整GH剂量。
本研究的不足和局限性:①本研究为回顾性研究,且随访时间仅为12个月,rhGH治疗的远期疗效无法判定;②样本量较小,无法准确建立预测模型。
[1]颜纯,王慕逖,主编.小儿内分泌学. 北京:人民卫生出版社.2006.127-128
[2]Ranke MB, Lindberg A, Price DA, et al. Age at growth hormone therapy start and first-year responsiveness to growth hormone is major determinants of height outcome in idiopathic short stature. Horm Res, 2007, 68(2): 53-62
[3]Su Z(苏喆), Du ML, Li YH, et al. 重组人生长激素治疗不同生长激素分泌状态青春期前矮小患儿追赶生长模式分析. Chinese Journal of Endocrinology And Metabolism(中华内分泌代谢杂志), 2008, 24(3): 239-243
[4]Su Z(苏喆),Du ML. Consensus statement on the diagnosis and treatment of children with idiopathic short stature:A summary of the Growth Hormone Research Society, the Lawson Wukins Pediatric Endocrine Society and the European Society for Paediatric Endocrinology Workshop. Chinese Journal of Endo-crinology And Metabolism(中华内分泌代谢杂志),2009,25(1):100-102
[5]李辉, 宗心南, 张亚钦,主编. 中国儿童生长标准与生长曲线.上海:第二军医大学出版社,2009
[6]Cole TJ, Green PJ. Smoothing reference centile curves: the LMS method and penalized likelihood. Stat Med, 1992,11(10):1305-1319
[7]Ranke MB, Lindberg A, Chatelain P, et al. Derivation and validation of a mathematical model for predicting the response to exogenous recombinant human growth hormone (GH) in prepubertal children with idiopathic GH deficiency .KIGS International Board. J Clin Endocrinol Metab, 1999,84(4):1174-1183
[8]Keni J, Cohen P. Optimizing growth hormone dosing in children with idiopathic short stature . Horm Res,2009,71(S1):70-74
[9]Hu NY( 胡女元), Yu YF, Yu CH, et al. Effect of recombinant human growth hormone therapy in prepuberty children with idlopathic short stature. International Medicine and Health Guidance News (国际医药卫生导报), 2009,13(24): 13-16
[10]Wit JM, Rekert-Mombarg LT, Culter GB. Growth hormone (GH) treatment to final height in children with idiopathic short stature evidence for a dose effect. J Pediatr,2005,146(1): 45-53
[11]Zhang Y(张宇), Lu WL, Yang LC, et al. Effect of recombinant human growth hormone therapy in prepuberty children with idiopathic short stature . J Clin Pediatr(临床儿科杂志), 2007, 25(5): 393-395
[12]Bryant J, Baxter L, Cave CB, et al. Recombinant growth hormone for idiopathic short stature in children and adolescents. Cochrane Database Syst Rev, 2007,18(3): 1-32
[13]Albertsson-Wikland K, Aronson AS, Gustafsson J, et al, Dose-dependent effect of growth hormone on final height in children with short stature without growth hormone deficiency. J Clin Endocrinol Metab, 2008, 93(11): 4342-4350
[14]Wh HH(武华红), Li H, Sun SY.Effect of recombinant human growth hormone therapy on GHD patients and establishment of predictionmodel. Chinses Journal of Practical Pedirtrics(中国实用儿科杂志), 2011, 26(4):289-293
[15]Brook C, Kelnar C, Betts P. Which children with idiopathic short stature should receive growth hormone therapy? Nat Clin Pract Endocrinol Metab, 2008, 4(3): 118-119
[16]Moore WV, Dana K, Frane J, et al. Growth hormone responsiveness: peak stimulated growth hormone levels and other variables in idiopathic short stature (ISS): data from the National Cooperative Growth Study. Pediatr Endocrinol Rev,2008,6(1):5-8
[17]Moore WV, Dana K, Frane J, et al. Growth hormone responsiveness: peak stimulated growth hormone levels and other variables in idiopathic short stature (ISS): data from the National Cooperative Growth Study. Pediatr Endorcrinol Rev, 2008, 6(1): 5-8
[18]Wikland KA, Kriström B, Rosberg S, et al. Validated multivariate models predicting the growth response to GH treatment in individual short children with a broad range in GH secretion capacities. Pediatr Res, 2000, 48(4): 475-484
[19]Ko JM, Park JY, Yoo HW. Common exon 3 polymorphism of the GH receptor (GHR) gene and effect of GH therapy ongrowth in Korean children with idiopathic short stature (ISS). Clin Endocrinol (Oxf), 2009, 70(1): 82-87
[20]叶义言,主编. 儿童青少年骨龄的评分法图谱应用.湖南:湖南科学技术出版社,1994.72-179
[21]Wit JM, Rekers-Mombarg LT.Dutch Growth Hormone Advisory Group. Final height gain by GH therapy in children with idiopathic short stature is dose dependent. J Clin Endocrinol Metab ,2002,87(2):604-611
[22]Cutfield WS, Lundgren F.Insulin-like growth factor I and growth responses during the first year of growth hormone treatment in KIGS patients with idiopathic growth hormone deficiency, acquired growth hormone deficiency, turnersyndrome and born small for gestational age. Horm Res,2009,71 (S1):39-45
[23]Cohen P, Germak J, Rogol AD, et al.Variable degree of growth hormone (GH) and insulin-like growth factor (IGF) sensitivity in children with idiopathic short stature compared with GH-deficient patients: evidence from an IGF-based dosing study of short children. J Clin Endocrinol Metab,2010,95(5):2089-2098

