L-和DL-福多司坦的太赫兹光谱分析
赵容娇 何金龙 李 璟 郭昌盛 杜 勇 洪 治
(中国计量学院太赫兹技术与应用研究所,杭州310018)
L-和DL-福多司坦的太赫兹光谱分析
赵容娇 何金龙 李 璟*郭昌盛 杜 勇 洪 治
(中国计量学院太赫兹技术与应用研究所,杭州310018)
利用太赫兹时域光谱技术(THz-TDS)在室温下对L-福多司坦和DL-福多司坦进行测量,发现L-和DL-福多司坦在THz波段都有特征吸收峰,且两者的吸收谱有明显差异.运用密度泛函理论的B3LYP方法计算了L-和DL-福多司坦在太赫兹波段的吸收谱,并对L-和DL-福多司坦的特征吸收峰进行了指认,理论计算与实验结果基本吻合.此外,还对福多司坦胶囊成品药进行了测量,发现该胶囊的吸收谱与L-福多司坦非常吻合,证明胶囊药的主要成分为L-福多司坦.这项研究对手性物质的检测以及化合物有效成分的鉴别有一定的参考作用.
L-、DL-福多司坦;太赫兹光谱;密度泛函理论;振动模式
1 引言
太赫兹(terahertz,THz)是对频率在0.1-10 THz (1 THz=1012Hz)区间的电磁波的总称,1其光子能量与大部分有机分子及分子团的振动和转动能级之间跃迁的能量大致相当,因此物质的THz谱包含丰富的物理和化学信息.2近年来,它被广泛应用于化学和生物医药等领域.3德国科学家Walther等4首次利用太赫兹时域光谱(THz-TDS)技术研究了视黄醛分子不同异构体9-顺式视黄醛、13-顺式视黄醛和全反-视黄醛的THz吸收谱,发现这些异构体的吸收谱都有着显著差异,这是由于THz-TDS技术可测定物质结构存在的微小差异,且对其变化非常灵敏.5-7因此,利用THz谱可以区分一些红外谱难以区分的手性药物.目前已经有研究开始关注利用THz技术分析手性物质和其消旋体.8-10
手性药物对映体常具有不同的药理活性和毒性,在体内的代谢作用也往往不同.11当前药物研究的发展趋势是追求疗效高、毒副作用小、用药量少,所以一般要求手性药物以光学纯的单一异构体形式应用于临床.手性药物的检查逐渐成为药学领域的一个研究热点.新一代祛痰药福多司坦正是一种手性药物,其分子结构中有一个手性中心,存在一对对映异构体,具有药理活性的是左旋体福多司坦(L-Fudosteine,S-(3-羟丙基)-半胱氨酸)),而右旋体D-Fudosteine无生物活性,消旋体DL-Fudosteine是L-和D-福多司坦两种对映体以等量的形式共存于晶格中.福多司坦对咳嗽、慢性支气管炎、支气管扩张症、尘肺病、肺气肿、非定型抗酸菌症等疾患均有很强的祛痰效果,并且具有药效强、副作用小、市场潜力大等优点.12,13
本文利用THz-TDS技术在0-3.0 THz波段对L-和DL-福多司坦进行了测量,并运用密度泛函理论对L-和DL-福多司坦进行了模拟计算,模拟结果与实验结果都表明它们的特征吸收谱有很大差距.此外,我们还对福多司坦胶囊成品药进行了测量,结果表明胶囊药的吸收谱与L-福多司坦的吸收谱基本一致.本研究为检测手性物质,以及鉴别化合物的主要成分有一定的参考意义.
2 实验和数据处理
2.1 实验系统和样品
实验装置是美国Zomega公司的Z-2太赫兹时域光谱系统,如图1所示.掺钛蓝宝石飞秒锁模激光器输出中心波长为780 nm、重复频率为80 MHz、脉冲宽度为100 fs的激光.激光束经分束镜分为泵浦光和探测光.泵浦光经过斩波器调制,入射到砷化镓基底的光电导天线激发THz脉冲,另一组作为探测光与THz脉冲一同通过ZnTe电光晶体,利用电光效应探测太赫兹波,并通过改变延迟线长度的方法取样探测太赫兹信号的整个时域波形.测量环境为干燥的氮气环境,相对湿度小于1%.
实验所用L-和DL-福多司坦来自于中国药品生物制品检定所,纯度均大于98%,使用前未经过进一步纯化处理,福多司坦胶囊(由L-福多司坦及辅料制成)来自于正大青春宝药业有限公司.L-、D-福多司坦,以及其消旋体DL-的分子结构见图2.所有样品都是多晶体粉末.
实验将纯L-、DL-福多司坦和福多司坦胶囊,分别与聚乙烯(PE)粉末按1:9的质量比混合均匀,经研磨后,用7 MPa的压力压成试片.
2.2 数据处理方法
样品在THz波段的折射率及消光系数利用Timothy和Duvillaret等14,15提出的如下物理模型获得:
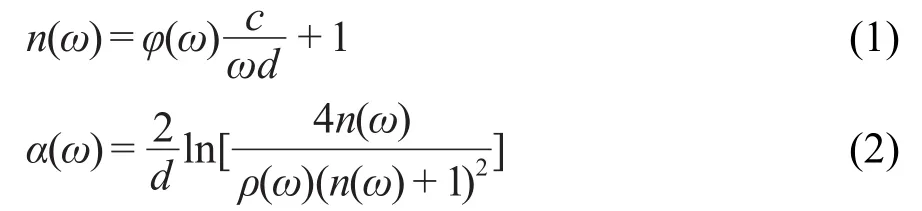
其中n(ω)为样品的实折射率,简称折射率,α(ω)为样品的吸收系数,d为样品厚度,ω为频率,φ(ω)和ρ(ω)分别是样品和参考信号的相位差和振幅比值.

图1 太赫兹时域光谱(THz-TDS)实验装置示意图Fig.1 Experimental setup for terahertz time-domain spectroscopy(THz-TDS)
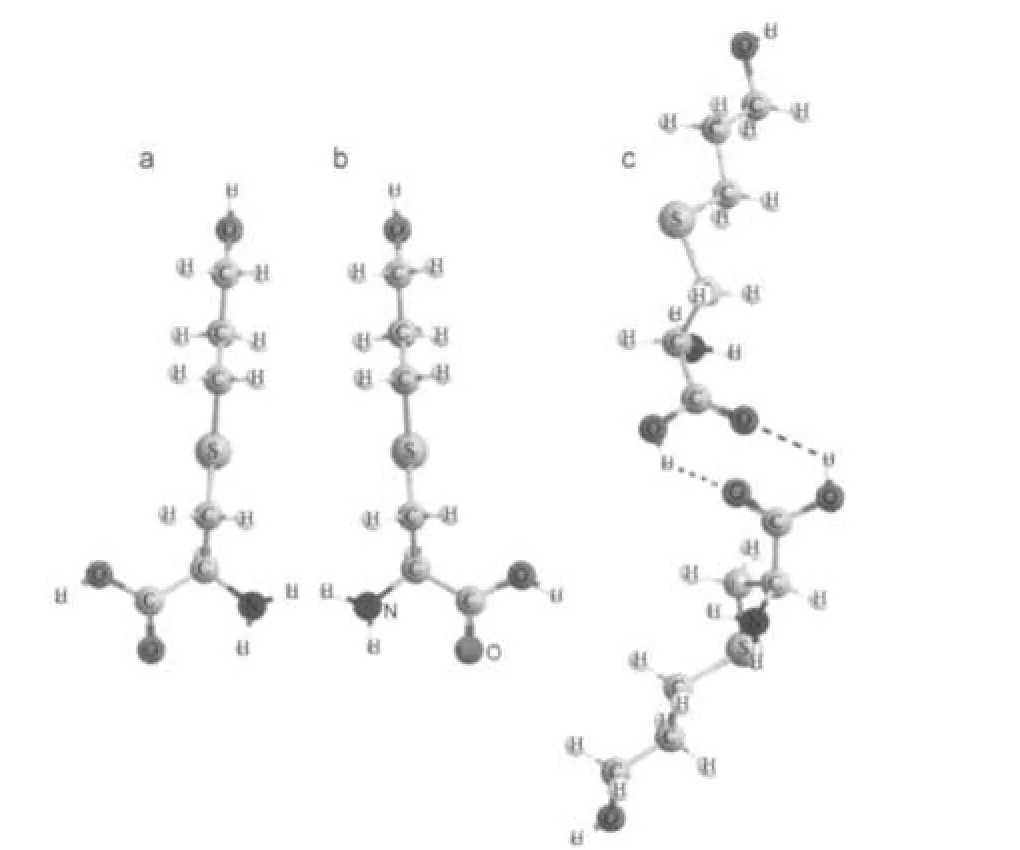
图2 福多司坦的分子结构Fig.2 Molecule structures of Fudosteine(a)L-Fudosteine;(b)D-Fudosteine;(c)DL-Fudosteine
由于所测样品是L-、DL-福多司坦与聚乙烯(PE)混合而成的,根据朗伯-比尔定律,16混合物的吸收系数为其中αi为组分i的吸收系数,bi为混合物中组分i的质量比.由于实验样品中L-和DL-福多司坦纯品的质量比例都是1/10,故纯品的吸收系数计算公式为:

其中,αs表示样品的吸收系数,αpure为纯品的吸收系数,αPE为PE的吸收系数.
3 实验结果与讨论
室温下,通过THz-TDS装置测量得到待测样品的时域谱,经傅里叶变换得到频域谱.利用公式(2)计算得到吸收系数αs.考虑到TDS系统的动态范围(DR),及其对光谱有效频率范围(或光谱置信区间)的影响,定义了参数amax:17

式中的DR我们用信噪比代替,实验中通过对10次测试获得的参考信号在频域中计算振幅均值与其均方误差的比值.
当吸收系数αs超过了αmax,其数值不再可信,则αmax和αs两曲线的交点即为待测样品光谱的可信频率上限.图3为DL-福多司坦样品实验得到的αmax和αs曲线,从图中可得出DL-福多司坦的有效频率上限为2.450 THz,同理L-福多司坦、PE及福多司坦胶囊的有效频率上限分别为2.330、2.470和2.090 THz.
图4为L-及DL-福多司坦实验样品在0.2-2.0 THz区间的吸收谱,从图中可以看出这两种样品吸收谱的强度和吸收峰的位置都存在明显的差别,这说明可以利用THz光谱分析对L-及DL-福多司坦进行有效鉴别.
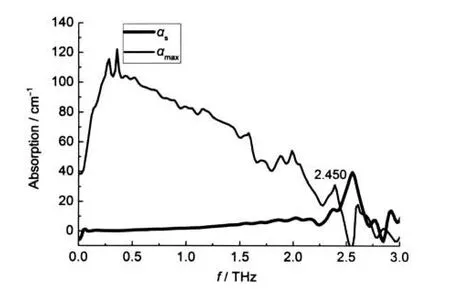
图3 DL-福多司坦的有效频率上限Fig.3 Upper limit of effective frequency of DL-Fudosteine
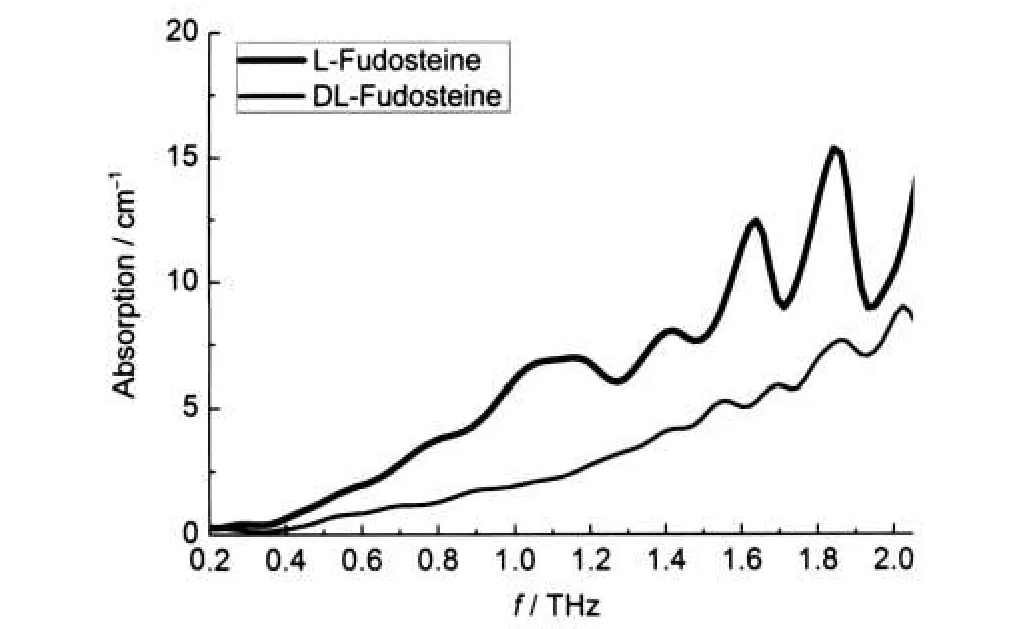
图4 0.2-2.0 THz范围L-、DL-福多司坦的吸收光谱Fig.4 Absorption spectra of L-,DL-Fudosteine in the range of 0.2-2.0 THz
4 DFT计算与分析
本文对福多司坦进行了理论计算,选用密度泛函理论(DFT)中准确度非常高的Becke-3-Lee-Yang-Parr(B3LYP)方法,18,19以及6-31G*基组对孤立L-和DL-福多司坦分子进行了模拟计算.选取了D-和L-福多司坦分子的二聚体(如图2c)近似模拟其消旋体.两者通过两个CO2…HO氢键相连,氢键键长为0.17721 nm,呈反式构型,其氢键相关的部分参数见表1.其中R、A、D分别代表键长、键角、二面角,数字表示原子的相应序列.
结果没有出现虚频,说明几何优化结果是分子的最小能量结构.考虑到Gaussian模拟中没有完全考虑电子相关作用和其对非简谐性效应的忽略,以及我们对基组的选择等因素的影响,20,21故采用了B3LYP/6-31G*的矫正因子0.961.22,23
利用公式(3)计算得到纯L-和DL-福多司坦的吸收系数,并将模拟结果分别与实验结果进行比较(见图5),发现实验和模拟的吸收峰位置基本相吻合.L-福多司坦实验的吸收峰在1.108、1.426、1.844 THz恰好分别对应模拟计算的吸收峰1.106、1.496和1.846 THz;DL-福多司坦的实验吸收峰1.896、1.050 THz处,恰好对应模拟计算的1.931和1.040 THz.模拟和实验之间有少许偏移,这是因为实验是在常温下进行的,而理论模拟是在绝对零度下进行的,没有考虑这种热效应.
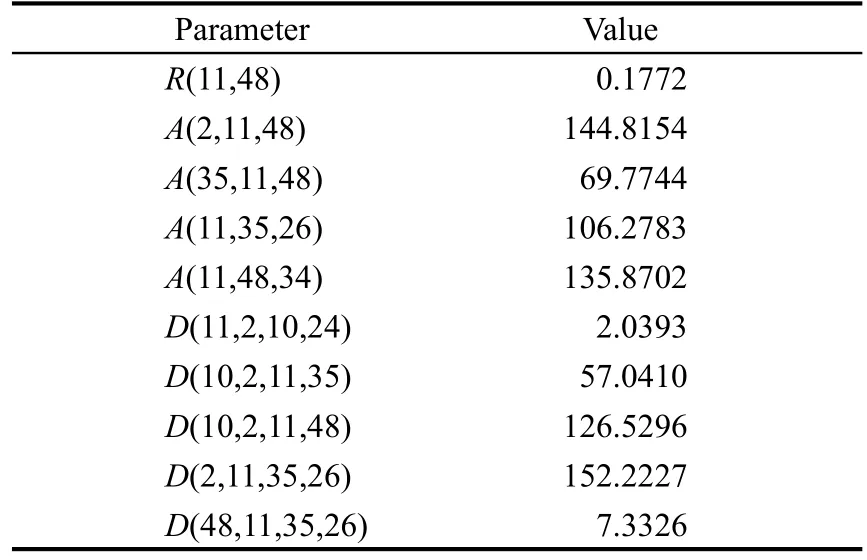
表1 氢键相关的部分参数Table 1 Some parameters of hydrogen bond
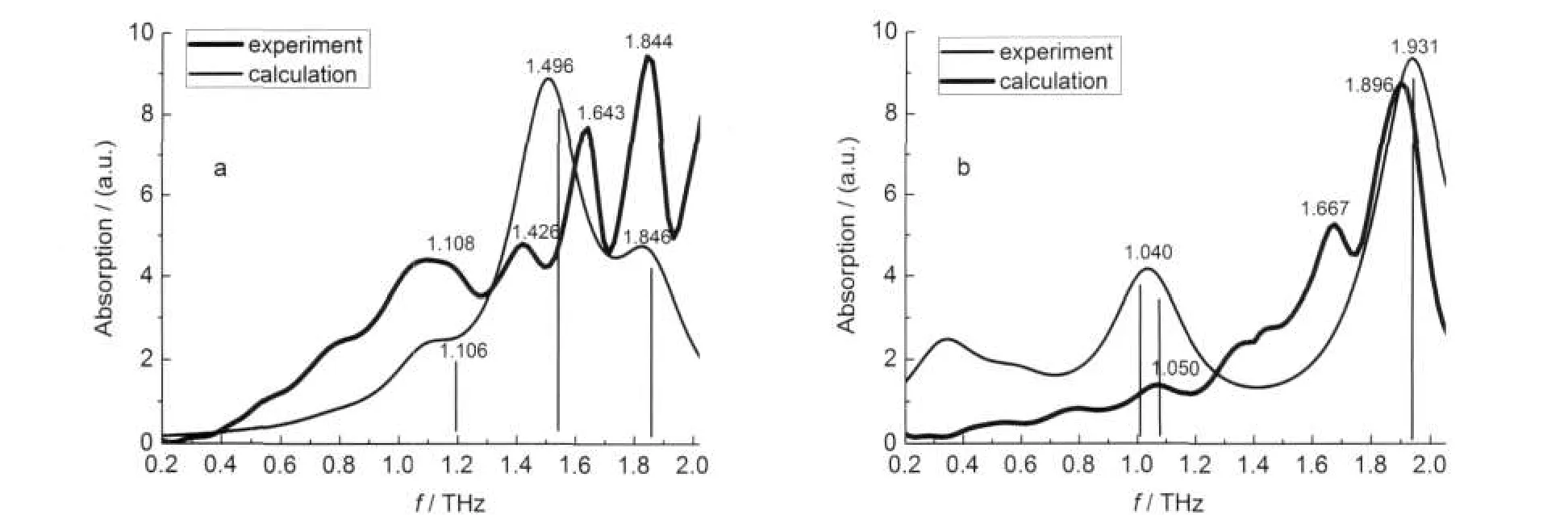
图5 L-福多司坦(a)和DL-福多司坦(b)计算光谱与实验光谱的比较图Fig.5 Comparison between experimental and calculated spectra of L-Fudosteine(a)and DL-Fudosteine(b)
此外,实验结果中L-福多司坦在1.643 THz、DL-福多司坦在1.667 THz存在吸收峰,这两个吸收峰没有对应的模拟结果.这是由于实验测量的是多分子的晶体结构,晶格中存在分子间的弱相互作用,导致样品的特征THz波吸收,24而模拟计算的模型是单分子,25未考虑到分子间的相互作用,26,27所以认为不能与理论计算结果对应的振动模式是由分子间振动模式引起的.28
计算结果表明,分子在THz低频波段的振动主要源于多个原子参与的变形振动、扭动振动和弯曲振动.29不同峰位的振动模式不同,借助于Gaussian-View 3.0的视频功能,通过动态观察,可以对福多司坦的振动模式进行大致的指认,结果见表2.L-福多司坦分子在1.106 THz处的吸收是由于O9-C8-C7-C6链扭动,以及N3氨基团和O10氢氧键以链O10-C2-C1-N3为轴的扭动,如图6a所示;在 1.496 THz处的吸收峰是由于O11-C2键的摇摆振动,以及C7和C8两个甲基团的扭动,C7甲基的振动还带动了与之相连的C6甲基团的摇摆振动,如图6b所示;在1.846 THz处的吸收是由于C7甲基团和C8甲基团的扭动,该扭动模式还带动了整条链O9-C9-C7-C6-S5-C4-C1-C2-O10集体振动,并引起N3氨基团的摆动振动,如图6c所示; DL-福多司坦分子在1.931 THz处的吸收是由于C7甲基和C8甲基的扭动,以及C31甲基和C32甲基的扭动,如图6d所示;1.040 THz处的吸收,一部分是由于C6甲基、C7甲基和C8甲基的扭动,如图6e-1所示;另一部分由于C30甲基、C31甲基和C32甲基的扭动,如图6e-2所示.这些吸收都属于基团集体振动模式的范畴.
实验结果和理论计算都表明L-福多司坦和DL-福多司坦的吸收谱确实有很大的差异,这是因为消旋体中存在分子间的弱相互作用(如氢键等),其低频区的振动导致太赫兹吸收光谱发生变化.26
另外,我们还对福多司坦胶囊进行了测量,并分别与L-、DL-福多司坦纯品吸收谱进行了比较,如图7所示.可见,福多司坦胶囊与L-福多司坦的吸收谱大致相同,至于吸收强度上的差异,则是因为胶囊成品药中的添加物影响.福多司坦胶囊与DL-福多司坦的吸收谱差距较大,特别是胶囊在1.1和1.5THz附近有很明显的吸收峰,而DL-福多司坦则不明显.这表明以整个或部分吸收谱作为化合物指纹特征,可实现化合物主要成分的有效鉴别.

表2 福多司坦的振动模式Table 2 Vibration modes of Fudosteine
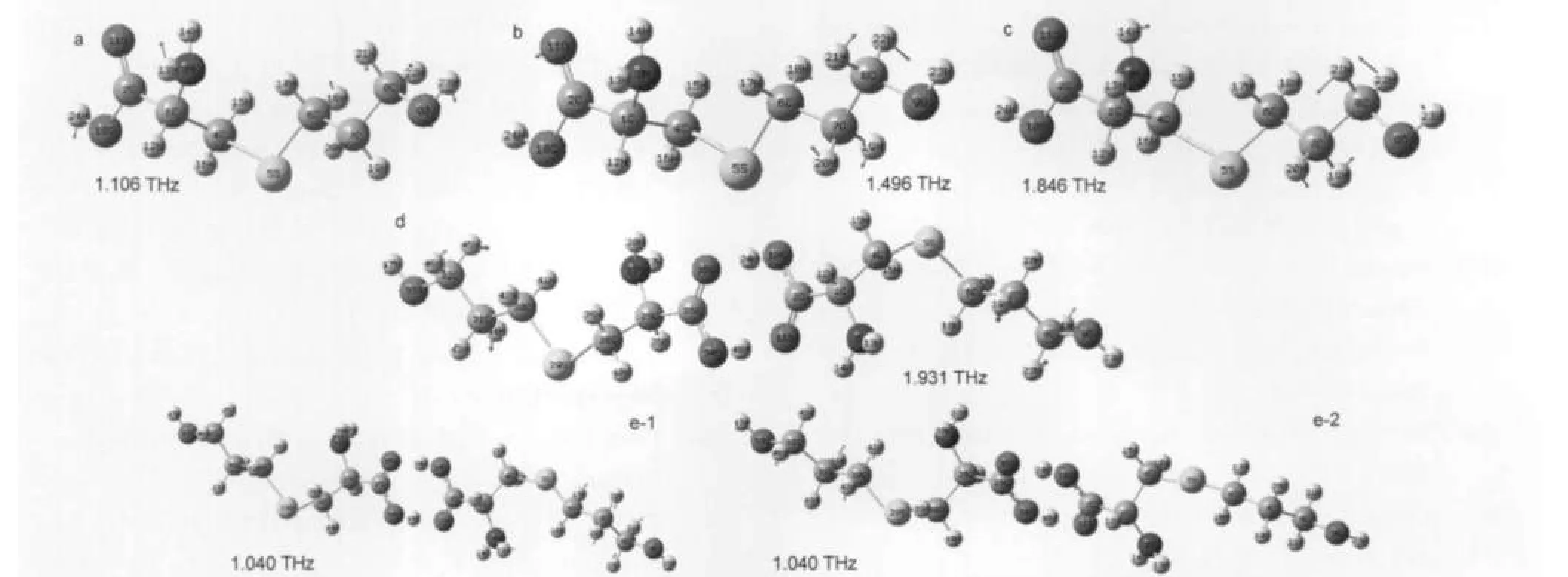
图6 福多司坦的振动模式Fig.6 Vibration modes of Fudosteinea,b,c are vibration modes of L-Fudosteine;d,e-1,e-2 are vibration modes of DL-Fudosteine.
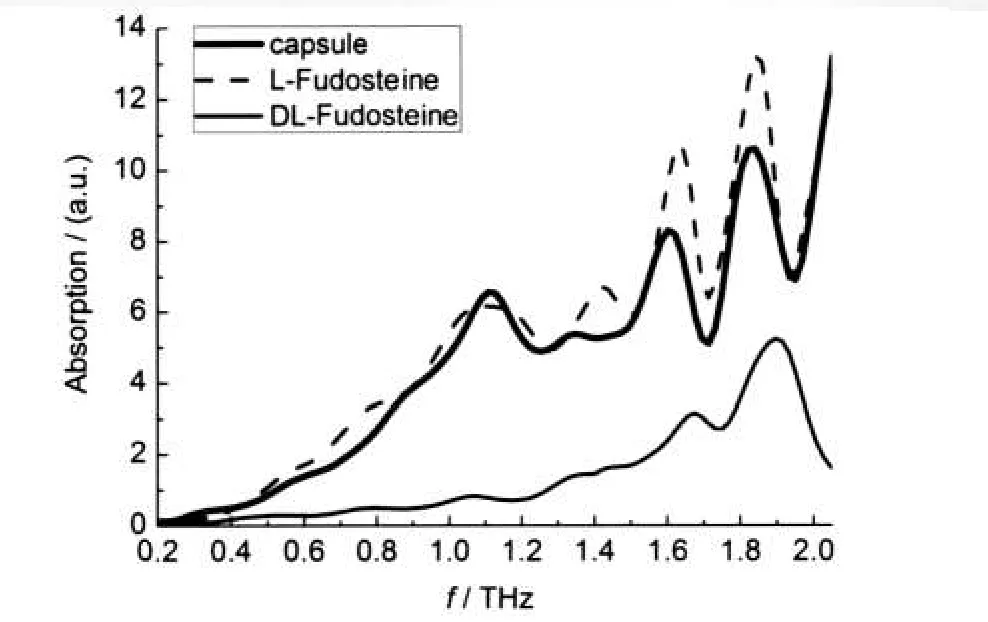
图7 福多司坦胶囊、纯L-和DL-福多司坦的吸收谱Fig.7 Absorption spectra of Fudosteine capsule,pure L-and DL-Fudosteine
5 结论
利用THz-TDS系统在室温下测量了L-和DL-福多司坦的THz光谱,在实验样品的有效频率范围内进行分析,发现L-和DL-福多司坦在吸收峰的位置、吸收强度等方面都有明显差异.选用密度泛函理论对L-和DL-福多司坦在太赫兹波段的吸收光谱进行了模拟,并对福多司坦吸收峰的振动模式进行了指认,发现都是以基团和链的扭动为主要特征,不同峰位的扭转模式及振动幅度不同.此外,我们还对福多司坦胶囊成品药进行了测量,结果表明胶囊药的吸收谱与L-福多司坦的吸收谱基本一致.这一研究结果为利用THz技术检测手性物质和进一步分析分子内和分子间相互作用提供了参考.
(1) Xu,J.Z.;Zhang,X.C.Technology and Applications of Terahertz Wave;Peking University Press:Beijing,2007; pp 1-5.[许景周,张希成.太赫兹科学技术和应用.北京:北京大学出版社,2007:1-5.]
(2) Li,J.R.;Li,J.S.Journal of the Chinese Cereals and Oils Association 2010,25(3),112. [李建蕊,李九生.中国粮油学报,2010,25(3),112.]
(3) Siegel,P.H.IEEE Transactions on Microwave Theory and Techniques 2004,52(10),2438.
(4)Walther,M.;Fischer,B.;Schall,M.;Helm,H.;Jepsen,P.U. Chem.Phys.Lett.2000,332,389.
(5)Yamaguchi,M.;Miyamaru,F.;Yamamoto,K.;Tani,M.; Hangyo,M.Appl.Phys.Lett.2005,86(5),053903.
(6)Wang,W.N.;Yue,W.W.;Yan,H.T.;Zhang,C.L.;Zhao,G.Z. Chinese Science Bulletin 2005,50(15),1561.
(7) Shi,Y.L.;Wang,L.J.Phys.D-Appl.Phys.2005,38,3741.
(8)Ge,M.;Zhao,H.W.;Ji,T.;Yu,X.H.;Wang,W.F.;Li,W.X. Sci.China Ser.B-Chem.2005,35(6),441. [葛 敏,赵红卫,吉 特,余笑寒,王文锋,李文新.中国科学B辑:化学,2005, 35(6),441.]
(9)Gi,T.;Zhao,H.W.;Zhang,Z.Y.;Ge,M.;Wang,W.F.;Yu,X. H.;Xu,H.J.Acta Phys.-Chim.Sin.2006,22,1159.[吉 特,赵红卫,张增艳,葛 敏,王文锋,余笑寒.徐洪杰.物理化学学报,2006,22,1159.]
(10) Xu,H.;Yu,X.H.;Zhang,Z.Y.;Han,J.G.;Li,Q.N.;Zhu,Z.Y.; Li,W.X.Journal of the Graduate School of the Chinese Academy of Sciences 2005,22,90.[徐 慧,余笑寒,张增燕,韩家广,李晴暖,朱志远,李文新.中国科学院研究生院学报, 2005,22,90.]
(11) Zhang,L.;Yao,T.W.;Zeng,S.Chinese Journal of Modern Applied Pharmacy 1999,16(2),4.[章 立,姚彤炜,曾 苏.中国现代应用药学杂志,1999,16(2),4.]
(12) Takahashi,K.;Kai,H.;Mizuno,H.;Koda,T.;Miyata,T. J.Pham.Phamacol.2001,53(6),911.
(13) Wang,Y.J.;Liu,F.J.Tianjin Pharmacy 2006,18(5),73. [王亚江,刘福景.天津药学,2006,18(5),73.]
(14)Timothy,D.D.;Richard,G.B.;Daniel,M.M.J.Opt.Soc.Am.A 2001,18(7),1562.
(15) Duvillaret,L.;Garet,F.;Coutaz,J.L.IEEE J.Sel.Top.Quant. 1996,2(3),739.
(16) Markelz,A.G.;Roitberg,A.;Heilweil,E.J.Chem.Phys.Lett. 2000,320,42.
(17) Jepsen,P.U.;Fischer,B.M.Opt.Lett.2005,30,29.
(18)Axel,D.B.J.Chem.Phys.1993,98,5648.
(19) Scoot,P.;Radom,L.J.Chem.Phys.1996,100,16502.
(20)Anthony,P.S.;Leo,R.J.Chem.Phys.Lett.1996,100,16502.
(21) Halls,M.D.;Velkovski,J.;Schlegel,H.B.Theor.Chem.Acc. 2001,105,413.
(22) Liu,J.Y.;Wu,S.B.Chemical Graphic Design and Molecular Calculations;South China Science and Technology University Press:Guangzhou,2009;pp 253-256.[刘江燕,武书彬.化学图文设计与分子模拟计算.广州:华南理工大学出版社,2009: 253-256.]
(23) Wong,M.Chem.Phys.Lett.1996,256,391.
(24) Ma,J.L.;Xu,K.J.;Li,Z.;Jin,B.B.;Fu,R.;Zhang,C.H.;Ji, Z.M.;Zhang,C.;Chen,Z.X.;Chen,J.;Wu,P.H.Acta Physica Sinica 2009,58(9),6101. [马金龙,徐开俊,李 哲,金飚兵,傅 荣,张彩虹,吉争鸣,张 仓,陈兆旭,陈 健,吴培亨.物理学报,2009,58(9),6101.]
(25) Takahashi,M.;Ishikawa,Y.;Nishizawa,J.;Hiromasa,I.Chem. Phys.Lett.2005,401,475.
(26)Chen,Y.Q.;Liu,H.B.;Zhang,X.C.Proceedings of SPIE 2006,6212,62120P-l.
(27) Walther,M.;Plochocka,P.;Fischer,B.;Helm,H.;Uhd,J.P. Biopolymers 2002,67,310.
(28) Chen,Y.Q.;Liu,H,B.;Deng,Y.Q.;Schauki,D.;Fitch,M.J.; Osiander,R.;Dodson,C.;Spicer,J.B.;Shur,M.;Zhang,X.C. Chem.Phys.Lett.2004,400,357.
(29)Yu,B.;Zeng,F.;Yang,Y.;Xing,Q.;Chechin,A.;Xin,X.; Zeylikovich,I.;Alfano,R.R.Biophysical Journal 2004,86, 1649.
July 26,2011;Revised:September 19,2011;Published on Web:October 10,2011.
Terahertz Time-Domain Spectroscopy of L-and DL-Fudosteine
ZHAO Rong-Jiao HE Jin-Long LI Jing*GUO Chang-Sheng DU Yong HONG Zhi
(Centre for Terahertz Research,China Jiliang University,Hangzhou 310018,P.R.China)
The absorption spectra of L-and DL-Fudosteine were measured using terahertz time-domain (THz-TDS)system at room temperature.Experimental results show that L-and DL-Fudosteine both have distinct fingerprint spectra in the THz region and their characteristics are different from each other.The absorption frequencies for the vibration and rotation of Fudosteine in the THz spectral range were simulated and the results are consistent with the experimental results.We also interpret the origin of the absorption peaks using a simulation.Finally,the absorption spectra of the Fudosteine capsule,pure L-Fudosteine and DL-Fudosteine are compared.The results verify that the main component of the capsule is L-Fudosteine.This study provides a reference for the analysis of the main ingredients of compounds.
L-,DL-Fudosteine;Terahertz spectrum;Density functional theory;Vibration mode
10.3866/PKU.WHXB20112743
∗Corresponding author.Email:lijing@cjlu.edu.cn;Tel:+86-571-86875672.
The project was supported by the National Natural Science Foundation of China(61001064)and Natural Science Foundation of Zhejiang Province, China(Y1090912).
国家自然科学基金(61001064)和浙江省自然科学基金(Y1090912)资助项目
O641;O657.61

