Ag-BiVO4催化剂的制备及其可见光催化活性
胡 蕾,叶芝祥,杨 浩,徐成华,杨怀金,曲 兵
(成都信息工程学院 资源环境学院,四川 成都 610225)
Ag-BiVO4催化剂的制备及其可见光催化活性
胡 蕾,叶芝祥,杨 浩,徐成华,杨怀金,曲 兵
(成都信息工程学院 资源环境学院,四川 成都 610225)
以Bi2O3和V2O5为原料,通过高温固相反应合成BiVO4;并采用浸渍法对BiVO4进行Ag掺杂,制备具有较好可见光催化活性的Ag-BiVO4。采用X射线衍射仪、紫外-可见分光光度仪、比表面分析仪对所制得的Ag-BiVO4进行了表征。实验结果表明:Ag掺杂不会引起BiVO4的晶型变化,可提高其对可见光的吸光性能;在Ag掺杂量为4%、溶液pH为7.0、Ag-BiVO4加入量为7 g/L的条件下,光催化反应6 min后碱性品红的脱色率最高,可达90%以上。
钒酸铋;光催化剂;银;掺杂;可见光;碱性品红
印染废水具有水量大、有机污染物含量高、色度深、碱性大等特点,属难处理的工业废水[1]。近年来,随着化学纤维织物仿真丝工业的兴起与发展,更多难生化降解的有机物进入印染废水,使COD上升至2 000~3 000 mg/L,从而使原有的生物处理系统COD去除率由70%下降到50%左右,甚至更低[2]。目前印染废水的常用处理方法有物理法、化学法和生物降解法,而这些方法工序繁琐,成本高,且不能完全降解有机污染物[3-4]。
自Fujishima等[5]发现n型TiO2半导体电极上可以发生光催化分解水分子反应以来,半导体光催化剂迅速受到研究者的广泛关注。近年来,研究发现BiVO4对波长小于525 nm的光具有较好的吸收,可用于可见光催化反应[6],如有机物的光催化降解[7]、光解水制O2[8]和光电催化分解水[9],但光催化效率均较低。因此,需对BiVO4光催化剂进行改性,以提高其可见光催化降解有机污染物的性能。有人发现[10-12]用贵金属(Ag和 Pd)掺杂可提高BiVO4可见光催化降解多环芳香烃和4-烷基苯酚的活性。
本工作采用固相反应法合成BiVO4,采用浸渍法制备了Ag-BiVO4光催化剂,研究了其在可见光照射下光催化降解碱性品红的性能。
1 实验部分
1.1 试剂和仪器
实验用试剂均为分析纯。
DX-2500型X射线衍射(XRD)仪:辽宁丹东方圆仪器厂;SGY-I型多功能光化学反应仪:南京斯通柯电气设备有限公司;721E型可见分光光度计:上海光谱仪器有限公司;UV-2550型紫外-可见分光光度仪:日本岛津公司;SSA-4200型孔隙比表面分析(BET)仪:北京彼奥得电子有限公司。
1.2 BiVO4和Ag-BiVO4的制备
将摩尔比为1∶1的Bi2O3和V2O5混合,充分研磨后,以5oC/min的升温速率升至750℃,固相反应7 h,制得BiVO4。
将BiVO4固体粉末浸渍于一定量的硝酸银溶液中5 min,80℃烘干,300oC焙烧5 h,得到不同Ag掺杂量(Ag与BiVO4的质量比,%)的改性BiVO4催化剂。
1.3 实验方法
取10 m L质量浓度为5 mg/L的碱性品红溶液,经磷酸氢二钠-柠檬酸缓冲液调节pH后,加入一定量的光催化剂,将反应体系置于多功能光化学反应仪中进行光催化降解反应,以350 W氙灯为光源,反应一定时间后,取样进行分析。
1.4 分析方法
采用XRD仪分析 Ag-BiVO4的晶型;采用BET仪进行比表面积及孔径分布测定;采用可见分光光度计在543 nm处测定碱性品红溶液的吸光度,计算脱色率。
2 结果与讨论
2.1 Ag-BiVO4的表征
在Ag掺杂量为4%的条件下,Ag-BiVO4催化剂的XRD谱图见图1。
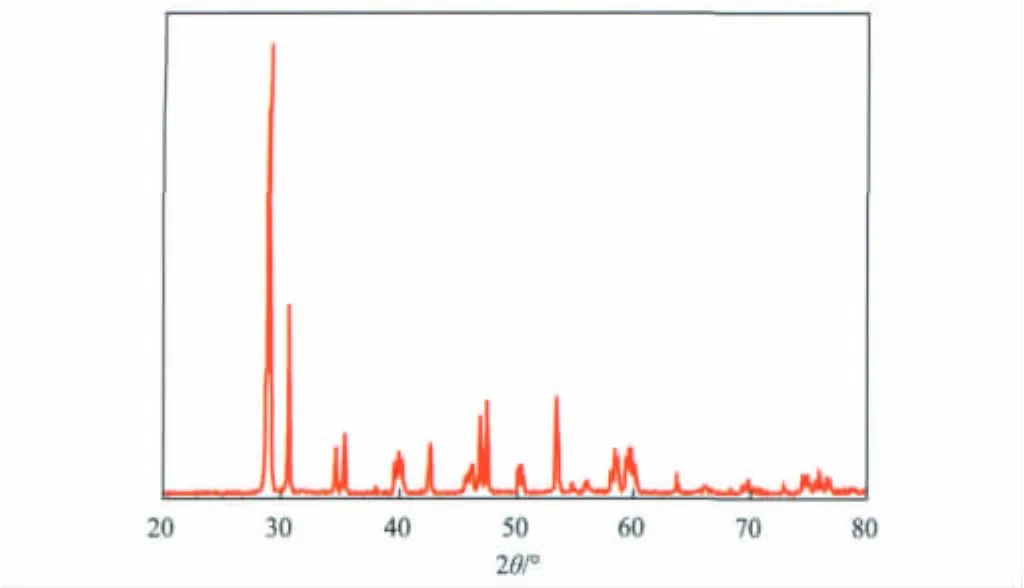
图1 Ag-BiVO4的XRD谱图
由图1可见:在2θ为29.06,30.68,35.30,39.90,50.40o出现了明显的BiVO4特征衍射峰,且具有单斜白钨矿结构;掺杂的Ag主要以单质形式存在于BiVO4催化剂中,部分Ag被空气中的O2氧化形成AgO。根据单斜相BiVO4(112)晶面的2θ为29.06°的衍射峰,采用 Scherrer公式计算得到Ag-BiVO4的平均粒径为30.1 nm[13]。
Ag掺杂量对Ag-BiVO4催化剂的紫外光谱性能的影响见图2。由图2可见,试样在波长为200~500 nm处出现一宽吸收谱带,随着Ag掺杂量的增大,BiVO4的吸收谱带发生一定程度的红移。
BET测定结果表明,当Ag掺杂量为4%时,Ag-BiVO4的比表面积为1.7 m2/g,最可几半径为11.5 nm,平均孔半径为7.8 nm,总孔体积为0.019 m L/g。
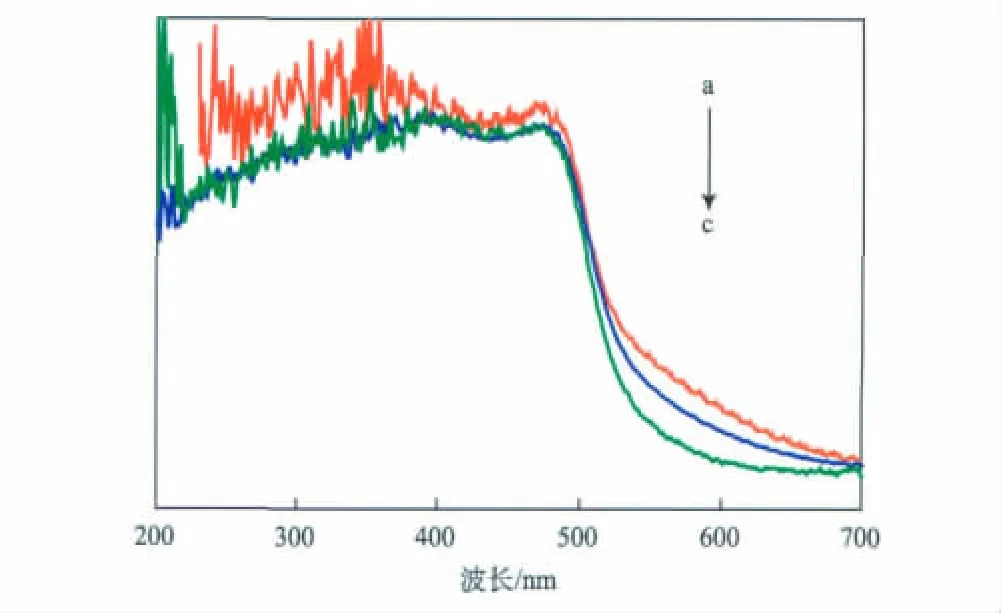
图2 Ag掺杂量对Ag-BiVO4催化剂的紫外光谱性能的影响
2.2 Ag掺杂量对碱性品红溶液脱色率的影响
Ag掺杂量对碱性品红溶液脱色率的影响见图3。
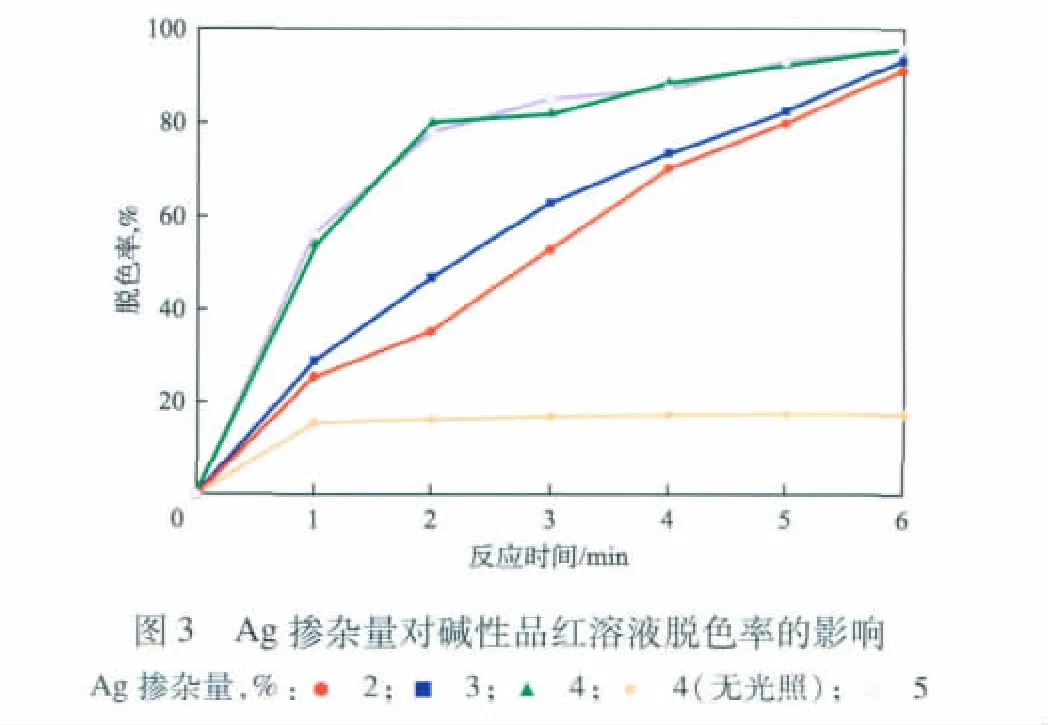
由图3可见:当反应在无光照条件下进行时,反应开始时脱色较为迅速,但随着反应的进行,脱色率变化不大,这主要是因为在此条件下Ag-BiVO4催化剂只能对碱性品红进行吸附,而不能发生光催化反应[14];在有光照的条件下,碱性品红溶液脱色率随Ag-BiVO4催化剂中Ag掺杂量的增加而升高,掺杂量大于4%后,脱色效果相差不大。由此可见,Ag掺杂可提高BiVO4对碱性品红降解的光催化性能。这主要是由于Ag的掺杂提高了BiVO4催化剂对可见光的吸收能力,这与紫外-可见光谱的表征结果相吻合。另外,电子受体Ag可捕获受光照作用而激发的BiVO4导带上的电子,使得BiVO4光催化剂的导带与价带变得更稳定,不易复合,从而增强Ag-BiVO4的光催化性能[15]。
2.3 溶液pH对碱性品红溶液脱色率的影响
碱性品红溶液在强酸性和碱性条件下因自身结构发生变化而褪色明显[16]。本实验首先考察了溶液pH为2.2~7.8时碱性品红的自身脱色情况。溶液pH对碱性品红溶液吸光度的影响见图4。由图4可见,溶液pH为3.8~7.0时,吸光度变化不大,碱性品红较为稳定。
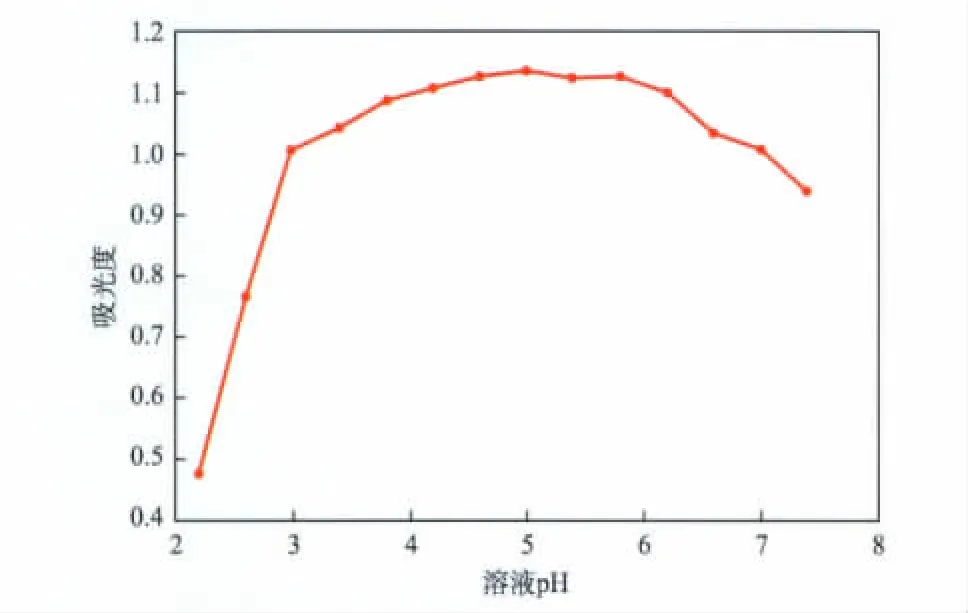
图4 溶液pH对碱性品红溶液吸光度的影响
在Ag掺杂量为4%的条件下,溶液pH对碱性品红溶液脱色率的影响见图5。由图5可见:在溶液pH为5.9~7.0时,碱性品红溶液的脱色率随溶液pH的增大而逐渐升高;当溶液pH达6.5后,脱色率趋于稳定(大于85%)。这主要是因为随着溶液pH的升高,Ag-BiVO4在光照作用下会加速体系中·OH自由基的生成,从而加快·OH氧化碱性品红的速率,使脱色率升高[16]。
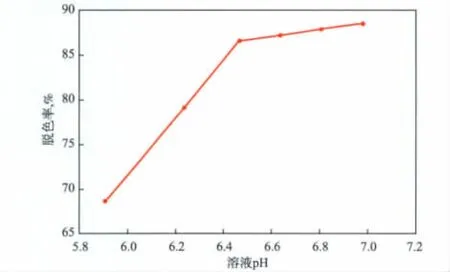
图5 溶液pH对碱性品红溶液脱色率的影响
2.4 Ag-BiVO4加入量对碱性品红溶液脱色率的影响
Ag-BiVO4加入量对碱性品红溶液脱色率的影响见图6。由图6可见:随Ag-BiVO4加入量的增加,碱性品红溶液脱色率逐渐升高;当Ag-BiVO4加入量达到7 g/L后,继续增加Ag-BiVO4的加入量,脱色率变化不大。这主要是因为光催化剂颗粒越多,在光照作用下单位时间内产生的·OH自由基的量越多;但当催化剂加入量达到一定值后,悬浮体系中的颗粒浓度达到一定程度,对光的遮蔽、反射作用导致催化剂对光的利用率降低。
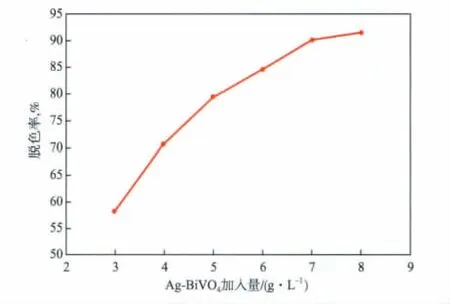
图6 Ag-BiVO4加入量对碱性品红溶液脱色率的影响
2.5 Ag-BiVO4光催化降解碱性品红机理
Ag-BiVO4光催化降解碱性品红的紫外-可见光谱谱图见图7。
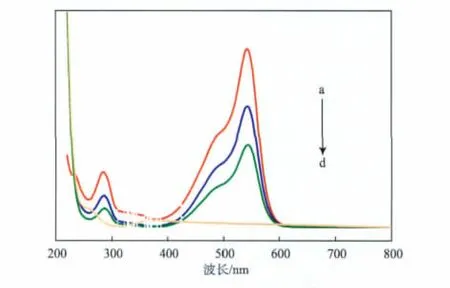
图7 Ag-BiVO4光催化降解碱性品红的紫外-可见光谱谱图
由图7可见:碱性品红在250~300 nm(紫外光区)和400~600 nm(可见光区)两个区间出现吸附带,前者为苯环的吸附峰,后者是碱性品红分子中具有共轭体系的发色基团产生的吸收峰;随反应时间的延长,两个吸收谱带的强度随之变弱;反应6 min后,两个吸收谱带基本消失。由图7还可见,碱性品红在光催化作用下,不仅发色基团得到降解,而且分子中的苯环基团也消失了。由此可推断Ag-BiVO4被激发的表面上产生大量的·OH自由基,具有高活性的·OH自由基可使苯环发生羟基化,并进一步开环,形成脂肪烃等简单化合物,而这些简单化合物又可继续被·OH自由基进行深度氧化[17]。
综上所述,在 Ag掺杂量为4%、溶液 pH为7.0、Ag-BiVO4加入量为7 g/L的条件下,光催化反应6 min后碱性品红溶液的脱色率可达90%以上。
3 结论
通过高温固相合成法和浸渍法制备具有较高可见光催化活性的Ag-BiVO4光催化剂。Ag掺杂可提高BiVO4在可见光区的光吸收能力;并且随着Ag掺杂量的增加,Ag-BiVO4对碱性品红溶液的脱色率也随之增加。在Ag掺杂量为4%、溶液pH为7.0、Ag-BiVO4加入量为7 g/L的条件下,光催化反应6 min后碱性品红溶液的脱色率最高,可达90%以上。
[1] 齐普荣,王光辉,于荣.TiO2光催化氧化处理偶氮染料废水的研究进展[J].化工环保,2007,27(1):32-35.
[2] 阮新潮,曾庆福,黎谦.纺织印染废水处理技术进展[J].武汉科技学院学报,2001,14(2):66-71.
[3] 邱丽娟,陈亮,黄满红.UASB反应器处理染料及印染废水的研究进展[J].化工环保,2009,29(5): 416-419.
[4] 帅佳慧,龚文琪.内电解法处理偶氮染料废水[J].化工环保,2007,27(2):149-151.
[5] Fujishima A,Honda K.Electrochem ical photolysis of water at a sem iconductor electrode[J].Nature,1972,238:37-38.
[6] 龙明策,蔡俊,蔡伟民.设计新型可见光响应的半导体光催化剂[J].化学进展,2006,18(9):1065-1075.
[7] Kohtani S,Koshiko M,Kudo A,et al.Photodegradation of 4-alkylphenols using BiVO4photocatalyst under irradiation with visible light from a solar simulator[J].Appl Catal B,2003,46:573-586.
[8] Kudo A,Ueda K,Kato H,et al.Photocatalytic O2evolution under visible light irradiation on BiVO4in aqueous AgNO3solution[J].Catal Lett,1998,53: 229-230.
[9] Sayama K,Nomura A,Zou Zhigang,et al.Photoelectrochem ical decomposition of water on nanocrystalline BiVO4film electrodes under visible light[J].Chem Commun,2003,23:2908-2909.
[10] Kohtani S,Tomohiro M,Tokumura K,etal.Photoxidation reactions of polycyclic aromatic hydrocarbons over pure and Ag-loaded BiVO4photocatalysts[J].Appl Catal B,2005,58:265-272.
[11] Kohtani S,Hiro J,Yamamoto N,et al.Adsorptive and photocatalytic properties of Ag-loaded BiVO4on the degradation of 4-n-alkylphenols under visible light irradiation[J].Catal Commun,2005,6:185-189.
[12] Ge L.Synthesis and characterization of novel visiblelight-driven Pd/BiVO4composite photocatalysts[J].Mater Lett,2008,62:926-928.
[13] 索静,柳丽芬,杨凤林.负载型Cu-BiVO4复合光催化剂的制备及可见光降解气相甲苯[J].催化学报,2009,30(4):323-327.
[14] Bhattacharya A K,Mallick K K,Hartridge A.Phase transition in BiVO4[J].Mater Lett,1997,30:7-13.
[15] 戈磊,崔立山.新型可见光活性氧化钯/钒酸铋复合光催化剂的制备及其光催化性能[J].硅酸盐学报,2008,36:320-324.
[16] 谢复青.碱性品红染料废水处理研究[J].大众科技,2005,10:167-168.
[17] 张静,张惠灵,麻园,等.Fe2O3/膨润土微波诱导氧化处理染料废水[J].化工环保,2010,30(3):214-218.
Preparation of Ag-BiVO4Catalyst and Its Photocatalytic Activity
Hu Lei,Ye Zhixiang,Yang Hao,Xu Chenghua,Yang Huaijin,Qu Bing
(College of Resources and Environment,Chengdu University of Information Technology,Chengdu Sichuan 610225,China)
BiVO4was synthesized by high-temperature solid-state reaction using Bi2O3and V2O5as raw materials,and then doped with Ag by dipping method to prepare Ag-BiVO4which has a good photocatalytic activity under visible light.The prepared Ag-BiVO4was characterized by XRD,UV-Vis spectroscopy and BET.The experimental results show that:Ag-doping w ill not change the crystal type of BiVO4,but can improve its visible light absorption performance;Under the conditions of Ag doping amount4%,solution pH 7.0,Ag-BiVO4dosage 7 g/L and reaction time 6 min,the decoloration rate of the basic fuchsin solution is over 90%.
bismuth vanadate;photocatalyst;silver;doping;visible light;basic fuchsin
TQ426.8
A
1006-1878(2011)03-0273-04
2010-09-26;
2011-01-10。
胡蕾(1983—),女,四川省广安市人,硕士生,主要从事环境催化、污染控制及资源化等方面的研究。电话13194877604,电邮 daim i4126@cuit.edu.cn。联系人:叶芝祥,电话028-85966089,电邮yzxiang@cuit.edu.cn。
(编辑 王 馨)

