聚苯乙烯支载井冈霉素树脂的合成及对葛根异黄酮的吸附
刘 丽,危冬梅,齐风佩,王春风,钟世华*
(1.湖南师范大学化学化工学院,中国 长沙 410081;2.益阳市灯泡厂,中国 益阳 413001)
大孔吸附树脂[1]是一类不含离子交换基团,具有大孔结构的高分子吸附剂.理化性质稳定,不溶于酸、碱及有机溶媒,且不受无机盐类及强离子、低分子化合物的干扰.其吸附性能与活性炭相似,与范德华力或氢键有关.引入极性基团可以改变表面电性或使其与某些被分离的化合物形成共轭和氢键吸附作用.
葛根异黄酮[2]是葛根中黄酮类化合物的总称,主要包括葛根素、大豆苷、大豆苷元等化合物.目前,葛根异黄酮的提取方法[3-4]主要有:醇回流法、醇渗滤法、浸渍法、微波辅助萃取法等;高纯度葛根异黄酮的提取方法主要是树脂吸附提取法.袁怀波[5]等利用大孔吸附树脂纯化葛根异黄酮的最大静态吸附量为80.25 mg·g-1(干树脂);周媛[6]等用AB-8树脂吸附葛根异黄酮的吸附容量为103.2 mg·g-1(干树脂);作者利用发酵产物井冈霉素分子结构(结构式如图1)含仲胺基和多间、邻羟基的特点,将井冈霉素与氯甲基化聚苯乙烯交联微球进行胺化反应,得到一种新型两亲树脂,与葛根异黄酮形成氢键和共轭作用,吸附提取得到高含量的黄酮提取物,吸附容量达到123.7 mg·g-1(干树脂).

图1 井冈霉素分子结构式
1 实验部分
1.1 实验试剂与主要仪器
氯球(工业品,南开大学化学试剂厂);井冈霉素(工业品,由武汉科诺生物科技有限公司);野葛根(市购),葛根素标准品(天津奎青商贸公司);95%乙醇(AR,湖南师范大学化学实业有限公司);苯(AR,湖南师范大学化学实业有限公司);甲苯(AR,湖南师范大学化学实业有限公司);N,N-二甲基甲酰胺(DMF)(AR,上海国药集团化学试剂有限公司);其余试剂均为分析纯.
DF-101s磁力搅拌器(巩义市予华仪器有限责任公司);SHZ-D循环水式真空泵(巩义市予华仪器有限责任公司);SHA-2000数显全温水浴振荡器(长沙素拓科学仪器设备有限公司);BT-100B数显恒流泵(上海沪西分析仪器厂有限公司);BSZ-100自动部分收集器(上海沪西分析仪器厂有限公司);Nicolet 370 FT-IR光谱仪(美国热电尼高力公司);PE-2400 (Ⅱ)型元素分析仪(美国 PE公司);Agilent 8453紫外吸收分光光度计(美国安捷伦科技有限公司);Tristar-3000型比表面积及孔隙分布测定仪(美国Micromenrities公司)及其他常用仪器与装置.
1.2 实验步骤
1.2.1 胺化反应 在250 mL三颈烧瓶中加入10.000 g氯球和5倍量的DMF,搅拌溶胀12 h,称取20.0 g井冈霉素用100 mL DMF使其溶解后将其转移到三颈烧瓶中,在常温下接着搅拌溶胀过夜.在3 h内均匀升温至120 ℃反应24 h.反应结束后,冷却、抽滤、水洗,然后用甲醇抽提12 h,再用水洗至无甲醇存在,真空低温干燥.
1.2.2 树脂的结构表征和性能测定 树脂经干燥、研细,用KBr压片法在Necolet 370型傅立叶变换红外光谱仪上测定.比表面、孔容、孔径分布用比表面分析仪Tristar 3000测定.
树脂的含水量按国家标准GB 5757-86测定.采用数码照相法,将树脂干燥后的状态拍摄下来,测定照片中树脂的直径,记作D0.将室温下该树脂在不同溶剂中溶胀24 h后的状态拍摄下来,测定照片中树脂的直径,记作Dt.根据下式计算处树脂的溶胀比Rv=(Dt/D0)3.
1.2.3 树脂对葛根异黄酮的静态吸附 葛根异黄酮溶液是由野葛根经70 %乙醇溶液在80 ℃下提取3次,每次提取3 h,合并3次的滤液,浓缩提取液至相当于0.5 g·mL-1的溶液,然后在12 000 r·min-1下高速离心15 min,取上清液备用,用紫外分光光度法[8]测得总黄酮含量为67.64 mg·L-1.
每次量取备用的葛根异黄酮溶液20.00 mL,放入50 mL锥形瓶中,加入0.100 g干树脂,放入多用恒温振荡器中振荡24 h,取样用紫外分光光度法检测葛根异黄酮的质量浓度,按下式计算吸附量:
q=(C0-Ce)V/m,
(1)
式中,q为吸附容量(mg·g-1),C0为吸附前葛根异黄酮的质量浓度(mg·L-1),Ce为吸附平衡后溶液中葛根异黄酮的质量浓度(mg·L-1),V为溶液的体积(L),m为树脂的质量(g).以平衡浓度C为横坐标,吸附量q为纵坐标,作出树脂在不同温度下对葛根异黄酮溶液的吸附等温线.
1.2.4 树脂对葛根异黄酮的动态吸附及洗脱 用内径为10 mm层析柱湿态装柱,床体积为10 cm3,流速为20 cm3·h-1,醇提法提取出来的葛根异黄酮溶液直接上柱,检测流出液中葛根异黄酮的含量.洗脱前,先用30 cm3去离子水洗出上柱液.用70 %的乙醇溶液为洗脱液,洗脱速度为10 cm3·h-1.
树脂经过4 %氢氧化钠溶液再生之后可以重复使用.
2 结果与讨论
2.1 树脂的红外光谱及元素分析

图2 氯球(a) 和新型树脂(b)的红外光谱图
图2为氯球和新型树脂的红外光谱图.从图中可以看出,合成的新型树脂与氯球相比有几处明显变化:增加了1 007 cm-1、3 302 cm-1处的吸收峰,1 007 cm-1是C—N胺基的伸缩振动吸收,3 302 cm-1是O—H分子间氢键的伸缩振动;而675 cm-1、1 265 cm-1处的C—Cl吸收峰减弱很多.
同时对该新型树脂的元素分析结果表明:N的质量分数1.94%,Cl的质量分数由16.09%下降到0.91%.新型树脂中Cl原子被井冈霉素(MA= 515.51)完全取代后,其N原子的理论质量分数为2.04 %,而实际数据为1.94%,胺解率达94%,与氯球残余氯6%相吻合.由此可知此胺解实验已经成功将井冈霉素支载到氯球上.

表1 新型树脂和氯球的元素分析数据
2.2 树脂的比表面和孔径分布分析
用Tristar 3000比表面分析仪测得氯球的BET表面积为31.67 m2·g-1,平均孔径为21.88 nm;胺解后树脂的BET表面积为37.62 m2·g-1,平均孔径为20.26 nm.胺解后树脂BET表面积比胺解前增大,主要是因为功能基化反应导致树脂中多孔结构发生了坍陷,部分大孔塌缩成介孔或微孔,从而导致了比表面的增加和平均孔径的减小.
2.3 树脂的含水量和溶胀性能分析
按标准GB 5757-86,树脂的含水量为55.61 %,同时树脂在不同的溶剂中的溶胀比如下表所示:

表2 新型树脂在不同溶剂中的溶胀比
从表2数据可以看出,新型两亲树脂在这些溶剂中的溶胀比差异,这是因为这种树脂具有两亲的结构,既可以在水中溶胀,也可以在有机溶剂中溶胀.综合这5种溶剂,该树脂在苯甲醇中的溶胀比最大,这是因为苯甲醇中既有疏水的苯基又有亲水的羟基,而且苯环的疏水作用强于乙醇中的乙基,因此树脂在苯甲醇中的溶胀比最大.由此溶胀性能可推测该树脂中疏水性的苯乙烯/二乙烯苯具有疏水的吸附性能、亲水性的井冈霉素具有氢键的吸附性能.
2.4 树脂对葛根异黄酮溶液的吸附等温线
图3为聚苯乙烯井冈霉素树脂对葛根异黄酮溶液的吸附等温线.从图3可以看出,此树脂在试验浓度范围内,在293 K时,对葛根异黄酮的最大吸附量可达到123.7 mg·g-1(干树脂),而且这些吸附等温线都是Ⅰ型吸附等温线.
根据图3,求得等吸附量下溶液的平衡浓度C,以lnC为纵坐标,1/T为横坐标作出吸附等量线,如图4所示.从图4可知,lnC与1/T呈良好的线性关系,根据Clapeyron-Clausius方程[9-11]:
lnC=ΔH/(RT) +K
(2)
(2)式中,ΔH是聚苯乙烯井冈霉素树脂对葛根异黄酮的吸附焓(kJ·mol-1),T为绝对温度(K),R是理想气体常数,K是常数.线性回归法求出各吸附等量线的斜率,即可求出聚苯乙烯井冈霉素树脂在不同吸附量时对葛根异黄酮溶液的吸附焓ΔH(见表3).
以lnq对lnC作图,如图5所示,用线性回归法求出直线所对应的斜率,得到参数n,再由方程ΔG=-nRT[10-12]求出吸附自由能ΔG.由方程ΔS=(ΔH-ΔG)/T求出各吸附熵ΔS.各热力学函数数据如表3所示.

图3 树脂对葛根异黄酮的吸附等温曲线 图4 树脂对葛根异黄酮的吸附等量线

图5 树脂吸附葛根异黄酮的lnq-lnC图 图6 树脂对葛根异黄酮的动态吸附曲线

q /(mg·g-1) ΔH /(kJ·mol-1)ΔG /(kJ·mol-1)ΔS /(J·mol-1·K-1)293 K298 K303 K308 K293 K298 K303 K308 K20-22.05 -1.63 -1.55 -1.54 -1.53 -69.71 -68.81 -67.71 -66.62 40-23.92 -1.63 -1.55 -1.54 -1.53 -76.08 -75.06 -73.86 -72.68 60-31.06 -1.63 -1.55 -1.54 -1.53 -100.46 -99.04 -97.44 -95.87 80-32.69 -1.63 -1.55 -1.54 -1.53 -106.03 -104.51 -102.83-101.17
从图3~5和表3可以看出:随着温度的升高,树脂对葛根异黄酮的吸附量降低,吸附焓ΔH小于0,表明吸附过程是放热的,该放热过程与文献相一致[13].在实验浓度范围内,葛根异黄酮溶液的微分吸附焓在8~50 kJ·mol-1之间,比范德华力要大,但是在氢键的范围内,且吸附后的树脂可以用乙醇很容易的解吸下来,排除了离子键的可能,因此,该树脂吸附葛根异黄酮溶液主要是由于氢键和共轭作用.ΔG小于0,说明吸附过程能够自发进行.ΔS小于0,是因为在吸附过程中,葛根异黄酮分子因为氢键作用和共轭作用被吸附在树脂的吸附位点上,从而使分子更为有序.
2.5 树脂对葛根异黄酮的动态吸附及脱附
图6和图7分别为树脂对葛根异黄酮溶液的动态吸附和解吸曲线.从图中可以看出,在流出液为200 cm3时出现泄露,在以70 %的乙醇溶液为洗脱剂时,葛根异黄酮很容易洗脱下来且没有拖尾现象,解吸率达到97 %.在装柱使用过程中,树脂机械强度好,未破损,可重复使用.重复再生之后的树脂对葛根异黄酮的吸附容量仍然可以达到105 mg·g-1以上(图8),重复利用率为85 %以上.
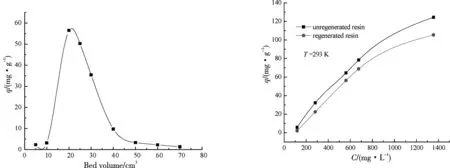
图7 树脂对葛根异黄酮的动态解析 图8 树脂再生后对葛根异黄酮的吸附对比
3 结论
合成了聚苯乙烯支载井冈霉素大孔两亲吸附树脂,树脂中特有的多邻、间羟基能够与葛根异黄酮形成氢键作用,苯基的双键能够与葛根异黄酮中的双键形成共轭作用,对葛根异黄酮表现出良好的吸附性能,对葛根异黄酮的最大吸附量达到123.7 mg·g-1.
参考文献:
[1] 何炳林, 黄文强. 离子交换与吸附树脂[M]. 上海:上海科技教育出版社,1995.
[2] 姚新生, 赵守训, 潘得济, 等. 天然药物化学[M]. 北京:人民卫生出版社,1996.
[3] 詹 永, 杨 勇. 葛根异黄酮的提取方法与应用[J]. 广州食品工业科技, 2004,20(2):169-170.
[4] 郭建平, 孙其荣, 周 全, 等. 葛根总黄酮不同提取工艺探讨[J]. 中草药, 1995, 26(10): 522-523.
[5] 袁怀波, 赵国华, 李洪军, 等. 利用大孔吸附树脂纯化葛根异黄酮的研究[J]. 食品与发酵工业, 2003,29(2):62-65.
[6] 周 媛, 程 凡, 罗少华. 大孔树脂对葛根异黄酮的吸附及分离纯化研究[J]. 时珍国医国药, 2007,18(12):3008-3010.
[7] GB/T 9553-1993. 井冈霉素水剂[S].北京:中国标准出版社,1993.
[8] 董华强, 刘福来, 林丽超, 等.合水粉葛异黄酮含量的紫外分光光度法和HPLC法分析研究[J]. 食品科学,2008,29(10):477-479.
[9] GARCIA-DELGADO R A, COTORUELO-MINGUEZ L M, RODRIGUEZ J J. Equilibrium study of single-solute adsorption of anionic surfactants with polymeric XAD resins[J]. Sep Sci Technol, 1992, 27(7): 975-987.
[10] 李爱民, 张全兴, 刘福强. 一种亲水的酚羟基修饰聚苯乙烯树脂对酚类化合物的吸附热力学[J]. 离子交换与吸附, 2001, 17(6): 515-525.
[11] 王 重, 史作清. 酚醛型吸附树脂吸附VB12的热力学研究[J]. 功能高分子学报,2003,16(1): 1-5.
[12] JOHN P B, MARIOS T. Removal of hazardous organic pollutants by biomass adsorption[J]. Water Pollut Control Fed, 1987, 59(4): 191-198.
[13] 李剑君, 李稳宏, 高 新, 等. AB-8型大孔吸附树脂吸附葛根素过程的研究[J]. 西安交通大学学报,2000,34(4): 78-81.

