参芪扶正注射液红外光谱质量控制方法研究Δ
肖树雄,周清,钟桂雄,温金莲(1.广东省药品检验所,广州市510180;.广东药学院药科学院,广州市510006;.丽珠集团利民制药厂,韶关市 5108)
参芪扶正注射液红外光谱质量控制方法研究Δ
肖树雄1*,周清2,钟桂雄3,温金莲2(1.广东省药品检验所,广州市510180;2.广东药学院药科学院,广州市510006;3.丽珠集团利民制药厂,韶关市 512028)
目的:建立参芪扶正注射液质量控制的新方法。方法:采用傅里叶变换红外光谱(FTIR)技术获取图谱,并利用数学软件对图谱进行求导及相关系数比对。结果:获得了10批次参芪扶正注射液、4批次党参/黄芪药材及各药材提取物、阴性注射液等的红外光谱图,找出了参芪扶正注射液的特征吸收峰;各批次间参芪扶正注射液的相关系数均>0.99。结论:该方法取样量小、简便、迅速、特征性强,有一定的推广应用价值。
参芪扶正注射液;红外光谱法;质量控制;党参;黄芪
中药制剂的组成十分复杂,其红外光谱是其中多个组分光谱的叠加。中药中各种化学成分只要在质和量方面相对稳定,并且样品处理方法按统一要求进行,其红外光谱就应该具有一定的稳定性和可重复性。红外光谱的宏观指纹性可以反映中药混合物中各种成分的叠加谱,不同种的混合物其相应的化学组成不同也就引起分子光谱整体谱图的变化,凭借这些变化特征直接或稍作数学处理就可以直接用在质控上[1,2]。参芪扶正注射液的主要组分为党参和黄芪[3],通过中药制剂常用的“水提醇沉”法制得。它具有益气扶正之功效,用于气虚证肺癌、胃癌的辅助治疗,能提高气虚患者免疫功能,与化疗合用有助于提高化疗效果。目前,该产品虽有高效液相色谱(HPLC)指纹图谱定性鉴别等方法,但该法前处理过程耗时、操作烦琐。本试验试图利用红外光谱法的优势建立一种简便、快捷的方法,以作为该产品日常生产的内部质控方法。
1 仪器与试药
Spectrum 110型傅里叶变换红外光谱(FT-IR)仪(美国Perkin Elmer公司)。
党参、黄芪(膜荚黄芪)对照药材(中国食品药品检定研究院,批号分别为121057-200805、121462-200702);药材提取物、参芪扶正注射液(批号:0810530、0903126、0909445、0909446、0909447、0909448、090652、0904153、0907249、0907248)、阴性注射液及注射液中其他添加物等均由丽珠集团利民制药厂提供;KBr为光谱纯。
2 方法
2.1 样品处理方法
2.1.1 液体样品处理 采用KBr吸附法。取0.15mL参芪扶正注射液置于蒸发皿中,加80mg KBr,于水浴锅上蒸干,刮下,再加70mg KBr混合研磨充分均匀后压片,置FT-IR仪中进行检测,收集扫描得到的谱图。
2.1.2 固体样品处理 用粉碎机将药材粉碎,研磨,取样品粉末约3mg与150mg KBr(碎晶)混合研磨充分均匀后压片,其余同“2.1.1”项下。
2.2 测试及数据处理方法
2.2.1 仪器条件 光谱范围:4000~400cm-1;检测器:中红外氘化三甘氨酸硫酸酯(DTGS)检测器;分辨率:4cm-1;扫描信号累加16次;扫描实时扣除H2O和CO2的干扰。
2.2.2 谱图处理 使用美国Perkin Elemer公司Spectrum软件和相似度分析软件进行谱图处理。
2.2.3 二阶导数谱 采用Spectrum软件中的求导数功能,13点平滑,获得各样品的红外二阶导数光谱图。
3 结果
3.1 药材的红外吸收图谱
取党参和黄芪对照药材各4批次,于60℃干燥2h,按“2.1.2”项下方法处理后绘制红外吸收图谱,分别见图1、图2。
4批党参药材红外图谱的相关系数分别为0.9999、0.9842、0.9707、0.9665,均在 0.96以上;特征峰值在779、818、868、936、1056、1257、1408、1637、1735cm-1附近,特别是779、818、868、936cm-1处对应的峰值非常明显,经与文献对比发现其特征性强,不容易被混淆,说明党参药材均一稳定。
4批黄芪药材红外图谱的相关系数分别为0.9999、0.9520、0.9652、0.9483,均在0.94以上;特征峰值在850、867、1050、1104、1240、1637cm-1附近,其中1050、1104、1240cm-1处对应的峰值比较明显,可作为鉴别的依据,说明黄芪药材均一稳定。
3.2 药材提取物的红外吸收图谱
3.2.1 未精制及精制党参提取物、未精制及精制黄芪提取物
取各药材提取物,分别按“2.1.2”项下方法处理后绘制红外吸收图谱,分别见图3、图4(图中a、b、c分别代表该药材未精制、精制提取物及药材的红外吸收图谱)。

图1 党参药材的红外吸收图谱Fig 1 IR absorption spectrum of Codonopsis pilosula

图2 黄芪药材的红外吸收图谱Fig 2 IR absorption spectrum ofAstrogalus mongholicus
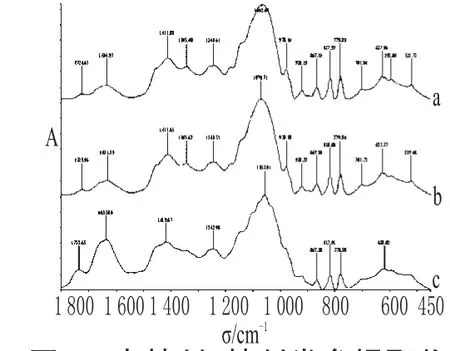
图3 未精制、精制党参提取物及党参药材的红外吸收图谱Fig 3 IR absorption spectrum of unrefined,refined extracts and C.pilosula

图4 未精制、精制黄芪提取物及黄芪药材的红外吸收图谱Fig 4 IR absorption spectrum of unrefined,refined extracts andA.mongholicus
由图3可见,党参提取物是否精制,与党参药材的红外图谱均基本一致,说明提取对党参红外光谱的影响很小。对黄芪,由图4也可以得出同样的结论。
3.2.2 未精制及精制参芪提取物 取参芪药材提取物,按“2.1.2”项下方法处理后绘制红外吸收图谱,详见图5。
由图5可见,参芪提取物是否精制,与参芪扶正注射液的红外图谱均基本一致,同样也说明制作工艺不同对参芪扶正注射液红外光谱的影响很小。
从图3~图5的分析可知,中药注射剂的原料、中间体与成品的红外光谱有很大的关联性,这与色谱指纹图谱类似,提示可建立红外指纹图谱的评价方法。
3.3 阴性注射液的红外吸收图谱
取阴性注射液a(缺党参)、阴性注射液b(缺黄芪)、阴性注射液c(缺党参、黄芪),分别按“2.1.1”项下方法处理后绘制红外吸收图谱,详见图6。
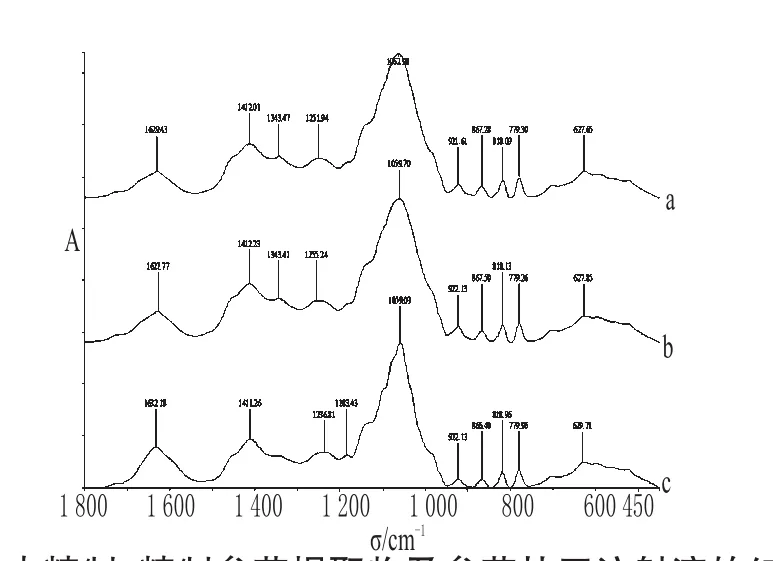
图5 未精制、精制参芪提取物及参芪扶正注射液的红外吸收图谱Fig 5 IR absorption spectrum of unrefined,refined extracts and Shenqi fuzheng injection

图6 阴性注射液红外吸收图谱Fig 6 IR absorption spectrum of negative injection
由图6可见,阴性注射液a不体现党参的特征峰值,能部分体现黄芪的特征峰值;阴性注射液b不体现黄芪特征峰值,能体现党参的特征峰值,与党参药材的红外图谱基本一致;阴性注射液c不体现党参及黄芪的的特征峰值。这从反面再次说明,参芪扶正注射液的原料、中间体与成品的红外吸收光谱有很大的关联性。
3.4 10批参芪扶正注射液的红外吸收图谱
取不同批次参芪扶正注射液,分别按“2.1.1”项下方法处理后绘制红外吸收图谱,详见图7。
10批参芪扶正注射液的相关系数分别为0.9999、0.9978、0.9951、0.9917、0.9948、0.9962、0.9934、0.9920、0.9928、0.9923,说明各批次的相关性良好。对其图谱求二阶导数,13点平滑,以增大其差异性,详见图8。
由图8可见,增大差异性后,其特征峰值基本无变化,进一步说明参芪扶正注射液各批次间基本无差异。
4 讨论
通过上述试验数据及大量文献对比发现,参芪扶正注射液与原料和中间体的红外光谱关联性很强,稳定工艺制成的产品批次间重现性也很高。由此可见,红外光谱法用于参芪扶正注射液质量控制的特征性很强,可应用于产品的质量控制中。
含水物质红外光谱测试中常用的样品制备技术有结晶压片法、吸附压片法、蒸发涂片法、蒸发成膜法、液池参比法等[4]。本试验通过KBr吸附、蒸发、压片等步骤对液体样品进行处理,较好地解决了红外光谱检测液体样品处理的技术难题。
本试验对参芪扶正注射液的质量实施监控,主要依据为标准图谱和图谱的特征数据,总的来讲就是相似度,10批样品的相似度均>0.99,远远好于色谱法规定相似度不得低于0.85的要求。相似度反映的是注射液(残渣)各物质红外光谱的叠加结果,但实际上,正如色谱指纹图谱鉴别[5]一样,红外指纹图谱也跟物质响应灵敏度有关,各物质在总体的权重不一样,相似度高只能部分说明产品的一致性强。红外光谱法是一种整体性的模糊方法,真正要反映产品的质量好坏还需要进一步通过大量的试验数据,特别是已经确证不合格样品的试验数据来确定。
由于采用红外光谱分析样品既非分离提取,不使用有毒、有害试剂,又系无损分析,保持中成药原有特性,兼有操作简单、分析成本低、周期短等优点,因此本方法的建立可为中药注射剂的质量控制提供一种新的简便、快捷的分析方法,有一定的推广应用价值。
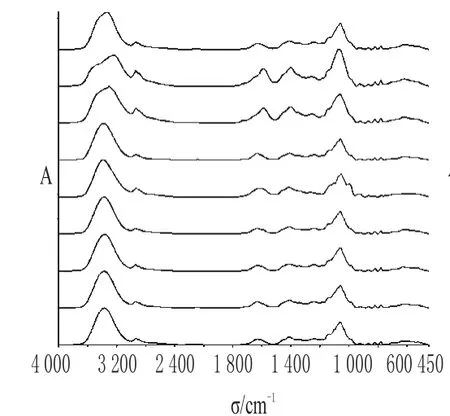
图7 参芪扶正注射液的红外吸收图谱Fig 7 IR absorption spectrum of Shenqi fuzheng injections
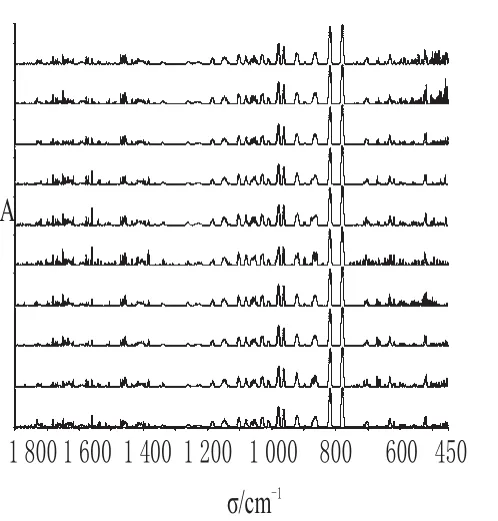
图8 参芪扶正注射液红外吸收二阶导数图谱Fig 8 Second derivative IR absorption spectrum of Shenqi fuzheng injections
[1] 关瑾光.近代傅立叶变换红外光谱技术及应用(上卷)[M].北京:科学技术文献出版社,1994:2-53.
[2] 孙素琴,周 群,秦 竹.中药二维相关红外光谱鉴定图集[M].北京:化学工业出版社,2003:3-11.
[3] 张 磊,聂 磊,王唯红.红外光谱法结合化学计量学方法鉴别黄芪产地[J].中国药房,2010,21(19):1772.
[4] 谢狄霖,陈 忠.含水物质红外光谱测试的样品制备[J].分析仪器,2003,4:15.
[5] 谢培山.中药制剂色谱指纹图谱(图像)鉴别[J].中成药,2000,22(6):391.
Study on Quality Control Method of Shenqi Fuzheng Injection by Infrared Spectroscopy
XIAO Shu-xiong(Guangdong Institute for Drug Control,Guangzhou 510180,China)
ZHOU Qing,WEN Jin-lian(School of Pharmaceutical Science,Guangdong Pharmaceutical University,Guangzhou 510006,China)
ZHONG Gui-xiong(Lizhu Group Limin Pharmaceutical Factory,Shaoguan 512028,China)
OBJECTIVE:To establish a new quality control method for Shenqi fuzheng injection.METHODS:FT-IR spectrometric technique was adopted to obtain spectrograms,and the second derivative and correlation coefficient of spectrograms were achieved by mathematical software.RESULTS:Infrared spectrograms of 10batches of Shenqi fuzheng injection,4batches of Codonopsis pilosula/Astragalus mongholicus,as well as their extractive,negative injection were obtained.The unique absorption peaks of Shenqi fuzheng injection were found,and the correlation coefficients of all injection were higher than 0.99.CONCLUSION:The method was low usage volume,convenient,quick and strong characteristics,and it could be applied in practical production.
Shenqi fuzheng injection;Infrared spectroscopy;Quality control;Codonopsis pilosula;Astragalus mongholicus
R283.61;R927
A
1001-0408(2011)47-4465-03
Δ 2007年粤港关键领域重点突破项目(TC07BF09-11)
*主任药师。研究方向:中药检验、新药研发。电话:020-81079652。E-mail:13527622441@139.com
2011-03-09
2011-10-14)

