电渗析法从谷氨酸发酵液中提取谷氨酸铵的研究
艾社芳,石绍渊,王金梅,张胜琴,李 春,3,丛 威,*
(1.石河子大学化学化工学院/新疆兵团化工绿色过程重点实验室,新疆石河子832003;2.中国科学院过程工程研究所,生化工程国家重点实验室,北京100080;3.北京理工大学生命学院,北京100081)
电渗析法从谷氨酸发酵液中提取谷氨酸铵的研究
艾社芳1,石绍渊2,王金梅1,张胜琴1,李 春1,3,丛 威2,*
(1.石河子大学化学化工学院/新疆兵团化工绿色过程重点实验室,新疆石河子832003;2.中国科学院过程工程研究所,生化工程国家重点实验室,北京100080;3.北京理工大学生命学院,北京100081)
探讨了利用电渗析法从谷氨酸发酵液中直接分离提取谷氨酸铵。通过模拟谷氨酸发酵液对提取工艺进行了单因素优化实验,获得了如电流密度、料液与浓缩液体积比、循环流量等优化操作条件。采用优化条件对真实谷氨酸发酵液进行电渗析分离提取谷氨酸铵,当料室pH4.7左右可观察到结晶现象。通过补加氨水调节料室pH,可明显改善电渗析的整体效果,其中浓室谷氨酸浓度达到120g/L,回收率为78.8%。
电渗析,谷氨酸铵,谷氨酸发酵液,氨水
电渗析[1]是在直流电场的作用下,离子透过选择性离子交换膜而发生迁移,使带电离子从水溶液和其他不带电组分中分离出来的一种电膜分离过程,已在各种天然水淡化[2]、海水浓缩制盐、废水处理[3]等行业中得到广泛应用。由于电渗析技术具有操作简便、不污染环境,可不添加酸碱等化学试剂[4],有望大幅度降低发酵产品生产过程的酸碱消耗,可实现清洁生产等优点,将电渗析技术用于发酵液处理和发酵产品回收中尤其受到关注。如电渗析技术在氨基酸和蛋白质生产中的应用,主要用于氨基酸脱盐以及分离氨基酸和糖类物质[5-6]。王辉等[7]利用电渗析进行了氨基酸的分离,避免了杂质离子的引入,提高了氨基酸的纯度。目前味精生产厂家普遍采用发酵法生产谷氨酸,然后采用一次低温等电点法提取工艺来分离谷氨酸。离心分离后的母液中还含有1.5%~2%谷氨酸,2.0%~2.5%氯化铵及葡萄糖、菌体等,采用离子交换法提取等电母液中的谷氨酸会产生大量的高盐有机废水[8-9]。广州奥桑味精食品有限公司[10]对谷氨酸发酵液进行了新工艺的研究,运用膜分离技术将谷氨酸发酵液的菌体与超滤清液分离、多效蒸发浓缩、连续等点结晶、晶体转型等工序相结合,虽然得到高浓度饲料蛋白,但是仍存在投资成本大、循环周期长、用水量大等问题。采用电渗析法将发酵液中的谷氨酸盐进行浓缩分离,除去部分杂质[11],可简化后续精制提纯等工艺,避免水洗过程大量用水的问题。文中利用模拟谷氨酸发酵液,对提取工艺进行了单因素优化实验,根据实验所得优化条件用于对真实谷氨酸发酵液进行电渗析分离提取谷氨酸铵,并通过补加氨水调节料室内pH来改善分离提取效果。
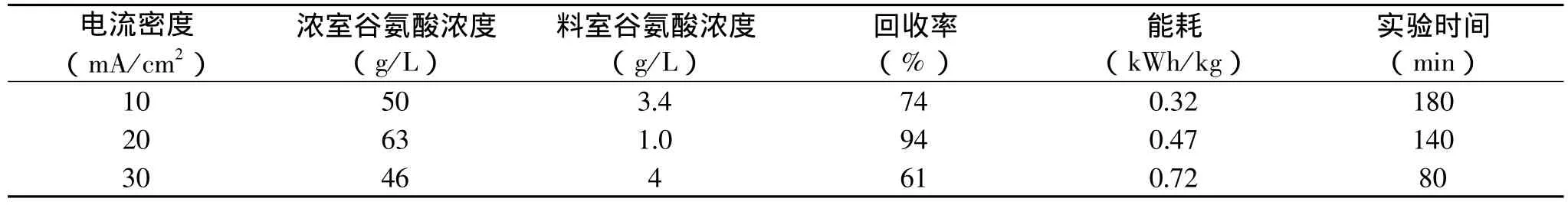
表1 不同电流密度的电渗析实验结果
1 材料与方法
1.1 材料与仪器
L-谷氨酸分析纯 北京欣经科生物技术有限公司提供;谷氨酸发酵液 本课题组刘辉提供;硫酸钠、氢氧化钠 北京化学试剂公司;氨水 天津化学试剂公司。
电渗析器 北京三元八达科技股份有限公司提供;电导仪DDS-307A 上海雷磁仪器厂;低温恒温仪DS-1015 宁波市海曙天恒仪器;pH计DELTA-320梅特勒托利多(上海)仪器有限公司。
1.2 实验方法
1.2.1 电渗析法提取谷氨酸铵的实验原理 谷氨酸是两性电解质,如在pH大于3.22时,谷氨酸大多以阴离子状态存在,在直流电场作用下,透过阴膜而被阳膜阻留在浓缩室中,铵根离子带正电荷,透过阳膜而被阴膜阻留在浓缩室中,但残糖、蛋白质等非电解质却仍留在发酵液中,由此可以达到把发酵液中的谷氨酸铵与其他非电解质组分分离而提纯的目的[12]。实验中所用离子交换膜均为均相膜,JAM-15、JCM-15分别表示交联度为15%的阴离子交换膜和阳离子交换膜,阴阳膜交替共由四对组成,单张膜的面积为22cm×6.8cm。
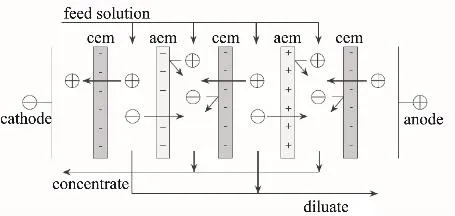
图1 电渗析法提取谷氨酸铵的膜堆结构(aem:阴离子交换膜;cem:阳离子交换膜)
1.2.2 谷氨酸的测定 谷氨酸采用离子色谱法测定,离子色谱仪为瑞士万通公司生产的761型离子色谱仪。所用色谱柱的测试条件为:MetrosepC4-150阳离子色谱柱,柱长150mm。测定条件为:洗脱液为1mmol/L吡啶二羧酸及4mmol/L酒石酸,流速为0.9mL/min,最大压力为15MPa,进样体积20μL。谷氨酸回收率R按下式计算:
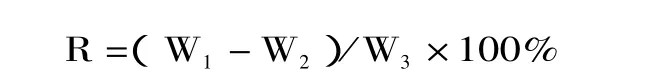
式中:W1表示实验结束后浓室内谷氨酸的质量,g;W2表示实验开始时浓室内谷氨酸的质量,g;W3表示实验开始时料室内谷氨酸的质量,g。
1.2.3 实验操作 准确称取100.00g L-谷氨酸溶入1000mL的纯净水中,并用质量分数为25%的氨水调节pH在6~7之间,即为配制好的模拟谷氨酸铵溶液,用作电渗析的进料液;称取3.68g L-谷氨酸溶入500mL纯净水中,即为0.05mol/L的谷氨酸溶液,用作浓室的循环溶液;称取30.00g硫酸钠充分溶入1000mL水中,用作电渗析极室的循环溶液。其中,极室、料室和浓室的溶液循环流速根据实验要求来定。电渗析提取谷氨酸铵实验在恒电压条件下操作,其能耗计算如下:
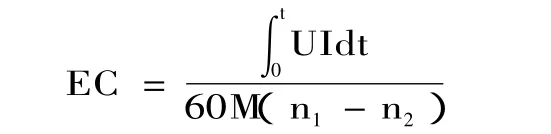
式中:EC-能耗,kWh·kg-1;U-操作电压,V;I-电流,A;t-操作时间,min;M-盐的摩尔质量,g· mol-1;n1-料室初始摩尔浓度,mol;n2-料室t时刻摩尔浓度,mol。
在电渗析运行过程中,每20min对浓室、料室溶液进行取样分析,并记录实验过程中电压、各溶液的体积、pH以及电导率的变化。
2 结果与讨论
2.1 单因素实验
2.1.1 电流密度 电流密度的大小直接关系到离子迁移推动力的大小。电流密度较小,工作电压较低,离子的迁移推动力较小,不能充分发挥电渗析器的效能;但当电流密度增加到某一数值时,由于发生极化现象而可能导致膜的面电阻增加,部分电能消耗在水的电离及其他离子的迁移上,所以选择合适的电流密度对电渗析过程非常重要。实验选择了三个不同电流密度,结果如表1所示。
不同的电流密度对谷氨酸收率及料室浓度的影响见表1。当电流密度由10mA/cm2上升到20mA/ cm2时,谷氨酸铵回收率由74%上升到94%,料室中剩余的谷氨酸浓度由3.4g/L降低到1.0g/L。结果表明,增加电流密度,操作时间相对缩短,仍可提高谷氨酸铵的回收率,且浓室回收谷氨酸的浓度有所升高,有利于提高电渗析器的效能。但当电流密度由20mA/cm2上升到30mA/cm2时,谷氨酸回收率仅为61%,且其单位能耗也明显增加,这可能是由于高电流密度下体系发生极化现象所致。表1结果表明,当电流密度为20mA/cm2时,谷氨酸铵的回收率最高,因此在后续实验中都选择电流密度为20mA/cm2。
2.1.2 料液与浓缩液的体积比 料液与浓液的体积比可影响谷氨酸铵的回收率和浓室中的谷氨酸浓度等。实验选择了三个不同的体积比进行比较,料液与浓液的体积比分别采用1∶1、2∶1、3∶1,考察不同体积比对浓室和料室中谷氨酸铵浓度的影响,实验结果如图2和图3所示。
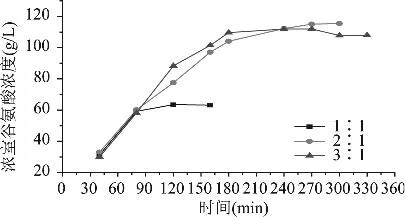
图2 体积比对浓室中谷氨酸铵浓度的影响
由图2和图3可见,增大体积比,谷氨酸的回收浓度有所提高。当体积比为1∶1时,谷氨酸最终回收的浓度60g/L左右,回收率74%。当料室与浓室的体积比为2∶1、3∶1时,其能耗分别为0.46、0.61kWh/kg,谷氨酸回收浓度分别迅速升高至115、110g/L,但谷氨酸的回收率分别为89%和76%。在体积比1∶1、2∶1时,料室内剩余谷氨酸浓度均在1g/L左右,但体积比3∶1时料室剩余谷氨酸浓度较高。
由此可见,料液与浓液体积比2∶1和3∶1时,浓室回收的谷氨酸浓度较高,但当体积比3∶1时的能耗较高,体积比是1∶1时谷氨酸铵回收浓度较低,不利于谷氨酸提取及后续工序的进行。
2.1.3 溶液循环流速 电渗析操作过程中,当溶液循环线速度较大时,会对膜的冲击力较大,可能会引起膜堆渗漏和能耗增加;当线速度较低时,则会降低液流的紊流程度,导致扩散滞留层加厚,不利于离子的跨膜迁移。实验采用溶液的循环流量分别为12、17L/h,考察不同流速对浓缩液中谷氨酸浓度的影响,实验结果如图4所示。
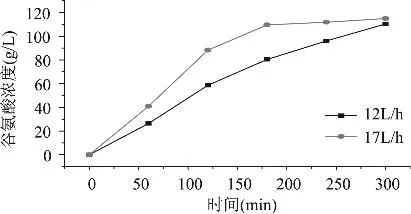
图4 流速对浓缩液中谷氨酸浓度的影响
两种不同的线速度条件下最终浓室谷氨酸的浓度基本相当。在实验初始阶段,线速度为17L/h时浓室谷氨酸浓度的增加较快,线速度为12L/h时谷氨酸浓度增加相对较慢。这可能是由于溶液线速度增大,使单位时间内的循环流量增加和湍流程度加大,促进了氨基酸及无机离子的迁移,使得实验开始时浓室谷氨酸浓度迅速升高。
综合单因素实验结果,选用优化操作条件:电流密度为20mA/cm2、流量12L/h、浓室与料室的体积比2∶1,连续操作140min。结果显示,经过优化后电渗析整体效果如浓室回收谷氨酸浓度、料室残余浓度、回收率和能耗等有了明显的改善。其中浓室谷氨酸浓度达到104g/L,料室谷氨酸剩余浓度为0.1g/L,回收率高达99.93%,能耗为0.43kWh/kg。
2.2 采用优化的条件从谷氨酸发酵液分离提取谷氨酸铵实验
采用优化操作条件,进行真实谷氨酸发酵液的电渗析分离谷氨酸铵。实验结果如表2所示。

表2 谷氨酸发酵液电渗析分离谷氨酸铵实验结果
实验过程中发现,当实验进行到370min时,由于料室出现严重结晶现象,导致实验无法继续进行。这是由于谷氨酸发酵液pH一般低于7,在进行谷氨酸铵分离过程中,一方面由于氨基酸根离子较铵根离子迁移较慢,这种不对等的迁移会导致料室内pH不断下降;另一方面,由于谷氨酸等电点为3.22,随着料室内的pH逐渐降低,当下降到4.5~3.2之间时就会出现结晶,致使电渗析过程无法进行。为了避免由于pH下降所导致的沉淀现象,通过向料室内补加氨水,使得pH在6~7范围内,实验结果如表3所示。
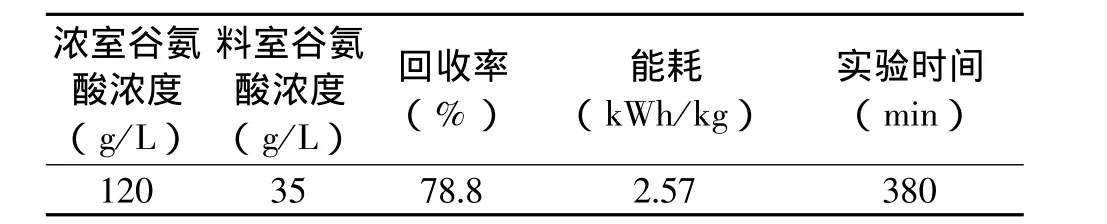
表3 补加氨水实验
通过补加氨水调节pH时,浓室内的谷氨酸浓度可达到120g/L,回收率由46.47%升高到78.8%,但此时料液中的谷氨酸仍剩余较多,有35g/L未能分离。从真实谷氨酸发酵液中提取谷氨酸铵的收率未能达到如模拟料中的高回收率,有很多因素导致,一方面是由于发酵液中含有的残糖、胶体物质等各种杂质,可能会将一部分谷氨酸包裹其中;另一方面,发酵液中的其他氨基酸如丙氨酸等与谷氨酸存在竞争性迁移所致。另外,当料液中的谷氨酸铵脱除到一定程度时,如果继续在较高的恒电流密度下操作会导致极化现象发生,因此会影响到谷氨酸的进一步迁移分离和降低电流效率。
3 结论
单因素实验显示,当选择电流密度20mA/cm2、料液与浓液体积比2∶1、循环流量12L/h时,电渗析分离谷氨酸的效果最佳。采用优化条件实验,如浓室回收谷氨酸浓度、料室残余浓度、回收率和能耗等都有显著改善,其中浓缩谷氨酸浓度达到104g/L,料室谷氨酸剩余浓度为0.1g/L,回收率高达99.93%,能耗也有明显的降低。
采用经单因素优化的实验条件,用于从谷氨酸发酵液中电渗析浓缩分离谷氨酸铵,当料液pH4.7左右时会出现结晶现象,此时料室谷氨酸浓度为70g/L,浓室浓度92g/L。由于谷氨酸根与铵根离子在溶液中的迁移速度及其跨膜迁移的难易程度不同,这种离子迁移的不对等性会造成料液中铵根离子减少和谷氨酸增多,使料液pH下降而导致谷氨酸等出现结晶现象。通过添加氨水调节料室pH,浓室内谷氨酸浓度可达到120g/L,回收率为78.8%。
[1]张维润.电渗析工程学[M].北京:科学出版社,1995:3-4.
[2]马成良.我国电渗析技术发展浅析[J].膜科学与技术,1998(4):58-60.
[3]杨洪渊.用填充床电渗析直接处理废水同时制取纯水[J].水处理技术,1985(5):53-56.
[4]邵刚.膜法水处理技术[M].北京:冶金工业出版社,1992:11-12.
[5]李福勤,杨云龙.电渗析技术发展方向的思考[J].科技情报开发与经济,2001(4):56-57.
[6] Elisseeva T V,Elisseeva V A,Shaposhnik IG. Demineralization and separation of amino acids byelectrodialysis with ion-exchange membranes[J].Desalination,2002,149:405-409.
[7]Shaposhnik V A,Eliseeva T V.Barrier effect during theelectrodialysis of ampholytes[J].J Membrane Sci,1999,161(1):223-228.
[8]王辉,余立新.用双极膜电渗析法分离混合氨基酸[J].清华大学学报,2004,44(12).
[9]李广,梁艳玲.电渗析技术的发展及应用[J].化工技术与开发,2007,37(7):28-30.
[10]广州奥桑味精食品有限公司.谷氨酸发酵液清洁生产新工艺[J].发酵科技通讯,2007,36(3):28-29.
[11]任洪艳.操作条件对双极膜电渗析性能和膜污染的影响[J].膜科学与技术,2008,28(5):45-51.
[12]氨基酸工艺学[M].北京:轻工业出版社,1983.
Study on the separation of monoammonium L-glutamate from glutamic acid broth using electrodialysis
AI She-fang1,SHI Shao-yuan2,WANG Jin-mei1,ZHANG Sheng-qin1,LI Chun1,3,CONG Wei2,*
(1.Chemistry and Chemical Engineering,Shihezi University,Shihezi 832003,China;2.State Key Lab of Biochemical Engineering,Institute of Process Engineering,Chinese Academy of Sciences,Beijing 100080,China;3.School of Life Science and Technology,Beijing Institute of Technology,Beijing 100081,China)
The feasibility of monoammonium L-glutamate separation directly from the glutamic acid broth using electrodialysis was investigated.The electrodialysis experiments have been performed with the simulated glumatic broth by the way of single factor test to optimize the operation conditions including current density,volume ratio of feed solution and concentrated solution and flow rate.Under the optimized conditions the monoammonium L-glutamate was separated directly from the glutamic acid broth and the crystallization phenomenon occurred at pH4.70 in the feed solution.The separation performance of electrodialysis was obviously improved by adding ammonia to adjust the pH of feed solution,the concentration of glutamate in the concentrated solution could attain to 120g/L and the recovery of monoammonium L-glutamate was 78.8%.
electrodialysis;monoammonium L-glutamate;glutamic acid broth;ammonia
TS201.1
B
1002-0306(2011)01-0195-04
2010-01-18 *通讯联系人
艾社芳(1984-),女,硕士研究生,研究方向:生物化工。
863重点项目(2006AA020301);973项目子课题(2007CB714306)资助。

